SPEKTROMETRI INFRA MERAH IR Sri Wahyu Murni Jurusan







































- Slides: 46

SPEKTROMETRI INFRA MERAH (IR) Sri Wahyu Murni Jurusan Teknik Kimia FTI UPN “Veteran” Yogyakarta 1

Deskripsi Bab ini membahas tentang dasar spekrometri infra merah (IR), prinsip kerja alat spektrometer IR serta penggunaannya untuk analisis kualitatif dan kuantitatif. 2

Tujuan Instruksional Khusus (TIK) Setelah membaca bab ini, mahasiswa mampu menjelaskan dasar spektrometri infra merah (IR), cara kerja alat spektrometer infra merah (IR) dan penggunaannya untuk analisis kualitatif dan kuantitatif 3

Pendahuluan Analisa menggunakan Infra Merah (IR) dipakai: 1. Analisa kualitatif untuk penentuan gugus fungsional yang tidak diketahui dari suatu senyawa, jadi bukan untuk penentuan unsur 2. Analisa kuantitatif menggunakan Hukum Lambert-Beer. 4

Pendahuluan (lanjutan) ¡ Apabila molekul cuplikan dilewati sinar IR, maka sebagian sinar akan diserap dan sebagian diteruskan. ¡ Molekul hanya menyerap sinar IR pada frekuensi tertentu, yaitu jika dalam molekul ada transisi energi sebesar E=h. ¡ Transisi yang terjadi akibat serapan sinar IR berkaitan dengan perubahan vibrasi di dalam molekul. ¡ Jadi bila sinar IR (4000 -650 cm-1) diabsorbsi oleh molekul, maka energi radiasi diubah menjadi energi vibrasi dan rotasi. 5

1. Vibrasi Molekul ¡ Vibrasi molekul tidak terjadi secara random, tetapi pada frekuensi khusus yang ditentukan oleh massa atom dan kekuatan ikatan kimianya. ¡ Untuk molekul diatomik: (Ingat H. Hook) = frekuensi c= kec. cahaya k=tetapan m 1, m 2 = masa atom = m 1. m 2/(m 1+m 2) =massa tereduksi 6

Contoh 1. 1. Hitung frekuensi rentangan ikatan C=C, C-H; C-O dalam metanol; C=O dalam aseton; serta C N. Penyelesaian: a. Ikatan C=C k= 10 x 105 dyne/cm 7

Contoh 1 (lanjutan) b. Ikatan C-H k=5 x 105 dyne/cm 8

Contoh (lanjutan) c. Ikatan C-O dalam metanol k=5 x 105 dyne/cm d. C=O dalam aseton k=5 x 105 dyne/cm 9

Contoh (lanjutan) d. C N k=15 x 105 dyne/cm 10

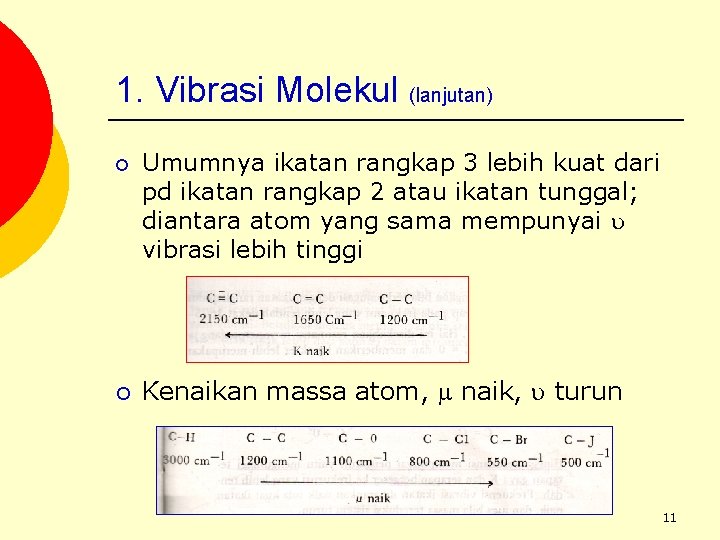
1. Vibrasi Molekul (lanjutan) ¡ ¡ Umumnya ikatan rangkap 3 lebih kuat dari pd ikatan rangkap 2 atau ikatan tunggal; diantara atom yang sama mempunyai vibrasi lebih tinggi Kenaikan massa atom, naik, turun 11

Vibrasi Molekul (lanjutan) o Gerakan lengkung/bending lebih mudah dari pada gerakan rentangan/streching, sehingga k lebih kecil ü Senyawa dengan gugus yang sama dapat menyerap pada yang berbeda, karena mengikat gugus lain yang berbeda 12

2. Macam-Macam Vibrasi Posisi relatif atom dalam molekul tidak tetap melainkan berubah-ubah karena vibrasi ¡ Molekul dengan 2 atau 3 atom sederhana, gerak vibrasi dan energinya dapat dihitung dengan mudah. ¡ Untuk molekul poliatomik menjadi sukar. ¡ 13

Macam-Macam Vibrasi (lanjutan) Dalam molekul triatom (AX 2) dapat terjadi vibrasi: 1. Streching (rentangan) perubahan secara kontinu dalam jarak antar atom, sepanjang sumbu ikatan antar atom yang berikatan 14

Macam-Macam Vibrasi (lanjutan) 2. Bending (lengkungan) perubahan kontinu dalam sudut ikatan dibagi 4 macam gerakan: a) b) c) d) scissoring (menggunting) Rocking Wagging Twisting 15

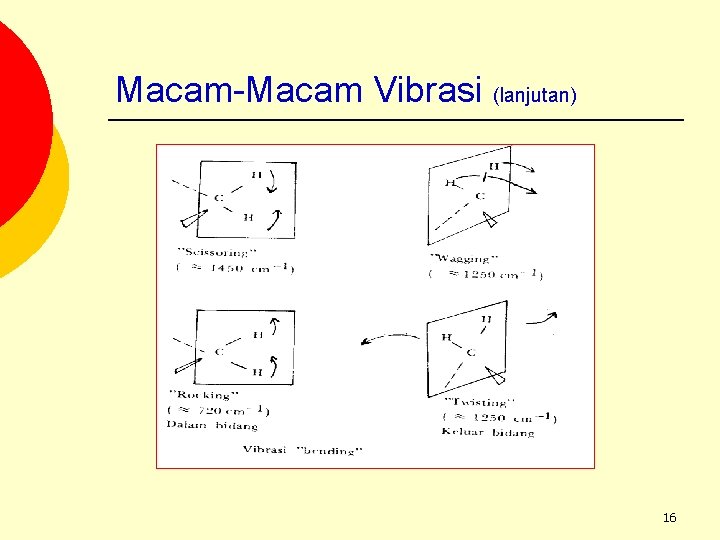
Macam-Macam Vibrasi (lanjutan) 16

Macam-Macam Vibrasi (lanjutan) a) Scissoring Kedua atom yang terikat pada atom pusat bergerak menuju dan menjauh satu dengan yang lainnya dengan deformasi sudut ikatan (dalam bidang) b) Rocking Seluruh unit bergerak maju mundur dalam bidang simetri (dalam bidang) c) Wagging Seluruh unit bergerak maju mundur dalam bidang tegak lurus pada bidang simetri (keluar bidang) d) Twisting seluruh unit berputar maju mundur mengelilingi ikatan (keluar bidang) 17

v Agar terjadi absorbsi sinar IR, molekul 2 harus mengalami perubahan momen dipol selama vibrasi Contoh: ¡ Molekul NO dan CO mempunyai distribusi elektron yang tidak simetris, atom yang satu mempunyai kerapatan elektron lebih besar dari yang lain ¡ Bila jarak antara 2 pusat atom berubah, seperti terjadi pada vibrasi; maka akan terjdi medan listrik yang akan beraksi dengan medan listrik radiasi Ø Bila radiasi = molekul, maka akan terjdi perpindahan energi yang menyebabkan perubahan amplitudo vibrasi molekul. Inilah penyebab terjadinya absorbsi o Molekul simetri: O 2, N 2, Cl 2 tidak dapat mengabsorbsi sinar IR. 18

3. Spektra Infra Merah (IR) A. B. § Sumbu horizontal : bilangan gelombang -1 (cm-1) Sumbu vertikal: %T -1 IR : 4000 cm-1 - 625 cm-1 ü ü -1 : 900 cm-1 - 1400 cm-1: finger print -1 : < 900 cm-1 dan >1400 cm-1: vibrasi pokok 19

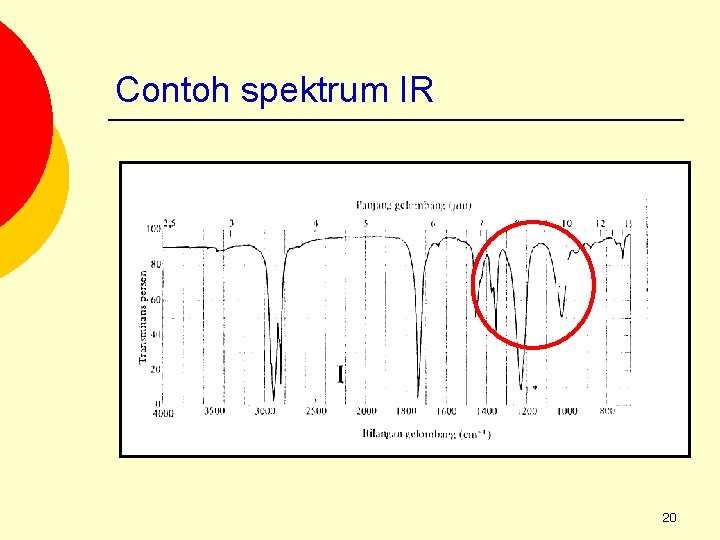
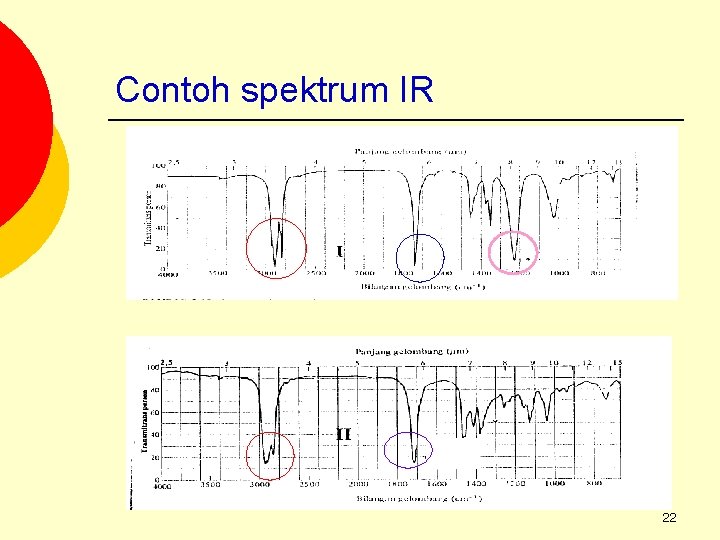
Contoh spektrum IR 20

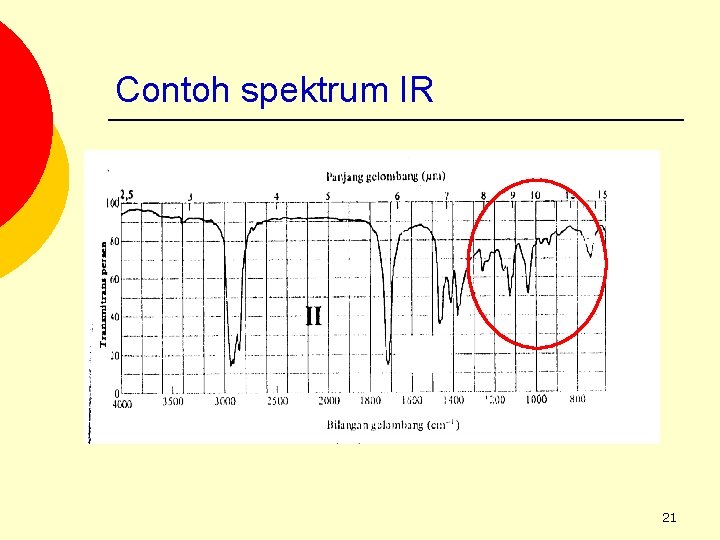
Contoh spektrum IR 21

Contoh spektrum IR 22

4. Penggunaan Spektrum IR 1. Identifikasi finger print -1 : 900 cm-1 - 1400 cm-1 ü Tidak dapat untuk identifikasi gugus, spektra pada daerah ini rumit tetapi karakteristik ü Untuk identifikasi senyawa tak dikenal bandingkan spektra IR dengan sederet spektra standar yang dibuat pada kondisi yang sama 23

2. Identifikasi gugus fungsional -1 : < 900 cm-1 dan >1400 cm-1 24

5. Cara Menganalisa Spektra IR ¡ Untuk analisa spektra yang tidak diketahui, pusatkan pada atau tidaknya gugus-gugus fungsional utama: C=C, O-H, N-NH, C=C, C N, NO 2 25

Langkah analisa spektra IR 1. Apakah terdapat gugus karbonil? C=O: 1820 -1600 cm-1 2. Bila gugus C=O ada, ujilah daftar berikut. Bila tidak ada, lanjutkan ke no. 3 § § § Asam: apa ada OH, serapan melebar 3400 -2400 cm-1 Amida: apa ada –NH, serapan medium 3500 cm-1 Ester: apa ada C-O, srapan kuat dekat 1300 -1000 cm-1 Anhidrida: mempunyai 2 serapan C=O dekat 1810 dan 1760 cm-1 Aldehida: apa ada C-H aldehida, 2 serapan lemah dekat 2850 dan 2750 cm-1 Keton: bila ke-5 kemungkinan di atas tidak ada 26

Langkah analisa spektra IR 3. (lanjutan) Bila gugus C=O tidak ada § alkohol: uji O-H serapan melebar 3600 -3300 cm-1 selanjutnya C-O dekat 1300 -1000 cm-1 § Amida: uji N-H serapan medium dekat 3500 cm-1 § Eter: uji C-O (serapan OH tidak ada) dekat 1300 -1000 cm-1 27

Langkah analisa spektra IR (lanjutan) Ikatan rangkap 2 dan atau aromatik 4. § § § C=C : serapan lemah 1650 cm-1 Cincin aromatik: serapan medium tinggi kuat 1650 -1450 cm-1 Buktikan kemungkinan di atas dengan memperhatikan serapan daerah C-H aromatik dan vinil, sebelah kiri 3000 cm-1 C-H alifatik: sebelah kanan 3000 cm-1 28

Langkah analisa spektra IR 5. Ikatan rangkap 3 § § 6. (lanjutan) C N: serapan medium tajam dekat 2250 cm-1 C C: serapan lemah tapi tajam dekat 2150 cm-1 uji C-H asetilen dekat 3300 cm-1 Gugus Nitro dua serapan kuat 1600 -1500 cm-1 dan 1390 -1300 cm-1 29

Langkah analisa spektra IR (lanjutan) Hidrokarbon 7. § § § Ke enam serapan di atas tidak ada Serapan utama untuk C-H dekat 3000 cm-1 Spektrum sangat sederhana, hanya terdapat serapan lain-lain dekat 1450 cm-1 30

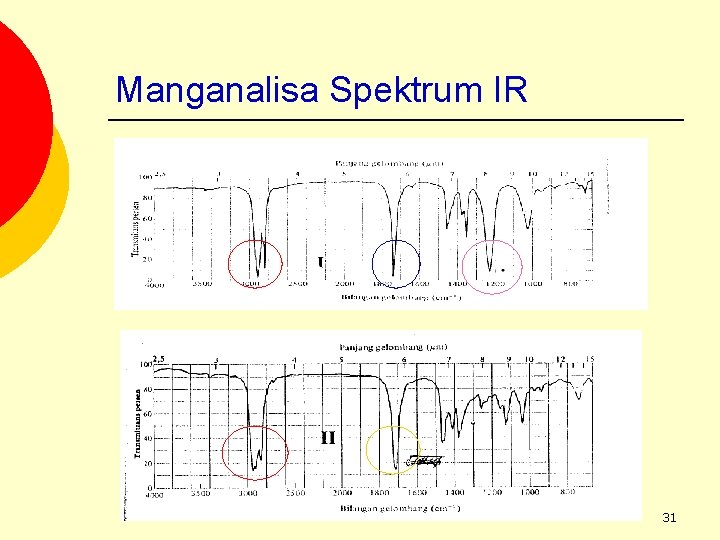
Manganalisa Spektrum IR 31

Interpretasi senyawa gugus Senyawa II 1740, C=O ada 1710; C=O ada Tidak ada b. Amida –NH serapan medium dekat 3500 cm-1 Tidak ada c. ester: C-O serapan kuat dekat 1300 -1000 cm-1 Serapan kuat 1220 cm-1, C-O ada Tidak ada, C-O tidak ada d. Anhidrida Tidak ada e. Aldehida Tidak ada 7. Gugus alkil serapan CH dekat 3000 cm-1 Serapan kuat sekitar 2800 cm-1 Kesimpulan Ester keton 1. Gugus karbonil C=O; 1820 -1600 cm-1 2. a. asam: -OH serapan melebar dekat 3400 -2400 cm-1 f. Keton 32

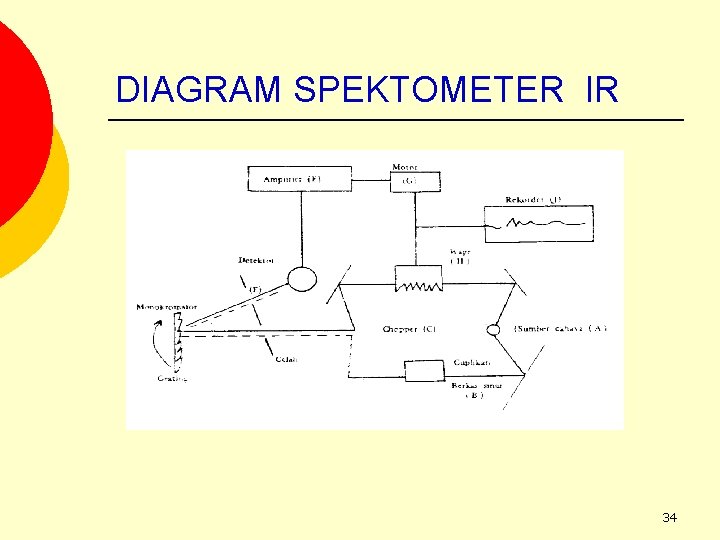
6. Instrumentasi Bagian-bagian pokok Spektrofotometer IR 1. Sumber cahaya IR 2. Monokromator 3. detektor 33

DIAGRAM SPEKTOMETER IR 34

1. Sumber Cahaya Sumber cahaya IR: a. Nerst glower: batang/tabung yang panjangnya 3 cm dan diameter 2 mm, terbuat dari campuran oksida Se, Zr, Th dan Y. Stabil pada suhu tinggi dan tidak teroksidasi oleh udara b. Campuran globar: batang dari Si. C, ukuran lebih besar dari Ners glower, p=5 cm dan diameter 4 mm. dapat bekerja s/d T=1300 o. C c. Bahan keramik 35

2. Monokromator q q Dapat digunakan : grating atau prisma Prisma terbuat dari Na. Cl, karena transparan Grating memberi hasil yang lebih baik Na. Cl bersifat higroskopis, sehingga cermin harus dilindungi dari uap air 36

3. Detektor q Jenis: detektor thermopile q Cara kerja: Jika 2 kawat logam yang berbeda dihubungkan antara ujung kepala dan ekor menyebabkan adanya arus yang mengalir dalam kawat q Arus sebanding dengan intensitas yang jatuh pada thermopile q 37

7. Kalibrasi Skala Frekuensi ¡ ¡ Sebelum melakukan pekerjaan, skala pencatat harus dikalibrasi Senyawa yang digunakan sebagai standar adalah polistirena l Frekuensi telah diketahui dg tepat l Puncak yang biasa dipakai sebagai kalibrasi dari polistirena adalah 1601 cm -1 38

8. Cara penanganan Cuplikan Beda dengan cara-cara yang digunakan spektrometer lainnya 1. Gas Cuplikan harus dimasukkan dalam sel gas (hampa). Sel menghadap langsung berkas sinar dan dipantulkan berulangkali melalui cuplikan, untuk menaikkan intensitas 39

8. Cara penanganan Cuplikan 2. Cairan § § Satu tetes cairan ditempatkan sebagai film tipis diantara 2 lapis Na. Cl yang transparan terhadap IR Na. Cl setelah dipakai dicuci dengan toluen, CH 3 Cl dll Na. Cl harus tetap kering Cuplikan yang mengandung air: digunakan Ca. F 2 40

8. Cara penanganan Cuplikan 3. Padatan a. b. c. Pelet KBr 0, 1 -2% berat cuplikan dan KBr, dicampur kemudian ditekan; sehingga diperoleh pelet yang trasparan. Selama pengerjaan harus dihindari kondensasi uap dr atmosfer Mull/Pasta cuplikan dicampur dengan 1 tetes minyak. Pasta kemudian dilapiskan diantara 2 keping Na. Cl yang trasparan. Bahan pasta harus transparan terhadap IR Lapisan tipis padatan 41

Soal-soal 1. Bagaimanakah membedakan pasangan senyawa berikut menggunakan infra merah. Tunjukkan pita serapan karakteristik dari masing-masing senyawa. dan 2. Berlangsungnya reaksi oksidasi isopropanol menjadi aseton dapat diikuti dengan spektroskopi infra merah. Jelaskan. 3. Pita serapan C=O selalu kuat, sedangkan pita serapan gugus C=C intensitasnya bervariasi. Mengapa demikian? jelaskan 42

Soal-soal 4. Dua macam komponen penyusun minyak sereh mempunyai rumus molekul yang sama. Spektra inframerah komponen A (C 10 H 12 O) mempunyai pita serapan kuat pada 1700 cm-1 dan lemah pada 1640 cm-1 disamping pita C-H lemah didekat 3050 cm-1, 2800 dan 2700 cm-1. Komponen B mempunyai serapan kuat dekat 3500 cm-1 dan serapan lemah pada 3050 dan 1640 cm-1. Senyawa A dapat direduksi menjadi senyawa B. Tunjukkan masing-masing gugus fungsional pada senyawa A dan B. 43

Jawaban soal-soal 1. 2. Gugus keton dan aldehid dapat dibedakan dari adanya serapan C-H aldehida yaitu dua serapan lemah pada 2850 dan 2750 cm-1. Gugus –OH pada alkohol serapan melebar dekat 3600 -3300 cm-1 gugus C=O pada keton serapan pada 1820 -1600 cm-1. Jadi reaksi oksidasi isopropanol menjadi aseton dapat diikuti dengan menghilangnya serapan melebar pada 33600 -3300 cm-1 munculnya gugus C=O serapan pada 1820 -1600 cm-1. 44

3. Pita serapan C=O selalu kuat karena jenisa vibrasi C=O adalah streching, vibrasi strechinh selalu kuat. Pita serapan C=C intensitasnya bervariasi, karena jenis vibrasinya berbeda-beda mengingat struktur ikatan C=C juga berbeda, misalnya: C=C trans, maka C-H def 970 cm-1 C=C cis, maka C-H pada 700 cm-1 45

Senyawa A: Serapan kuat pada 1720 cm-1 adalah gugus C=O C-H lemah 3050, 2800 dan 2700 cm-1 adalah C-H aldehida Senyawa B: serapa kuat dekat 3500 cm-1 adalah gugus OH alkohol Lemah di 3050 dan 1640 cm-1. Adalah gugus…. 4. Maka Senyawa A: aldehida senyawa B: alkohol 46