Spectromtrie de Masse Bases de la spectromtrie de

Spectrométrie de Masse Bases de la spectrométrie de Masse Principaux modes d’ionisation Pr Olivier Laprévote olivier. laprevote@parisdescartes. fr 1
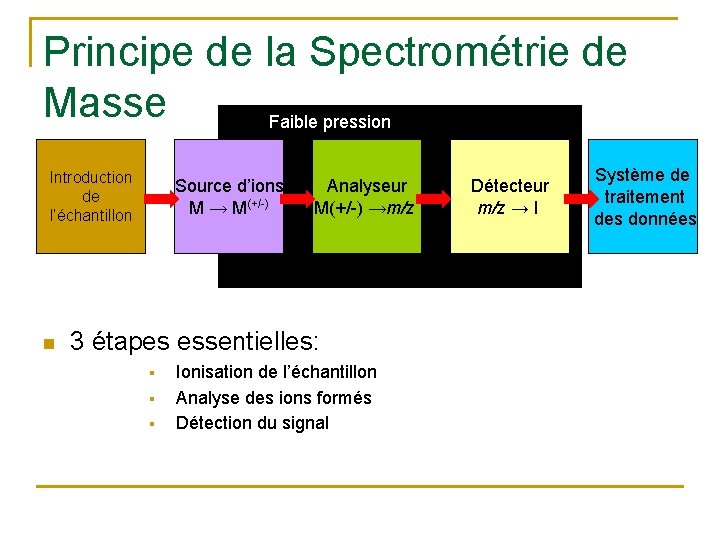
Principe de la Spectrométrie de Masse Faible pression Introduction de l’échantillon n Source d’ions M → M(+/-) Analyseur M(+/-) →m/z 3 étapes essentielles: § § § Ionisation de l’échantillon Analyse des ions formés Détection du signal Détecteur m/z → I Système de traitement des données
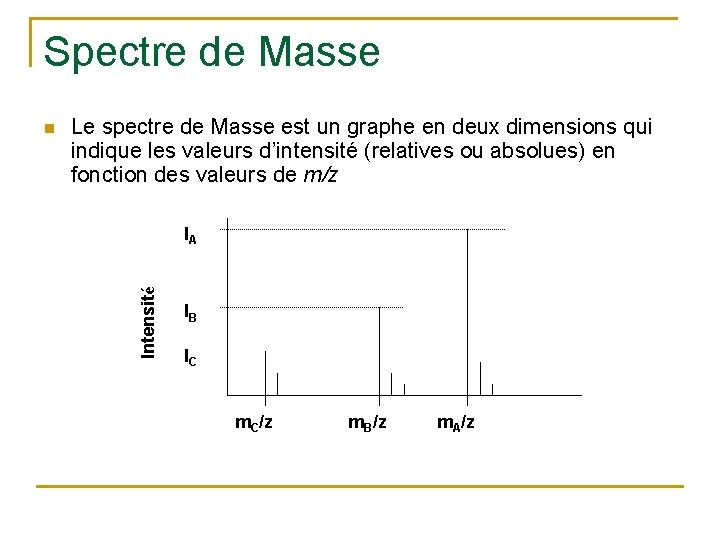
Spectre de Masse Le spectre de Masse est un graphe en deux dimensions qui indique les valeurs d’intensité (relatives ou absolues) en fonction des valeurs de m/z IA Intensité n IB IC m. C/z m. B/z m. A/z
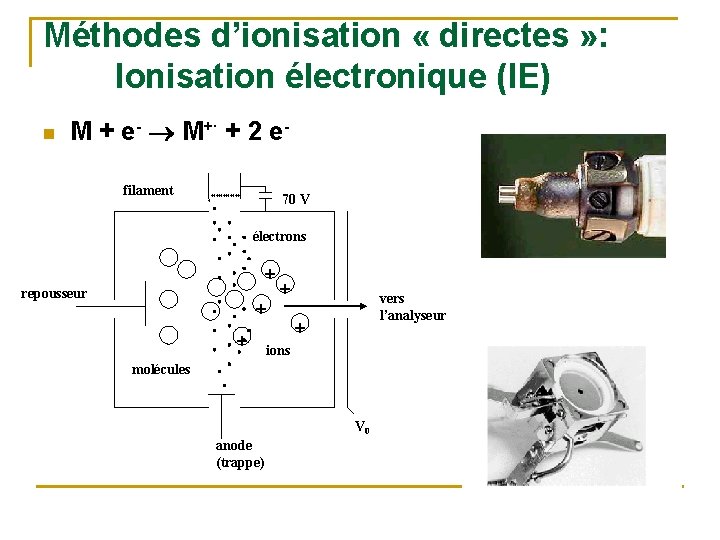
Méthodes d’ionisation « directes » : Ionisation électronique (IE) n M+ e- . + M filament ℓ + 2 e 70 V ℓℓℓℓℓℓℓ électrons + repousseur + + + vers l’analyseur + ions molécules V 0 anode (trappe)
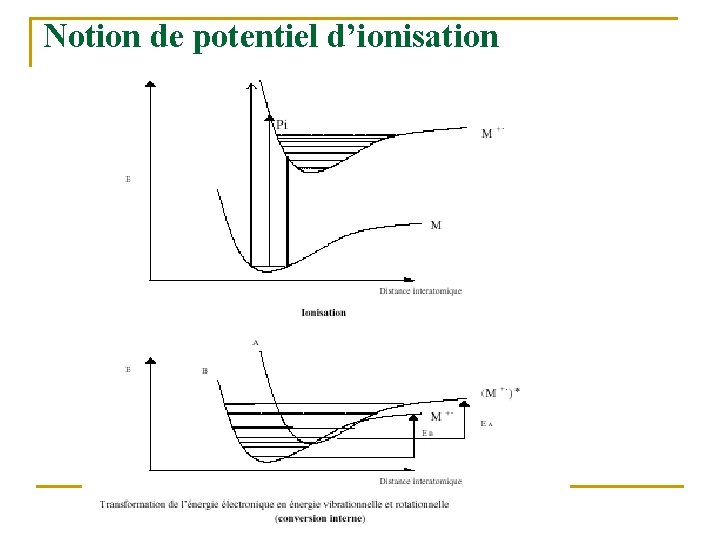
Notion de potentiel d’ionisation

Ionisation Chimique (IC) n Première étape: Ionisation d’un gaz réactif (exemple: l’ammoniac): NH 3 + e- → NH 3+. + 2 e. NH 3+. + NH 3 → NH 4+ + NH 2. n Deuxième étape: protonation de la molécule M par l'ion ammonium M + NH 4+ → (M …. . H…. . NH 3)+ → m/z 18 n m/z M+18 MH+ + NH 3 m/z M+1 Lorsque l'on utilise un gaz réactif GH+, la réaction qui se produit avec la molécule M peut s'écrire de la façon suivante: M + GH+ → MH+ + G GH+ → G + H+ MH+ → M + H+ ΔH°G = AP(G) ΔH°M = AP(M) n Les enthalpies de ces deux réactions s'appellent "affinités protoniques" (respectivement du gaz et de la molécule à analyser); elles correspondent au terme enthalpique de la basicité en phase gazeuse. n La réaction de protonation a lieu lorsque APG < APM n Concrètement, on choisira un gaz réactif adapté à la molécule étudiée (de plus faible AP), en général dans le but de limiter les phénomènes de fragmentation.
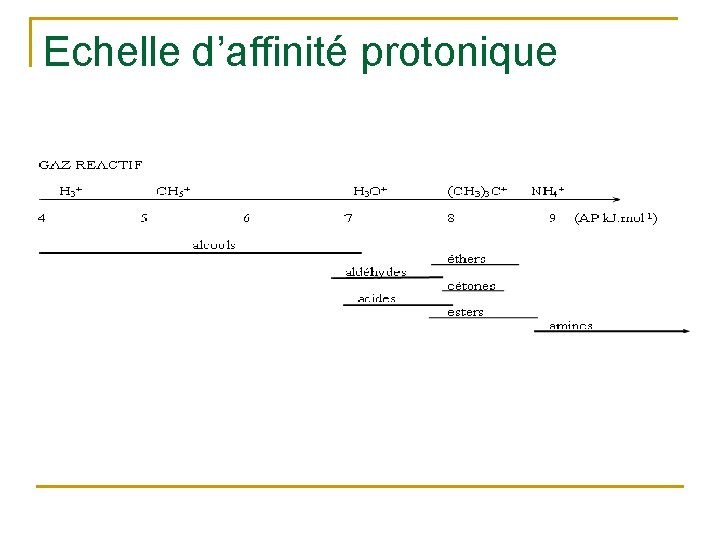
Echelle d’affinité protonique
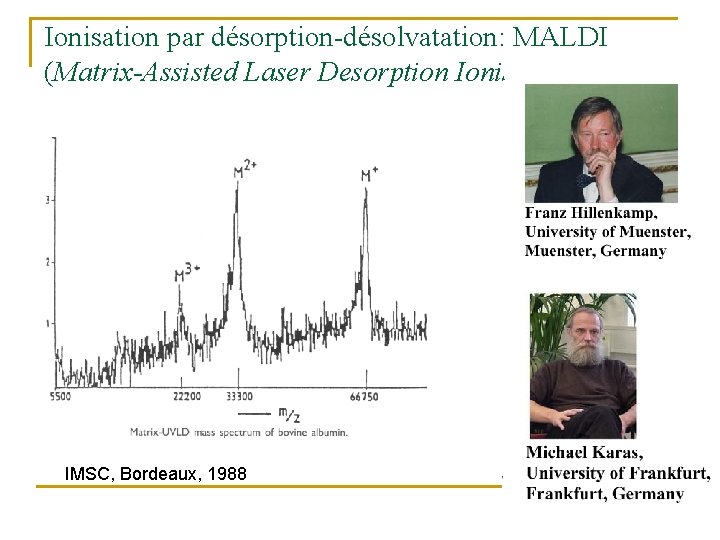
Ionisation par désorption-désolvatation: MALDI (Matrix-Assisted Laser Desorption Ionisation) IMSC, Bordeaux, 1988
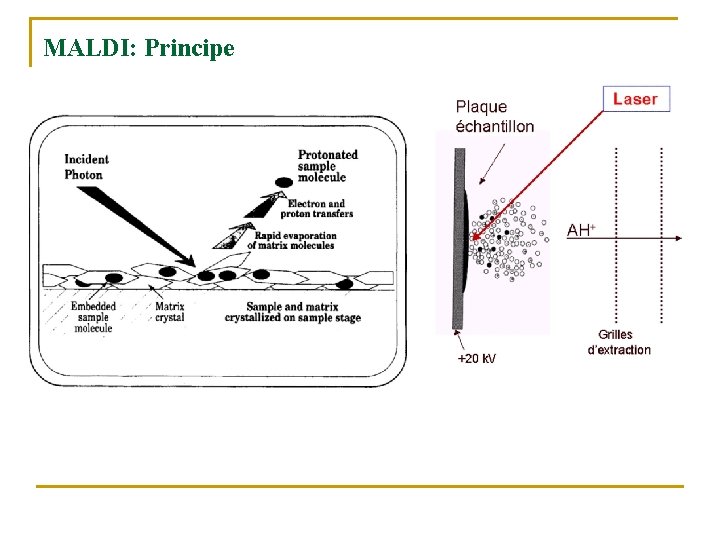
MALDI: Principe
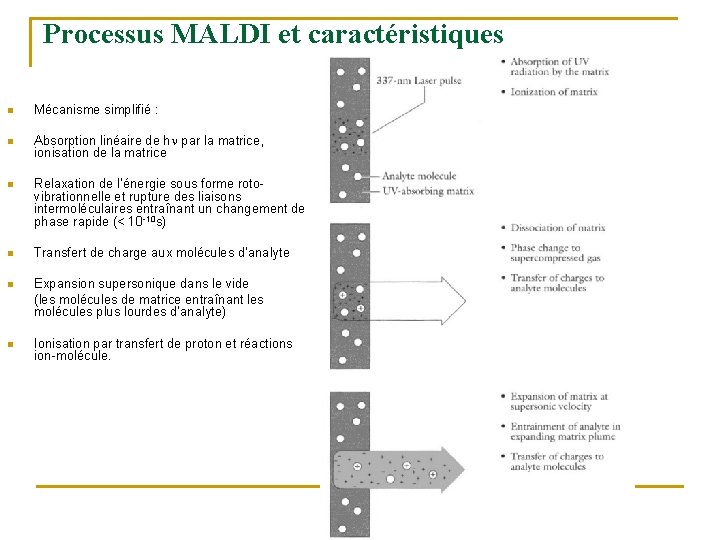
Processus MALDI et caractéristiques n Mécanisme simplifié : n Absorption linéaire de h par la matrice, ionisation de la matrice n Relaxation de l’énergie sous forme rotovibrationnelle et rupture des liaisons intermoléculaires entraînant un changement de phase rapide (< 10 -10 s) n Transfert de charge aux molécules d’analyte n Expansion supersonique dans le vide (les molécules de matrice entraînant les molécules plus lourdes d’analyte) n Ionisation par transfert de proton et réactions ion-molécule.

MALDI: cible et sas d’introduction

MALDI: cible réfrigérée (384 puits)
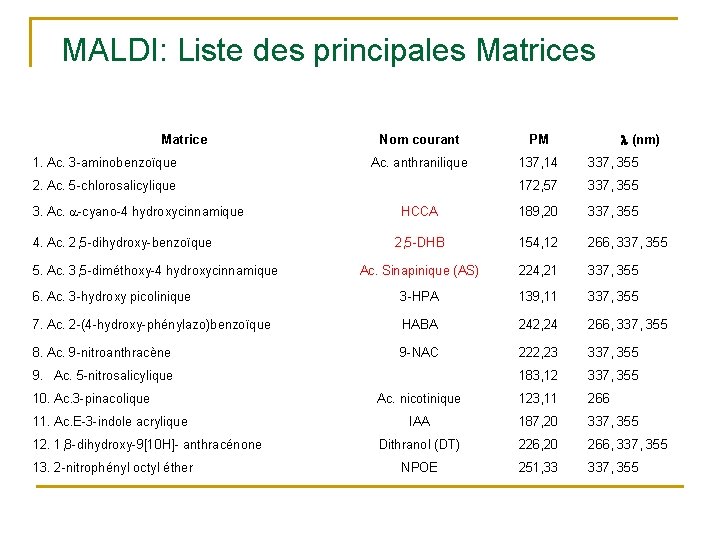
MALDI: Liste des principales Matrice (nm) Nom courant PM Ac. anthranilique 137, 14 337, 355 172, 57 337, 355 HCCA 189, 20 337, 355 2, 5 -DHB 154, 12 266, 337, 355 Ac. Sinapinique (AS) 224, 21 337, 355 6. Ac. 3 -hydroxy picolinique 3 -HPA 139, 11 337, 355 7. Ac. 2 -(4 -hydroxy-phénylazo)benzoïque HABA 242, 24 266, 337, 355 8. Ac. 9 -nitroanthracène 9 -NAC 222, 23 337, 355 183, 12 337, 355 Ac. nicotinique 123, 11 266 IAA 187, 20 337, 355 Dithranol (DT) 226, 20 266, 337, 355 NPOE 251, 33 337, 355 1. Ac. 3 -aminobenzoïque 2. Ac. 5 -chlorosalicylique 3. Ac. -cyano-4 hydroxycinnamique 4. Ac. 2, 5 -dihydroxy-benzoïque 5. Ac. 3, 5 -diméthoxy-4 hydroxycinnamique 9. Ac. 5 -nitrosalicylique 10. Ac. 3 -pinacolique 11. Ac. E-3 -indole acrylique 12. 1, 8 -dihydroxy-9[10 H]- anthracénone 13. 2 -nitrophényl octyl éther
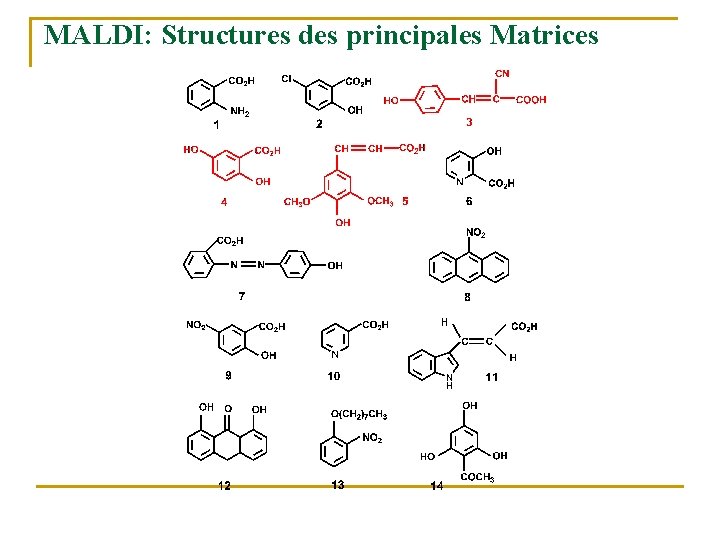
MALDI: Structures des principales Matrices
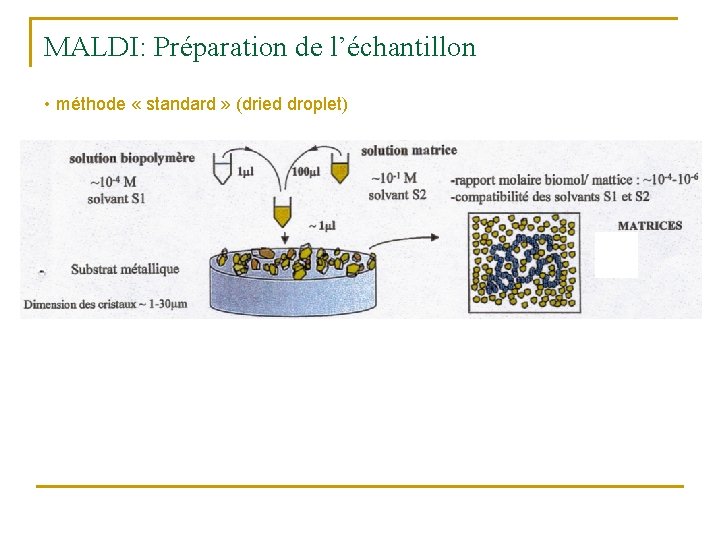
MALDI: Préparation de l’échantillon • méthode « standard » (dried droplet)
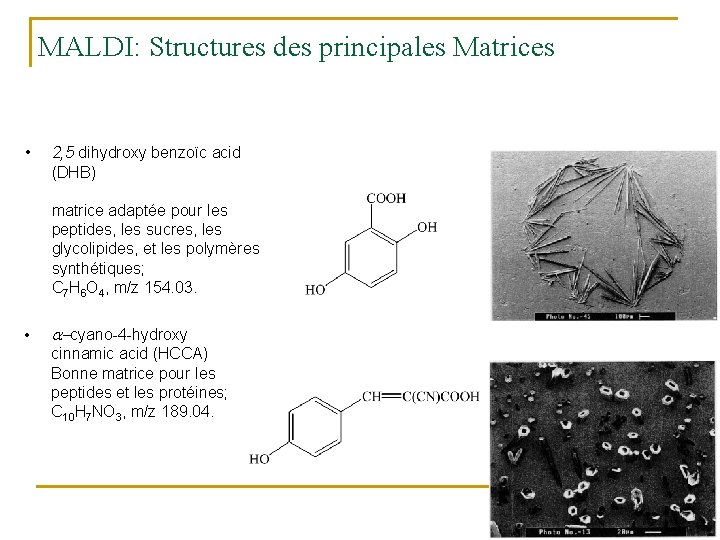
MALDI: Structures des principales Matrices • 2, 5 dihydroxy benzoïc acid (DHB) matrice adaptée pour les peptides, les sucres, les glycolipides, et les polymères synthétiques; C 7 H 6 O 4, m/z 154. 03. • a-cyano-4 -hydroxy cinnamic acid (HCCA) Bonne matrice pour les peptides et les protéines; C 10 H 7 NO 3, m/z 189. 04.
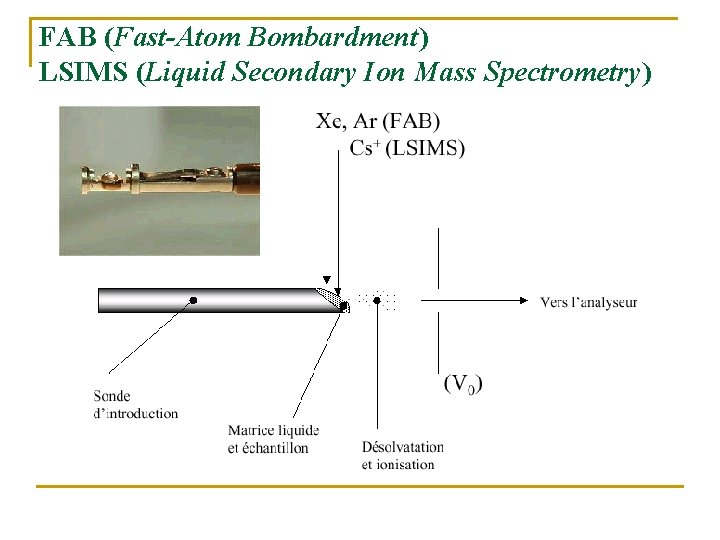
FAB (Fast-Atom Bombardment) LSIMS (Liquid Secondary Ion Mass Spectrometry)
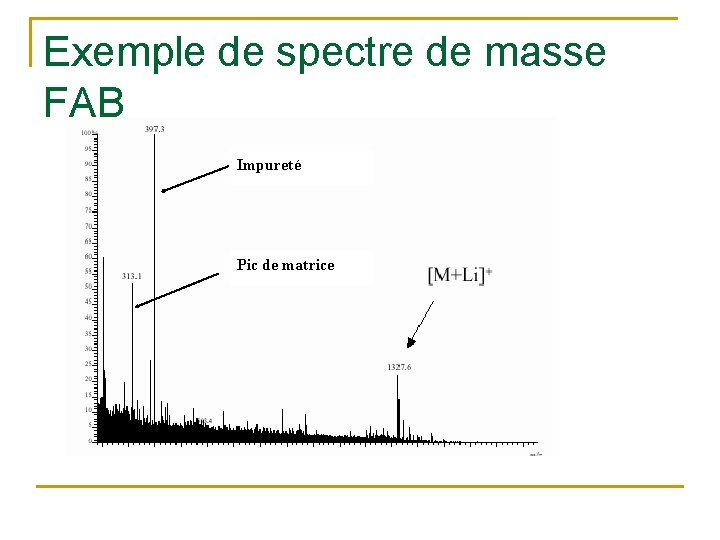
Exemple de spectre de masse FAB Impureté Pic de matrice
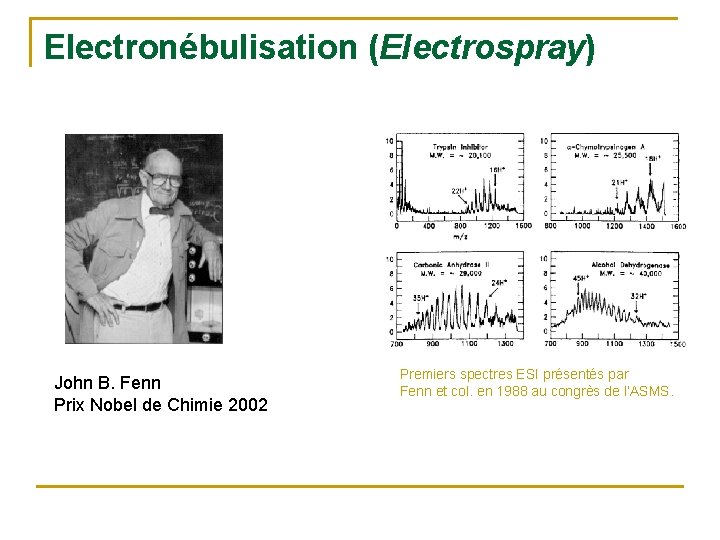
Electronébulisation (Electrospray) John B. Fenn Prix Nobel de Chimie 2002 Premiers spectres ESI présentés par Fenn et col. en 1988 au congrès de l’ASMS.
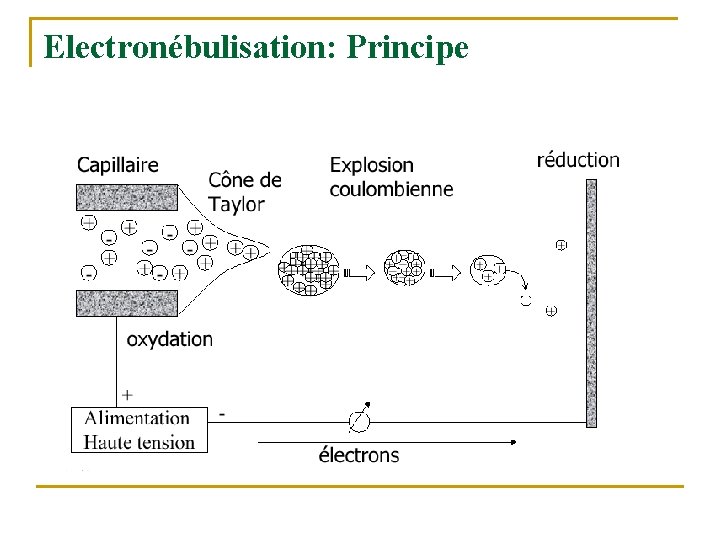
Electronébulisation: Principe

Source d’ions par électronébulisation: Schéma général

Electronébulisation: formation du nébulisat (spray)
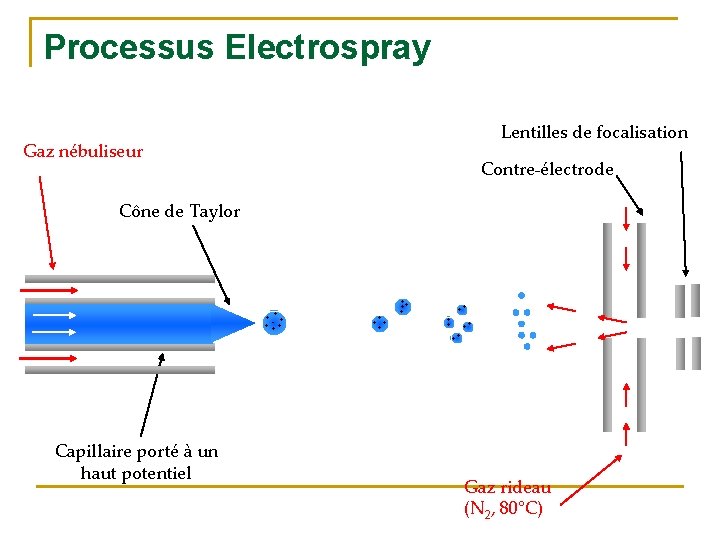
Processus Electrospray Lentilles de focalisation Gaz nébuliseur Contre-électrode Cône de Taylor + + - + + + + ++ + + + Capillaire porté à un haut potentiel + + + Gaz rideau (N 2, 80°C)
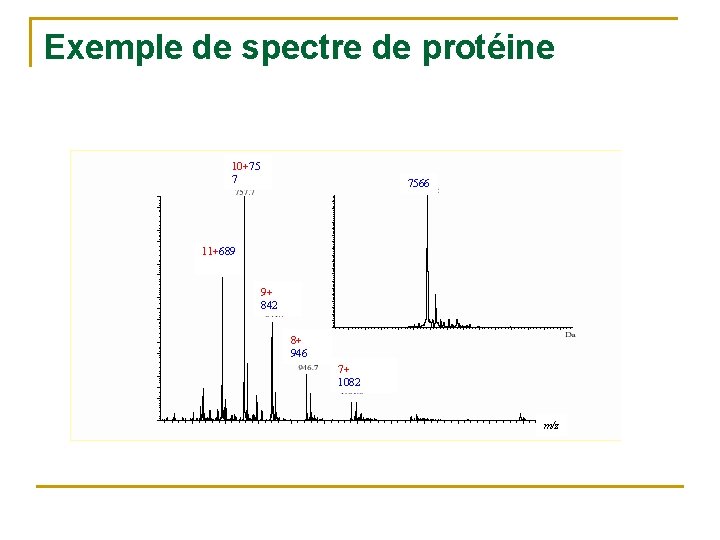
Exemple de spectre de protéine 10+75 7 7566 11+689 9+ 842 8+ 946 7+ 1082 m/z
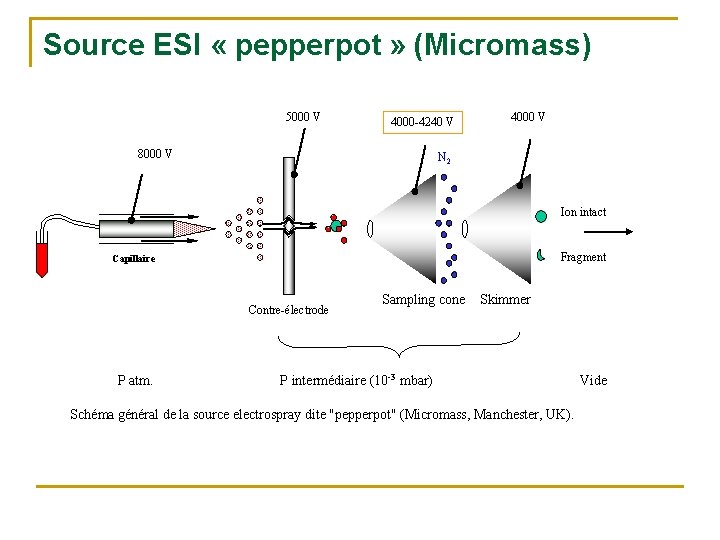
Source ESI « pepperpot » (Micromass) 5000 V 4000 -4240 V 8000 V 4000 V N 2 Ion intact Fragment Capillaire Contre-électrode P atm. Sampling cone Skimmer P intermédiaire (10 -3 mbar) Schéma général de la source electrospray dite "pepperpot" (Micromass, Manchester, UK). Vide
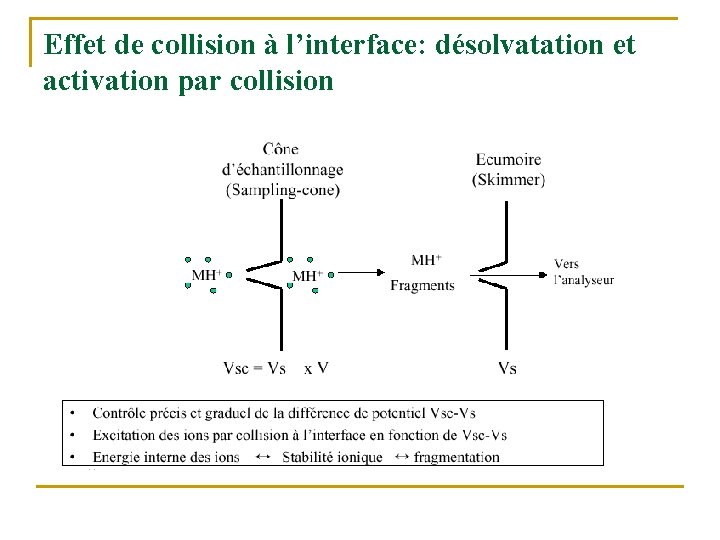
Effet de collision à l’interface: désolvatation et activation par collision
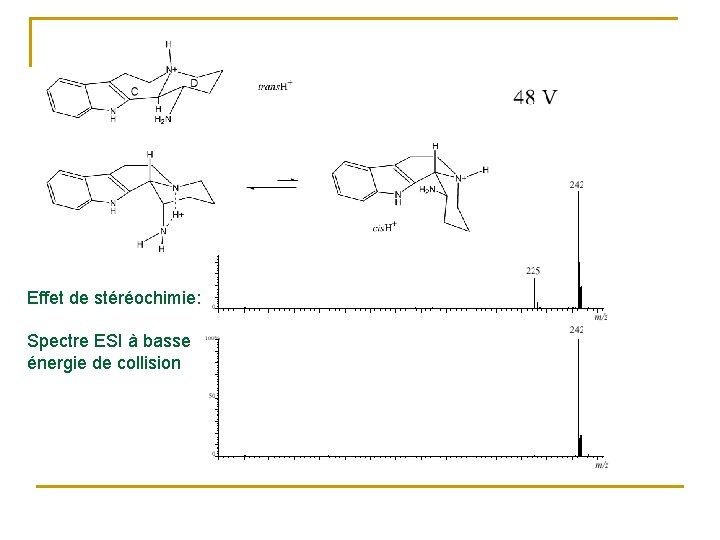
Effet de stéréochimie: Spectre ESI à basse énergie de collision
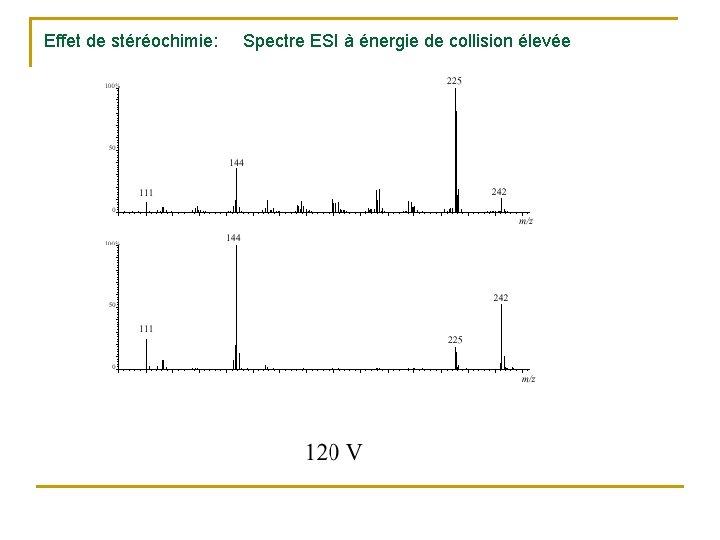
Effet de stéréochimie: Spectre ESI à énergie de collision élevée

Miniaturisation de la source electrospray: le nanospray


Source nanospray (Sciex)

Ionisation Chimique à Pression Atmosphérique (APCI) • • • L’APCI, procède de réactions ion-molécule en phase gazeuse à Patm. La solution est introduite en solution (50 m. L à 1. 5 m. L/min) où elle est nébulisée l’aide d’un courant d’azote. La désolvatation est favorisée par chauffage. Les ions sont produits par décharge électrique (électrons) sur l’aérosol de solvant contenant l’échantillon. Les molécules sont ionisées chimiquement par transfert de proton en mode positif, d’électron ou de proton en mode négatif. L ’ionisation est très efficace car elle se passe à Patm, où la fréquence des collisions est élevée.
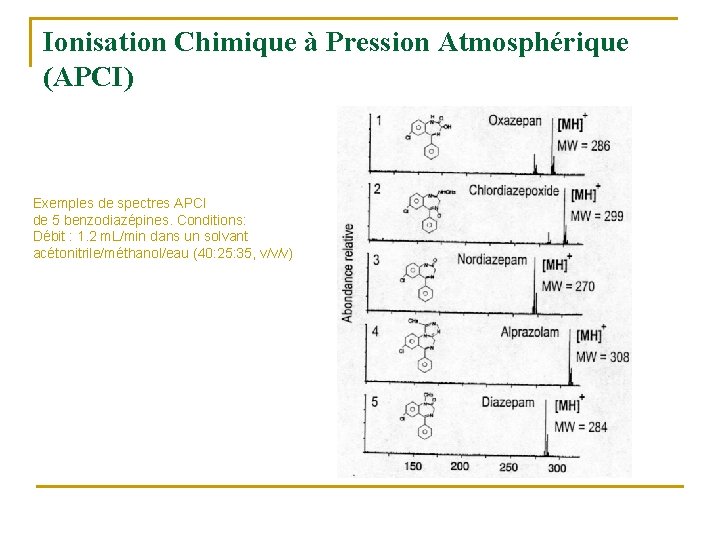
Ionisation Chimique à Pression Atmosphérique (APCI) Exemples de spectres APCI de 5 benzodiazépines. Conditions: Débit : 1. 2 m. L/min dans un solvant acétonitrile/méthanol/eau (40: 25: 35, v/v/v)

Photoionisation à pression atmosphérique (APPI): principe Ionisation à un photon dès lors que hν > PI M + hν M+. + e- Energie interne < hν - PI Eint ( M+. ) = (hν - PI ) – E(e-)
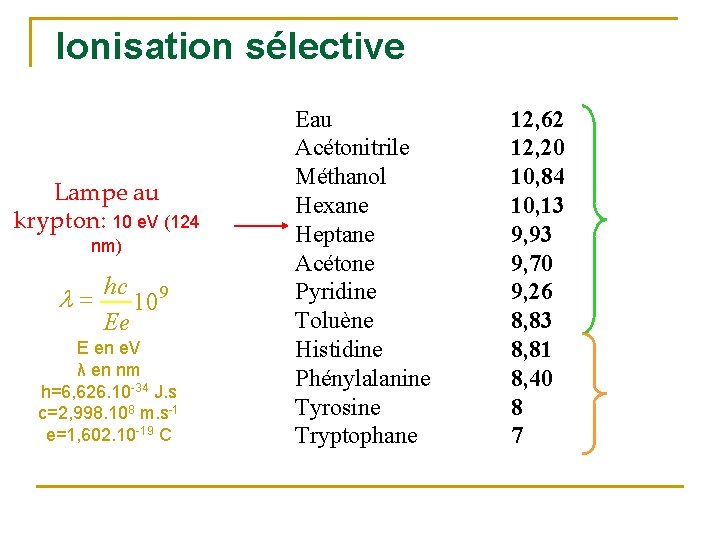
Ionisation sélective Lampe au krypton: 10 e. V (124 nm) l= hc 9 10 Ee E en e. V λ en nm h=6, 626. 10 -34 J. s c=2, 998. 108 m. s-1 e=1, 602. 10 -19 C Eau Acétonitrile Méthanol Hexane Heptane Acétone Pyridine Toluène Histidine Phénylalanine Tyrosine Tryptophane PI (e. V) 12, 62 12, 20 10, 84 10, 13 9, 93 9, 70 9, 26 8, 83 8, 81 8, 40 8 7
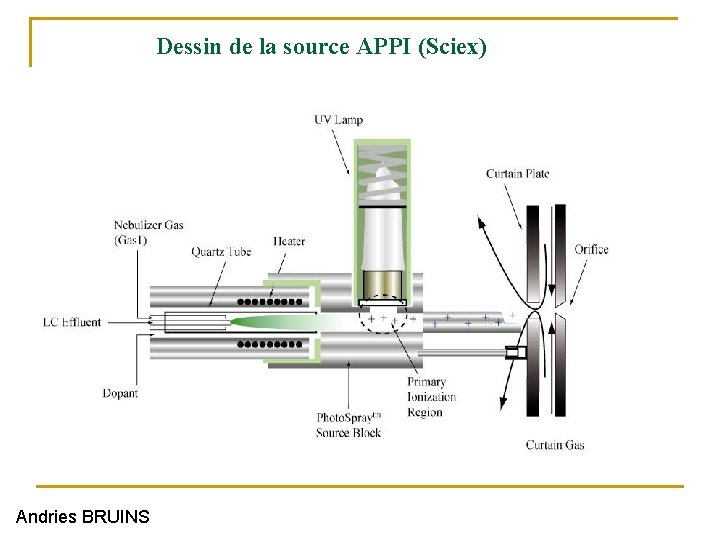
Dessin de la source APPI (Sciex) Expérience de Andries Bruins Andries BRUINS
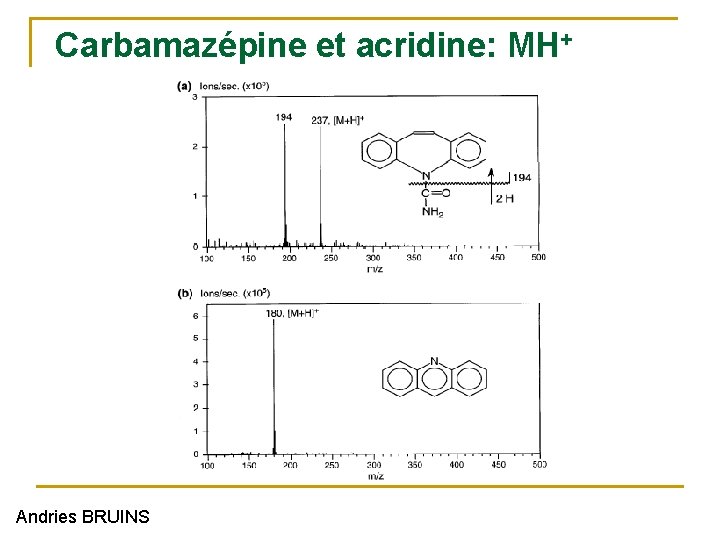
Carbamazépine et acridine: MH+ Andries BRUINS
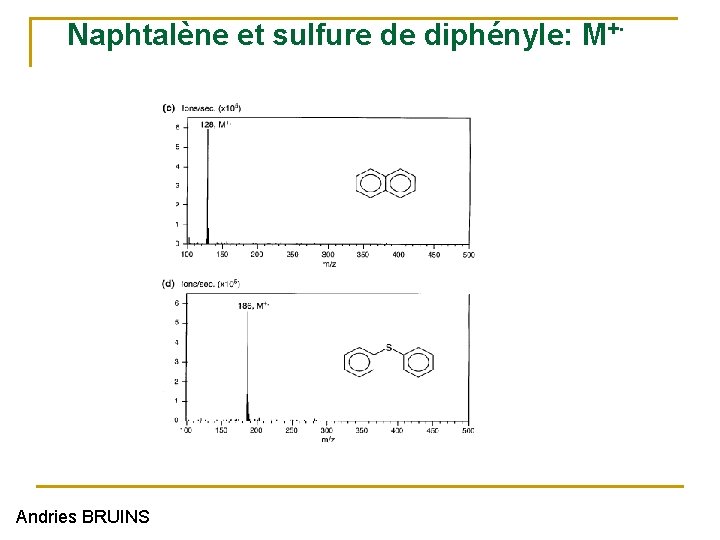
Naphtalène et sulfure de diphényle: Andries BRUINS . + M
- Slides: 38