Spectrometrie UVVIS en AAS Laboratorium techniek 1 Doel

Spectrometrie (UV-VIS en AAS) Laboratorium techniek 1

Doel en soorten spectrometrie Doel: - bepaling van lage concentratie’s in oplossing - 1*10 -3 tot 1*10 -9 mol∙L-1 Principe - absorptie van energie (licht) door moleculen / atomen Soorten: Colorimetrie : visueel (Nessler buizen) Fotometrie : optisch systeem (spectrofotometer) 2

colorimetrie Doel: - bepaling van concentratie m. b. v. kleurintensiteit Beperkingen: - oplossing moet een kleur hebben - standaardreeks vereist - schatting - beperking door ons oog (de “detector”) 3

spectrofotometrie Principe: detector meet de hoeveelheid doorgelaten licht! - Transmissie (T) - T = I 1/I 0 - T% = T*100% 4
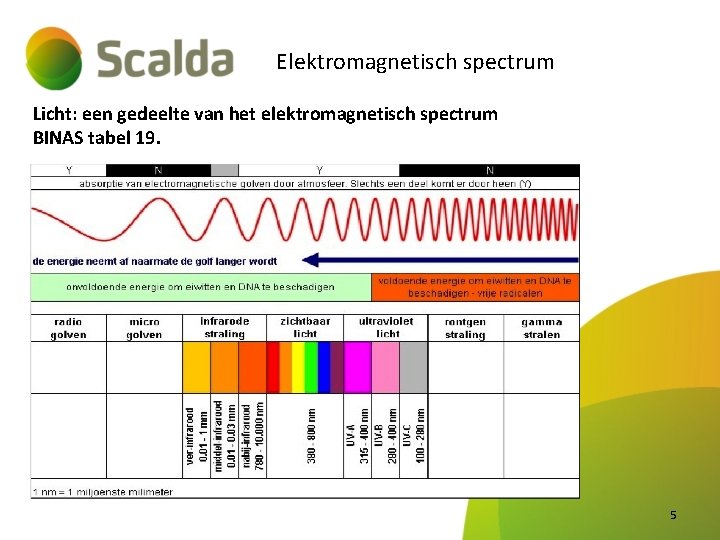
Elektromagnetisch spectrum Licht: een gedeelte van het elektromagnetisch spectrum BINAS tabel 19. 5
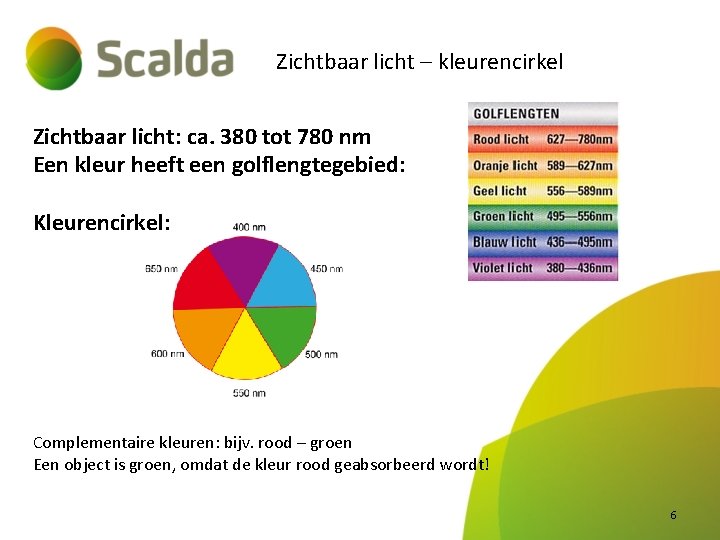
Zichtbaar licht – kleurencirkel Zichtbaar licht: ca. 380 tot 780 nm Een kleur heeft een golflengtegebied: Kleurencirkel: Complementaire kleuren: bijv. rood – groen Een object is groen, omdat de kleur rood geabsorbeerd wordt! 6
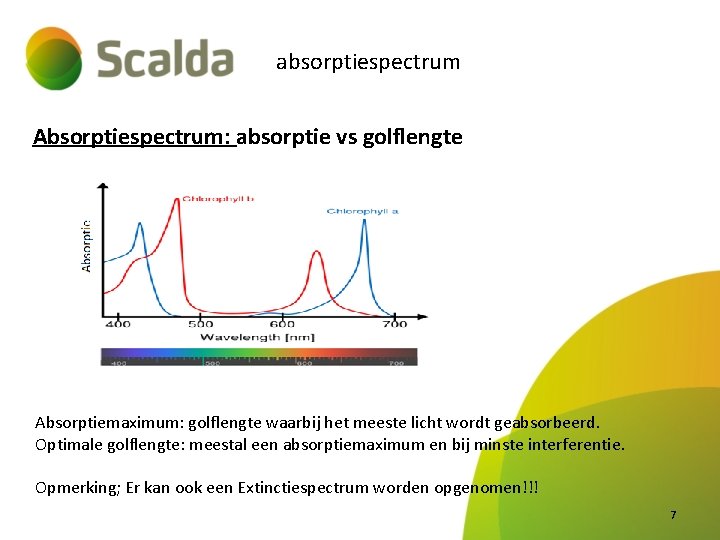
absorptiespectrum Absorptiespectrum: absorptie vs golflengte Absorptiemaximum: golflengte waarbij het meeste licht wordt geabsorbeerd. Optimale golflengte: meestal een absorptiemaximum en bij minste interferentie. Opmerking; Er kan ook een Extinctiespectrum worden opgenomen!!! 7

spectrofotometrie Principe: detector meet de hoeveelheid doorgelaten licht! Spectrofotometer schematisch: Monochromatisch : éénkleurig Polychromatisch : veelkleurig (bijv. wit licht) 8

Transmissie - Extinctie Principe: detector meet de hoeveelheid doorgelaten licht! - Transmissie (T) of doorlaatbaarheid - T = I 1/I 0 - T% = T*100% - E = -log (T) (Extinctie = Absorbance) - T = 10 -E 9

Wet van Lambert en Beer - E = -log (T) = absorbance E λ = ελ * l * c - Grootheden en eenheden: E : Extinctie (geen eenheid) l : optische weglengte (cm) c : concentratie (mol. L-1) ε : molaire extinctiecoëfficient (L. mol-1. cm-1) Indien c niet in mol. L-1 (bijv. mg. L-1 of zelfs ppm): Dan specifieke extinctiecoëfficient εs 10
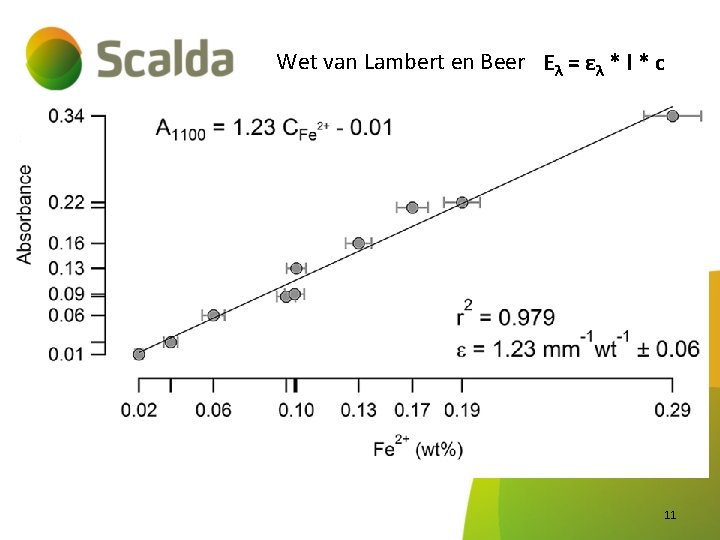
Wet van Lambert en Beer Eλ = ελ * l * c 11

Wet van Lambert en Beer Voorwaarden: 1. 2. 3. 4. 5. 6. Monochromatisch licht Verdunde oplossingen (ivm lineariteit) Heldere oplossingen (ook geen bubbels!) Temperatuur constant Geen chemische reacties Matrix matching- Standaarden en monsters gelijk qua oplosmiddel en zuurgraad (p. H) 12

Oefeningen Spectro 11. Tussen welke golflengtegrenzen ligt rood licht? 12. Wat is de complementaire kleur van licht met de kleur: a. rood b. blauw c. groen 13. Welke kleur licht wordt door een rode oplossing geabsorbeerd? 17. Wat wordt met een Extincitiespectrum weergegeven? 18. Teken schematisch een spectrofotometer en benoem de onderdelen. Marco Houtekamer; Afd. Laboratorium techniek; 13 oktober 2017 11. 650 – 780 nm 12. a. Groen b. Oranje c. Rood 13. Vooral groen, maar eigenlijk alle kleuren behalve rood 17. E vs golflengte 18. Zie blz 9 13

Oefeningen Spectro 28. Bereken de T als T% is a. 46, 5 b. 3, 45 29. Bereken T% als T is: a. 0, 439 b. 0, 0012 30. Bereken E indien de transmissie in % is: a. 4, 30 b. 14, 64 c. 24, 86 d. 34, 78 e. 87, 65 f. 98, 45 28. T = %T/100 a. T = 0, 465 b. T = 0, 0345 29. T% = T*100 a. T% = 43, 9 b. T% = 0, 12 30. E = -log(T) = -log(T%/100) a. E = 1, 37 b. E = 0, 8344 c. E = 0, 6045 d. E = 0, 4587 e. E = 0, 05725 f. E = 6, 784*10 -3 14

Oefeningen Spectro 31. Bereken de transmissie in % indien de extinctie is: a. 0, 235 b. 0, 034 c. 0, 986 d. 1, 45 e. 0, 500 32. Bereken de extinctie als a. T% = 50, 5 b. T = 0, 345 33. Bereken de transmissie in procenten indien a. E = 0, 456 b. E = 0, 0234 31. E = -log(T) => T = 10 -E => T% = T*100 a. b. c. d. e. T = 0, 582 ; T% = 58, 2 % T = 0, 925 ; T% = 92, 5 % T = 0, 103 ; T% = 10, 3 % T = 0, 0355; T% = 3, 55 % T = 0, 316 ; T% = 31, 6 % 32. a. E = -log(0, 505) = 0, 297 b. E = -log(0, 345) = 0, 462 33. a. T = 10 -0, 456 = 0, 350 ; T% = 35, 0 % b. T = 10 -0, 0234 = 0, 948 ; T% = 94, 8 % 15
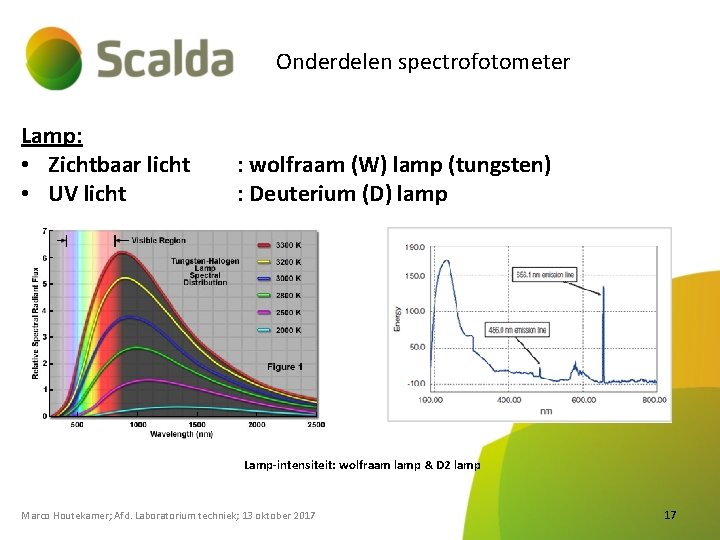
Onderdelen spectrofotometer Lamp: • Zichtbaar licht • UV licht : wolfraam (W) lamp (tungsten) : Deuterium (D) lamp Lamp-intensiteit: wolfraam lamp & D 2 lamp Marco Houtekamer; Afd. Laboratorium techniek; 13 oktober 2017 17
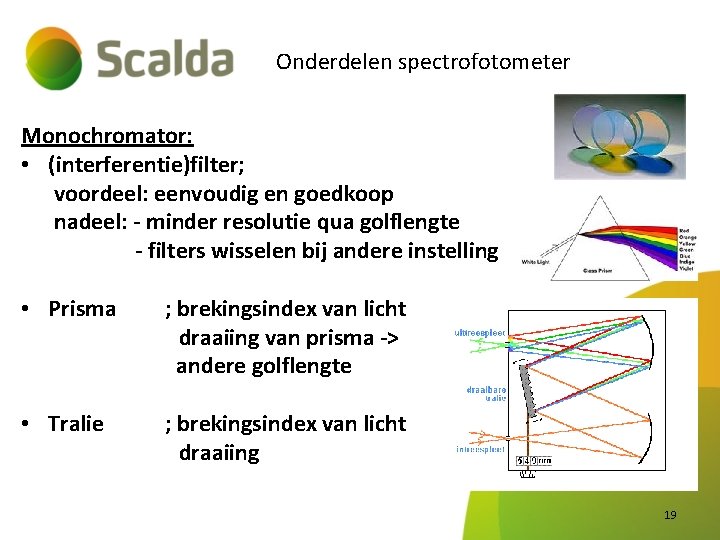
Onderdelen spectrofotometer Monochromator: • (interferentie)filter; voordeel: eenvoudig en goedkoop nadeel: - minder resolutie qua golflengte - filters wisselen bij andere instelling • Prisma ; brekingsindex van licht draaiing van prisma -> andere golflengte • Tralie ; brekingsindex van licht draaiing 19

Onderdelen spectrofotometer Slit: • Intree (entry) slit Regelt de hoeveelheid licht wat op de monochromator valt • Uittree (exit) slit Het afbakenen van het golflengtegebied van het uitgaande licht vanaf de monochromator (0. 1 – 8 nm) 20

Onderdelen spectrofotometer Kuvet: • Quartz; voor UV analyses • Glas of plastic; voor zichtbaar licht • meestal rechthoekig (1*1 cm of 5*1 cm of 10*0, 5 cm) Functie: - Licht doorlaten! Wet van Lambert-Beer! - Kuvet schoon - Geen bubbels of troebeling - Geen interferentie met te meten oplossing - Kuvet ¾ vullen i. v. m. morsen 22

Onderdelen spectrofotometer Detector: doel: intensiteit (I) licht wordt omgezet naar electrisch signaal (S) Eigenschappen: • Zo groot mogelijke gevoeligheid voor groot λ gebied • I rechtevenredig met S • Optimaal meetgebied: E = 0. 2 – 0. 8 Voorbeeld van een detector: • fotomultiplicator (photomultiplier) 23

Oefeningen 19. Waarom maken we gebruik van een monochromator? 19. Voor monochromatisch licht; anders geldt wet L-B niet! 21. tralie, prisma, 21. Geef drie soorten monochromatoren die in interferentiefilter de spectrometrie worden gebruikt. 23. Er worden bij spectrometrie twee soorten spleten gebruikt. a. Met welke spleet kunnen we het doorgelaten golflengtegebied bij een prismamonochromator regelen? b. Wat is de functie van de andere spleet? 23. a. uittrede slit b. Intrede slit; beperking hoeveelheid licht op de monochromator 26
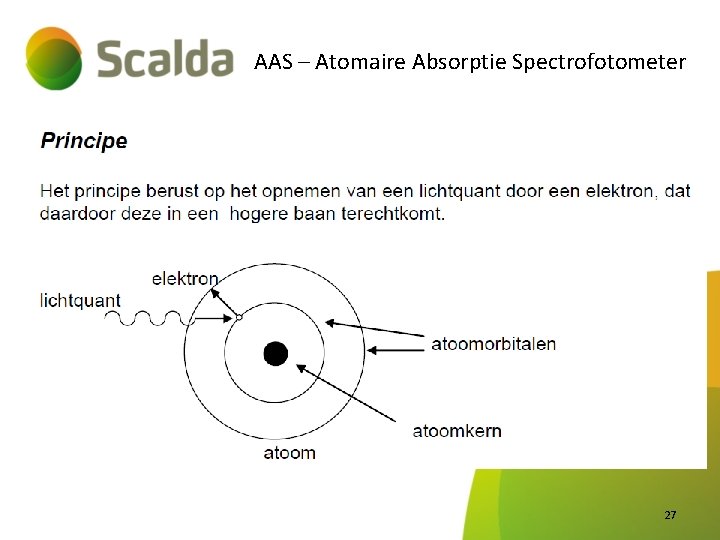
AAS – Atomaire Absorptie Spectrofotometer 27

AAS – Atomaire Absorptie Spectrofotometer 28

AAS – Atomaire Absorptie Spectrofotometer Omdat bandbreedte zo klein is => speciale lamp (HKL) 29
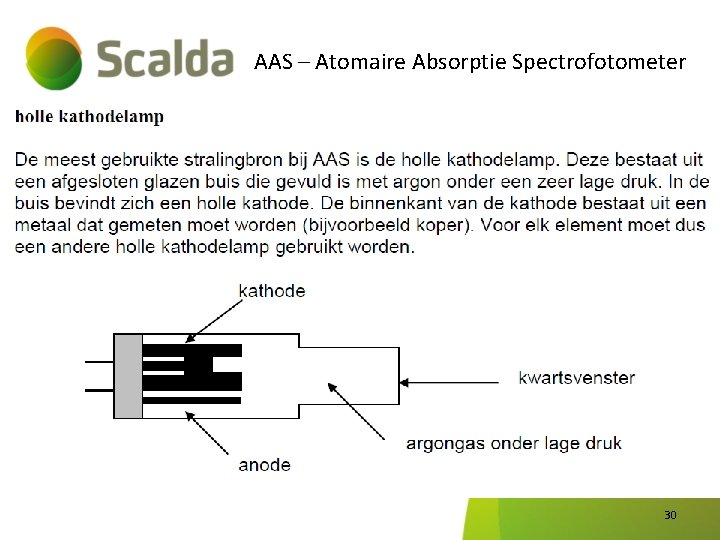
AAS – Atomaire Absorptie Spectrofotometer 30
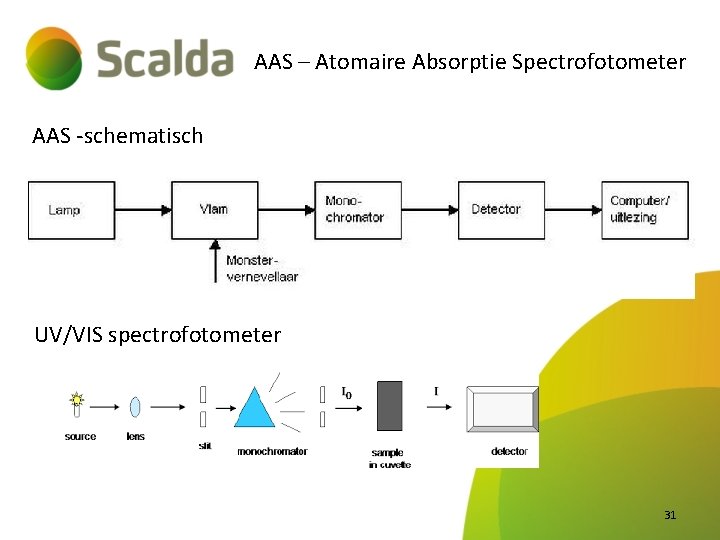
AAS – Atomaire Absorptie Spectrofotometer AAS -schematisch UV/VIS spectrofotometer 31
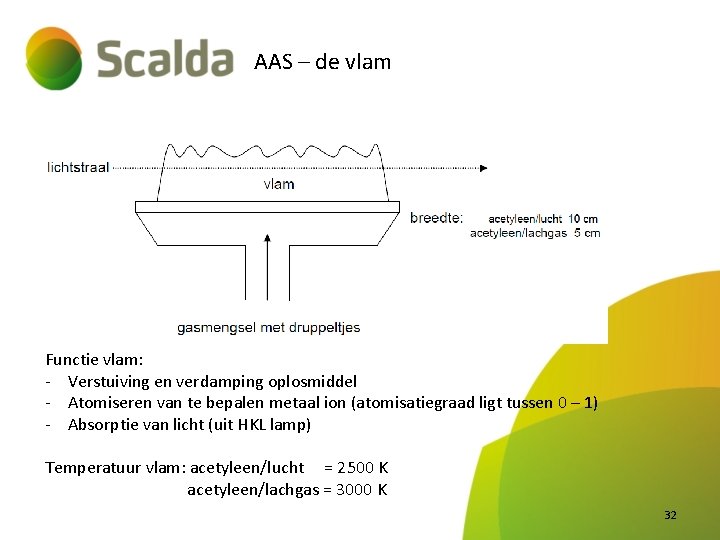
AAS – de vlam Functie vlam: - Verstuiving en verdamping oplosmiddel - Atomiseren van te bepalen metaal ion (atomisatiegraad ligt tussen 0 – 1) - Absorptie van licht (uit HKL lamp) Temperatuur vlam: acetyleen/lucht = 2500 K acetyleen/lachgas = 3000 K 32

AAS – wet van Lambert-Beer! Bij de AAS wordt als detector een fotomultiplier gebruikt. Deze is al bekend uit de moleculaire spectrometrie. De lichtintensiteit wordt gemeten met de oplossing (I) en met oplosmiddel (meestal demiwater), dus zonder absorptie (I 0). Hieruit is de transmissie te berekenen: T = I / I 0 en uit de transmissie de extinctie: E = - log T Volgens de wet Lambert Beer geldt: E = ε · l · c(X) Waarin: E = extinctie ε = molaire extinctie coëfficiënt l = weglengte van het licht door de vlam (dus de grootte van de branderkop) c(X) = molaire concentratie X (X is het atoom in de opgeloste stof) 33

AAS – praktisch 1. “Kookboek” ; details van elk element (bereiding standaarden, golflengte, concentratiegebied, vlam-lucht of lachgas, ) 2. Optimalisatie; lamp en branderkop 3. Matrix-matching; oplosmiddel moet gelijk zijn qua viscositeit, brandbaarheid en oppervlaktespanning 4. Veiligheid; afzuiging i. v. m. mogelijke schadelijke dampen, waterslot, borging branderkop, afvalstoffen in afvalvat 34

AAS – wet van L-B 35
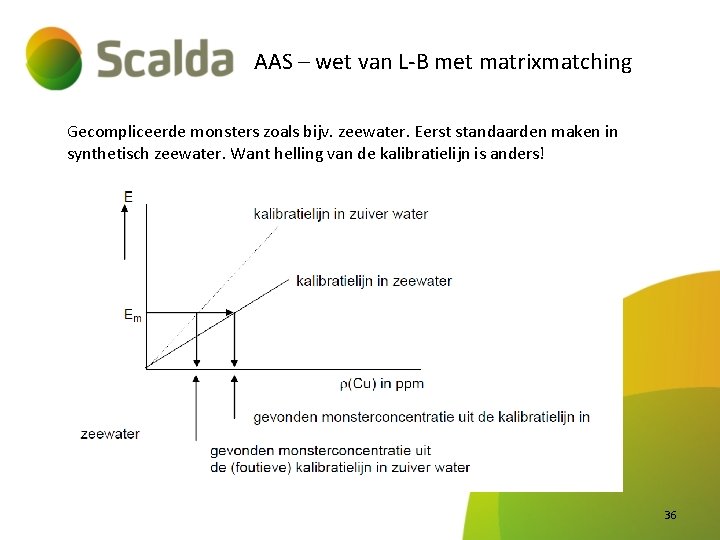
AAS – wet van L-B met matrixmatching Gecompliceerde monsters zoals bijv. zeewater. Eerst standaarden maken in synthetisch zeewater. Want helling van de kalibratielijn is anders! 36
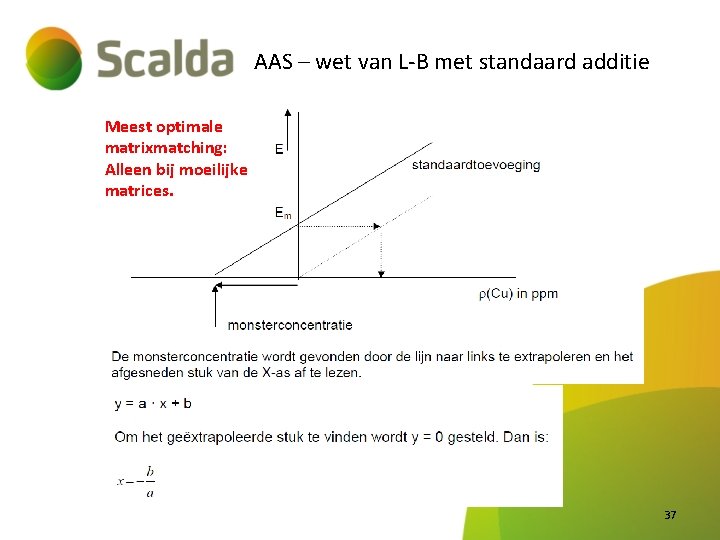
AAS – wet van L-B met standaard additie Meest optimale matrixmatching: Alleen bij moeilijke matrices. 37
- Slides: 32