Spect 2 Apakah Spektroskopi itu Sinar atau gelombang

Spect 2

Apakah Spektroskopi itu Sinar atau gelombang berinteraksi dengan molekul • Sinar X terpancar • Gelombang radio membuat inti beresonansi • Sinar infra merah terserap Spektroskopi • Mengukur intereaksi ini • Membentuk gambaran serapan • Menghubungkan intereakasi dengan struktur Sinar X memberikan panjang dan sudut ikatan. Nmr memberikan gambaran kerangka karbon dan sinar infra merah memberi tahu macam gugus fungsi.
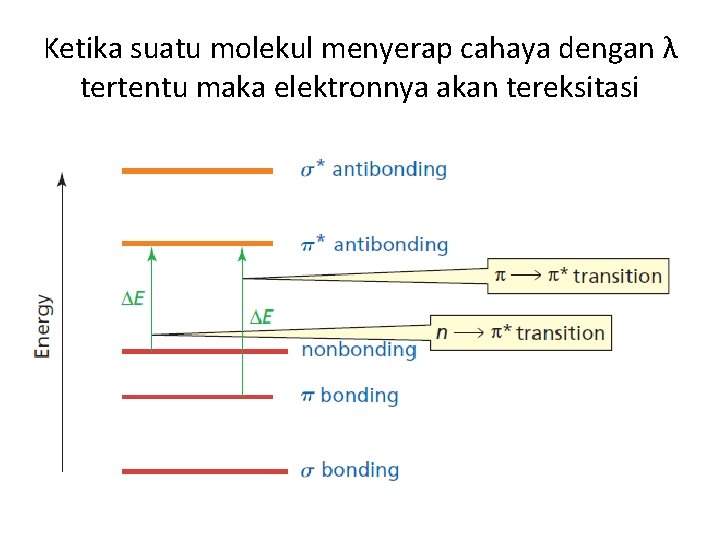
Ketika suatu molekul menyerap cahaya dengan λ tertentu maka elektronnya akan tereksitasi
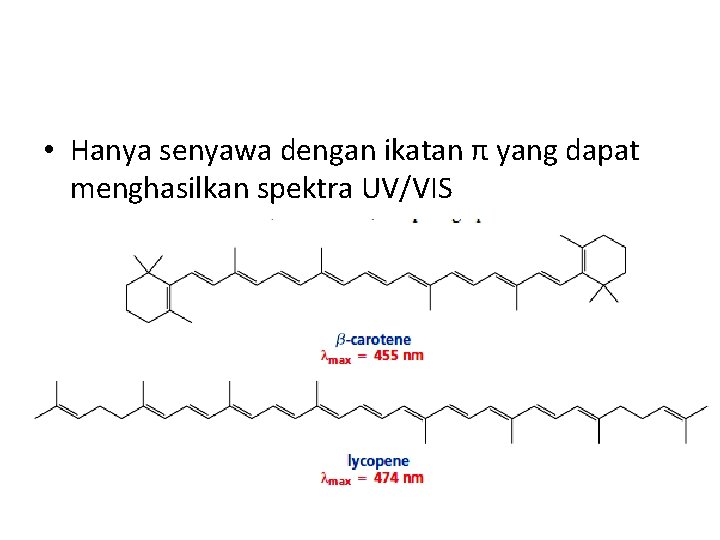
• Hanya senyawa dengan ikatan π yang dapat menghasilkan spektra UV/VIS
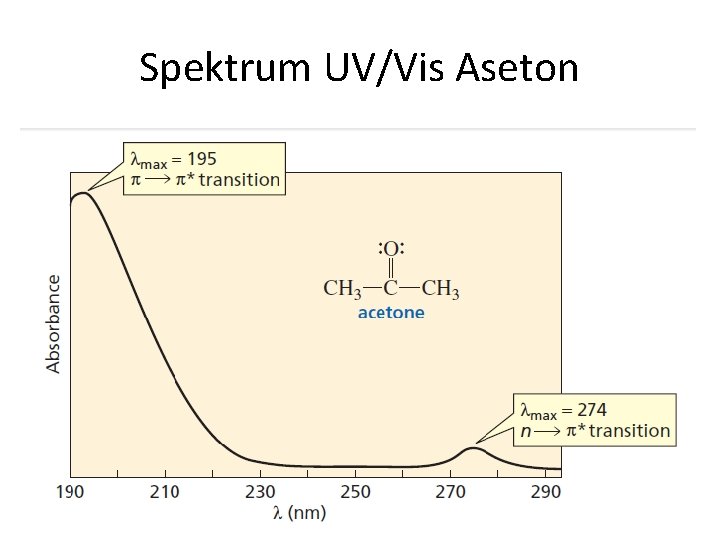
Spektrum UV/Vis Aseton

Warna dan panjang gelombang cahaya yang diserap λ cahaya yang diserap • • • 380 -460 380 -500 440 -560 480 -610 540 -650 380 -420 dan 610 -700 warna teramati • • • kuning oranye merah ungu biru hijau

NMR
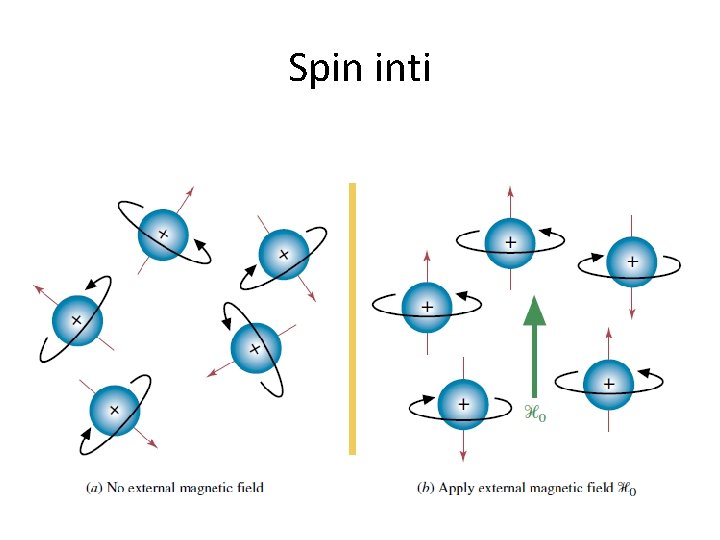
Spin inti
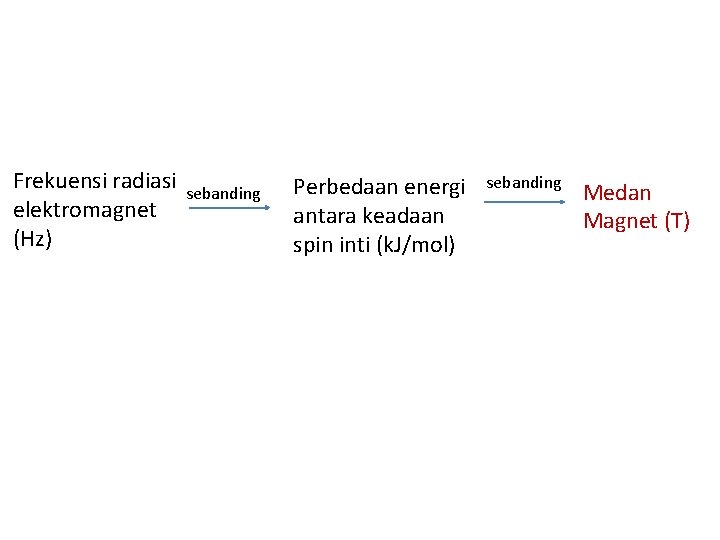
Frekuensi radiasi elektromagnet (Hz) sebanding Perbedaan energi antara keadaan spin inti (k. J/mol) sebanding Medan Magnet (T)
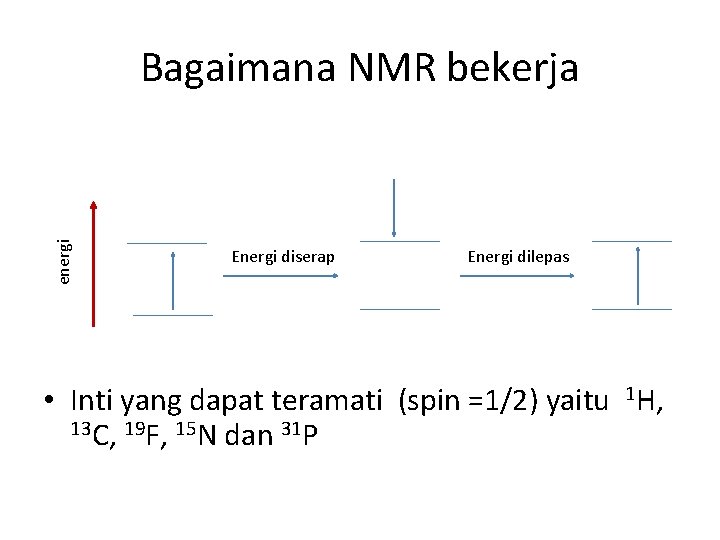
energi Bagaimana NMR bekerja Energi diserap Energi dilepas • Inti yang dapat teramati (spin =1/2) yaitu 1 H, 13 C, 19 F, 15 N dan 31 P

Nmr proton • Pergeseran kimia δ =nilai pergeseran kimia vs = frekuensi sampel v. TMS= frekuensi TMS(tetrametil silan) • Makin besar densitas elektron (σ), makin kecil frekuensinya, makin kecil pula nilai pergeseran kimianya
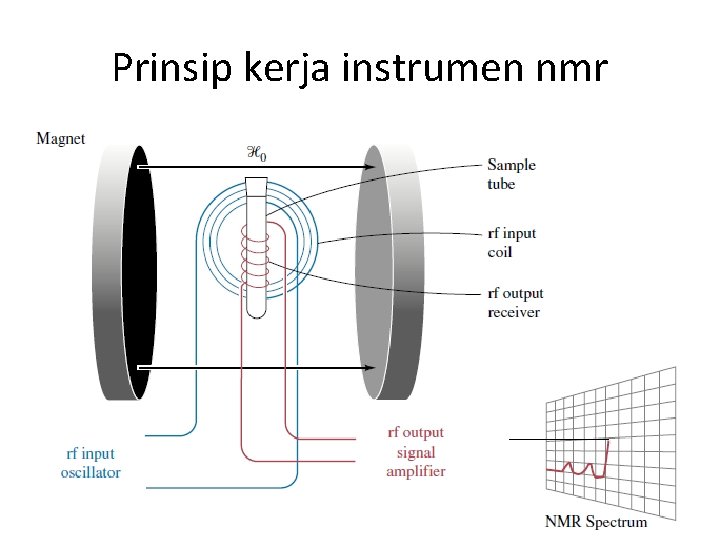
Prinsip kerja instrumen nmr
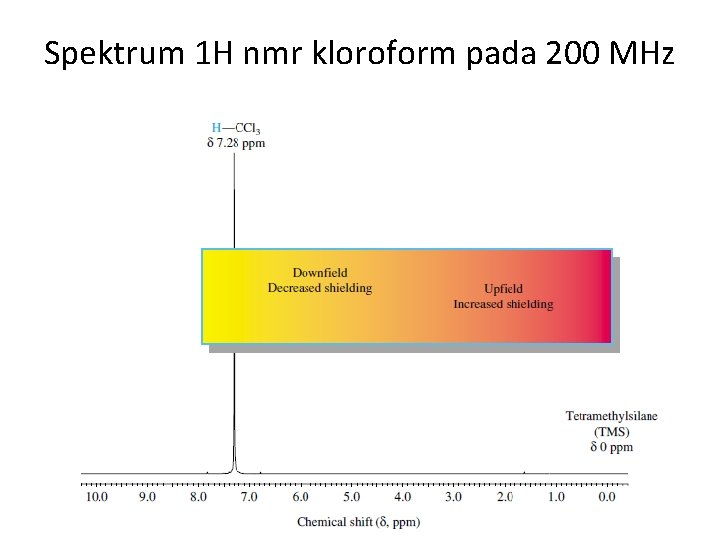
Spektrum 1 H nmr kloroform pada 200 MHz

Faktor yang mempengaruhi nilai δ • Faktor induktif→semakin elektronegatif, semakin downfield • Faktor anisotropik →adanya elektron π dalam ikatan rangkap • Faktor sterik →δCH> δCH 2> δCH 3 • Ikatan hidrogen • Pelarut yang dipakai
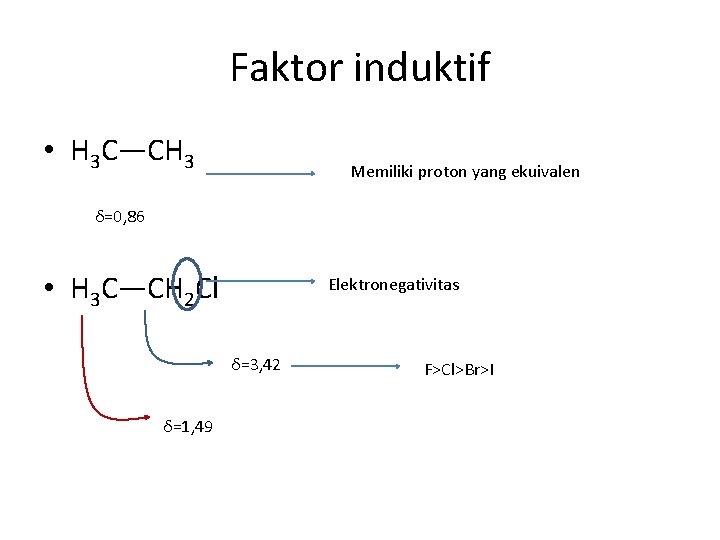
Faktor induktif • H 3 C―CH 3 Memiliki proton yang ekuivalen δ=0, 86 • H 3 C―CH 2 Cl Elektronegativitas δ=3, 42 δ=1, 49 F>Cl>Br>I

Faktor ikatan hidrogen • Pada molekul dengan gugus hidroksi (-OH), amina (NH dan NH 2 ) dan merkaptan (SH) • Pada konsentrasi rendah, ikatan hidrogen lemah, nilai δ rendah • Pada konsentrasi tinggi, ikatan hidrogen kuat, nilai δ tinggi

pelarut • pelarut lebih polar, nilai pergeseran bergeser sedikit lebih besar
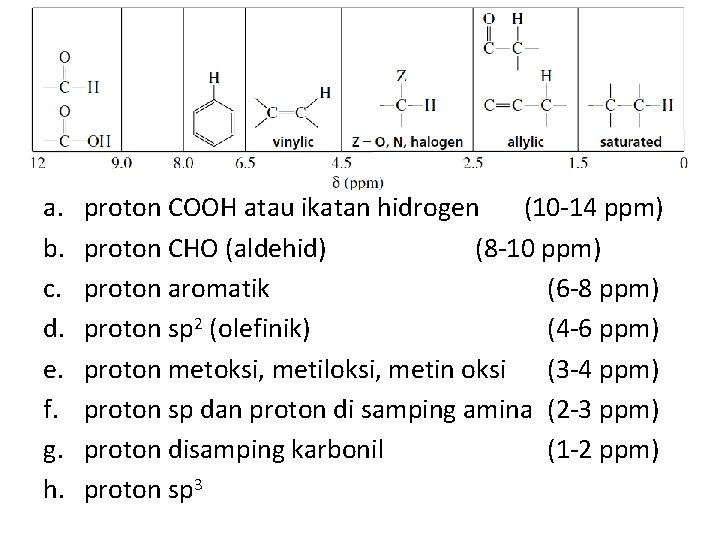
a. b. c. d. e. f. g. h. proton COOH atau ikatan hidrogen (10 -14 ppm) proton CHO (aldehid) (8 -10 ppm) proton aromatik (6 -8 ppm) proton sp 2 (olefinik) (4 -6 ppm) proton metoksi, metiloksi, metin oksi (3 -4 ppm) proton sp dan proton di samping amina (2 -3 ppm) proton disamping karbonil (1 -2 ppm) proton sp 3
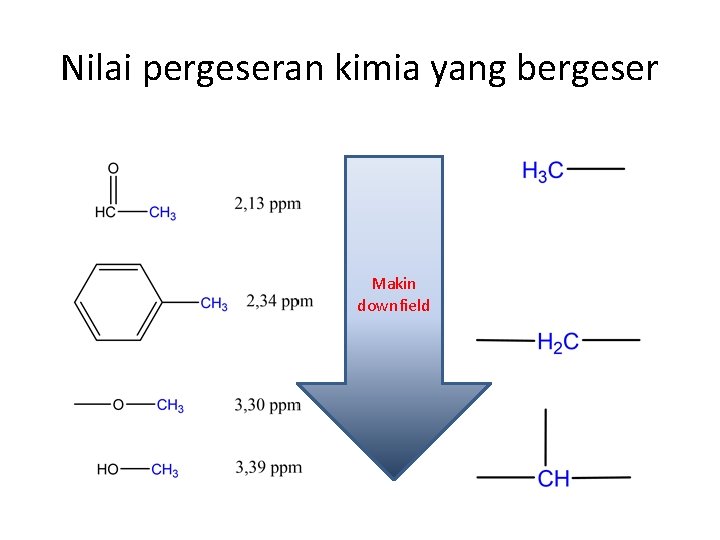
Nilai pergeseran kimia yang bergeser Makin downfield

Kopling Proton-proton • interaksi antara proton-proton yang bertetangga • mengikuti rumus 2 n. I +1 • bila tetangganya tidak ekuivalen (2 n 1 I+1)(2 n 2 I+1)

Segitiga Pascal 1 1: 2: 1 1: 3: 3: 1 1: 4: 6: 4: 1 1: 5: 10: 5: 1 1: 6: 15: 20: 15: 6: 1 1: 7: 21: 35: 21: 7: 1 1: 8: 28: 56: 70: 56: 28: 8: 1 singlet doublet trilplet quartet quintet sextet septet octet nonet

Tipe Proton yang tidak ekuivalen • Tipe proton AX dan AB • Tipe AMX, ABX dan ABC • Tipe Proton A 3 B

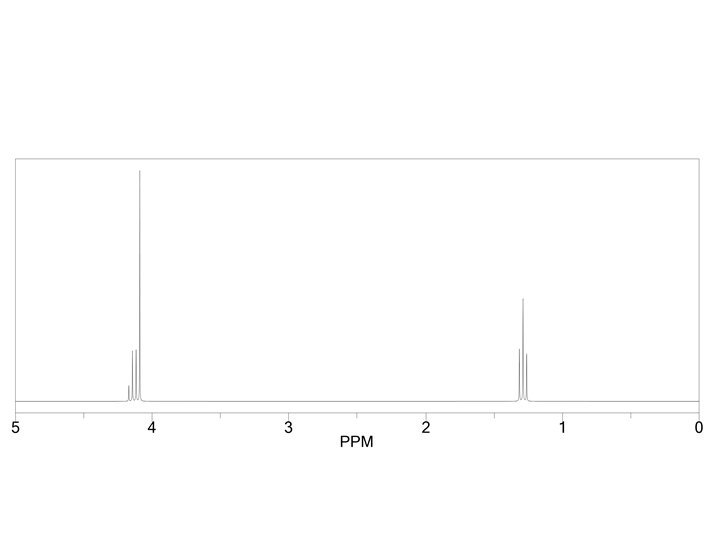
Informasi dari H nmr • • jumlah sinyal →tipe proton Integrasi atau luas area → jml proton Pergeseran kimia (δ) → lingkungan proton Bentuk sinyal → jumlah proton tetanggga
- Slides: 24