SP stavebn a Obchodn akademie Kladno Cyrila Boudy

SPŠ stavební a Obchodní akademie, Kladno, Cyrila Boudy 2954 Chemická vazba II Autor: Mgr. Simona Komárková

SPŠ stavební a Obchodní akademie, Kladno, Cyrila Boudy 2954 Tematický okruh Obecná chemie Anotace Žáci 1. ročníku, obor Ekonomické lyceum, předmět Chemie. Znázornění vzniku chemické vazby v molekulách vodíku, kyslíku, dusíku, vody a methanu. Metodický pokyn Prezentace doplněná výkladem Druh materiálu prezentace Datum tvorby 30. 9. 2013 Číslo materiálu VY_32_INOVACE_Km 1_18 EU peníze školám CZ. 1. 07/1. 5. 00/34. 0154 2

SPŠ stavební a Obchodní akademie, Kladno, Cyrila Boudy 2954 Znázornění vzniku chemické vazby Tvary atomových orbitalů jsou příliš složité, proto se znázorňuje vznik chemické vazby pouze schematicky, pomocí rámečkových diagramů. Vazba v molekule vodíku H 2 Postup: 1/ zapíšeme elektronovou konfiguraci všech atomů v molekule H: 1 s Každý atom vodíku má jeden nespárovaný elektron. Atom vodíku je jednovazný. Vazba vznikne překrytím valenčních orbitalů s nespárovaným elektronem. Elektrony tvořící pár, musí mít opačný spin. Překrytí znázorníme spojením čarou. V molekule vodíku je jednoduchá vazba. Je to vazba σ. EU peníze školám CZ. 1. 07/1. 5. 00/34. 0154 H - H 3

SPŠ stavební a Obchodní akademie, Kladno, Cyrila Boudy 2954 Vznik vazby v molekule kyslíku O 2 O: 1 s 2 p O: 1 s 2 s 2 p Valenční elektrony V molekule kyslíku je dvojná vazba, tvoří ji jedna vazba σ a jedna vazba π. Ve strukturním vzorci se mohou kromě vazebných elektronových párů vyznačit i nevazebné valenční elektronové páry. Ovlivňují prostorové uspořádání molekuly a vlastnosti. Tyto vzorce se nazývají strukturní elektronové vzorce nebo-li Lewisovy vzorce. (Lewis vychází z předpokladu, že vázaný atom je obklopen osmi elektrony, tzv. oktetové pravidlo). EU peníze školám CZ. 1. 07/1. 5. 00/34. 0154 4
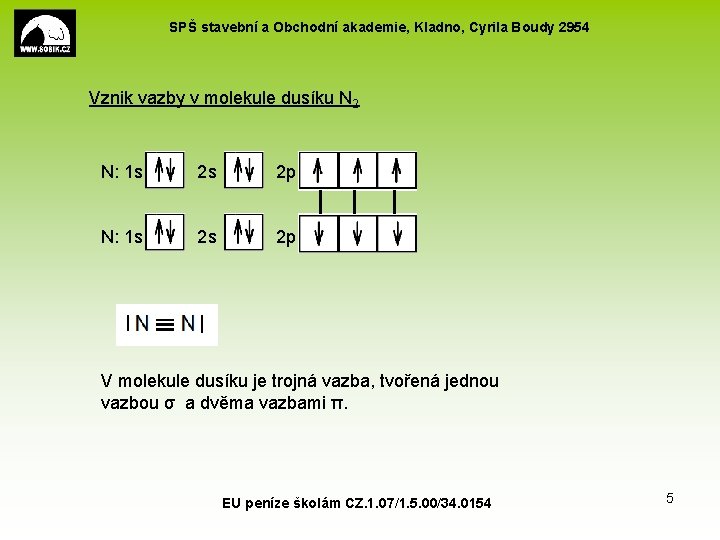
SPŠ stavební a Obchodní akademie, Kladno, Cyrila Boudy 2954 Vznik vazby v molekule dusíku N 2 N: 1 s 2 p N: 1 s 2 p V molekule dusíku je trojná vazba, tvořená jednou vazbou σ a dvěma vazbami π. EU peníze školám CZ. 1. 07/1. 5. 00/34. 0154 5
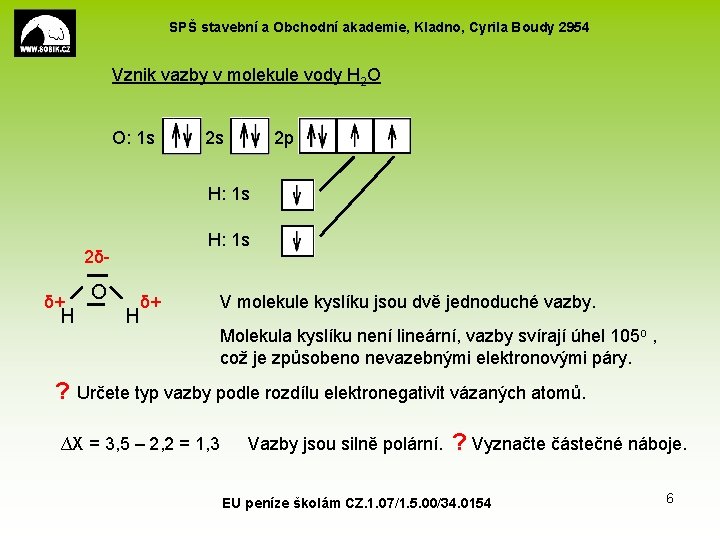
SPŠ stavební a Obchodní akademie, Kladno, Cyrila Boudy 2954 Vznik vazby v molekule vody H 2 O O: 1 s 2 p H: 1 s 2δ O δ+ δ+ H H H: 1 s V molekule kyslíku jsou dvě jednoduché vazby. Molekula kyslíku není lineární, vazby svírají úhel 105 o , což je způsobeno nevazebnými elektronovými páry. ? Určete typ vazby podle rozdílu elektronegativit vázaných atomů. ∆X = 3, 5 – 2, 2 = 1, 3 Vazby jsou silně polární. ? Vyznačte částečné náboje. EU peníze školám CZ. 1. 07/1. 5. 00/34. 0154 6
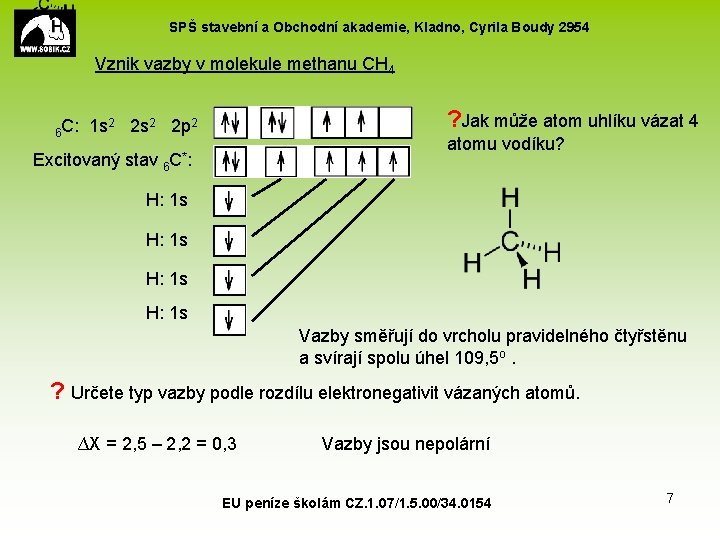
SPŠ stavební a Obchodní akademie, Kladno, Cyrila Boudy 2954 Vznik vazby v molekule methanu CH 4 ? Jak může atom uhlíku vázat 4 6 C: 1 s 2 2 p 2 Excitovaný stav 6 atomu vodíku? C*: H: 1 s Vazby směřují do vrcholu pravidelného čtyřstěnu a svírají spolu úhel 109, 5 o. ? Určete typ vazby podle rozdílu elektronegativit vázaných atomů. ∆X = 2, 5 – 2, 2 = 0, 3 Vazby jsou nepolární EU peníze školám CZ. 1. 07/1. 5. 00/34. 0154 7

SPŠ stavební a Obchodní akademie, Kladno, Cyrila Boudy 2954 Použité zdroje Benešová, M. , Satrapová, H. Odmaturuj z chemie. 1. vydání. Brno: Didaktis 2002. 208 s. ISBN 80 -86285 -56 -1 Blažek, J. , Fabini, J. Chemie pro studijní obory SOŠ a SOU nechemického zaměření. 5. vydání. Praha: SPN, 2005. 336 s. ISBN 80 -7235 -104 -4 Flemr, V. , Dušek, B. Chemie /Obecná a anorganická/ pro gymnázia I. 1. vydání. Praha: SPN, 2001. 120 s. ISBN 80 -7235 -147 -8 Vacík, J. , Barthová, J. , Pacák, J. , Strauch, B. , Svobodová, M. , Zemánek, F. Přehled středoškolské chemie. 1. vydání. Praha: SPN, 1995. 368 s. ISBN 80 -85937 -08 -5 http: //cs. wikipedia. org/wiki/Soubor: Methane-2 D-stereo. svg EU peníze školám CZ. 1. 07/1. 5. 00/34. 0154 8
- Slides: 8