Soojustehnika teoreetilised alused MSJ 0310 5 loeng Vanemteadur


























- Slides: 30


Soojustehnika teoreetilised alused - MSJ 0310 5. loeng Vanemteadur Alar Konist Soojustehnika instituut Hoone U 06, kabinet 136 Ehitajate tee 5, Tallinn, 19086 +372 620 3907 alar. konist@ttu. ee http: //staff. ttu. ee/~akonist/sti/Oppetoo. html

Soojuse mõiste Termodünaamika esimene printsiip on energia jäävuse seadus, millest järeldub siseenergia U kui olekufunktsiooni olemasolu. Kui ainehulk on jääv, siis siseenergia muutus ΔU=ΔQ-ΔW, kus ΔQ on süsteemi sisestatud soojushulk ja ΔW süsteemi tehtud töö. Süsteemi ja väliskeskkonna vahel võib energia vahetus toimuda kahes vormis: tööna ja soojusena: Küsimus on soojuses. Kuidas defineerida seda energia liiki mida nimetame soojuseks?

Olgu meil just keetetud kuum kartul või keedetud muna, mille me veest välja võtame: temperatuur 1000 C Ümbritseva keskkonna temperatuur 200 C Soojus Kartul (muna) jahtub, kuni tema temperatuur saab samaseks ümbritseva keskkonna temperatuuriga. Soojus on energiavorm, mida kandub kehade (süsteemide) vahel nende kehade (süsteemide) temperatuuride erinevuse tõttu. Protsessi ise nimetame soojusülekandeks ehk soojusvahetuseks.

Soojusega palju mõisted: • • keha soojuskadu soojussalvesti erisoojus…. jne ei ole termodünaamikast lähtudes seotud otseselt mõistega soojus, mis on seotud ikka soojusvahetuse ehk ülekandega. • kui süsteem saab väliskeskonnalt soojushulga, siis seda soojushulka nimetatakse positiivseks. • soojushulka, mida süsteem annab väliskeskonnale, loetakse negatiivseks. Soojuse vormis ülekantud energiat nimetame soojushulgaks, mõõteühikuks SI-süsteemis J Soojus ja töö ei ole energia vaid energia ülekande liigid. Ülekandega seotud suurused on protsessifunktsioonid.

Inglise keeles HEAT ja THERMAL ENERGY 2 k. J Thermal energy 2 k. J heat 2 k. J thermal energy Arvutame protsessis soojusülekandena vahetatud soojushulga Q keha massi kohta: siis saame tähistuse q ja tema ühikuks k. J/kg. Seome soojusülekande veel ajaga: Saagu keha, mille mass on 2 kg väliskeskkonnalt soojushulga 30 k. J ja seda 5 sekundi jooksul:

Järelikult: või analüütiliselt: Q=P Δτ (k. J), kus on soojusülekandeks kulunud ajavahemik Δτ=τ2 -τ1 Energiaülekanne soojuse ja töö näol ei ole samaväärne. Töö võib minna otseselt üle ükslõik milliseks energialiigiks, siis soojusena üleantav energia võib muunduda otseselt ainult siseenergiaks.

Ajalugu soojuse teooriast: Tänapäeval põhineb molekulaar-kineetilisel teoorial, kuid 1789 aastal loodi Prantuse keemiku Antoine Lavoisier (1743 -1794) nn. kalori (caloric) teooria. Substants kalor oli massita, värvita, lõhnata, ja ta kandis endas soojust. kui ta läks ainesse, siis aine temperatuur tõusis kui lahkus, siis temperatuur langes. Kriitika osaliseks sai teooria kohe. Benjamin Thompson näiteks näitas juba 1798 aastal soojuse genereerimist hõõrdumisel. James P. Joul purustas kalori teooria 1843 aastal.

Energia ülekanne Soojusülekande liigid Sissejuhatus Soojus võib üle kanduda (levib) kolmel erineval viisil: 1. juhtivuse e nn. soojusjuhtivus 2. konveksioonil 3. kiirgusena e. nn. soojuskiirgus Kui soojus levib samaaegselt mitmel erineval viisil, siis toimub liitsoojusülekanne. • Soojuslevi intensiivsuse määrab kindlaks temperatuuri ruumiline ja ajaline jaotus termodünaamilises süsteemis: t=f(x, y, x, τ) ehk: Kuna soojuse levik toimub termodünaamilise tasakaalu puudumise tingimustes, siis on mingi vaadeldava süsteemi erinevad kehad erineva temperatuuriga, mis ajajooksul võib teatava seaduspärasuse kohaselt muutuda. Seega tuleb temperatuuri vaadelda kui koordinaatidest x, y, z ja ajast τ sõltuvat suurust.

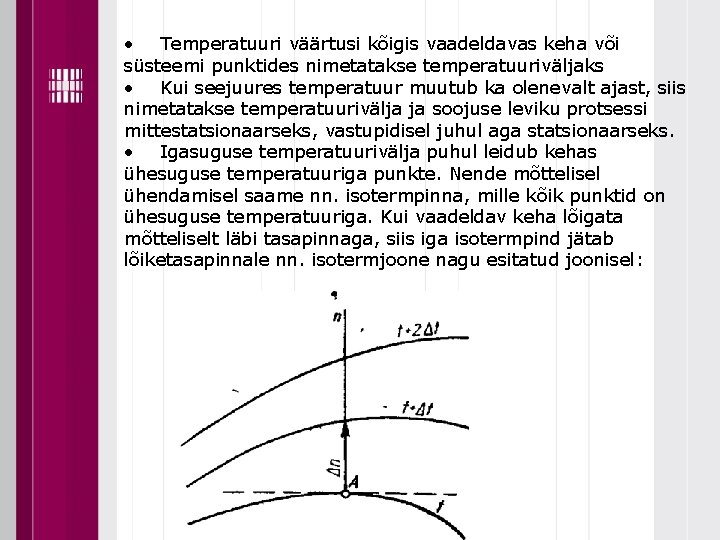
• Temperatuuri väärtusi kõigis vaadeldavas keha või süsteemi punktides nimetatakse temperatuuriväljaks • Kui seejuures temperatuur muutub ka olenevalt ajast, siis nimetatakse temperatuurivälja ja soojuse leviku protsessi mittestatsionaarseks, vastupidisel juhul aga statsionaarseks. • Igasuguse temperatuurivälja puhul leidub kehas ühesuguse temperatuuriga punkte. Nende mõttelisel ühendamisel saame nn. isotermpinna, mille kõik punktid on ühesuguse temperatuuriga. Kui vaadeldav keha lõigata mõtteliselt läbi tasapinnaga, siis iga isotermpind jätab lõiketasapinnale nn. isotermjoone nagu esitatud joonisel:

Temperatuuri muutus kehas oleneb suunast: • Isotermpinnaga (või -joonega) paralleelses suunas temperatuuri muutust ei esine, ristsuunas aga on temperatuuri muutus maksimaalne. • Seetõttu kasutatakse temperatuurivälja iseloomustamiseks lisaks isotermidele ka temperatuuri gradienti. • Temperatuuri gradiendiks mingis keha punktis A (joonisel ) nimetatakse selle punkti juures esineva temperatuuri muutuse ja muutusele vastavate isotermide vahelise ristlõigu Δn pikkuse suhte piirväärtust: Osatuletise märki kasutatakse valemis sellepärast, et temperatuur võib sõltuda ka ajast. • Soojuse levikut iseloomustatakse soojusvooluga energiahulgaga, mis antakse soojusena üle ühes ajaühikus. Tähistasime P, kuid kasutusel rohkem Q, ühik SI-süsteemis W. Soojusvoolu väärtust ühe pinnaühiku kohta nimetatakse soojusvooks ehk soojuskoormuseks ja tähistatakse q, W/m 2

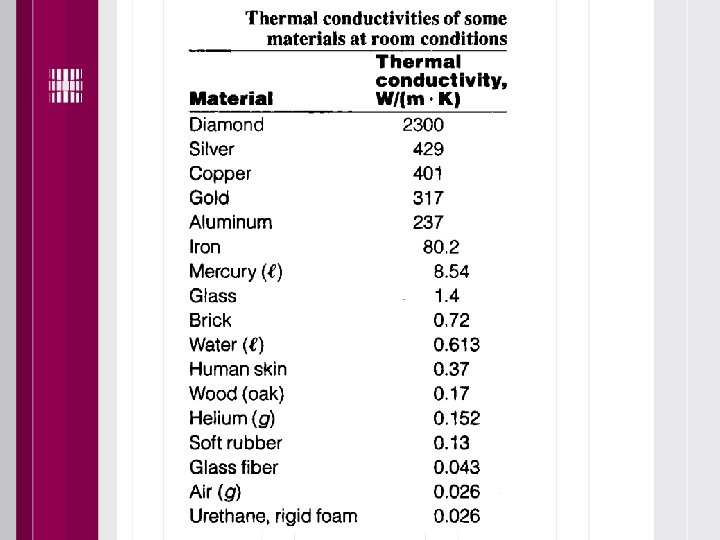
Soojusjuhtivus- Fourier' seadus Soojusjuhtivust iseloomustab soojuse edasiandmine kehas vahetu kontakti kaudu ilma keha osade märgatava liikumiseta või ümberpaiknemiseta. • soojusvoog kehas on võrdeline temperatuuri gradiendiga. Fourier' seadus: q=-λgrad t Kuna soojuse leviku suund on kõrgemalt temperatuurilt madalamale, siis on soojusvoog ja temperatuuri gradient vastupidiste suundadega. Võrdetegurit λ W/(m • deg) nimetatakse soojusjuhtivusteguriks. Soojusjuhtivustegur λ on ainet iseloomustav suurus ja on sõltuv aine omadustest ja olekust. Teoreetiliselt kõige kergemini on soojusjuhtivus käsitletav gaaside puhul. Gaasides on soojust edasikandvateks osakesteks molekulid, mis oma kaootilisel liikumisel ja kokkupõrgetel annavad edasi soojusenergiat kihist kihti.

Seetõttu oleneb gaaside soojusjuhtivustegur molekulide omadustest ja kiirusest. Et aga molekulide kiirus iseloomustab gaasi temperatuuri, siis mõjutab ka temperatuur soojusjuhtivusteguri väärtust. Vedelikkudes on molekulide liikumise iseloom keerulisem. Soojusjuhtivustegur oleneb aga peamiselt samuti vedeliku füüsikalistest omadustest ja temperatuurist. Seejuures on iseloomulik, et gaaside soojusjuhtivustegur temperatuuri tõusuga suureneb, enamikul vedelikel aga väheneb. Näide:

Soojusvoog on arvutatav: (W) kus F on soojusvahetuspind m 2 λ- alumiiniumi soojusjuhtivustegur W/(m. K) ΔT- temperatuuride vahe T 2 -T 1 (K) Δx- alumiiniumpurgi seina paksus m


Entroopia • Entroopia mõiste võttis kasutusele R. Clausius. 1865 a. Entroopia kaudu on otstarbeks analüüsida termodünaamilisi protsesse, anda termodünaamika teisele seadusele üldistatud formuleering jne. • Entroopia mõiste selgitamiseks meenutame, et termodünaamilistest protsessidest osavõttev soojus on protsessifunksioon ega oma täisdiferentsiaali. Soojushulga arvutamiseks termodünaamika esimese seaduse matemaatilisest väljendusest (diff. kujul): dq=du+pdv peame teadma rõhu ja erimahu sõltuvust vaadeldavas protsessis. Matemaatiliselt on võimalik diferentsiaal kaksikliiget du+pdv muuta täisdiferentsiaaliks, kui tema liikmeid korrutata läbi integreerimiskordajaga. Integreerimiskordajaks on absoluutse temperatuuri pöördväärtus. Saame võrrandi:

Avaldis dq/T mida tähistame ds on täisdiferentsiaal. Suurus s nimetame entroopiaks, mille mõõteühikuks on J/(kg K), J/(mool deg). • Entroopia on olekufunktsioon, ning siis tema muutus ringprotsessis on võrdne nulliga ehk • Olekufunktsioonina entroopia on avaldatav näiteks rõhu p ja erimahu v kaudu: ja analoogselt s(T, p) või s(T, v) • Kasutame mõistet entroopia muutus protsessis

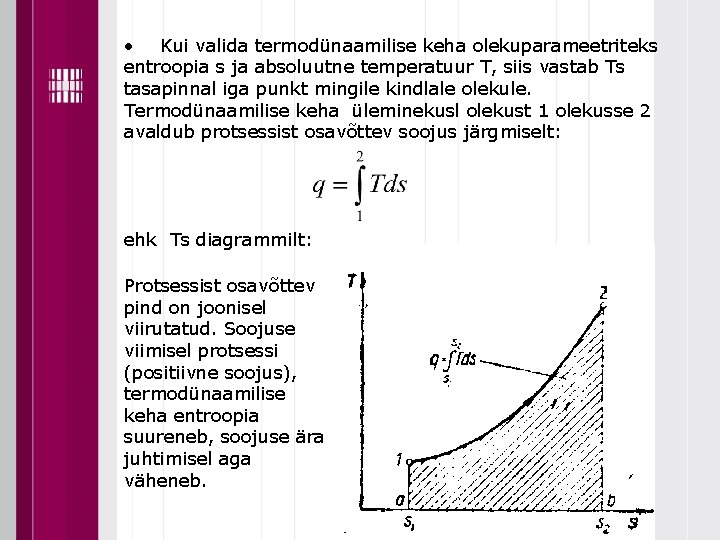
• Kui valida termodünaamilise keha olekuparameetriteks entroopia s ja absoluutne temperatuur T, siis vastab Ts tasapinnal iga punkt mingile kindlale olekule. Termodünaamilise keha üleminekusl olekust 1 olekusse 2 avaldub protsessist osavõttev soojus järgmiselt: ehk Ts diagrammilt: Protsessist osavõttev pind on joonisel viirutatud. Soojuse viimisel protsessi (positiivne soojus), termodünaamilise keha entroopia suureneb, soojuse ära juhtimisel aga väheneb.

Termodünaamiliste protsesside tagastamatus • Kui protsessi saab tagastada algolekusse ilma ühegi soojusliku mõjutuseta siis protsess on tagastatav. Selline protsess on ideaalne • Reaalsed protsessid on tagastamatud ehk seotud entroopia kasvuga kus entroopia on: ds= dq/T Näide: Kolvi liikumine silindris Tagastamatus ainuüksi sellegi pärast, et protsessides (kolvi liikumisel) esineb hõõrdumine pindade vahel. Hõõrdumise ületamiseks on vaja teha mehaanilist tööd, mis muundub soojuseks. Protsessi tagastamatuse määraks on täiendav töö, mis on vajalik süsteemi viimiseks algolekusse. Termodünaamika esimene seadus kehtib ka tagastamatus protsessis, ainult asendame välistöö l uue tähisega l', hõõrdesoojuse q' ja protsessist osavõtva välissoojuse q', hõõrdetöö lh ja hõõrdesoojuse qh siis: dq'+dqh=du+dl'+dlh et dlh=qh siis dq'=du+dl'

Soojus viimine protsessi või sealt ära viimine rikub süsteemi termodünaamilise tasakaalu (esineb temperatuuride vahe) ning muudab protsessid tagastamatuteks Entroopia muutus tagastamatutes protsessides Termodünaamika esimese seaduse väljendatuna kujul: Tds=du+pdv on kehtiv ainult tagastatavates protsessides. Isoleeritud süsteemis toimuvates tagastamatutes protsessides siseenergia u muutus hõõrdumise olemasolul on suurem võrreldes tagastatavatest protsessides samade parameetrite juures, siis peab ka entroopia muutus tagastamatus protsessis olema suurem. Järelikult: dq<Tds ehk saame üldisemalt kirjutada: Võrdus märk tähendab tagastatava protsessi juhtu, võrratuse märk aga tagastamatu protsessi juhul.

Vaatame adiabaatilist protsessi dq=0, siis ka tagastaval protsessil entroopia ei muutu ds=0 ehk s=konstantne. Sellest tulenevalt nimetatakse adiabaatilist protsessi ka isoentroopiliseks Üheks tagastamatu protsessi näiteks on kehadevaheline soojusülekanne. Viimane on võimalik ainult kõrgema temperatuuriga kehalt madalama temperatuuriga kehale. Vastupidi, soojust võib madalama temperatuuriga kehalt üle kanda kõrgema temperatuuriga kehale, tarbides selleks tööd või soojust. Seome soojusülekande nähtuse entroopiaga. Olgu antud väliskeskkonnast adiabaatiliselt isoleeritud kaks erineva temperatuuriga keha, kusjuures esimese keha temperatuur on kõrgem teise keha temperatuurist (T 1>T 2). Esimeselt kehalt teisele kehale üleantud soojushulga d. Q korral muutub esimese keha entroopia d. S 1=(d. Q/T 1) ja teise keha entroopia d. S 2=(d. Q/T 2) võrra. Entroopia muutus tähendatud kahest kehast moodustatud süsteemis võrdub:

Kuna. T 1>T 2, siis d. S>0. Seega süsteemi entroopia suureneb. Vastupidi, kui oleks täidetud tingimus d. S<0, võiks soojus iseenesest üle minna madalama temperatuuriga kehalt kõrgema temperatuuriga kehale. Viimane on aga vastuolus objektiivse loodusseadusega. Avalduv mõte, millega väljendatakse soojuse ülekandumise võimalikkust ainult kõrgema temperatuuriga kehalt madalama temperatuuriga kehale, on termodünaamika teise seaduse sisuks. Temperatuuride T 1 ja T 2 pideval lähenemisel teineteisele soojuslikult isoleeritud süsteemi entroopia suureneb ning saavutab maksimumi kui T 1=T 2 siis ka d. S=0. Soojuslikult isoleeritud süsteemi entroopia vähenemine aga ei ole võimalik, sest sellisel juhul ületaks teise keha temperatuur peale temperatuuride võrdsustumist esimese keha temperatuuri. Järelikult on termilises tasakaalus oleva adiabaatilise termodünaamilise süsteemi entroopia väärtus maksimaalne. Sellises olukorras (S=max) aga kehadevaheline soojuseülekanne puudub.

Ringprotsesside mõiste Masinat, kus toimub soojuse muundamine mehaaniliseks tööks (üldisemal juhul ka mingiks teiseks töö liigiks), nimetatakse soojusjõumasinaks. Selleks et muundada soojust tööks on vaja minimaalselt kahte erineva temperatuuriga keha. Sellises süsteemis olevat kõrgema temperatuuriga keha (T 1) nimetame soojusallikaks ning madalama temperatuuriga keha (T 2) jahutajaks. Soojusjõumasinates muundatakse soojus kasulikuks tööks ringprotsesside vahendusel. Soojusjõumasina katkematu töö tagamiseks lastakse termodünaamilisel kehal algul masinas paisuda ning sellele järgnevail taastatakse komprimeerimisega tema algolek. Kasulikku tööd saadakse ainult siis, kui komprimeerimisel tarbitava töö (lk) absoluutväärtus on väiksem paisumistöö (lp) absoluutväärtusest. Selliseid termodünaamilisi protsesse, kus termodünaamiline keha perioodiliselt paisub ning komprimeerimisprotsessiga taastatakse tema algolek, nimetatakse ringprotsessideks. Ringprotsessid väljenduvad nii pv kui ka Ts-diagrammil kinniste kontuuridena. Soojusjõumasinates esinevad nn. päripidised ringprotsessid (lp>lk), moodustades olekudiagrammidel päripäeva suunatud kontuuri. aluseks.

Alljärgnevalt on esitatud pv ja Ts-diagrammil soojusjõumasinas toimuvad protsessid Ringprotsessi kontuurisisene pindala nii Tsdiagrammil kui ka pvdiagrammil väljendab ringprotsessi kasulikku tööd.

Tagastatavas ringprotsessis tehtud kasuliku töö ja ringprotsessi antud soojushulga suhet nimetatakse ringprotsessi termiliseks kasuteguriks. Ringprotsessi termiline kasutegur: Carnot' ringprotsess Allpool vaadeldav ringprotsess avastati 1824. a. prantsuse inseneri ja õpetlase S. Carnot' poolt. Carnot' ringprotsessil on kõigist võimalikest ringprotsessidest soojusallika ja jahutaja antud temperatuurivahemikus kõrgeim termiline kasutegur. Tagastatava Carnot' ringprotsessi koostisosadeks on kaks isotermilist ja kaks isoentroopilist protsessi. Kujutame Carnot' ringprotsessi nii pv- kui ka Ts-diagrammil.

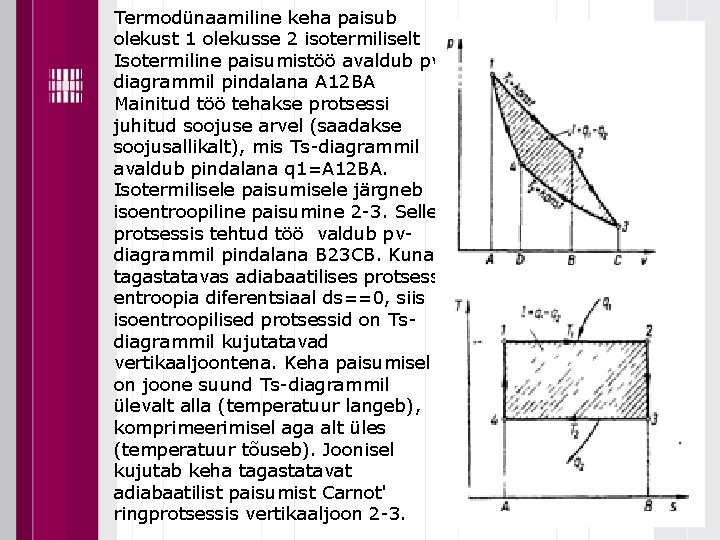
Termodünaamiline keha paisub olekust 1 olekusse 2 isotermiliselt Isotermiline paisumistöö avaldub pvdiagrammil pindalana A 12 BA Mainitud töö tehakse protsessi juhitud soojuse arvel (saadakse soojusallikalt), mis Ts-diagrammil avaldub pindalana q 1=A 12 BA. Isotermilisele paisumisele järgneb isoentroopiline paisumine 2 -3. Selles protsessis tehtud töö valdub pvdiagrammil pindalana B 23 CB. Kuna tagastatavas adiabaatilises protsessis entroopia diferentsiaal ds==0, siis isoentroopilised protsessid on Tsdiagrammil kujutatavad vertikaaljoontena. Keha paisumisel on joone suund Ts-diagrammil ülevalt alla (temperatuur langeb), komprimeerimisel aga alt üles (temperatuur tõuseb). Joonisel kujutab keha tagastatavat adiabaatilist paisumist Carnot' ringprotsessis vertikaaljoon 2 -3.

Termodünaamiline keha tuuakse olekust 3 olekusse 1 kahejärgulise komprimeerimisega, millest esimene (3 -4) toimub isotermiliselt ning teine (4 -1) isoentroopiliselt. Isotermiliseks ja adiabaatiliseks komp-rimeerimiseks tarbitud töö avaldub pv-diagrammil vastavalt pindaladena C 34 DC ja D 41 AD. Isotermilisel komprimeerimisel jahutajale üleantav soojushulk avaldub Ts-diagrammil pindalana q 2=B 34 AB Jooniselt järeldub, et soojusallikalt ringprotsessi antud soojushulk: q 1= ds. T 1 ning ringprotsessist jahutajale üleantud soojushulk q 2= ds. T 2 Carnot' ringprotsessi termiline kasutegur kus T 1 ja T 2 on vastavalt soojusallika ja jahutaja absoluutsed temperatuurid.

Carnot' ringprotsessi termilise kasuteguri avaldisest nähtub, et ta on määratud ainult soojusallika ja jahutaja absoluutse temperatuuri suhtega. Mida suurem on erinevus protsessi maksimaalse ja minimaalse temperatuuri vahel, seda kõrgem on Carnot' ringprotsessi termiline kasutegur ning seda suurem osa soojusallikalt saadavast soojusest q 1 muudetakse ringprotsessis kasulikuks tööks. Soojusallika ja jahutaja temperatuuri muutus mõjub Carnot' ringprotsessi termilisele kasutegurile erinevalt. Soojusallika temperatuuri muutus avaldab Carnot' ringprotsessi termilisele kasutegurile väiksemat mõju kui jahutaja temperatuuri muutus.

Tänan tähelepanu eest!
