SOLUZIONI TITOLATE DI BASI Generalmente si usano gli

SOLUZIONI TITOLATE DI BASI Generalmente si usano gli idrossidi di sodio o di potassio: Na. OH e KOH Non sono sostanze madri perché contengono sempre piccole quantità dei loro carbonati e assorbono velocemente dall’aria CO 2. L’idrossido di sodio è preferito perché il suo carbonato è insolubile nelle soluzioni alcaline concentrate. Preparazione soluzione concentrata di Na. OH Disciogliere 50 g di Na. OH in 50 m. L di acqua distillata, lasciando riposare la soluzione ben protetta dall’aria per almeno 48 -72 ore.

Calcolare il volume di Na. OH concentrata necessario per preparare 1 L di soluzione 0, 1 N circa, usando acqua distillata bollita di fresco e raffreddata. Anche questa soluzione deve essere ben protetta dall’anidride carbonica dell’aria. In pratica Per preparare 1 L di soluzione 0, 1 N di Na. OH peseremo velocemente alla bilancia tecnica 4 g di Na. OH, sciogliendola in 1 L di acqua distillata. La soluzione deve rimanere ben protetta dall’aria.

SOLUZIONI TITOLATE DI ACIDI Generalmente si usano l’acido cloridrico e l’acido solforico: HCl e H 2 SO 4 Non sono sostanze madri quindi occorre preparare soluzioni di concentrazione approssimata da standardizzare con standard a natura basica. Preparazione soluzione 0, 1 N (1 L) di HCl Sapendo che l’acido cloridrico concentrato (37 -38%) è circa 12 N, per calcolare il volume da prelevare per ottenere 1 L di soluzione 0, 1 N basta applicare l’uguaglianza: 12 N x V = 0, 1 N x 1000 V = 8, 33 m. L di HCl conc

Quindi in un cilindro graduato si prelevano 8 -9 m. L di HCl concentrato e si trasfericono in una bottiglia da 1 L contenente 800 m. L circa di acqua distillata; dopo aver agitato bene il volume della soluzione acida verrà portato ad 1 L con acqua distillata. Preparazione soluzione 1 N (1 L) di H 2 SO 4 Sapendo che l’acido solforico concentrato è circa 18 M e quindi 36 N, per calcolare il volume da prelevare per ottenere 1 L di soluzione 1 N basta applicare l’uguaglianza: 36 N x V = 1 N x 1000 V = 27, 7 m. L di H 2 SO 4 conc Quindi in un cilindro graduato si prelevano 28 m. L di acido solforico concentrato e si trasferiscono in una bottiglia da 1 L contenente 800 m. L circa di acqua distillata; dopo aver agitato bene, il volume della soluzione acida verrà portato ad 1 L con acqua distillata.

Calcoli in Analisi Volumetrica Si basano sull’uguaglianza degli equivalenti tra soluzione incognita e soluzione standard. meq = m. L N V AN A = V B N B Per conoscere la quantità in mg di sostanza contenuta in un dato campione basta moltiplicare i meq di titolante consumati per il PE della sostanza in esame (analita). mg analita = meq PEanalita mg analita = m. L(titol) x N(titol) x PE(anal)

Esempio 20, 00 m. L di una soluzione di Na 2 CO 3 neutralizzati con 18, 50 m. L di HCl 0, 1 N. sono stati mg di Na 2 CO 3? 18, 50 x 0, 1 x PE(sodio carbonato) = 18, 50 x 0, 1 x PM/2 18, 50 x 0, 1 x (105, 989/2) = 98, 03 mg % (g/100 m. L)? 98, 03 x 5 = 490, 15 mg in 100 m. L 0, 4901 g/100 m. L N soluzione di sodio carbonato? (18, 50 x 0, 1)/20 = 0, 0925 N Titolo del campione avendo pesato 0, 500 g esatti (0, 4901/0, 500) x 100 = 98, 02%

Standardizzazione delle soluzioni di idrossidi alcalini Acido Ossalico biidrato (COOH)2. 2 H 2 O Potassio Ftalato Acido Benzoico Soluzione standardizzata di HCl (H 2 SO 4) Acido ossalico. 2 H 2 O. PM 126, 065 PE = PM/2 = 63, 03 Sostanza cristallina bianca non igroscopica e non efflorescente; si conserva in essiccatori in presenza di Na. Br (deliquescente). Acido biprotico, indicatore fenolftaleina. Ka 1 = 5, 6 10 -2 Ka 2 = 5, 4 10 -5

Ftalato Acido di Potassio. PM 204, 221 Sostanza incolore e inodore ad elevato grado di purezza e PE molto elevato; uno dei migliori standard che si possa usare. Viene titolato solo il secondo protone per cui è indicata la fenolftaleina. Ka 1 = 1, 1 10 -3 Ka 2 = 3, 9 10 -6 Acido Benzoico. PM 122, 121 Sostanza di colore bianco ad elevato grado di purezza ma poco solubile in acqua; per questo viene sciolto nella minima quantità di etanolo, previamente neutralizzato con lo stesso indicatore con cui viene effettuata la standardizzazione, generalmente la fenolftaleina. Ka = 6, 5 10 -5

Standardizzazione soluz di Na. OH 0, 1 N con acido ossalico biidrato (COOH)2. 2 H 2 O Calcolare la quantità di acido ossalico biidrato (da pesare esattamente) che dovrebbe reagire con 25 m. L di Na. OH 0, 1 N. 25 m. L x 0, 1 x PE (ac ossalico biidrato) = 157, 58 mg = 0, 1576 g Considerando il nostro intervallo teorico: x 0, 8 = 0, 1261 g 0, 1576 x 1, 2 = 0, 1891 g Solubilizzare il solido in 25 m. L circa di acqua distillata, aggiungere 3 -4 gc di fenolftaleina e titolare con la soluzione di Na. OH (eseguire almeno tre titolazioni).

Preparazione (COOH)2. 2 H 2 O soluzione 0, 1 N (100 m. L) di Calcolare la quantità di acido ossalico biidrato necessario a preparare 100, 00 m. L di una soluzione 0, 1 N. 100 x 0, 1 x 63, 033 = 630, 33 mg = 0. 6303 g Considerare l’intervallo 0, 8 -1, 2, effettuare la pesata esatta, trasferire il solido nel matraccio da 100 m. L, aggiungere poca acqua distillata lavando bene l’imbuto e le pareti; solo quando il solido è completamente disciolto portare a volume e agitare fino a soluzione omogenea. La titolazione viene eseguita prelevando esattamente con la pipetta 20, 00 m. L della soluzione così preparata (almeno tre prelievi).

Standardizzazione delle soluzioni di Acidi forti Sodio Carbonato Na 2 CO 3 Potassio Bicarbonato KHCO 3 Borace Na 2 B 4 O 7. 10 H 2 O Ossido di Hg(II) Hg. O Soluzione standardizzata di Na. OH (KOH)

Sodio carbonato. PM 105, 99 PE = PM/2 = 52, 99 Polvere cristallina di colore bianco di PE non molto elevato; base bivalente con Kb 1/Kb 2 > 104, quindi due punti equivalenti. Nessuno dei due punti finali è ben netto a causa del sistema tampone carbonato-bicarbonato-acido carbonico; indicatore per il primo punto è la fenolftaleina mentre per il secondo è il metilarancio (o rosso di metile). Si può scaldare la soluzione ad ogni aggiunta di acido, oppure titolare fino a viraggio, poi riscaldare (il colore cambia nuovamente) e finire la titolazione. Per non incorrere in errori di pesata, generalmente si preferisce preparare una soluzione a titolo noto in matraccio tarato e da questa prelevare delle aliquote. Kb 1 = 2, 1 10 -4 Kb 2 = 2, 2 10 -8

Carbonato acido di potassio. PM 100, 12 Polvere cristallina di colore bianco; base monovalente, indicatore metilarancio. Anche in questo caso si seguono le stesse indicazioni date per il sodio carbonato. Borace. PM 381, 37 PE = PM/2 = 190, 70 Polvere cristallina di colore bianco e di consistenza morbida. Alto PE. Deve essere conservato in recipienti chiusi altrimenti tende a perdere l’acqua di cristallizzazione (sfiorire). In soluzione acquosa si dissocia dando luogo alla reazione: Na 2 B 4 O 7. 10 H 2 O 2 Na+ + 2 H 3 BO 3 + 2 H 2 BO 3 - + 5 H 2 O In pratica si ha la seguente reazione (indicatore rosso di metile): H 2 BO 3 - + H 3 O+ H 3 BO 3 + H 2 O Ka 1 = 5, 8 10 -10

Ossido Mercurico. PM 216, 59 PE = PM/2 = 108, 30 Polvere cristallina di colore rosso o amorfa di colore giallo. PE abbastanza elevato, ma data la tossicità è caduto in disuso. Si ottiene anidro e della purezza desiderata, non è igroscopico e non si altera nel tempo. Il suo uso in aci-alcalimetria è legato alla reazione: Hg. O + H 2 O + 4 I- Hg. I 42 - + 2 OH- In pratica si ha la seguente reazione (qualsiasi indicatore nel range 4 < p. H < 8): OH- + H 3 O+ H 2 O

Standardizzazione di una soluz di HCl 0, 1 N con Na 2 CO 3 Calcolare la quantità di sodio carbonato (da pesare esattamente) che dovrebbe reagire con 25 m. L di HCl 0, 1 N. 25 m. L x 0, 1 x PE (sodio carbonato) = 132, 47 mg = 0, 1325 g Considerando il nostro intervallo teorico: x 0, 8 = 0, 1060 g 0, 1325 x 1, 2 = 0, 1590 g Solubilizzare il solido in 25 m. L circa di acqua distillata, aggiungere 3 -4 gc di metilarancio e titolare con la soluzione di HCl (eseguire almeno tre titolazioni).

Preparazione soluzione 0, 1 N (100 m. L) di Na 2 CO 3 Calcolare la quantità di sodio carbonato necessario a preparare 100, 00 m. L di una soluzione 0, 1 N. 100 x 0, 1 x 52, 99 = 529, 90 mg = 0. 5299 g Considerare l’intervallo 0, 8 -1, 2, effettuare la pesata esatta, trasferire il solido nel matraccio da 100 m. L, aggiungere poca acqua distillata lavando bene l’imbuto e le pareti; solo quando il solido è completamente disciolto portare a volume e agitare fino a soluzione omogenea. La titolazione viene eseguita prelevando esattamente con la pipetta 20, 00 m. L della soluzione così preparata (almeno tre prelievi).

DETERMINAZIONI Acido Citrico Acido organico tricarbossilico, con costanti acide vicine tra loro; quindi non è possibile dosare i tre protoni separatamente, ma vengono PM 192, 1 Ka 1 = 4, 0 10 -4 Ka 2 = 4, 0 10 -5 Ka 3 = 8, 0 10 -6 titolati in blocco con una soluzione standard di Na. OH, indicatore fenolftaleina. PE = PM/3. Quindi avremo che 1 m. L di Na. OH 0, 1 N corrisponde a 0, 006403 g di acido citrico anidro. [0, 1 x (192, 1/3)]/1000 = 0, 006403 g
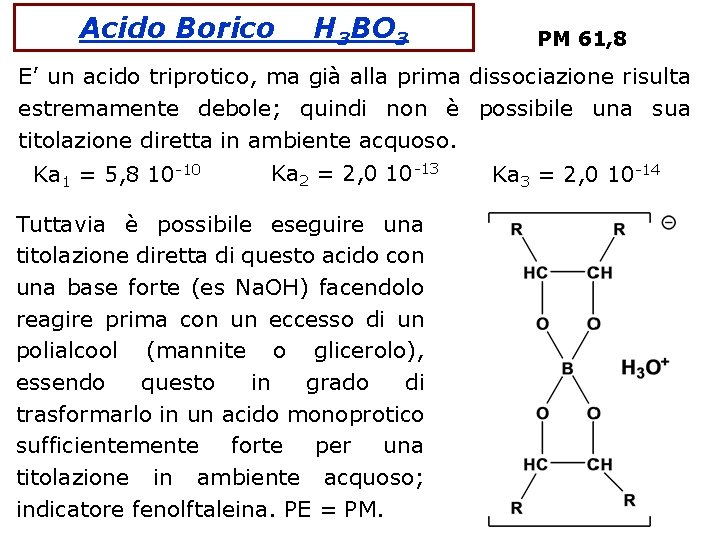
Acido Borico H 3 BO 3 PM 61, 8 E’ un acido triprotico, ma già alla prima dissociazione risulta estremamente debole; quindi non è possibile una sua titolazione diretta in ambiente acquoso. Ka 1 = 5, 8 10 -10 Ka 2 = 2, 0 10 -13 Tuttavia è possibile eseguire una titolazione diretta di questo acido con una base forte (es Na. OH) facendolo reagire prima con un eccesso di un polialcool (mannite o glicerolo), essendo questo in grado di trasformarlo in un acido monoprotico sufficientemente forte per una titolazione in ambiente acquoso; indicatore fenolftaleina. PE = PM. Ka 3 = 2, 0 10 -14

Acido Fosforico H 3 PO 4 PM 97, 99 Anche questo è un acido triprotico con costanti molto lontane tra di loro (rapporto > 104), quindi titolabili separatamente con una base forte. Ka 1 = 7, 1 10 -3 Ka 2 = 1, 7 10 -7 Ka 3 = 4, 2 10 -13 In ambiente acquoso possono essere titolati solo i primi due protoni, quindi PE = PM/2. Il terzo può essere titolato in ambiente non acquoso o per via argentometrica. p. H al 1° punto equivalente nettamente acido (Ka 2 >> Kb 3) p. H al 2° punto equivalente nettamente alcalino (Ka 3 << Kb 2) Indicatori metilarancio e fenolftaleina.
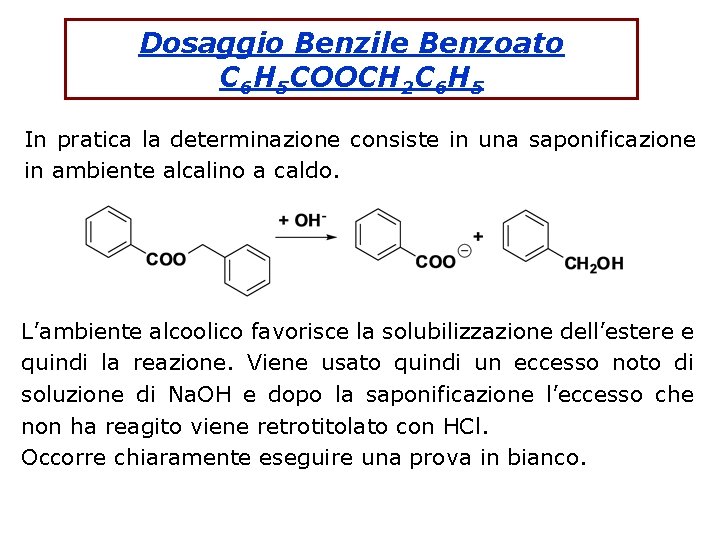
Dosaggio Benzile Benzoato C 6 H 5 COOCH 2 C 6 H 5 In pratica la determinazione consiste in una saponificazione in ambiente alcalino a caldo. L’ambiente alcoolico favorisce la solubilizzazione dell’estere e quindi la reazione. Viene usato quindi un eccesso noto di soluzione di Na. OH e dopo la saponificazione l’eccesso che non ha reagito viene retrotitolato con HCl. Occorre chiaramente eseguire una prova in bianco.

A 2, 0 g circa, esattamente pesati di benzile benzoato si aggiungono 40, 00 m. L di soluzione alcoolica di KOH 0, 5 N e si fa bollire lentamente a ricadere per un’ora. Si raffredda, si diluisce con 20 m. L di acqua e si titola con HCl 0, 5 N, indicatore fenolftaleina. 1 m. L di soluzione alcoolica di KOH 0, 5 N corrisponde a 0, 1061 g di benzile benzoato PM 212, 25. 2, 0375 g di benzile benzoato 40, 00 m. L di KOH fc = 1, 028 20, 95 m. L di HCl fc = 0, 997 40, 00 m. L di KOH fc = 1, 028 40, 15 m. L di HCl fc = 0, 997 (40 x 1, 028)-(20, 95 x 0, 997)=20, 23 m. L di KOH consumati titol. (40 x 1, 028)-(40, 15 x 0, 997)=1, 09 m. L di KOH consumati bianco 20, 23 -1, 09=19, 14 m. L di KOH esattamente 0, 5 N 19, 14 x 0, 1061=2, 0307 g di benzile benzoato (2, 0307/2, 0375)x 100=99, 67% titolo benzoato in esame

Determinazione Benzile benzoato Calcolare la quantità di Benzile benzoato (da pesare esattamente) che dovrebbe reagire con 20 m. L di Na. OH 0, 1 N. Aggiungere 10 -15 m. L di alcool etilico, si aggiungono 40, 00 m. L di Na. OH 0, 1 N facendo bollire la soluzione a ricadere per 60’. Una volta raffreddata la soluzione, si retrotitola l’eccesso di Na. OH con HCl 0, 1 N. Eseguire parallelamente una prova in bianco: Prendere 10 -15 m. L di alcool, aggiungere 40, 00 m. L di Na. OH 0, 1 N e riscaldare per lo stesso tempo. Controllare durante il riscaldamento il livello della soluzione e aggiustare con acqua deionizzata. Una volta raffreddata, aggiungere la fenolftaleina e titolare con HCl 0, 1 N.
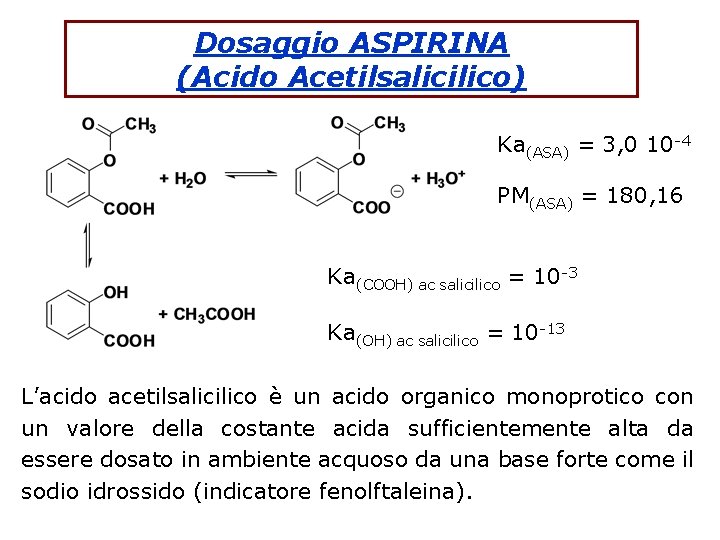
Dosaggio ASPIRINA (Acido Acetilsalicilico) Ka(ASA) = 3, 0 10 -4 PM(ASA) = 180, 16 Ka(COOH) ac salicilico = 10 -3 Ka(OH) ac salicilico = 10 -13 L’acido acetilsalicilico è un acido organico monoprotico con un valore della costante acida sufficientemente alta da essere dosato in ambiente acquoso da una base forte come il sodio idrossido (indicatore fenolftaleina).
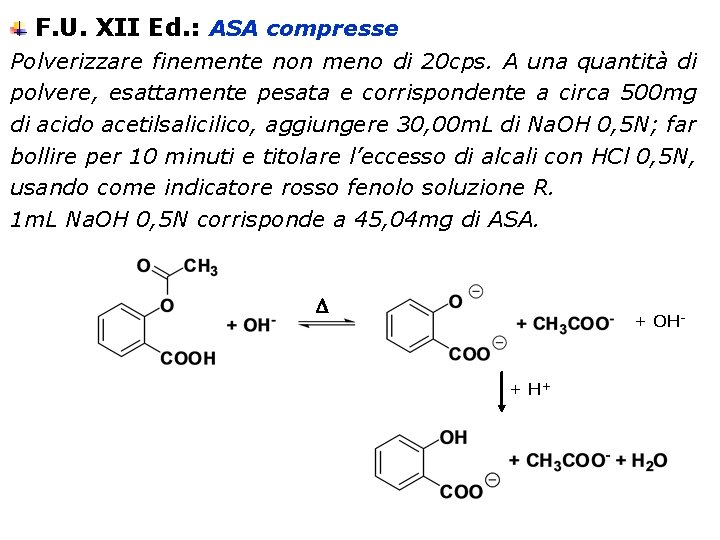
F. U. XII Ed. : ASA compresse Polverizzare finemente non meno di 20 cps. A una quantità di polvere, esattamente pesata e corrispondente a circa 500 mg di acido acetilsalicilico, aggiungere 30, 00 m. L di Na. OH 0, 5 N; far bollire per 10 minuti e titolare l’eccesso di alcali con HCl 0, 5 N, usando come indicatore rosso fenolo soluzione R. 1 m. L Na. OH 0, 5 N corrisponde a 45, 04 mg di ASA. + OH- + H+

Essendo presente nella molecola un gruppo estereo il principio attivo può essere soggetto a idrolisi con formazione di acido salicilico e acido acetico (odore caratteristico). In questo caso, titolando per via diretta con una base forte come Na. OH, sarebbe titolato anche l’eventuale acido acetico formatosi e il corrispondente acido salicilico (p. H punto equivalente sempre basico – fenolftaleina). Titolazione diretta: possibilità di dosare tutte le specie acide (dosaggio completo del carbossile). meq di Na. OH consumati nella titolazione diretta m. L di Na. OH consumati nella titolazione diretta (riportati ad esatta normalità) E’ possibile dosare l’estere sempre in una determinazione acido base in soluzione acquosa, utilizzando un eccesso noto di Na. OH e riscaldando per favorire l’idrolisi dell’acetile.

La soluzione si presenta sempre rossa per la fenolftaleina in ambiente fortemente basico. Dopo 15’ circa, la soluzione viene raffreddata e l’eccesso di Na. OH retrotitolato con HCl (metodica di ritorno). L’indicatore è sempre la fenolftaleina perché al punto equivalente le specie determinanti il p. H sono l’acetato e il salicilato. I meq di Na. OH consumato durante l’idrolisi saranno esattamente uguali ai meq di ASA realmenti presenti nella polvere (purezza del campione di aspirina). meq di Na. OH in eccesso – meq di HCl usati nella retrotitol m. L di Na. OH in eccesso – m. L di HCl usati nella retrotitol (riportati a esatta normalità)
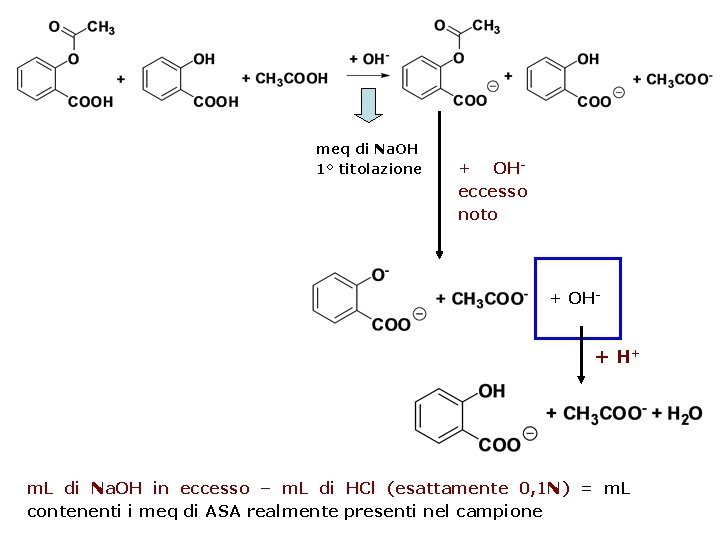
meq di Na. OH 1° titolazione + OHeccesso noto + OH- + H+ m. L di Na. OH in eccesso – m. L di HCl (esattamente 0, 1 N) = m. L contenenti i meq di ASA realmente presenti nel campione

Alla fine si possono presentare due possibilità: m. L Na. OH eccesso (0, 1 N) – m. L HCl (0, 1 N) = m. L Na. OH 1° titolazione (0, 1 N) Allora il campione era costituito da solo acido acetilsalicilico m. L Na. OH eccesso(0, 1 N) – m. L HCl (0, 1 N) ≠ m. L Na. OH 1° titolazione (0, 1 N) Allora il campione iniziale era parzialmente degradato m. L di Na. OH in eccesso – m. L di HCl (esattamente 0, 1 N) = m. L contenenti i meq di ASA realmente presenti nel campione x 0, 1 N x PE (ASA) = mg di ASA nel campione (mg di ASA nel campione/mg di ASA pesati) x 100 = titolo campione di ASA (%)

Osservazioni A. Riscaldamento in ambiente basico per alcale forte: errore carbonato; consumo da parte della CO 2 dell’aria di ioni OHche quindi non vengono retrotitolati dall’HCl. - Proteggere l’ambiente di reazionedall’anidride carbonica dell’aria (refrigerante provvisto di tappo a Ca. O) - Eseguire una prova inbianco nelle stesse condizioni in cui eseguo la titolazione (stessi volumi, stessi reattivi, stessi tempi, stesse temperature) ma in assenza dell’analita. A. Anche l’ossidrile fenolico viene salificato durante l’idrolisi con Na. OH (consumo di base); tuttavia essendo il fenato una base più forte del salicilato e dell’acetato è la prima ad essere retrotitolata (dopo l’ossidrile) con HCl senza che l’idicatore ancora si trovi nella sua zona di viraggio (consumo di idrogenioni).

Determinazione ASA Calcolare la quantità di ASA (da pesare esattamente) che dovrebbe reagire con 20 m. L di Na. OH 0, 1 N. Aggiungere 1015 m. L di alcool etilico, si aggiunge la fenolftaleina e si titola con il sodio idrossido. Alla soluzione neutra proveniente dalla prima titolazione si aggiungono 40, 00 m. L di Na. OH 0, 1 N, facendo bollire la soluzione a ricadere per 15’. Una volta raffreddata la soluzione, si retrotitola l’eccesso di Na. OH con HCl 0, 1 N. Eseguire parallelamente una prova in bianco: Prendere 10 -15 m. L di alcool, aggiungere la fenolftaleina, 40, 00 m. L di Na. OH e riscaldare per lo stesso tempo. Controllare durante il riscaldamento il livello della soluzione e aggiustare con acqua deionizzata. Una volta raffreddata, titolare con HCl 0, 1 N.

COMPLESSOMETRIA Preparazione di una soluzione 0, 05 M (1 L) di EDTA Una soluzione a titolo noto di EDTA può essere preparata a partire o dall’acido libero o dal suo sale bisodico biidrato. H 4 Y, PM = 292, 25 Na 2 H 2 Y. 2 H 2 O, PM = 372, 24 L’acido si trova in commercio con il grado di purezza desiderato e può essere conservato in stufa a 110 °C, per cui si potrebbe preparare una soluzione a titolo noto per pesata diretta. L’unico inconveniente è costituito dalla sua assai scarsa solubilità in acqua per cui occorre aggiungere Na. OH per portarlo in soluzione.

In pratica si pesano esattamente circa 14, 6 g di acido purissimo in un matraccio tarato e si sciolgono in 200 -300 m. L di acqua deionizzata in cui sono stati precedentemente disciolti 9, 0 g di Na. OH. Si agita fino a completa solubilizzazione e poi la soluzione viene portata al volume finale di 1 L con acqua deionizzata. Il sale bisodico, invece, risulta essere più pratico perché solubile in acqua e di purezza tale da poter comunque preparare una soluzione a titolo noto per pesata diretta. Prima di utilizzarlo però, va eliminata l’umidità superficiale, seccandolo in stufa a temperature non superiori a 80 °C (a temperature superiori tende a perdere l’acqua di cristallizzazione). In pratica si pesano esattamente circa 18, 6 g di sale bisodico biidrato in un matraccio tarato e si sciolgono in 200 -300 m. L di acqua deionizzata; solo quando il solido è completamente disciolto si porta al volume del matraccio.

Osservazioni A. L’acqua utilizzata per preparare la soluzione di EDTA dovrebbe essere esente da eventuali cationi per non alterarne il titolo e per non interferire con l’indicatore (anch’esso un chelante) e quindi con l’individuazione del punto finale (eventuale errore nella titolazione). A. Le soluzioni di EDTA se non sono utilizzate appena preparate vanno trasferite in un contenitore di plastica, perché nel tempo l’EDTA interagisce con il vetro sottraendo cationi (diminuizione del titolo e degradazione della vetreria volumetrica).

Controllo del titolo della soluzione 0, 05 N di Na 2 H 2 Y. 2 H 2 O Si pesano esattamente circa 0, 125 g di Ca. CO 3 (PM = 100, 087) puro per analisi, si sciolgono aggiungendo cautamente (goccia a goccia per evitare la forte effervescenza) 10 m. L di HCl 1 N e si riscalda per allontanare l’anidride carbonica. La soluzione viene quindi neutralizzata con NH 3 1 N e quindi addizionata di 20 m. L di tampone ammoniacale a p. H = 10. A questo punto occorre aggiungere un’opportuna quantità di complesso Mg[EDTA]2 - per poi titolare con la soluzione di EDTA, indicatore NET con viraggio dal rosso al blu. L’indicatore può essere addizionato o sotto forma di soluzione alcoolica (0, 5%, 4 -5 gc) che però si degrada rapidamente e quindi va preparata di fresco o solido, diluito 1: 99 con sodio cloruro.

Questa stessa metodica può essere applicata alla determinazione della percentuale di Calcio in un carbonato o in un altro suo sale. In questo caso la % di Ca 2+ nel carbonato, per esempio, sarà data da: % Ca = m. LEDTA x NEDTA x PACa x 100 mg Ca. CO 3 pesati

DETERMINAZIONI VOLUMETRICA di Ca 2+ e Mg 2+ con EDTA Nelle acque naturali In un campione di Ca. Mg(CO 3)2 (dolomite) In una polvere costituita ad es da Ca. CO 3 e Mg. Cl 2

Determinazione Ca 2+ e Mg 2+ nelle acque naturali La DUREZZA di un’acqua esprime un indice di QUALITA’ sia per scopi civili sia industriali: -precipitazione di saponi e detergenti come Sali di Ca/Mg dei rispettivi acidi grassi: Ca 2+ + RCOO- (RPO 42 -) -calcolosi renali Ca(RCOO)2 (RPO 4 Ca) Ca. C 2 O 4 -formazione di Sali insolubili (Ca. CO 3) trasferimento di calore (barriera termica) Ca 2+ + 2 HCO 3 - pregiudica CO 2 + H 2 O + Ca. CO 3 il
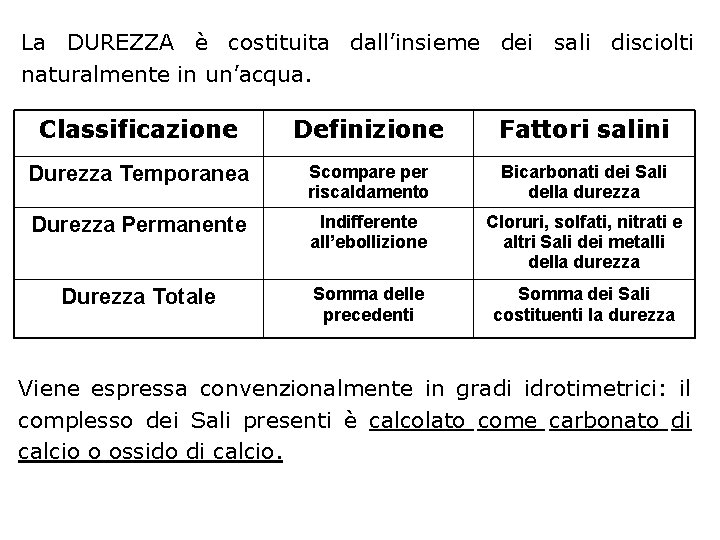
La DUREZZA è costituita dall’insieme dei sali disciolti naturalmente in un’acqua. Classificazione Definizione Fattori salini Durezza Temporanea Scompare per riscaldamento Bicarbonati dei Sali della durezza Durezza Permanente Indifferente all’ebollizione Cloruri, solfati, nitrati e altri Sali dei metalli della durezza Durezza Totale Somma delle precedenti Somma dei Sali costituenti la durezza Viene espressa convenzionalmente in gradi idrotimetrici: il complesso dei Sali presenti è calcolato come carbonato di calcio o ossido di calcio.
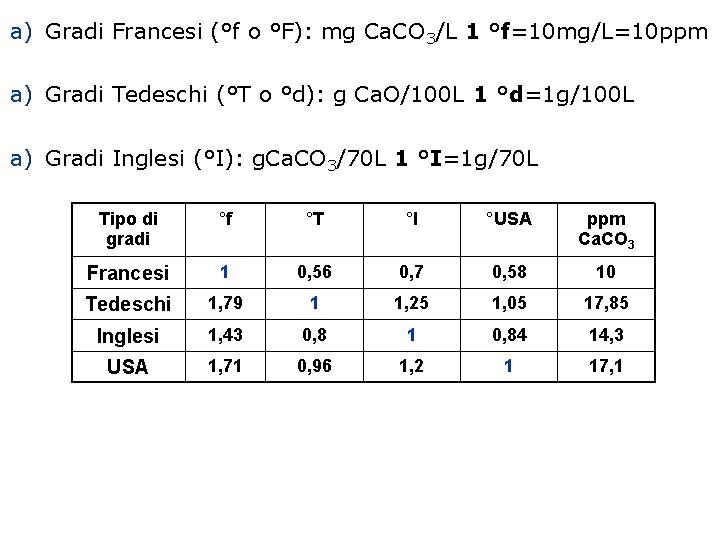
a) Gradi Francesi (°f o °F): mg Ca. CO 3/L 1 °f=10 mg/L=10 ppm a) Gradi Tedeschi (°T o °d): g Ca. O/100 L 1 °d=1 g/100 L a) Gradi Inglesi (°I): g. Ca. CO 3/70 L 1 °I=1 g/70 L Tipo di gradi °f °T °I °USA ppm Ca. CO 3 Francesi 1 0, 56 0, 7 0, 58 10 Tedeschi 1, 79 1 1, 25 1, 05 17, 85 Inglesi 1, 43 0, 8 1 0, 84 14, 3 USA 1, 71 0, 96 1, 2 1 17, 1
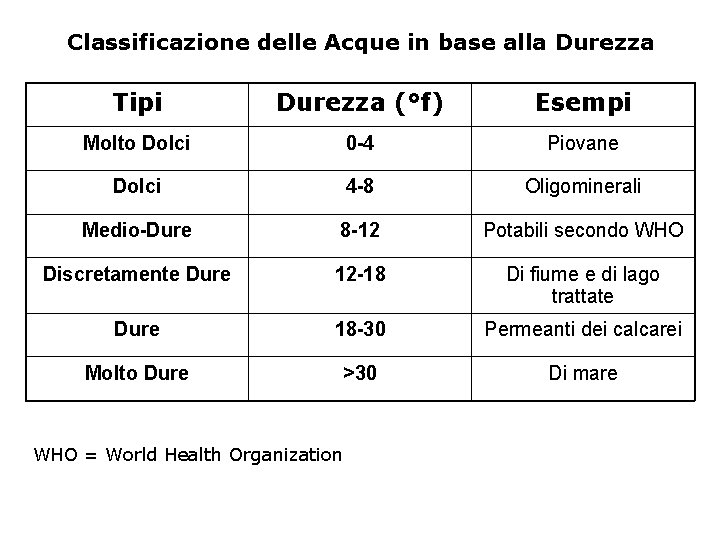
Classificazione delle Acque in base alla Durezza Tipi Durezza (°f) Esempi Molto Dolci 0 -4 Piovane Dolci 4 -8 Oligominerali Medio-Dure 8 -12 Potabili secondo WHO Discretamente Dure 12 -18 Di fiume e di lago trattate Dure 18 -30 Permeanti dei calcarei Molto Dure >30 Di mare WHO = World Health Organization

In pratica: Ca 2+ e Mg 2+ nelle acque Prelevare esattamente un campione di acqua del rubinetto (o 1, 000 m. L di acqua di mare e diluire a 50 m. L con acqua deionizzata), aggiungere 20 m. L di tampone ammoniacale a p. H=10, aggiungere l’indicatore NET (qualche cristallo) e titolare con la soluzione di EDTA fino a viraggio persistente da rosso vino a blu. Determinazione solo ione Ca 2+: prelevare esattamente la stessa quantità di acqua del rubinetto (o acqua di mare, come sopra), aggiungere KOH (o Na. OH) fino a neutralità e poi 1 m. L di KOH (o Na. OH) 2 N aspettando qualche minuto la precipitazione dell’idrossido di Mg (che può non essere visibile); aggiungere Muresside (o idrossinaftolo) come indicatore e titolare con la soluzione di EDTA fino a viraggio violaceo/blu. Se lasciando riposare il colore vira nuovamente aggiungere altro titolante. Dalla differenza tra i m. L di soluzione di EDTA della prima titolazione e quelli della seconda si ricavano i m. L di EDTA necessari a titolare il solo Mg (azione mascherante dello ione OH -).

In pratica: Ca 2+ e Mg 2+ campione Ca. Mg(CO 3)2 -Macinare finemente il campione in mortaio -Pesare esattamente (0, 1 mg) circa 100 mg di campione macinato, trasferendolo in un becker -Aggiungere 10 -15 m. L di HCl 3 N e lasciare reagire per 1015’, allontanando la CO 2 -Filtrare per eliminare eventuali residui solidi (silicati, ecc), raccogliendo il filtrato in un matraccio da 100. -Portare a volume il filtrato con acqua deionizzata -Prelevare esattamente 20, 00 m. L dal matraccio e trasferirli nella beuta, neutralizzare con NH 3, aggiungere 20 m. L di tampone ammoniacale (controllo del p. H), il NET e titolare con la soluzione di EDTA -Ripetere la titolazione tre volte (minimo)

In pratica: Ca 2+ e Mg 2+ campione Ca(CO 3)2/Mg. Cl 2 6 H 2 O/Na. Cl Si può avere una soluzione già pronta da cui vengono prelevati esattamente 20, 00 m. L oppure dovremo pesare la quantità di campione da titolare con 20 -25 m. L di EDTA 0, 1 M (0, 05 M) e poi scioglierlo cautamente con HCl 2 N allontanando la CO 2. PM Ca. CO 3=100, 09 PM Mg. Cl 2 6 H 2 O=203, 296 Sale di PM medio=(100, 9+203, 296)/2=151, 69 Risultato può essere espresso come mg/100 m. L (mg/L) o come p/p (%).
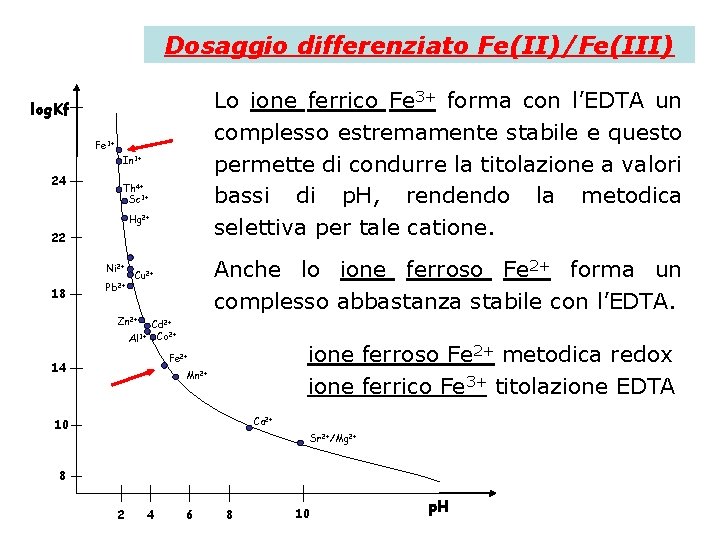
Dosaggio differenziato Fe(II)/Fe(III) Lo ione ferrico Fe 3+ forma con l’EDTA un complesso estremamente stabile e questo permette di condurre la titolazione a valori bassi di p. H, rendendo la metodica selettiva per tale catione. log. Kf Fe 3+ In 3+ 24 Th 4+ Sc 3+ Hg 2+ 22 Ni 2+ 18 Pb 2+ Anche lo ione ferroso Fe 2+ forma un complesso abbastanza stabile con l’EDTA. Cu 2+ Zn 2+ Al 3+ Cd 2+ Co 2+ ione ferroso Fe 2+ metodica redox ione ferrico Fe 3+ titolazione EDTA Fe 2+ 14 Mn 2+ Ca 2+ 10 Sr 2+/Mg 2+ 8 2 4 6 8 10 p. H
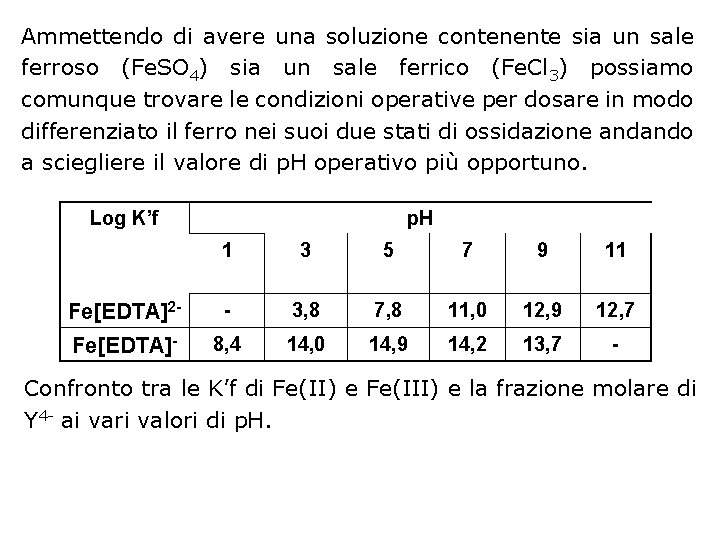
Ammettendo di avere una soluzione contenente sia un sale ferroso (Fe. SO 4) sia un sale ferrico (Fe. Cl 3) possiamo comunque trovare le condizioni operative per dosare in modo differenziato il ferro nei suoi due stati di ossidazione andando a sciegliere il valore di p. H operativo più opportuno. Log K’f p. H 1 3 5 7 9 11 Fe[EDTA]2 - - 3, 8 7, 8 11, 0 12, 9 12, 7 Fe[EDTA]- 8, 4 14, 0 14, 9 14, 2 13, 7 - Confronto tra le K’f di Fe(II) e Fe(III) e la frazione molare di Y 4 - ai vari valori di p. H.

p. H = 1 A questo valore di p. H l’EDTA si trova principalmente nelle forme H 5 Y+ e H 4 Y, lo ione Fe(III) riesce come acido di Lewis a spostare il protone e a formare il complesso in modo quantitativo. p. H = 3 Lo ione Fe(III) può essere dosato ancora in modo quantitativo in presenza di ione Fe(II) perché la K’f dello ione ferroso è estremamente bassa (<<<108). p. H = 5 È sempre possibile un dosaggio quantitativo dello ione ferrico in presenza di ione ferroso perché, pur cominciando ad essere stabile il complesso dell’EDTA con lo ione Fe(II) (K’f circa 8), il complesso che forma con lo ione Fe(III) è estremamente più stabile (K’f circa 15, rapporto tra le K’f = 107).

Fe(III) forma un idrossido Fe(OH)3 poco solubile Kps ~ 10 -36 E’ possibile che a p. H=5 la precipitazione dell’idrossido interferisca con la formazione del complesso? 1) Trovare la [Fe 3+] che a p. H 5 soddisfa il Kps p. H = 5 [OH-] = 10 -9 Kps = [Fe 3+][OH-]3 [Fe 3+] = 10 -36/(10 -9)3 = 10 -36/10 -27 = 10 -9 1) Trovare se la [Fe 3+] che rimane libera in soluzione , a p. H 5 finita la titolazione, soddisfa il Kps [[Fe. EDTA]-] = 10 -2 [Fe 3+]=[EDTA]=X K’f=1015=10 -2/x 2 x=(10 -2/1015)-2 ~ 10 -7/10 -8 > 10 -9 La titolazione viene condotta a p. H=3

In pratica: Prelevare esattamente 20, 00 m. L di soluzione di Fe. Cl 3 e Fe. SO 4 (Fe. Cl 3) acida per acido solforico. Aggiungere CH 3 COONa fino a p. H=3 (notare il cambiamento di colore da incolore a giallino tenue), aggiungere l’indicatore e titolare con EDTA standard.

Determinazione di Zn 2+ secondo F. U. I. P. A. = 65, 39 Pesare esattamente la quantità di campione necessaria a reagire con 20/25 m. L di EDTA 0, 05 M, scioglierli in 5 m. L di acido acetico diluito e aggiungere 50 -60 m. L di acqua deionizzata; la soluzione viene addizionata di arancioxilenolo miscela composta e esamina (esametilentetrammina) fino a colorazione rosa-violetto, poi 2 g di esamina in eccesso. Si titola con EDTA 0, 05 M fino a viraggio dal rosa-violetto al giallo. 1 m. L di sodio edetato 0, 1 M corrisponde a 6, 540 mg di Zn.

Determinazione di Mg 2+ secondo F. U. I. P. A. = 24, 305 Pesare esattamente la quantità di campione necessaria a reagire con 20/25 m. L di EDTA 0, 05 M, scioglierli in 50 -60 m. L di acqua deionizzata; aggiungere 10 m. L di soluzione tampone ammoniacale a p. H=10 e 50 mg di nero mordente 11 miscela composta. Si titola con EDTA 0, 05 M fino a viraggio dal violetto al blu. 1 m. L di sodio edetato 0, 1 M corrisponde a 2, 431 mg di Mg.

Determinazione di Bi 3+ secondo F. U. I. P. A. = 208, 98 In una beuta da 500 m. L si pone la soluzione nitrica indicata, si completa a 250 m. L con acqua deionizzata e si aggiunge goccia a goccia sotto agitazione ammoniaca fino a opalescenza incipiente e poi 0, 5 m. L di acido nitrico. Si scalda a 70 °C fino a che la soluzione ritorna limpida. Si aggiungono 50 mg circa di arancio-xilenolo miscela composta e si titola lentamente con sodio edetato 0, 1 M fino al viraggio dal violetto-rosa al giallo. 1 m. L di sodio edetato 0, 1 M corrisponde a 20, 90 mg di Bi.

TITOLAZIONI REDOX Permanganatometria KMn. O 4 PM 158, 04 Il permanganato di potassio non è uno standard primario perché è difficile ottenerlo allo stato puro, specialmente esente da Mn. O 2, per cui non è possibile prepararne una soluzione a titolo noto per pesata diretta. Anche la stessa acqua deionizzata può contenere tracce di sostanze in grado di ridurre il permanganato a Mn. O 2 (reazione in ambiente neutro). Lo stesso biossido catalizza la reazione di ossidazione dell’acqua.

Preparazione di una soluz di KMn. O 4 0, 1 N Si pesano, quindi, circa 3, 2 g di KMn. O 4 e si sciolgono in 1 L di acqua deionizzata. La soluzione così ottenuta viene bollita per 30 -40 minuti, oppure lasciata a riposo per alcuni giorni, in modo da ossidare tutte le specie riducenti eventualmente presenti. Quindi si filtra con gooch o imbuto e lana di vetro (no filtro di carta) in modo da allontanare l’eventuale biossido formatosi. La soluzione così preparata se mantenuta ben chiusa e al riparo dalla luce si conserva per un periodo di tempo sufficientemente lungo.

Standardizzazione di una soluz di KMn. O 4 0, 1 N Acido ossalico biidrato H 2 C 2 O 4. 2 H 2 O PM 126, 06 Si prelevano esattamente 20, 00 m. L di soluzione di acido ossalico biidrato 0, 1 N o si pesa esattamente la quantità di acido ossalico biidrato necessaria a reagire con 25 m. L di soluzione 0, 1 N di permanganato, sciogliendoli in 20 -30 m. L di acqua deionizzata. Si aggiungono circa 20 m. L di H 2 SO 4 al 10%, si diluisce fino a 80 -100 m. L e si scalda la soluzione a 70 -80 °C. La soluzione calda viene titolata con la soluzione di KMn. O 4 0, 1 N avendo cura di agitare bene in modo da evitare locali eccessi di ossidante. All’inizio della titolazione la soluzione stenta a decolorarsi, perché l’ossidazione dell’ossalato è lenta; tuttavia con il riscaldamento e la formazione di ioni Mn(II) che catalizzano l’ossidazione, questa poi procede rapidamente. Al termine della titolazione la soluzione dovrebbe essere ancora calda. l

5 H 2 C 2 O 4 + 2 Mn. O 4 - + 6 H 3 O+ 10 CO 2 + 2 Mn 2+ + 14 H 2 O 100 m. L di soluzione 0, 1 N si preparano pesando esattamente circa 0, 63 g di acido ossalico biidrato in matraccio da 100 m. L e sciogliendoli in acqua deionizzata fino a volume. PE = PM/2. Sodio ossalato Na 2 C 2 O 4 PM 134, 00

Determinazione Acqua Ossigenata soluzione secondo F. U. I. H 2 O 2 PM 34, 02 Soluzione al 30%, 27%, 3% Si prelevano esattamente 10, 00 m. L della soluzione al 3% e si diluiscono a 200 in pallone tarato. Quindi si prelevano esattamente 20, 00 m. L di questa soluzione, si aggiungono 5 m. L di acido solforico diluito e si titolano con permanganato di potassio 0, 1 N. 1 m. L di soluzione 0, 1 N di KMn. O 4 corrispondono a 0, 00170 g di H 2 O 2.

Determinazione Ferro(II) Fe. SO 4 PM 151, 907 Si prelevano esattamente 20, 00 m. L di una soluzione 0, 1 N di solfato di ferro (II), oppure si pesa esattamente la quantità di solfato ferroso che deve reagire con 20 -30 m. L della soluzione 0, 1 N di potassio permanganato e si scioglie in 20 m. L circa di acqua deionizzata; si aggiungono 10 -20 m. L di acido solforico al 10%, 10 gc di acido fosforico (75%) e si titolano con permanganato di potassio 0, 1 N. Determinare o i g/100 m. L di Fe. SO 4 o la % (p/p) di Fe nel campione.

- Slides: 58