SOLUZIONI TAMPONE NEL SANGUE PER SOLUZIONE TAMPONE SI








- Slides: 11

SOLUZIONI TAMPONE NEL SANGUE

PER SOLUZIONE TAMPONE SI INTENDE: una soluzione in cui non varia il p. H per piccole aggiunte di acido e di base Le condizioni per ottenere un sistema tampone sono: - una soluzione acquosa che deve contenere un acido debole e la sua base coniugata (sale) -una soluzione acquosa che deve contenere una base debole e il suo acido coniugato (sale)

Il p. H del sangue tende ad essere mantenuto costante da tre sistemi acido-base coniugati: (1)Acido carbonico bicarbonato (2) diidrogenofosfato (3) proteine / proteinati

. . . Nell’uomo sano a riposo il p. H del sangue è 7, 35 -7, 45 (arterioso 7, 4 venoso 7, 37) Il p. H è mantenuto costante da alcuni soluti che svolgono una efficace azione tampone: -Anidride carbonica/bicarbonato -Fosfato -Proteinati

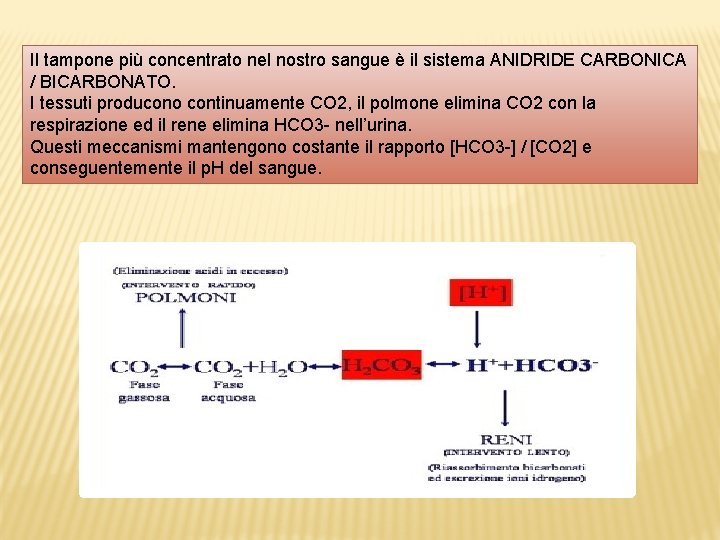
Il tampone più concentrato nel nostro sangue è il sistema ANIDRIDE CARBONICA / BICARBONATO. I tessuti producono continuamente CO 2, il polmone elimina CO 2 con la respirazione ed il rene elimina HCO 3 - nell’urina. Questi meccanismi mantengono costante il rapporto [HCO 3 -] / [CO 2] e conseguentemente il p. H del sangue.

L’acido carbonico nel plasma è in equilibrio con una grande riserva di CO 2 gas (polmoni) Se si verifica un aumento di H+ nel sangue il sistema tampone si attiva come previsto si ha un aumento di H 2 CO 3. Un aumento della CO 2 disciolta in fase acquosa e di conseguenza un aumento della CO 2 nei polmoni che viene eliminata con la respirazione. Se si verifica un aumento dell’ OH- il sistema tampone si attiva come segue un aumento di H 2 CO 3 e una diminuzione di CO 2 disciolta in soluzione acquosa provoca un aumento della SOLUBILIZZAZIONE della CO 2 nel plasma proveniente dalla respirazione cellulare. LA VELOCITA’ DELLA RESPIRAZIONE REGOLA e MANTIENE COSTANTE il p. H

TAMPONE FOSFATO Il sistema tampone H 2 PO 4 - / H 2 PO 4 -- è importante a livello renale Il sistema fosfato è anche un ottimo tampone intracellulare

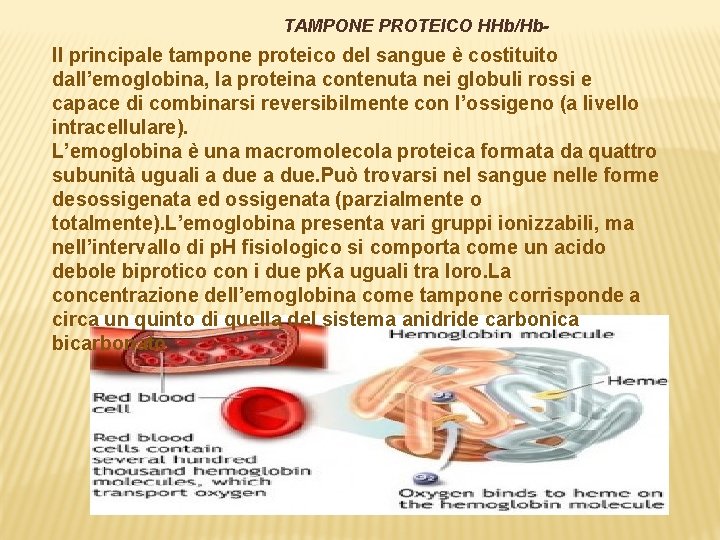
TAMPONE PROTEICO HHb/Hb- Il principale tampone proteico del sangue è costituito dall’emoglobina, la proteina contenuta nei globuli rossi e capace di combinarsi reversibilmente con l’ossigeno (a livello intracellulare). L’emoglobina è una macromolecola proteica formata da quattro subunità uguali a due. Può trovarsi nel sangue nelle forme desossigenata ed ossigenata (parzialmente o totalmente). L’emoglobina presenta vari gruppi ionizzabili, ma nell’intervallo di p. H fisiologico si comporta come un acido debole biprotico con i due p. Ka uguali tra loro. La concentrazione dell’emoglobina come tampone corrisponde a circa un quinto di quella del sistema anidride carbonica bicarbonato

Le oscillazioni del p. H fisiologico dipendono da una parte dai processi metabolici che possono produrre acidi organici (acido lattico, acido acetico, etc) e acidi inorganici (acido carbonico, ione diidrogenofosfato) , e dall'alimentazione che può far introdurre sali alcalini di Na+, K+, Ca++ e Mg++.

L’equilibrio acido base determina la funzionalità dei sistemi biologici facilitandone od ostacolandone le reazioni. La diversa concentrazione dei Sali minerali provoca lo svilupparsi di un ambiente acido o alcalino. La stabilità dell’equilibrio acido-base è condizione fondamentale e parte integrante degli scambi biochimici dell’organismo, i quali avvengono soltanto in una zona limitata del p. H, al di fuori della quale non esisterebbe forma di vita.

REALIZZATO DAGLI ALUNNI: -PICI ALESSANDRA -TREDANARI ANTONIO