Soluzione di un acido debole contiene es CH
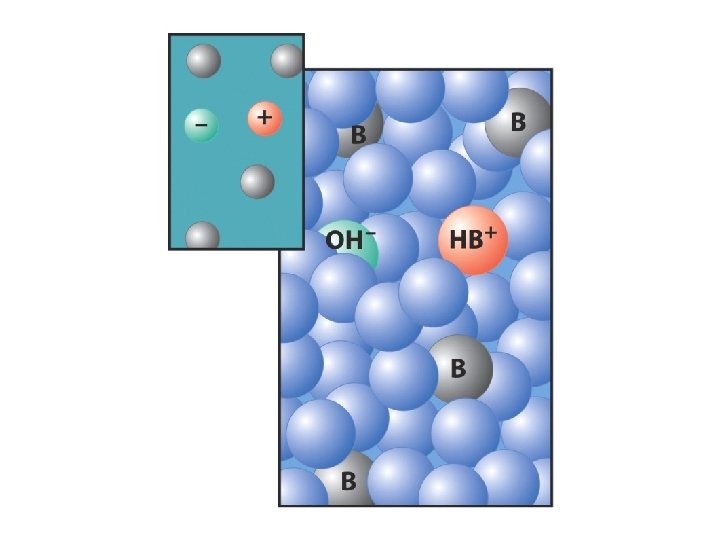
Soluzione di un acido debole contiene es. CH 3 COOH • molte molecole H 2 O solvente • molecole CH 3 COOH indissociate • pochi ioni CH 3 COO- dalla dissociazione • pochi ioni H 3 O+ dell'acido • pochissimi ioni OH- dall'acqua CH 3 COOH + H 2 O ⇆ CH 3 COO- + H 3 O+ 2 H 2 O ⇆ H 3 O+ + OH-
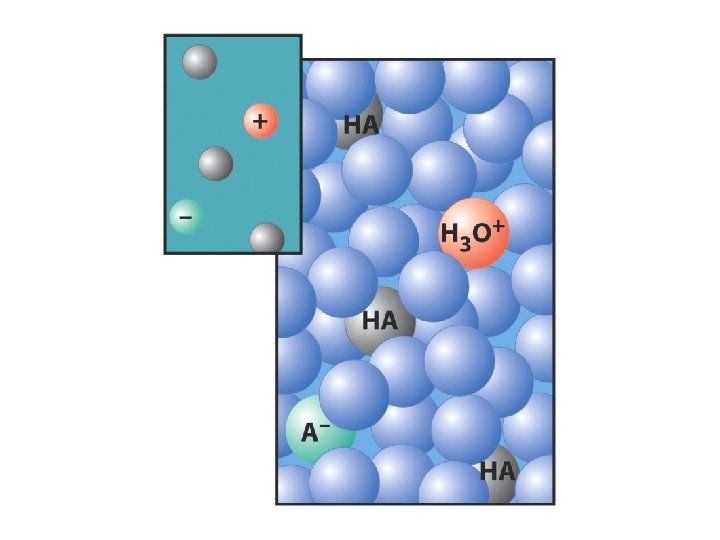
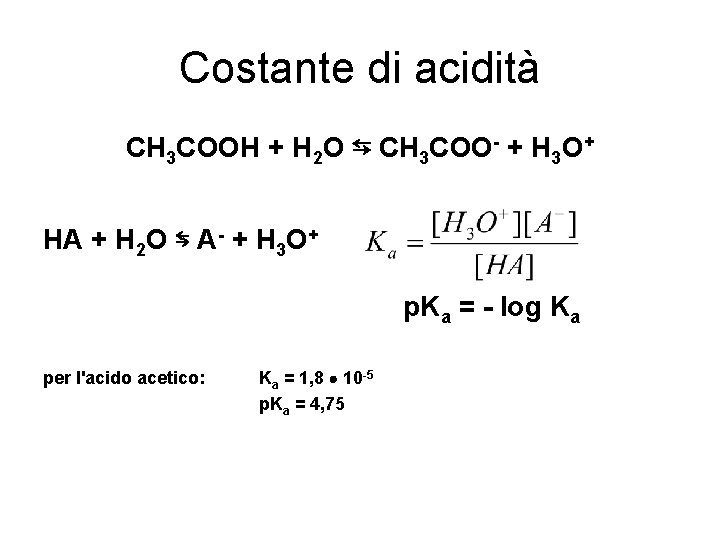
Costante di acidità CH 3 COOH + H 2 O ⇆ CH 3 COO- + H 3 O+ HA + H 2 O ⇆ A- + H 3 O+ p. Ka = - log Ka per l'acido acetico: Ka = 1, 8 10 -5 p. Ka = 4, 75

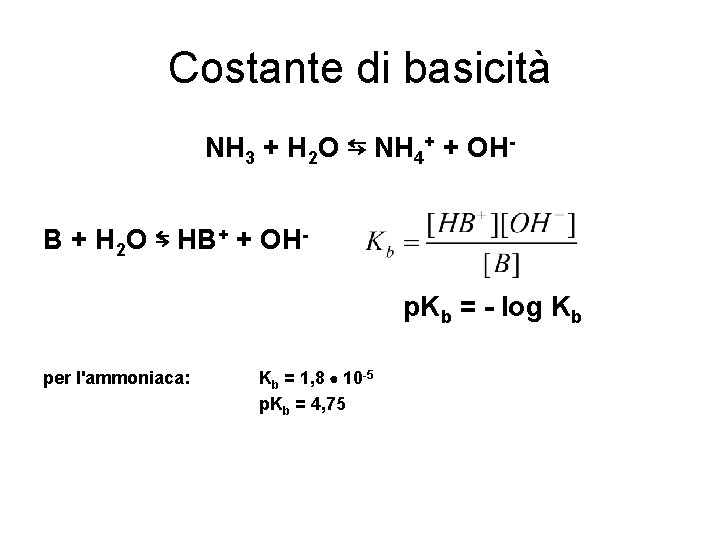
Costante di basicità NH 3 + H 2 O ⇆ NH 4+ + OHB + H 2 O ⇆ HB+ + OHp. Kb = - log Kb per l'ammoniaca: Kb = 1, 8 10 -5 p. Kb = 4, 75

p. H di acidi forti HCl 0, 020 M • HCl è completamente dissociato • [H 3 O+] = 0, 020 = 2, 0 • 10 -2 • p. H = - log [H 3 O+] = - log 2, 0 • 10 -2 = = - log 2, 0 - log 10 -2 = 2 - 0, 30 = = 1, 70

p. H di basi forti KOH 0, 040 M • KOH è completamente dissociato • [OH-] = 4, 0 • 10 -2 • p. H = - log [H 3 O+] = - log 2, 5 • 10 -13 = = 13 - 0, 40 = 12, 60
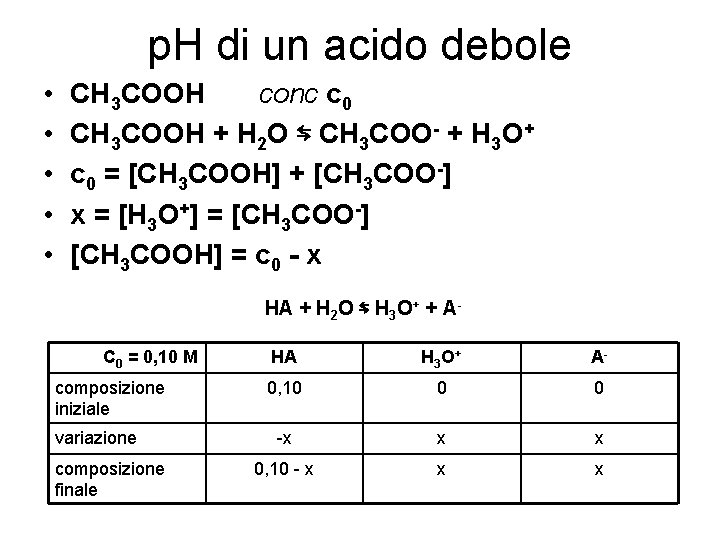
p. H di un acido debole • • • CH 3 COOH conc c 0 CH 3 COOH + H 2 O ⇆ CH 3 COO- + H 3 O+ c 0 = [CH 3 COOH] + [CH 3 COO-] x = [H 3 O+] = [CH 3 COO-] [CH 3 COOH] = c 0 - x HA + H 2 O ⇆ H 3 O+ + AC 0 = 0, 10 M composizione iniziale variazione composizione finale HA H 3 O + A- 0, 10 0 0 -x x x 0, 10 - x x x

segue p. H di un acido debole • CH 3 COOH + H 2 O ⇆ CH 3 COO- + H 3 O+ • HA + H 2 O ⇆ H 3 O+ + A- • p. H = - log [H 3 O+] = - log 1, 3 • 10 -3 = 2, 89
![Grado di dissociazione se c 0 = 0, 10 e [A-] = 1, 3 Grado di dissociazione se c 0 = 0, 10 e [A-] = 1, 3](http://slidetodoc.com/presentation_image_h/1f0208052a18c2874abb9e71c821849b/image-11.jpg)
Grado di dissociazione se c 0 = 0, 10 e [A-] = 1, 3 • 10 -3
![se [H 3 O+] = Ka allora [A-] = [HA] e le molecole indissociate se [H 3 O+] = Ka allora [A-] = [HA] e le molecole indissociate](http://slidetodoc.com/presentation_image_h/1f0208052a18c2874abb9e71c821849b/image-12.jpg)
se [H 3 O+] = Ka allora [A-] = [HA] e le molecole indissociate sono quante quelle dissociate. α = 0, 5 se Ka = 1, 8 • 10 -5 p. H [H 3 O+] [A-]/[HA] 2, 89 1, 3 • 10 -3 0, 013 2, 00 1, 0 • 10 -2 0, 0018 3, 00 1, 0 • 10 -3 0, 018 4, 74 1, 8 • 10 -5 1

p. H di una base debole • metilammina CH 3 NH 2 c 0 = 0, 20 M CH 3 NH 2 + H 2 O ⇆ CH 3 NH 3+ + OHB + H 2 O ⇆ HB+ + OH- C 0 = 0, 20 M composizione iniziale variazione composizione finale B OH- HB+ 0, 20 0 0 -x x x 0, 20 - x x x

segue p. H di una base debole e approssimando 0, 20 - x con 0, 20 • p. H = - log [H 3 O+] = - log 1, 2 • 10 -12 = 11, 93

Indicatori • cambiano colore col p. H • sono coppie acido-base deboli coniugati HIn - In • HIn e In- hanno colore diverso • si aggiungono in quantità minima: non cambiano [H 3 O+]
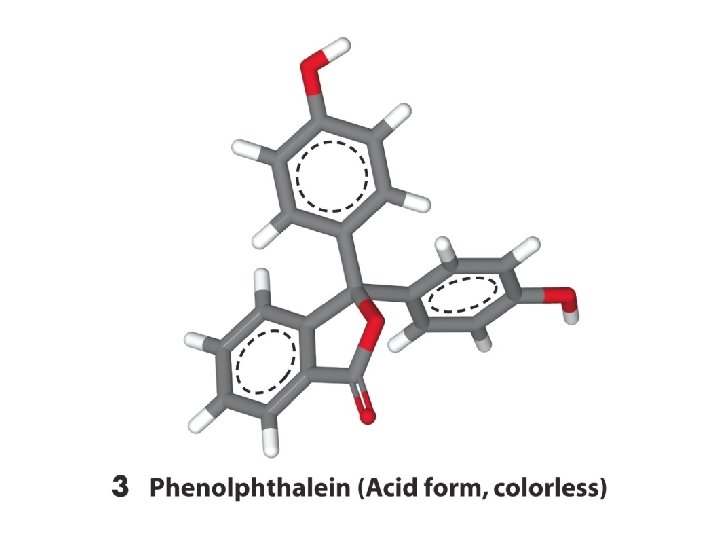
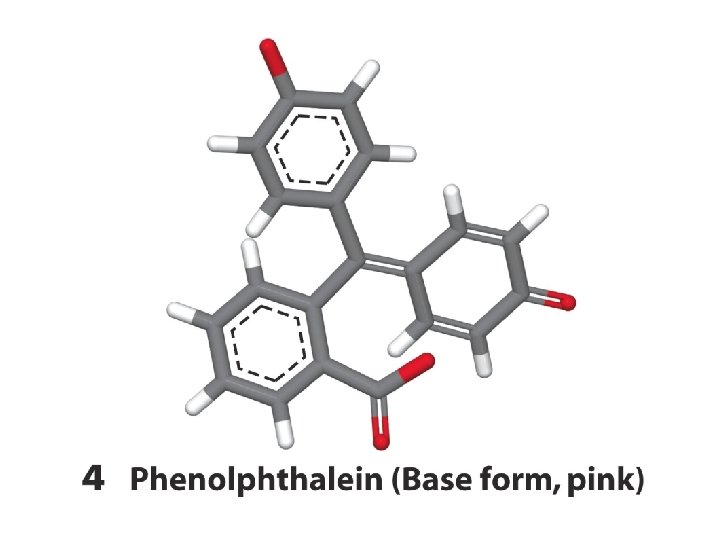

Cambiamento di colore e intervallo di viraggio di alcuni indicatori
![Indicatori [H 3 O+] = Kin [H 3 O+] = 10 Kin [H 3 Indicatori [H 3 O+] = Kin [H 3 O+] = 10 Kin [H 3](http://slidetodoc.com/presentation_image_h/1f0208052a18c2874abb9e71c821849b/image-19.jpg)
Indicatori [H 3 O+] = Kin [H 3 O+] = 10 Kin [H 3 O+] = 1/10 Kin p. H = p. Kin-1 p. H = p. Kin+1 [HIn] = [In-] [HIn] = 10 [In-] [HIn] = 1/10 [In-] p. Kin è il p. H a cui il colore vira per p. H < p. Kin-1 colore dell'acido per p. H > p. Kin+1 colore della base
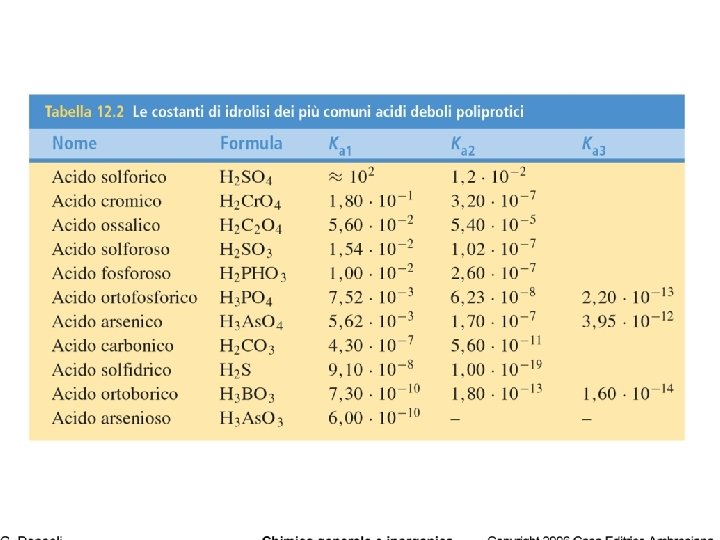

Keq di acidi e basi coniugati CH 3 COOH + H 2 O ⇆ CH 3 COO- + H 3 O+ CH 3 COO- + H 2 O ⇆ CH 3 COOH + OH- p. Ka + p. Kb = 14
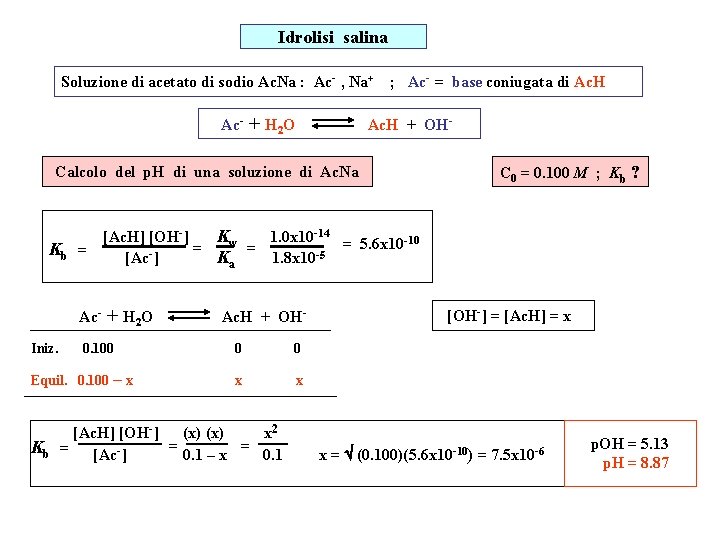
Idrolisi salina Soluzione di acetato di sodio Ac. Na : Ac- , Na+ ; Ac- = base coniugata di Ac. H Ac- + H 2 O Ac. H + OH- Calcolo del p. H di una soluzione di Ac. Na Kb = Ac. Iniz. C 0 = 0. 100 M ; Kb ? [Ac. H] [OH-] Kw 1. 0 x 10 -14 = 5. 6 x 10 -10 = = [Ac-] Ka 1. 8 x 10 -5 + H 2 O 0. 100 Equil. 0. 100 – x Ac. H + OH 0 0 x x [Ac. H] [OH-] (x) x 2 = = Kb = [Ac-] 0. 1 – x 0. 1 [OH-] = [Ac. H] = x x = (0. 100)(5. 6 x 10 -10) = 7. 5 x 10 -6 p. OH = 5. 13 p. H = 8. 87
- Slides: 22