SOLUCIONES QUMICAS Profesora Fernanda Salfate Flores Qumica 2













- Slides: 19


SOLUCIONES QUÍMICAS Profesora Fernanda Salfate Flores Química 2 do Medio Fer. salfate. flores@Gmail. com

OBJETIVO • Identificar los principales componentes de una disolución.

IMPORTANTE • La siguiente presentación tiene como motivo apoyar el autoaprendizaje por parte del alumno, el cual debe complementarse además con otras fuentes, tales como vídeos, revistas, artículos de formación científica, textos escolares, internet, entre otros. • Los trabajos deben ser entregados oportunamente dentro de la fecha indicada en cada guía. • El correo para enviar trabajos es fer. salfate. flores@gmail. com • En lo posible, enviar los trabajos en formato Word, ya que esto facilita la revisión y retroalimentación. Sin embargo, aquellos estudiantes que no cuenten con internet y/o computador, podrán utilizar otras plataformas de envío, tales como fotografías, actividad en el cuaderno, etc. • NO copies y pegues información de internet o de tus compañeros, recuerda que es de suma importancia mantener un nivel de aprendizaje adecuado durante esta crisis mundial que estamos atravesando. • FAVOR DE ENVIAR CONSULTAS Y TRABAJOS DENTRO DEL HORARIO

RECORDEMOS • ¿Qué tienen en común las siguientes imágenes?

• ¡Pues que todas constituyen un ejemplo de disolución! Recuerda que no siempre las disoluciones son líquidas, también pueden ser gaseosas (como el aire) e incluso sólidas (por ejemplo el acero, que es una mezcla de metales).

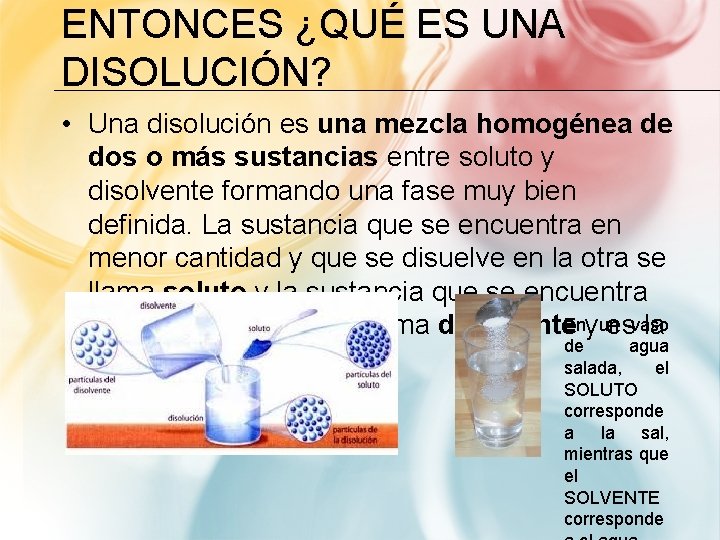
ENTONCES ¿QUÉ ES UNA DISOLUCIÓN? • Una disolución es una mezcla homogénea de dos o más sustancias entre soluto y disolvente formando una fase muy bien definida. La sustancia que se encuentra en menor cantidad y que se disuelve en la otra se llama soluto y la sustancia que se encuentra en mayor cantidad se llama disolvente. Enyunesvaso la de agua que disuelve al soluto. salada, el SOLUTO corresponde a la sal, mientras que el SOLVENTE corresponde


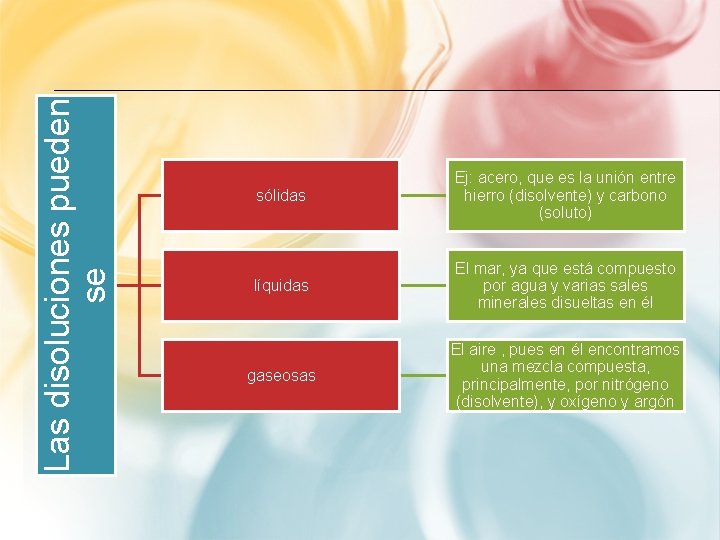
Las disoluciones pueden se sólidas Ej: acero, que es la unión entre hierro (disolvente) y carbono (soluto) líquidas El mar, ya que está compuesto por agua y varias sales minerales disueltas en él gaseosas El aire , pues en él encontramos una mezcla compuesta, principalmente, por nitrógeno (disolvente), y oxígeno y argón

LA SOLUBILIDAD • La solubilidad es la medida máxima de soluto que se puede disolver en un disolvente dado. • Por ejemplo, decimos que la solubilidad del azúcar (sacarosa) en agua es aproximadamente 200 g de sacarosa/100 g de agua a 25 °C. Esto significa que en 100 g de agua, aproximadamente 100 m. L, se pueden disolver hasta 200 g de azúcar a una temperatura de 25 °C.

CLASIFICAR SEGÚN SU CONTENIDO DE SOLUTO EN TRES GRUPOS: • Disolución sobresaturada Tiene más soluto del que el disolvente puede recibir a cierta temperatura. Suelen ser inestables y tienden a tener sólido no disuelto en su interior. A la disolución se le agrega más soluto del que puede ser disuelto, obteniendo así una solución sobresaturada.

DISOLUCIÓN SATURADA • Tiene la cantidad máxima de soluto que puede aceptar el disolvente a la temperatura en que se encuentra la disolución

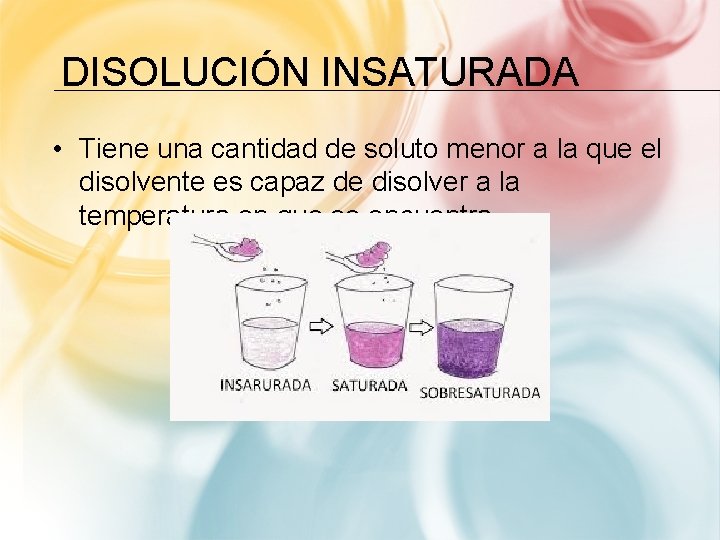
DISOLUCIÓN INSATURADA • Tiene una cantidad de soluto menor a la que el disolvente es capaz de disolver a la temperatura en que se encuentra

¿CÓMO PODEMOS DIFERENCIAR UNA SOLUCIÓN SOBRESATURADA DE UNA SATURADA? • Por lo general, una solución sobresaturada presentará un precipitado sólido que ya no puede seguir disolviéndose (esto ocurre si, por ejemplo, agregamos mucha sal a un vaso de agua), mientras que una solución saturada presentara un color menos intenso (si es que está coloreado) y un aspecto menos turbio.

• El agua se considera el disolvente universal y es usada en una amplia gama de procesos industriales y agrícolas. Esto se debe a su bajo precio comparado con otros disolventes, pero también a que gracias a su alta polaridad, puede disolver tanto otras sustancias igualmente polares, como sales que son capaces de formar iones en disolución.

• ¿QUÉ DISOLUCIONES PODEMOS ENCONTRAR EN NUESTRA VIDA COTIDIANA?

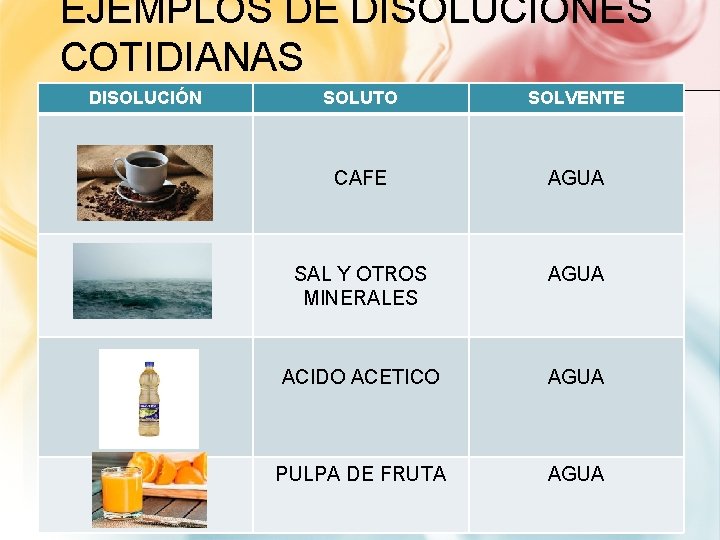
EJEMPLOS DE DISOLUCIONES COTIDIANAS DISOLUCIÓN SOLUTO SOLVENTE CAFE AGUA SAL Y OTROS MINERALES AGUA ACIDO ACETICO AGUA PULPA DE FRUTA AGUA

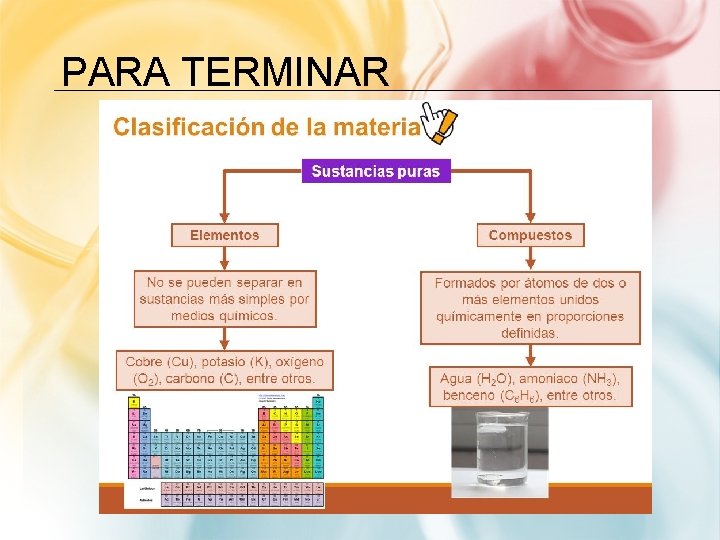
PARA TERMINAR

¿QUÉ OTRAS DISOLUCIONES QUE USES REGULARMENTE CONOCES? • Nombra algunas e identifica soluto y solvente.