SOLUCIONES AMORTIGUADORAS BUFFER SOLUCIONES TAMPN Profesora Lissette Gmez

SOLUCIONES AMORTIGUADORAS “BUFFER” “SOLUCIONES TAMPÓN” Profesora Lissette Gómez Curso: 4 to medio.
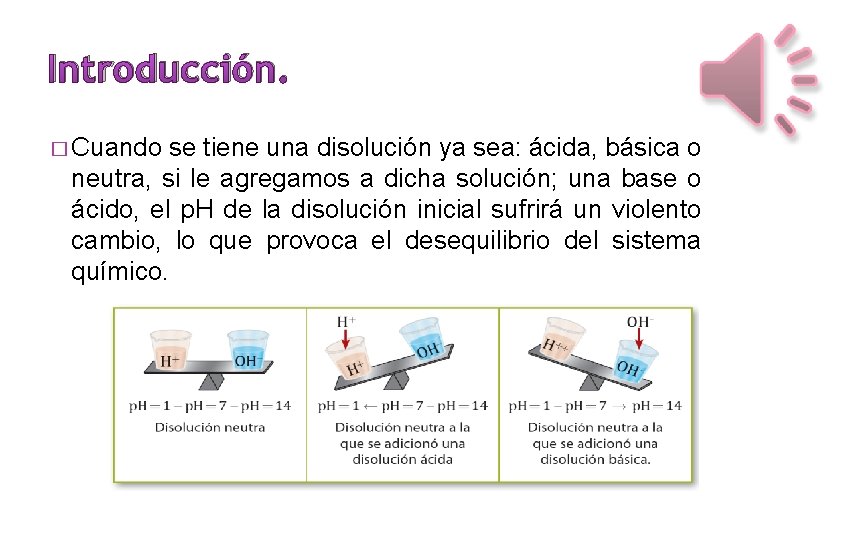
Introducción. � Cuando se tiene una disolución ya sea: ácida, básica o neutra, si le agregamos a dicha solución; una base o ácido, el p. H de la disolución inicial sufrirá un violento cambio, lo que provoca el desequilibrio del sistema químico.

Una solución Reguladora, Buffer , Tampón o Amortiguadora es: un sistema que tiende a mantener el p. H casi constante cuando se agregan pequeñas cantidades de ácidos (H+) ó bases (OH-).

Una solución amortiguadora reduce el impacto de los cambios drásticos de H+ y OH-. Se prepara con un ÁCIDO DÉBIL y una SAL del mismo ÁCIDO o empleando una BASE DÉBIL y una SAL de la misma BASE. La solución amortiguadora contiene especies que van a reaccionar con los iones H+ y OH- agregados.

Componentes: Buffer ácido: Formado por un ácido débil y su sal. Ejemplo: CH 3 COOH/CH 3 COONa Buffer básico: Formado por una base débil y su sal. Ejemplo: NH 3/NH 4 Cl
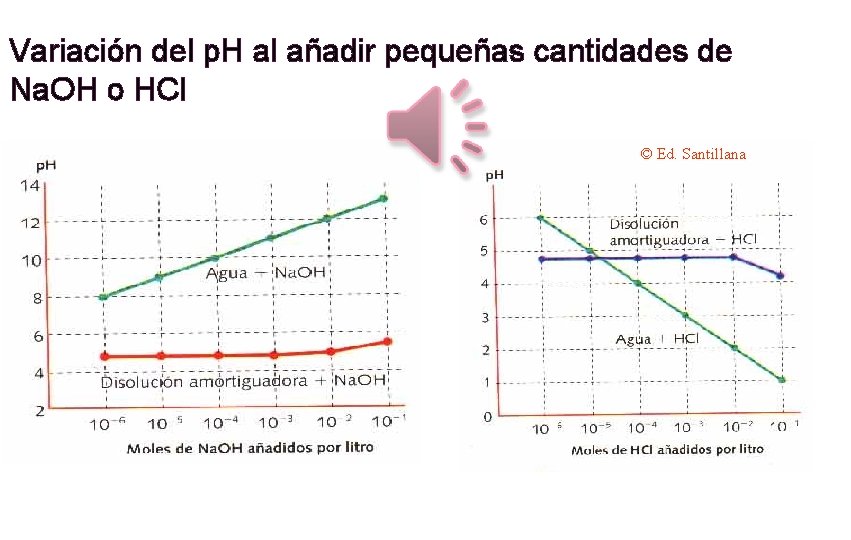
Variación del p. H al añadir pequeñas cantidades de Na. OH o HCl © Ed. Santillana
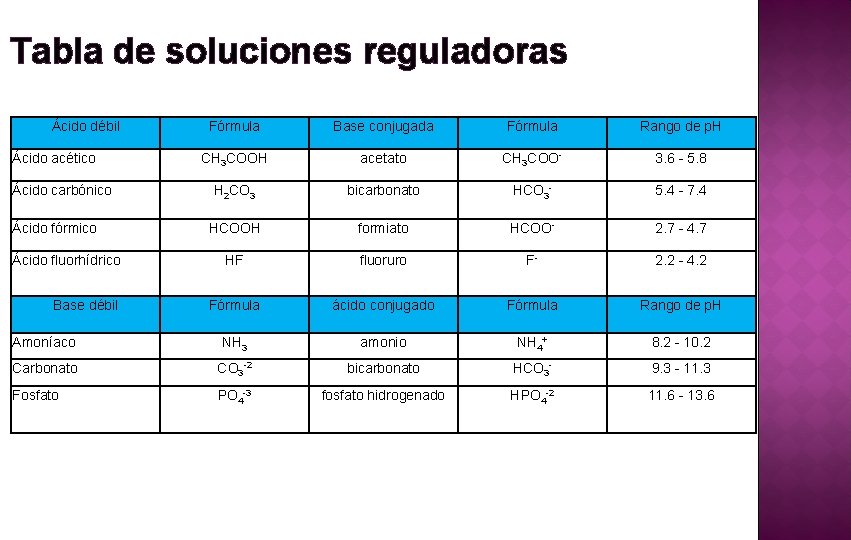
Tabla de soluciones reguladoras Ácido débil Fórmula Base conjugada Fórmula Rango de p. H CH 3 COOH acetato CH 3 COO- 3. 6 - 5. 8 H 2 CO 3 bicarbonato HCO 3 - 5. 4 - 7. 4 HCOOH formiato HCOO- 2. 7 - 4. 7 HF fluoruro F- 2. 2 - 4. 2 Fórmula ácido conjugado Fórmula Rango de p. H Amoníaco NH 3 amonio NH 4+ 8. 2 - 10. 2 Carbonato CO 3 -2 bicarbonato HCO 3 - 9. 3 - 11. 3 Fosfato PO 4 -3 fosfato hidrogenado HPO 4 -2 11. 6 - 13. 6 Ácido acético Ácido carbónico Ácido fórmico Ácido fluorhídrico Base débil

El p. H de una disolución amortiguadora se calcula aplicando la siguiente fórmula, conocida como ecuación de Henderson-Hasselbach p. H= p. Ka + Log [Sal] [Acido] Donde: p. Ka = -log Ka Y para las bases: p. OH= p. Kb + Log [Sal] [Base] Donde: p. Kb = -log Kb Donde: p. Ka : Corresponde al logaritmo negativo de la constante de acidez del ácido que forma el buffer. [Sal] : Representa la concentración molar de la sal derivada del ácido. [Ácido] : Corresponde a la concentración molar del ácido.
![Procedimiento para calcular p. H de Soluciones Buffer [H+] = Ka [ácido] [sal] [OH-] Procedimiento para calcular p. H de Soluciones Buffer [H+] = Ka [ácido] [sal] [OH-]](http://slidetodoc.com/presentation_image_h2/8ccfdc16817b50b6b4d490faa6034a96/image-9.jpg)
Procedimiento para calcular p. H de Soluciones Buffer [H+] = Ka [ácido] [sal] [OH-] = kb [base] [sal (del acido)] p. H = -log [H+] = 1 X 10 -14 [OH]

Ejemplo n° 1 Calcule el p. H de una solución Buffer formada por 0. 25 moles de CH 3 COOH (ácido acético) y 0. 4 moles de CH 3 COONa (acetato de sodio) disueltos en 500 ml de solución. Teniendo una Ka = 1. 8 x 10 -5

Paso 1. Determinar Datos: Paso 2. Determinar formulas. 0. 25 moles de CH 3 COOH (acido) 0. 40 moles de CH 3 COONa (sal) 500 ml de solución Ka= 1. 8 x 10 -5 Formula 1. Pasar de moles a molaridad. M = mol/litros Formula 2. [H+]= Ka [ácido] [sal] Paso 3. Desarrollo Formula 3. p. H= - Log [H+] a. Calcular : [CH 3 COOH]= 0. 25 moles= 0. 5 M 0. 5 L b. [CH 3 COONa] = 0. 40 moles = 0. 8 M 0. 5 L c. [H+] = 1. 8 x 10 -5 [0. 5 M] = 1. 125 x 10 -5 [0. 8 M] p. H = -log 1. 125 X 10 -5 = 4. 94
![Con la ecuación de Henderson-Hasselbach p. H = p. Ka + log [sal] [ácido] Con la ecuación de Henderson-Hasselbach p. H = p. Ka + log [sal] [ácido]](http://slidetodoc.com/presentation_image_h2/8ccfdc16817b50b6b4d490faa6034a96/image-12.jpg)
Con la ecuación de Henderson-Hasselbach p. H = p. Ka + log [sal] [ácido] Ka= 1. 8 x 10 -5 Donde: p. Ka = -log Ka p. Ka : Corresponde al logaritmo negativo de la constante de acidez del ácido que forma el buffer p. Ka= -log Ka p. Ka = -log ( 1. 8 x 10 -5) p. Ka = 4. 74 p. H = 4. 74 + log (0. 8 M) (0. 5 M) p. H= 4. 74 + 0. 20 = 4. 94

¿Cuál será el p. H del buffer inicial si añadimos 0. 02 moles HCl? [HCl]= 0. 02 moles = 0. 04 M 0. 5 L CH 3 COONa (base) + H+ ↔ CH 3 COOH + Na+ 0. 8 M 0. 04 M 0. 5 M 0. 8 M - 0. 04 M = 0. 76 M de CH 3 COO- 0. 5 M + 0. 04 M = 0. 54 M de CH 3 COOH
![NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p. NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p.](http://slidetodoc.com/presentation_image_h2/8ccfdc16817b50b6b4d490faa6034a96/image-14.jpg)
NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p. Ka = -log ( 1. 8 x 10 -5) = p. Ka =4. 74 p. H= 4. 74 + log (0. 76 M) (0. 54 M) p. H= 4. 74 + 0. 14= 4. 88

Aplicación bioquímica. Función e Importancia Biológica: � En los organismos vivos, las células deben mantener un p. H casi constante para la acción enzimática y metabólica. � Los fluidos intracelulares y extracelulares contienen pares conjugados ácido-base que actúan como buffer.
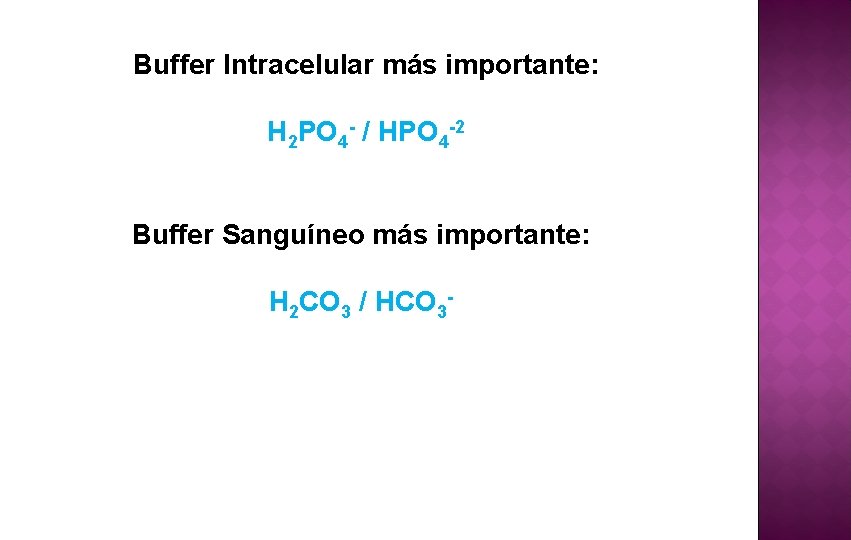
Buffer Intracelular más importante: H 2 PO 4 - / HPO 4 -2 Buffer Sanguíneo más importante: H 2 CO 3 / HCO 3 -

Otros sistemas que ayudan a mantener el p. H sanguíneo son: ØH 2 PO 4 - / HPO 4 -2 ØProteínas ØÁcidos Nucleicos ØCoenzimas ØMetabolitos intermediarios Algunos poseen grupos funcionales que son ácidos o bases débiles, por consiguiente, ejercen influencia en el p. H intracelular y éste afecta la estructura y el comportamiento de tales moléculas.
El p. H sanguíneo es de: 7. 35 -7. 45 Acidosis p. H debajo de 7. 35 Es una afección en demasiado ácido en corporales y el riñon correctamente, puede muerte. la cual hay los líquidos no funciona llevar a la Alcalosis p. H arriba de 7. 45 Los riñones y los pulmones mantienen el equilibrio apropiado (nivel de p. H adecuado) de químicos, llamados ácidos y bases en el cuerpo. La disminución del nivel de dióxido de carbono (un ácido) o el aumento del nivel de bicarbonato (una base) hacen que el cuerpo esté demasiado alcalino, una afección llamada alcalosis.
El nivel idóneo del p. H en la sangre debe oscilar entre 7. 35 y 7. 45, pero la contaminación atmosférica, los malos hábitos alimenticios o el estrés acidifican el cuerpo y alteran este p. H, la sangre reacciona y roba los nutrientes que necesita del resto de órganos vitales para compensar el desequilibro. Las consecuencias de un p. H ácido: Disminución de la actividad del sistema inmune Favorecimiento de la calcificación de los vasos sanguíneos. Pérdida de masa ósea y masa muscular Fatiga crónica Dolor y espasmos musculares Caída del cabello y deterioro de las uñas Piel irritada Cansancio generalizado

- Slides: 20