Soli Nzvoslov vznik a pouit sol hydrogensoli a


























- Slides: 29

Soli Názvosloví, vznik a použití solí, hydrogensoli a hydráty solí, hnojiva, použití solí ve stavebnictví Dostupné z Metodického portálu www. rvp. cz, ISSN: 1802 -4785, financovaného z ESF a státního rozpočtu ČR. Provozováno Výzkumným ústavem pedagogickým v Praze.

Definice solí n Sůl je sloučenina, složená z kationtu kovu, + případně kationtu amonného NH 4 a aniontu kyseliny.

Příklady solí Chlorid sodný – kuchyňská sůl Na. Cl n Dusičnan sodný - Chilský ledek Na. NO 3 n Pentahydrát síranu měďnatého – skalice modrá Cu. SO 4. 5 H 2 O n Hydrogenuhličitan sodný – jedlá soda Na. HCO 3 n

Rozdělení solí Soli můžeme dělit podle různých hledisek, např. : Podle rozpustnosti ve vodě n Podle kyseliny, od které se odvozují n Podle jiných hledisek n

Rozdělení solí podle rozpustnosti ve vodě Soli rozpustné ve vodě – např. halogenidy, většina ostatních solí n Soli nerozpustné ve vodě – např. uhličitan vápenatý, barnaté soli, dusičnan stříbrný n

Rozdělení solí podle kyselin, od kterých jsou odvozeny Halogenidy – fluoridy, chloridy, bromidy, jodidy (soli kyseliny fluorovodíkové…) n Sulfidy (soli kyseliny sirovodíkové) n Sírany (soli kyseliny sírové) n Siřičitany (soli kyseliny siřičité) n Uhličitany (soli kyseliny uhličité) n Dusičnany (soli kyseliny dusičné) n …………. . n

Jiné rozdělení solí – např. : Normální soli n Kyselé soli - hydrogensoli n Hydráty solí n Podle použití: n soli používané ve stavebnictví n v potravinářství n v zemědělství – hnojiva

Názvosloví solí bezkyslíkatých kyselin – jako názvosloví dvouprvkových sloučenin n Podstatné jméno Odvozeno od názvu prvku na druhém místě ve vzorci + koncovka –id n Přídavné jméno Název kationtu s koncovkou podle oxidačního čísla I Např. : -I K Cl Cl sůl kys. chlorovodíkové - chlorid -I chlorid draselný

Názvosloví solí kyslíkatých kyselin n Podstatné jméno Odvozeno od názvu kyseliny (aniontu) + koncovka –an n Přídavné jméno Název kationtu s koncovkou podle oxidačního čísla Např. : I V KN O -II -I 3 V N sůl kyseliny dusičné – dusičnan V N O -II –I 3 dusičnan draselný dusičnanový anion

Názvosloví hydrogensolí Tvoří se zařazením slova hydrogen- před podstatné jméno názvu soli n Počet atomů vodíku vázaných v aniontu hydrogensoli označujeme číslovkou: mono (pro 1 – zpravidla se neuvádí), di (2), tri (3) … V n Např. : Na. H 2 P O 4 dihydrogenfosforečnan sodný n

Hydráty solí n n n Některé soli vytvářejí krystaly, ve kterých jsou vázány molekuly vody. Takové soli se nazývají hydráty. Počet molekul vody v hydrátu se vyznačuje číslovkou. Např. : dihydrát síranu vápenatého Ca. SO 4. 2 H 2 O 1 – mono 6 - hexa 2 – di 7 - hepta 3 – tri 8 - okta 4 – tetra 9 - nona 5 – penta 10 - deka

Vznik solí Soli mohou vznikat různými chemickými reakcemi, např. : n Neutralizací n Reakcí kovu s nekovem n Reakcí kovu s kyselinou n Reakcí kyselinotvorného oxidu s hydroxidem n Reakcí hydroxidotvorného oxidu s kyselinou n Srážecí reakcí n …………

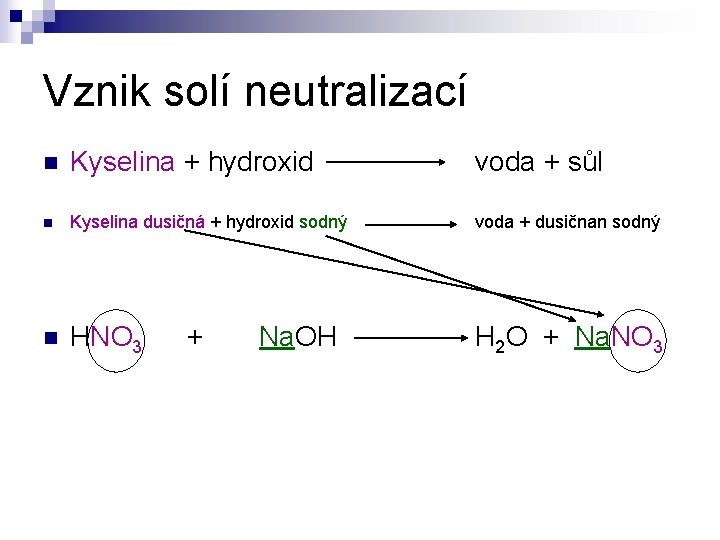
Vznik solí neutralizací n Kyselina + hydroxid voda + sůl n Kyselina dusičná + hydroxid sodný voda + dusičnan sodný n HNO 3 H 2 O + Na. NO 3 + Na. OH

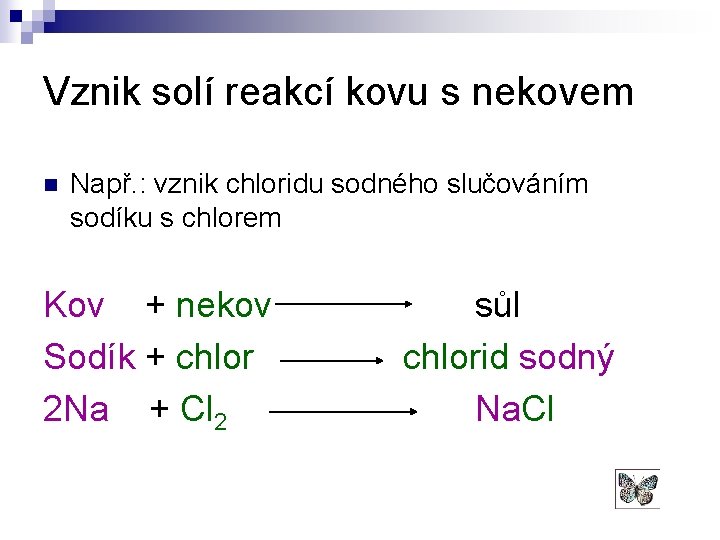
Vznik solí reakcí kovu s nekovem n Např. : vznik chloridu sodného slučováním sodíku s chlorem Kov + nekov Sodík + chlor 2 Na + Cl 2 sůl chlorid sodný Na. Cl

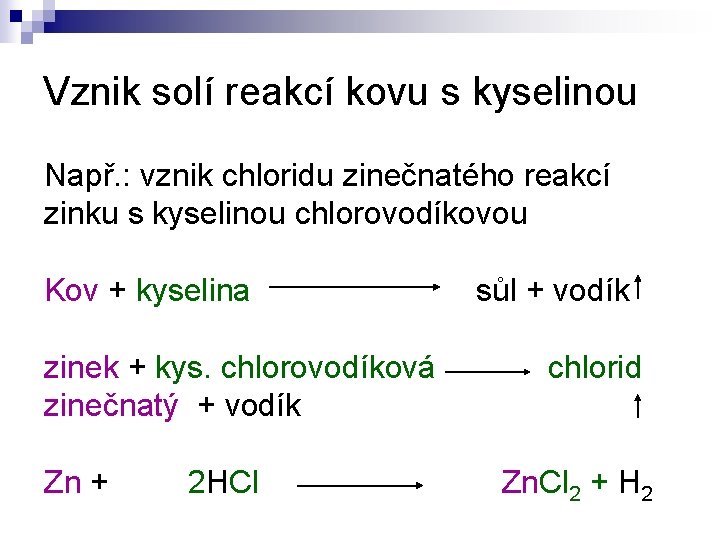
Vznik solí reakcí kovu s kyselinou Např. : vznik chloridu zinečnatého reakcí zinku s kyselinou chlorovodíkovou Kov + kyselina zinek + kys. chlorovodíková zinečnatý + vodík Zn + 2 HCl sůl + vodík chlorid Zn. Cl 2 + H 2

Použití solí V zemědělství – dusičnany, draselné soli a fosforečnany n Ve stavebnictví, sochařství – vápenaté soli n Výroba keramiky a porcelánu n Výroba pracích a čistících prostředků n V potravinářském průmyslu n Výroba chemických látek n

Dusičnany n n n Průmyslová hnojiva: Na. NO 3 dusičnan sodný (ledek sodný, chilský ledek) KNO 3 dusičnan draselný (ledek draselný) NH 4 NO 3 dusičnan amonný (ledek amonný) Lápis - Ag. NO 3 (dusičnan stříbrný) v kožním lékařství, výroba fotografických filmů a papírů

Sírany Síran vápenatý - nerost anhydrid (Ca. SO 4) a sádrovec (Ca. SO 4. 2 H 2 O) - výroba sádry (Ca. SO 4. 1/2 H 2 O) pro stavebnictví, sochařství a štukatérství n Skalice modrá – pentahydrát síranu měďnatého (Cu. SO 4. 5 H 2 O) – poměďování, k impregnaci dřeva proti hnilobě a k postřikům rostlin proti houbám a jiným škůdcům n

Uhličitany Uhličitan vápenatý Ca. CO 3 – v přírodě minerál vápenec (kalcit) a aragonit. Použití: n výroba páleného vápna, n stavební a sochařský kámen, n ozdobný kámen k obkladům budov (leštěný - mramor), n přísada při výrobě železa a cementu, n vápenaté průmyslové hnojivo n

Uhličitany Na 2 CO 3 – uhličitan sodný - výroba skla, mýdla, změkčování vody v prádelnách, papírnách, domácnostech (soda, krystalová soda Na 2 CO 3. 10 H 2 O) n K 2 CO 3 – uhličitan draselný - výroba skla a mazlavých mýdel n Na. HCO 3 – hydrogenuhličitan sodný – „užívací soda“ – součást prášků do pečiva, šumivých prášků pro přípravu nápojů n

Chloridy Na. Cl – chlorid sodný – výroba hydroxidu sodného, potravinářský průmysl n KCl – chlorid draselný – výroba hydroxidu draselného, draselné hnojivo n NH 4 Cl – chlorid amonný – salmiak – náplň suchých článků – baterií, čištění povrchu kovů při pájení n

Fosforečnany a křemičitany n Fosforečnany – fosforečná hnojiva (např. superfosfát), výroba fosforu a jeho sloučenin n Křemičitany - horninotvorné látky, např. živce, slídy – výroba stavebních materiálů a keramiky

Test na závěr Připravte se n Odpovídejte na následující otázky n

TEST – otázka č. 1 n která sůl se používá jako prostředek proti tzv. pálení žáhy (při překyselení žaludeční šťávy) a ke zmírnění bolestí při žaludečních vředech – zapiš správný chemický název a vzorec n odpověď

TEST – otázka č. 2 Která sůl se používá ve stavebnictví k výrobě páleného vápna? n Napiš správný chemický název a vzorec, uveď také mineralogický název n n odpověď

TEST – otázka č. 3 n Uveď název a vzorec soli zvané salmiak. K čemu se tato sůl používá? n odpověď

TEST – otázka č. 4 n Zapiš chemickou rovnicí vznik choridu sodného přímým slučováním prvků reakcí kovu s nekovem n odpověď

Hodnocení testu 1 za všechny odpovědi správně n 2 za jednu chybnou odpověď n 3 za dvě chybné odpovědi n 4 za tři chybné odpovědi n 5 pokud jsi žádnou z otázek nezodpověděl správně n

Použité zdroje: Čerpáno z: n Beneš, P. – Pumpr, V. – Banýr, J. : Základy chemie 1. díl pro 2. stupeň základní školy, nižší ročníky víceletých gymnázií a střední školy. 2. vydání. Nakladatelství Fortuna, 1996. ISBN 80 -7168 -234 -8. n www. wikipedia. cz