SOIL some basic concepts SOIL It doesnt matter

SOIL – some basic concepts

SOIL “It doesn’t matter who you are or where you are, your very existence and survival depend upon the chemical reactions taking place all the time in soil”… “ The term SOIL refers to “an extremely complex, variable and living medium and a non-renewable resource which performs many vital functions: food and other biomass production, storage, filtration and transformation of many substances including water, carbon, and nitrogen. These functions are worthy of protection because of their socio-economic as well as environmental importance" (Soil thematic strategy)
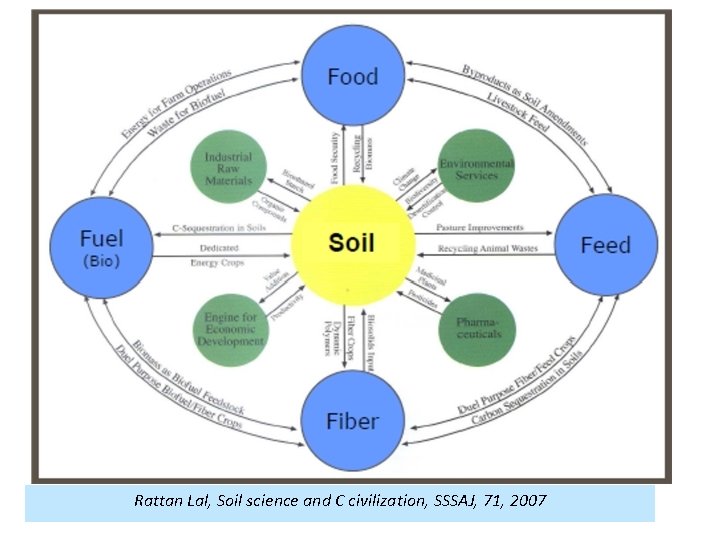
Rattan Lal, Soil science and C civilization, SSSAJ, 71, 2007

Il suolo è un sistema trifasico che, in condizioni ottimali per la vita delle piante, è costituito per circa il 50 % in peso da una fase solida, per circa il 25 % da una fase liquida (soluzione del suolo o soluzione circolante) e per circa il 25 % da una fase gassosa (aria tellurica). La fase solida è costituita prevalentemente da costituenti inorganici di natura e pezzatura variabili e contiene una frazione organica che si aggira in genere sull’ 1 3% (solo in casi particolari può essere inferiore o superiore) e che, a causa della minore massa volumica (circa 0, 5 g/cm 3) rispetto al materiale inorganico (circa 2, 7 g/cm 3), occupa, in proporzione della sua massa, un volume maggiore Per quanto riguarda l’origine, il suolo può essere definito come una formazione naturale di superficie, di spessore variabile, derivante dalla disgregazione fisica e dalla decomposizione chimica e biologica della roccia madre (detta anche substrato pedogenetico) e dei residui vegetali (che formano la lettiera)
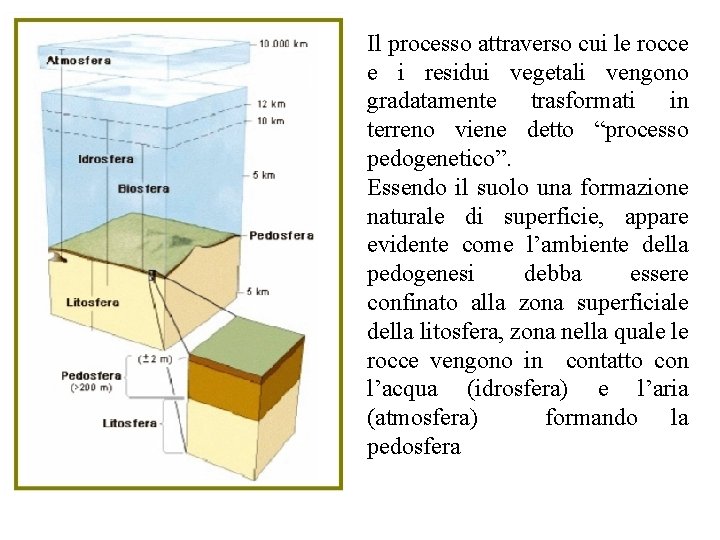
Il processo attraverso cui le rocce e i residui vegetali vengono gradatamente trasformati in terreno viene detto “processo pedogenetico”. Essendo il suolo una formazione naturale di superficie, appare evidente come l’ambiente della pedogenesi debba essere confinato alla zona superficiale della litosfera, zona nella quale le rocce vengono in contatto con l’acqua (idrosfera) e l’aria (atmosfera) formando la pedosfera
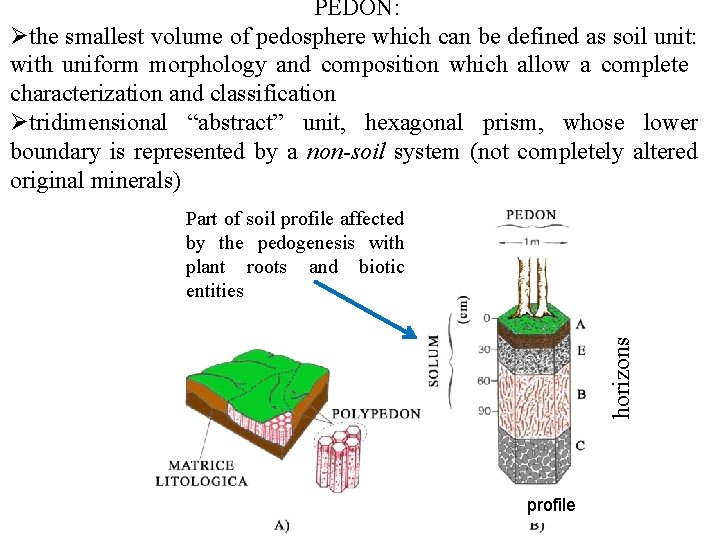
PEDON: Øthe smallest volume of pedosphere which can be defined as soil unit: with uniform morphology and composition which allow a complete characterization and classification Øtridimensional “abstract” unit, hexagonal prism, whose lower boundary is represented by a non-soil system (not completely altered original minerals) horizons Part of soil profile affected by the pedogenesis with plant roots and biotic entities profile
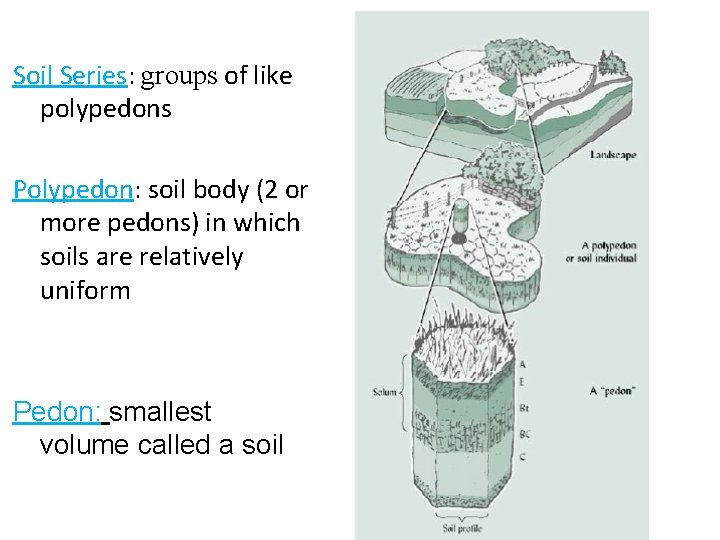
Soil Series: groups of like polypedons Polypedon: soil body (2 or more pedons) in which soils are relatively uniform Pedon: smallest volume called a soil

Idrosfera: L’idrosfera è rappresentata dal complesso delle masse di acqua che poggiano sulla litosfera. Fanno parte di tale complesso le acque degli oceani, dei fiumi e dei laghi e le acque radenti che cadono con la pioggia sul terreno e lo attraversano fino a giungere alle falde freatiche per essere poi convogliate ai fiumi e quindi al mare. Le acque, all’evaporazione, lasciano un residuo fisso costituito soprattutto da sali minerali oltre che da sostanze organiche disciolte e liberano gas che sono poi quelli atmosferici. L’acqua a causa della sua natura polare costituisce un solvente ideale per i composti inorganici che tutti, più o meno sensibilmente, si sciolgono in essa ionizzandosi in corrispondenza dei legami eteropolari. Tale fenomeno è provocato dall’azione schermante che l’acqua esercita quando viene attratta dalle cariche positive o negative del legame eteropolare. Ogni ione viene pertanto idratato, ossia circondato da una nube di molecole d’acqua opportunamente orientate. È a causa di tale fenomeno che tutti i sali in acqua subiscono la dissociazione elettrolitica scindendosi in cationi ed anioni.

Weak lnteractions in Aqueous Systems Hydrogen bonds between water molecules provide the cohesive forces that make water a liquid at room temperature and favor the extreme ordering of molecules that is typical of crystalline water (ice). Polar biomolecules dissolve readily in water because they can replace water interactions with more energetically favorable water solute interactions. In contrast, non polar biomolecules interfere with water interactions but are unable to form water salute interactions consequently, nonpolar molecules are poorly soluble in water. In aqueous solutions, nonpolar molecules tend to cluster together. Hydrogen bonds and ionic, hydrophobic (Greek, "water fearing"), and van der Waals interactions are individually weak, but collectively they have a very significant influence on the three dimensional structures of proteins, nucleic acids, polysaccharides, and membrane lipids.
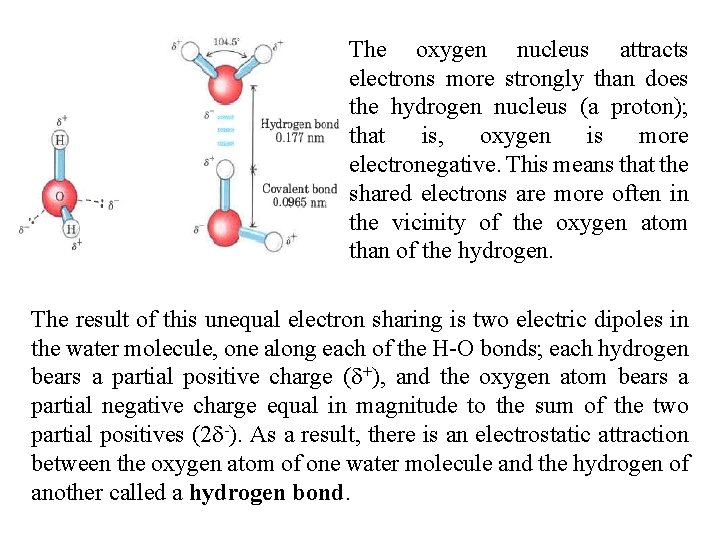
The oxygen nucleus attracts electrons more strongly than does the hydrogen nucleus (a proton); that is, oxygen is more electronegative. This means that the shared electrons are more often in the vicinity of the oxygen atom than of the hydrogen. The result of this unequal electron sharing is two electric dipoles in the water molecule, one along each of the H O bonds; each hydrogen bears a partial positive charge (d+), and the oxygen atom bears a partial negative charge equal in magnitude to the sum of the two partial positives (2 d ). As a result, there is an electrostatic attraction between the oxygen atom of one water molecule and the hydrogen of another called a hydrogen bond.

Water is effective in screening the electrostatic interactions between dissolved ions because it has a high dielectric constant, a physical property that reflects the number of dipoles in a solvent. The strength, or force (F), of ionic interactions in a solution depends on the magnitude of the charges (Q), the distance between the charged groups (r), and the dielectric constant (e, which is dimensionless) of the solvent in which the interactions occur: For water at 25 °C, e is 78. 5, and for the very nonpolar solvent benzene, e is 4. 6. Thus, ionic interactions between dissolved ions are much stronger in less polar environments
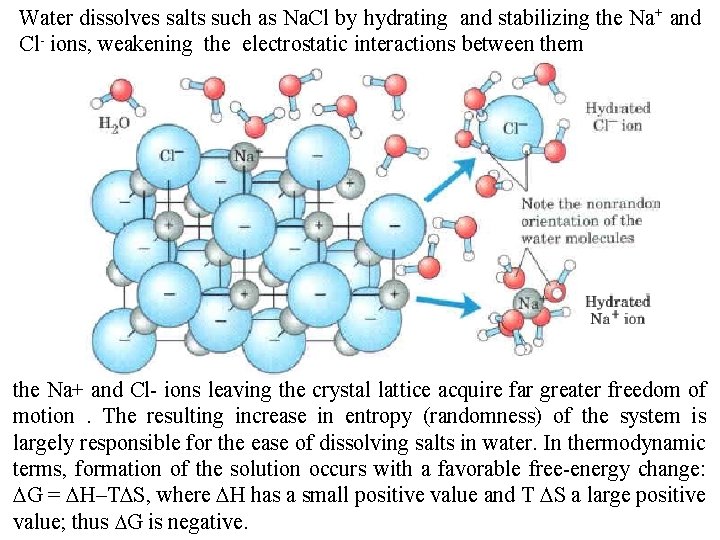
Water dissolves salts such as Na. Cl by hydrating and stabilizing the Na+ and Cl ions, weakening the electrostatic interactions between them the Na+ and Cl ions leaving the crystal lattice acquire far greater freedom of motion. The resulting increase in entropy (randomness) of the system is largely responsible for the ease of dissolving salts in water. In thermodynamic terms, formation of the solution occurs with a favorable free energy change: DG = DH–TDS, where DH has a small positive value and T DS a large positive value; thus DG is negative.

È a causa di tale fenomeno che tutti i sali in acqua subiscono la dissociazione elettrolitica scindendosi in cationi ed anioni. Questi, non essendo altro che acidi e basi, hanno tutti la possibilità teorica di reagire con l’acqua (che è un composto anfotero) con il seguente meccanismo di reazione: Tale fenomeno caratterizzato da una reazione acido base in cui il ruolo della base o quello dell’acido è svolto dall’acqua, si chiama idrolisi. L’idrolisi si definisce acida se l’acqua comportandosi da base si appropria di un protone dando luogo ad uno ione H 3 O+, diminuendo il p. H della soluzione. L’idrolisi si definisce basica se l’acqua comportandosi da acido cede un protone dando luogo ad un OH che favorendo l’aumento del p. H della soluzione.

Molti ioni non posseggono forza acida o basica sufficiente per reagire con l’acqua e vengono pertanto definiti ioni non idrolizzabili. Tale non reattività per gli ioni monoatomici è dovuta o al basso valore di elettronegatività che non consente loro di accettare elettroni (Na+, K+, Mg 2+, Ca 2+) o all’elevata elettronegatività che non consente loro di cedere elettroni (F , Cl , Br , I ). Per gli ioni poliatomici (NO 3 , SO 42 ) la non reattività è da mettere in relazione con la loro altissima stabilizzazione per risonanza, come accade per gli ioni nitrato e solfato:
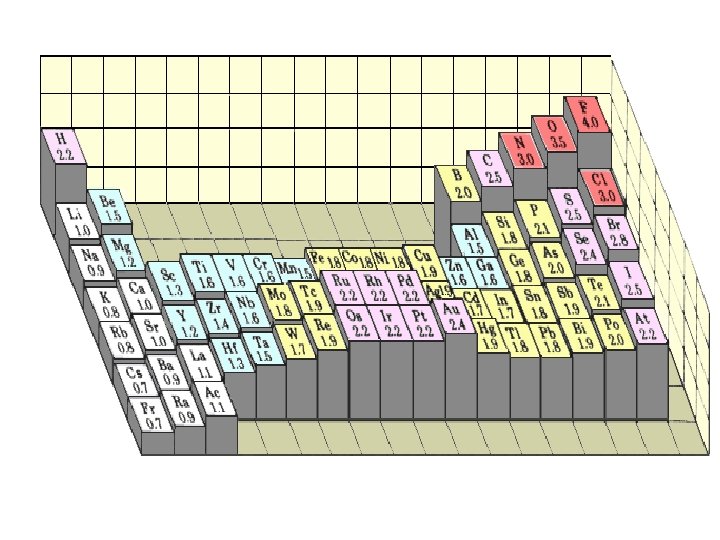
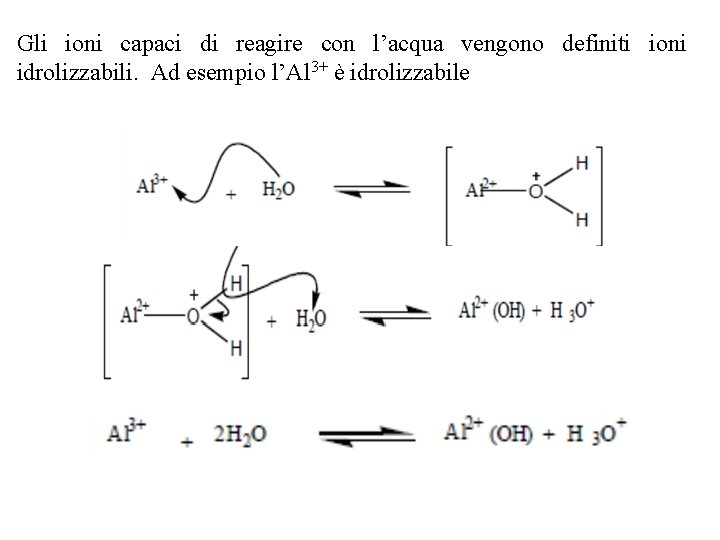
Gli ioni capaci di reagire con l’acqua vengono definiti ioni idrolizzabili. Ad esempio l’Al 3+ è idrolizzabile
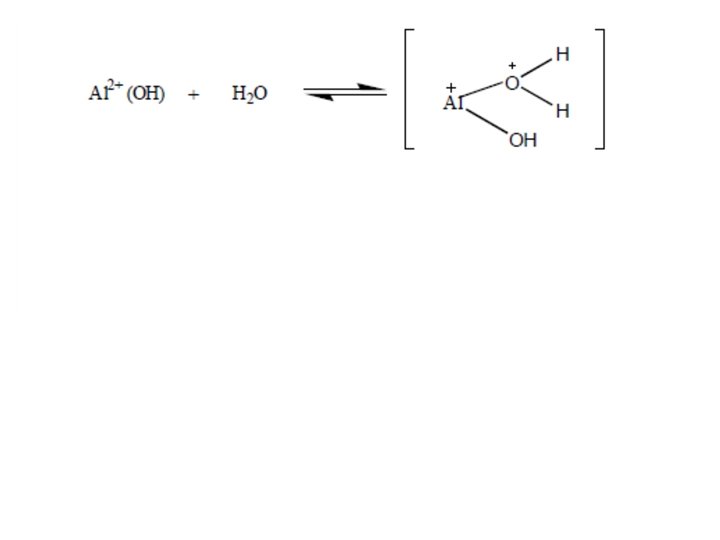
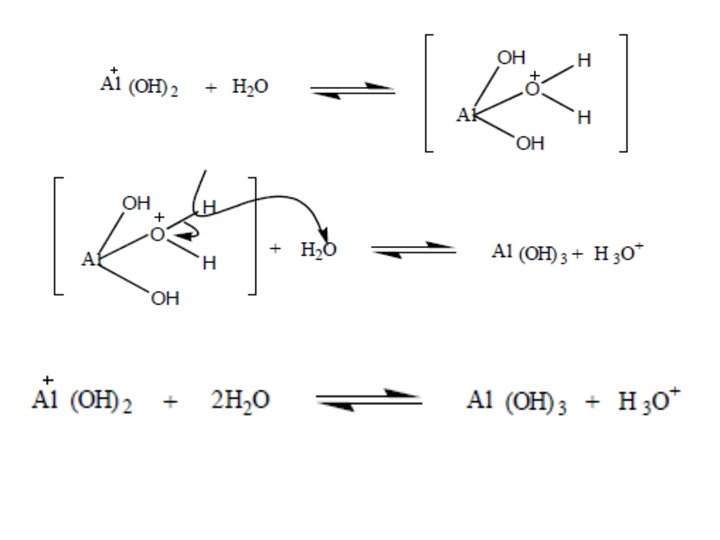
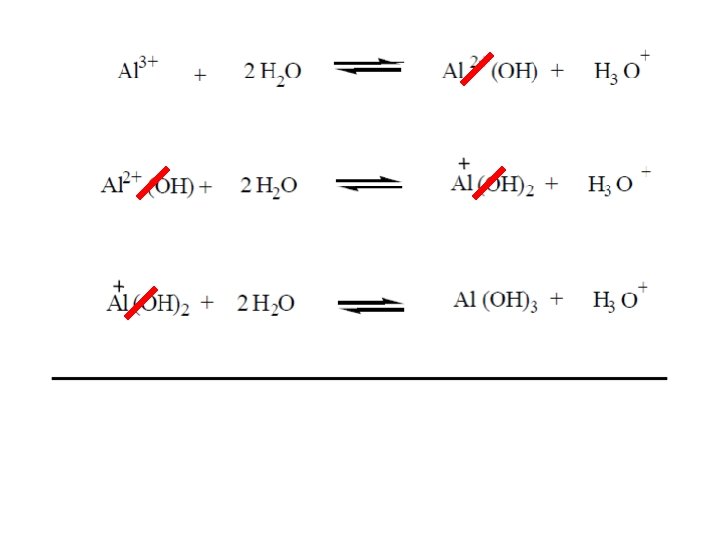

e idrolizzabili sono anche gli ioni Fe 2+, Fe 3+, Cu 2+, Zn 2+ e NH 4+. Per quanto riguarda gli anioni il CO 32 è idrolizzabile: idrolizzabili sono anche gli ioni HCO 3 , Si. O 44 , PO 43 , HPO 42 , H 2 PO 4 , L’idrolisi può non interessare solo gli ioni, ma anche molecole neutre come acidi o basi: In conclusione la soluzione circolante del suolo a causa del potere solvente dell’acqua e della sua capacità di comportarsi da acido e da base non è mai pura e risulta essere una soluzione contenente un numero elevatissimo di sostanze disciolte compresi inoltre disciolti in quantità variabile tutti i gas presenti nell’atmosfera ed, in sospensione, colloidi di varia natura.

L’atmosfera che avvolge la terra per uno spessore di qualche centinaio di chilometri è costituta da una miscela di gas, la cui composizione qualitativa e quantitativa è soggetta a variazioni mano che ci si allontana dalla crosta terrestre. La parte che più direttamente interessa la chimica del suolo è costituita da uno strato spesso una decina di chilometri che si trova ad immediato contatto con la superficie terrestre e che prende il nome di troposfera.

La concentrazione dei costituenti principali dell’aria si mantiene teoreticamente costante, in base al gran numero di trasformazioni a cui essi prendono parte. Si pensi ad esempio, a tutti i fenomeni ossidativi, spontanei o causati dall’uomo che, impegnando enormi quantitativi di ossigeno, riversano nell’atmosfera notevoli quantità di CO 2. A ristabilire in parte la concentrazione di CO 2 nell’aria provvedono altri fenomeni naturali come la fotosintesi e l’azione tamponante delle acque che è conseguenza della reazione tra H 2 O e CO 2. La solubilità dei gas normalmente presenti nell’atmosfera è regolata dalla legge di Henry: a temperatura costante la concentrazione di un gas poco solubile disciolto in un liquido è proporzionale alla pressione parziale del gas nella fase gassosa sovrastante la soluzione ossia è costante il rapporto tra pressione parziale di un gas poco solubile e la sua concentrazione nella fase liquida:
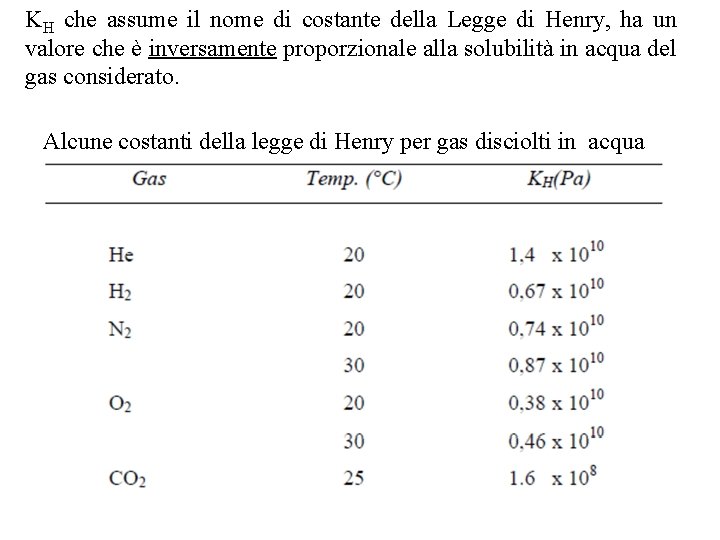
KH che assume il nome di costante della Legge di Henry, ha un valore che è inversamente proporzionale alla solubilità in acqua del gas considerato. Alcune costanti della legge di Henry per gas disciolti in acqua
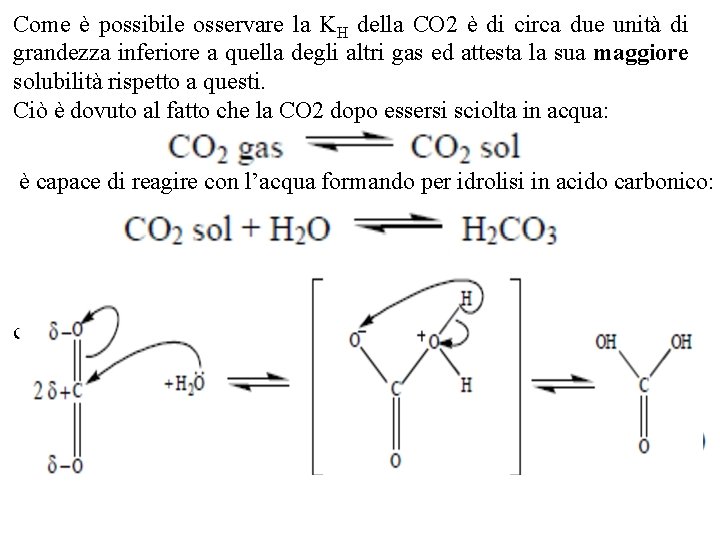
Come è possibile osservare la KH della CO 2 è di circa due unità di grandezza inferiore a quella degli altri gas ed attesta la sua maggiore solubilità rispetto a questi. Ciò è dovuto al fatto che la CO 2 dopo essersi sciolta in acqua: è capace di reagire con l’acqua formando per idrolisi in acido carbonico: che, a sua volta, da luogo alle seguenti reazioni di idrolisi:

Frazione molare È interessante osservare anche l’idrolisi della CO 2 da luogo a due anioni idrolizzabili quali l’HCO 3 ed il CO 32 che, come vedremo, rivestono nel sistema suolo un ruolo molto importante e la cui concentrazione nella soluzione del terreno è strettamente dipendente dal p. H. Gli aspetti quantitativi di tale dipendenza sono evidenziati applicando la legge di azione di massa alle reazioni precedenti: p. H Dissociazione dell’acido carbonico in ioni carbonato in funzione del p. H
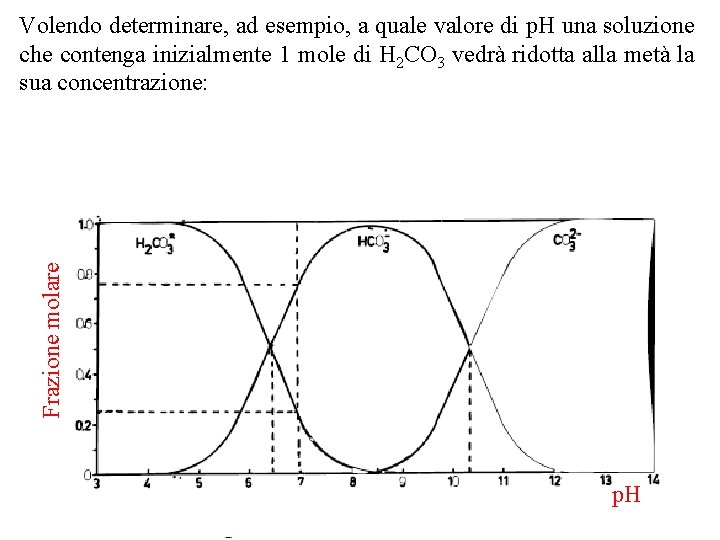
Frazione molare Volendo determinare, ad esempio, a quale valore di p. H una soluzione che contenga inizialmente 1 mole di H 2 CO 3 vedrà ridotta alla metà la sua concentrazione: p. H

In maniera analoga applicando la legge di azione di massa si può verificare che la concentrazione di ioni HCO 3 e CO 32 sono le stesse a p. H = 10, 25. Viceversa se vogliamo calcolare quali concentrazioni di HCO 3 e H 2 CO 3 si hanno a p. H = 7 :
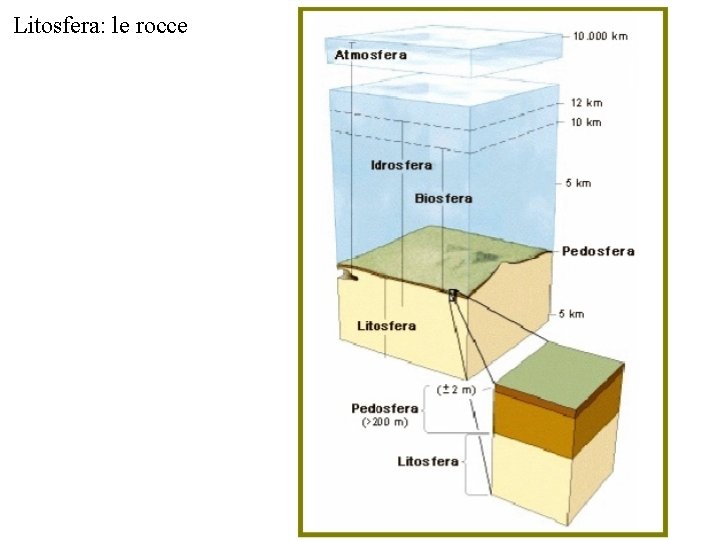
Litosfera: le rocce Si definisce litosfera lo strato roccioso che ricopre la superficie terrestre. Esso rappresenta il materiale principale per la formazione di terreno. Una roccia viene generalmente definita come un aggregato di minerali originatosi in conseguenza di un determinato fenomeno geologico. Le rocce possono includere minerali appartenenti tutti alla medesima specie, come i calcari formati da cristalli di calcite e le dolomie formate da cristalli di dolomite, ma più spesso comprendono minerali riferibili a più specie come il granito che risulta formato da un aggregato di cristalli di quarzo, di feldspati (es. ortoclasio) e da miche (generalmente biotite). Le rocce si dividono in tre gruppi: rocce eruttive o ignee, rocce sedimentarie e rocce metamorfiche o scistoso cristalline. Le rocce eruttive, che costituiscono circa l’ 88% della crosta terrestre ed il 25% delle rocce affioranti, derivano dalla consolidazione di masse fuse (magmi) presenti in zone più o meno profonde della crosta terrestre.
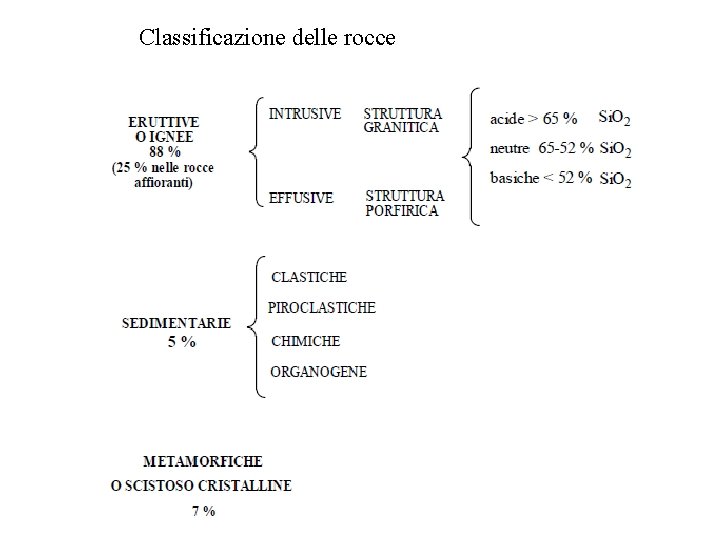
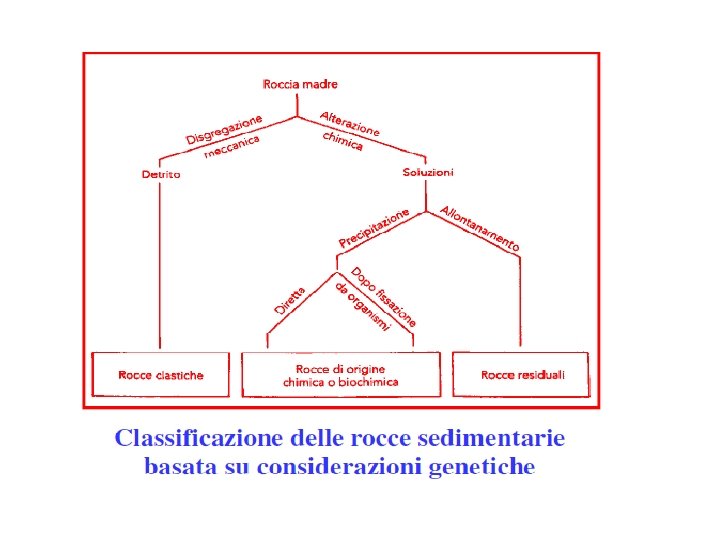
Classificazione delle rocce

Le rocce formatesi per attività magmatica possono essere classificate in intrusive, se si sono originate per consolidamento del magma in profondità, lentamente e sotto altissime pressioni dando alla massa il tempo per la sua completa cristallizzazione, e in effusive se il consolidamento è avvenuto in superficie, in modo rapido in seguito ad una repentina diminuzione della temperatura e della pressione. Nelle rocce intrusive, per il lento accrescimento di pochi centri di cristallizzazione, si ha la formazione di un numero ridotto di cristalli di dimensioni relativamente grandi. La roccia corrispondente si presenta più o meno equigranulare (struttura granulare o granitica). Le rocce effusive, al contrario, sono caratterizzate da un gran numero di centri di cristallizzazione che portano alla formazione di cristalli di piccole dimensioni. La roccia risulta costituita da pasta fondamentale microcristallina o vetrosa (struttura porfirica). Dal punto di vista della composizione chimica, le rocce eruttive vengono comunemente distinte in rocce acide o ipersiliciche, con più del 65% di Si. O 2, rocce neutre o mesosiliciche con il 65% 52% di Si. O 2 e rocce basiche o iposiliciche con meno del 52% di Si. O 2



Le rocce sedimentarie che costituiscono circa il 5% della crosta terrestre e, insieme alle rocce metamorfiche, il 75% delle rocce affioranti, sono costituite da rocce preesistenti di qualsiasi origine, che hanno subito un’alterazione più o meno profonda. Le rocce sedimentarie si suddividono in clastiche, piroclastiche, chimiche ed organogene. Le rocce sedimentarie clastiche sono quelle formatesi per degradazione, trasporto, eventuale trasformazione ed accumulo di frammenti di roccia. Le rocce sedimentarie piroclastiche sono quelle che derivano dalla deposizione subaerea e subacquea di materiali detritici proiettati nelle fasi esplosive dell’attività vulcanica. Le rocce sedimentarie chimiche sono quelle che si originano per insolubilizzazione di sali in seno all’acqua, generalmente per evaporazione di quest’ultima. I calcari ed il gesso sono i componenti più importanti di questo gruppo. Le rocce sedimentarie organogene sono quelle formatesi per accumulo di materiale organico e si distinguono in calcaree, carboniose (torba e carboni fossili), silicee (farina fossile), fosfatiche (guano e fosforiti) e bituminose (petrolio e bitumi). (https: //youtube/l 5 Xyak. Ig. Z 2 Y)



Le rocce metamorfiche o scistoso cristalline, infine, sono rocce che derivano da profonde trasformazioni subite dalle rocce eruttive e sedimentarie in particolari condizioni di temperatura, di elevate pressioni ed in presenza di acqua. Le caratteristiche della maggior parte delle rocce metamorfiche sono la cristallizzazione di tutti i componenti e la tessitura scistosa determinata da un particolare orientamento dei diversi elementi che si sviluppano in piani paralleli, normali alla direzione di massima pressione.
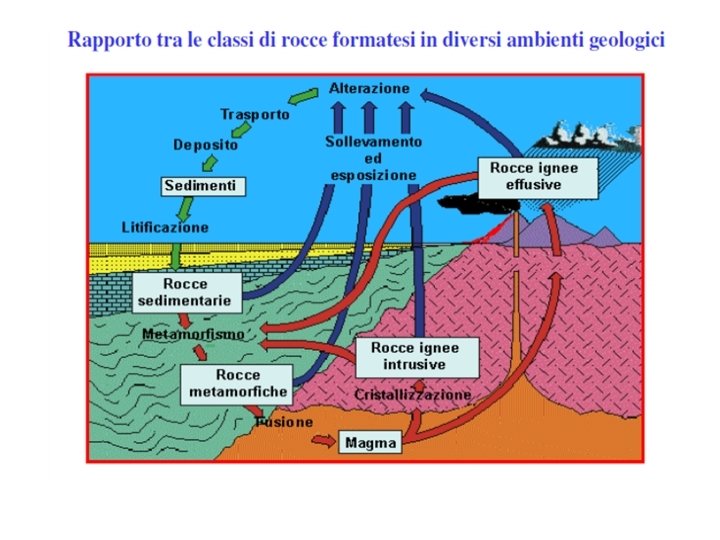
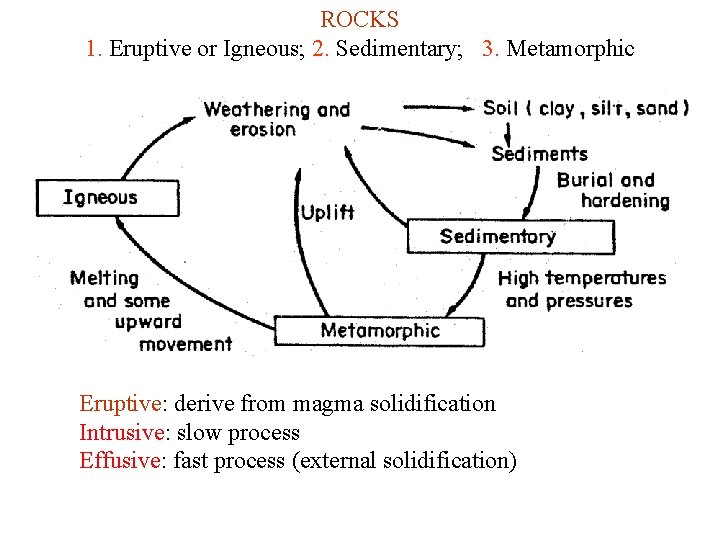
ROCKS 1. Eruptive or Igneous; 2. Sedimentary; 3. Metamorphic Eruptive: derive from magma solidification Intrusive: slow process Effusive: fast process (external solidification)
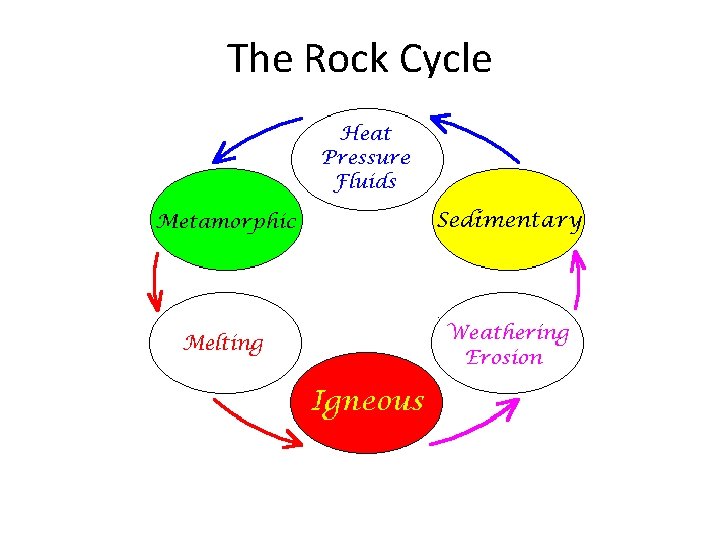
The Rock Cycle

I minerali: si definiscono minerali le sostanze inorganiche naturali con composizione chimica costante o variabile entro precisi limiti caratterizzate da specifiche proprietà fisiche a struttura cristallina con disposizione ordinata tridimensionale di atomi e ioni. Sono le unità fondamentali di cui sono costituite le rocce e si suddividono in primari, se formatisi nel processo di solidificazione del magma fuso e secondari, se provenienti da processi di alterazione. Gli strati superiori della litosfera risultano costituiti prevalentemente da silicati (92%) composti principalmente da silicio e ossigeno e per circa l’ 8% da minerali diversi (non silicati) : ossidi e idrossidi, carbonati, solfati, cloruri, solfuri, fosfati e nitrati. Tralasciando i minerali altamente solubili o meno rappresentati, che solo in condizioni eccezionali prendono parte alla formazione del suolo agrario, in questa sede si prenderanno in esame soltanto i carbonati, i solfati, i fosfati, gli ossidi e idrossidi e in modo particolare i silicati.
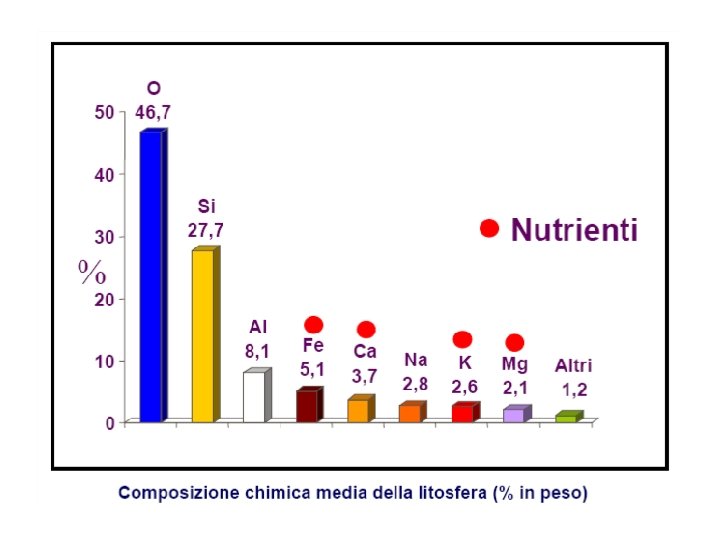

Carbonati: nella litosfera sono presenti carbonati di cationi alcalino terrosi (Ca, Mg e Ba) e di altri cationi bivalenti quali Zn, Fe, Mn, Sr e Pb perchè, essendo insolubili o comunque poco solubili, vengono sottratti alla lisciviazione. Tra questi il più importante è da considerare il carbonato di calcio in quanto può entrare in quantità anche piuttosto elevate nella composizione del terreno. Il Ca. CO 3, che fa parte delle rocce sedimentarie, può avere origine chimica ed organogena. La reazione tra ioni calcio contenuti nelle rocce eruttive e la CO 2 dell’atmosfera con il concorso dell’acqua spiega la genesi del carbonato di calcio di origine chimica.
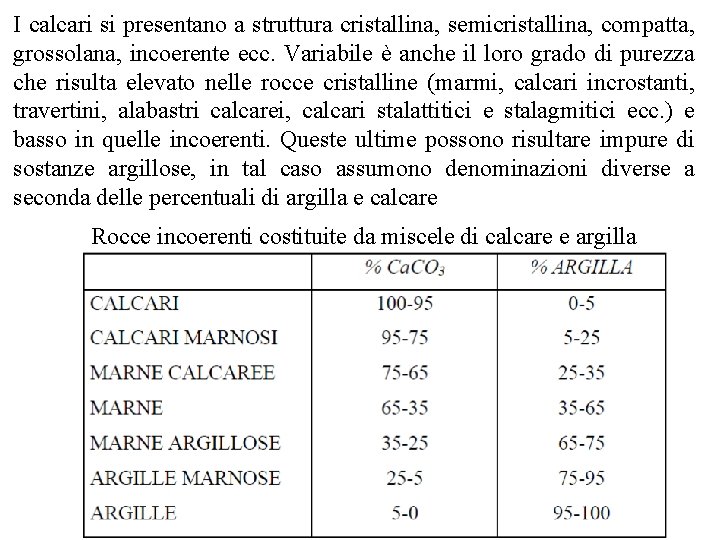
I calcari si presentano a struttura cristallina, semicristallina, compatta, grossolana, incoerente ecc. Variabile è anche il loro grado di purezza che risulta elevato nelle rocce cristalline (marmi, calcari incrostanti, travertini, alabastri calcarei, calcari stalattitici e stalagmitici ecc. ) e basso in quelle incoerenti. Queste ultime possono risultare impure di sostanze argillose, in tal caso assumono denominazioni diverse a seconda delle percentuali di argilla e calcare Rocce incoerenti costituite da miscele di calcare e argilla
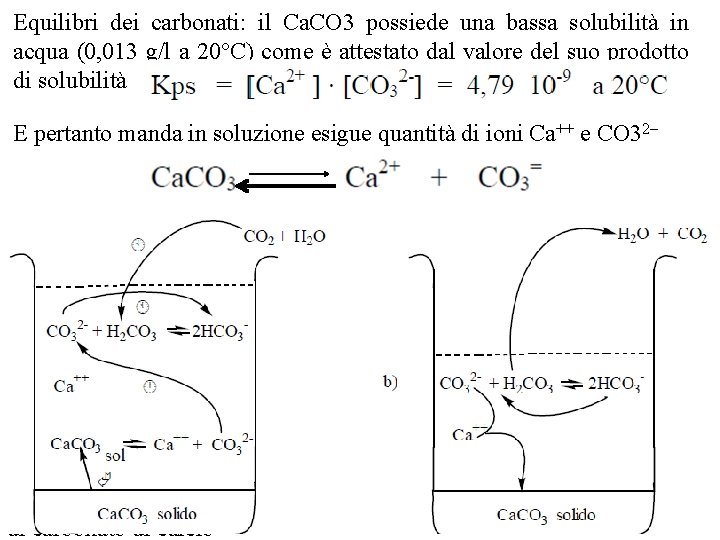
Equilibri dei carbonati: il Ca. CO 3 possiede una bassa solubilità in acqua (0, 013 g/l a 20°C) come è attestato dal valore del suo prodotto di solubilità E pertanto manda in soluzione esigue quantità di ioni Ca++ e CO 32– subisce un incremento di solubilità se l’acqua contiene CO 2. Questa, infatti, reagisce con l’acqua per dare acido carbonico che, a sua volta, si combina con la base CO 32 con formazione di ioni bicarbonato La diminuzione della concentrazione degli ioni CO 32 consente una ulteriore solubilizzazione di Ca. CO 3 fino a che gli ioni CO 32 prodotti ripristinano il valore originario del prodotto di solubilità. Quando le acque ricche di ioni Ca++ e HCO 3 perdono CO 2 (perchè, ad esempio, la pressione parziale nell’atmosfera diminuisce) o H 2 O (per evaporazione) tutti gli equilibri suindicati si spostano verso sinistra con riprecipitazione di carbonato di calcio
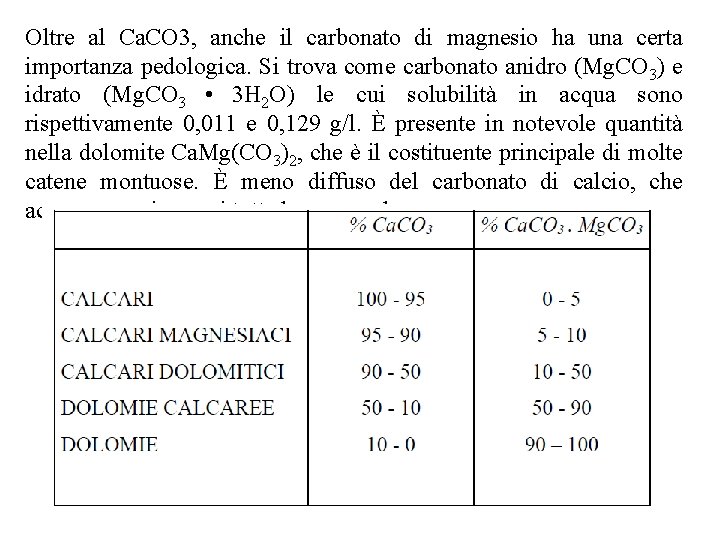
Oltre al Ca. CO 3, anche il carbonato di magnesio ha una certa importanza pedologica. Si trova come carbonato anidro (Mg. CO 3) e idrato (Mg. CO 3 • 3 H 2 O) le cui solubilità in acqua sono rispettivamente 0, 011 e 0, 129 g/l. È presente in notevole quantità nella dolomite Ca. Mg(CO 3)2, che è il costituente principale di molte catene montuose. È meno diffuso del carbonato di calcio, che accompagna in quasi tutte le rocce calcaree

Solfati Il solfato più importante dal punto di vista pedologico è quello di calcio. In natura si rinviene come gesso (Ca. SO 4 · 2 H 2 O) e come anidrite (Ca. SO 4) e si sarebbe formato per cristallizzazione in seguito all’evaporazione di ingenti masse di acque, marine o lacustri, rimaste intrappolate in ampi bacini. Il formarsi, durante l’evaporazione, dell’uno o dell’altro sale, dipende dalla temperatura e dal grado di salinità delle acque. Da soluzioni contenenti quasi esclusivamente ioni Ca++ e SO 42 si ha precipitazione di gesso sotto i 42°C e di anidrite al di sopra di tale temperatura. In presenza però di quantità crescenti di ioni Cl e Na+ la soglia critica (42°C) si abbassa fino a 25°C. Pertanto se la precipitazione avviene a temperature inferiori a 25°C si ha sempre formazione di gesso, se avviene a temperature superiori a 42°C si ha sempre formazione di anidrite, mentre nell’intervallo tra le due temperature la qualità della deposizione dipenderà dal tenore di cloruro di sodio dell’acqua. L’anidrite è presente normalmente negli strati profondi dove trova le indispensabili condizioni per la stabilità. Quando a causa di movimenti tellurici affiora in superficie e viene in contatto con l’acqua si trasforma in gesso con un aumento di volume del 60%. Il solfato di calcio di superficie è infatti esclusivamente sotto forma di gesso.

Fosfati Si rinvengono in natura soprattutto come apatite, la cui formula generale è 3 Ca 3(PO 4)2 ∙ Ca. X con X = CO 3, (OH, )2, F 2 etc si rinvengono anche come vivianite [Fe 3 (PO 4)2 · 8 H 2 O], strengite [Fe. PO 4 · 2 H 2 O], variscite [Al. PO 4 · 2 H 2 O] e come fosforite, che contiene una varietà di Ca 3(PO 4)2 amorfo detto collofanite Fosfato tricalcico è presente anche nei cosiddetti guani che si fanno derivare dalla mineralizzazione di spoglie e di escrementi di uccelli. I guani contengono, oltre al fosfato tricalcico, carbonato di calcio, sali potassici e composti azotati.

Silicati: la materia allo stato solido, presenta ben definite forme geometriche, in quanto le particelle materiali di cui è costituita sono legate le une alle altre da forze che le costringono a disporsi secondo particolari motivi geometrici. I reticoli cristallini, che si riscontrano nella maggior parte dei silicati, presentano legami tra le particelle che sono essenzialmente di tipo eteropolare e quindi non direzionale. Con poche eccezioni i minerali sono caratterizzati da strutture ioniche, in cui un catione è legato a ioni di carica opposta Nella disposizione spaziale delle particelle in seno ai reticoli cristallini il numero di atomi che possono disporsi intorno ad un’altro è limitato dalla possibilità che le particelle hanno di venire in intimo contatto tra di loro, possibilità che è direttamente legata alle dimensioni delle particelle stesse. Nel caso dei reticoli ionici, ad esempio, ogni catione attrarrà a se tanti anioni quanti possono essergli tangenti. Il numero di ioni che possono disporsi intorno ad un altro prende il nome di numero di coordinazione, che è appunto dipendente dalle dimensioniche delle particelle che costituiscono l’edificio cristallino.
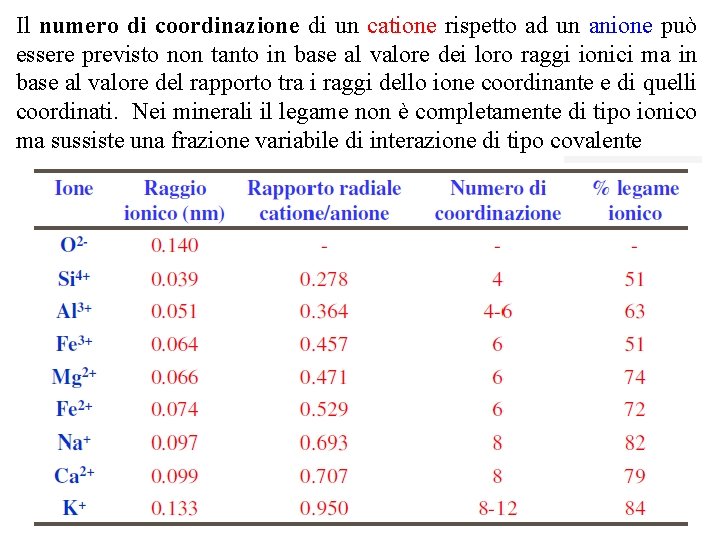
Il numero di coordinazione di un catione rispetto ad un anione può essere previsto non tanto in base al valore dei loro raggi ionici ma in base al valore del rapporto tra i raggi dello ione coordinante e di quelli coordinati. Nei minerali il legame non è completamente di tipo ionico ma sussiste una frazione variabile di interazione di tipo covalente

In base a considerazioni geometriche, se il rapporto tra il raggio ionico del catione e quello dell’anione (r+/r ) assume valori ideali o teorici pari a 0. 225, 0. 414, 0. 732 e 1. 000, i numeri di coordinazione teorici diventano 4, 6, 8 e 12, corrispondenti alle classi tetraedrica, ottaedrica, esaedrica ed icosaedrica, rispettivamente. I rapporti anzidetti dovrebbero essere vincolanti se gli ioni fossero sfere rigide e indeformabili. Essendo invece sfere elastiche (nucleo e orbitali elettronici) e quindi deformabili il valore del rapporto r+/r non è necessario sia esattamente quello ideale, ma basta che vi si avvicini. Coordinazione tetraedrica Coordinazione ottaedrica
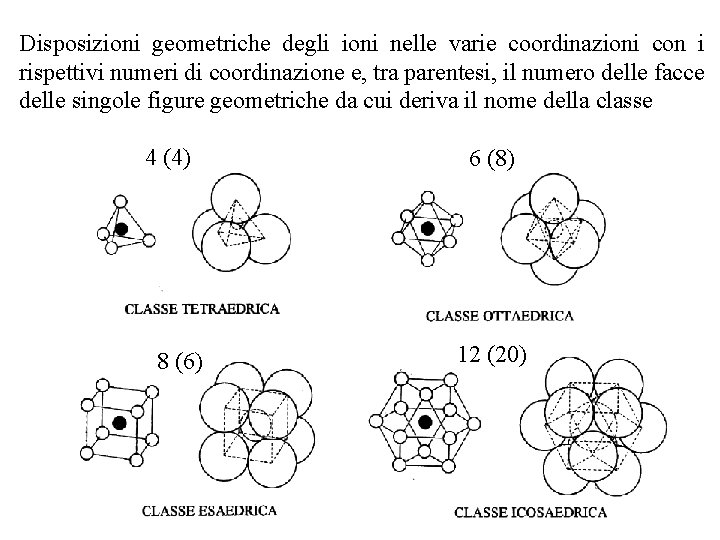
Disposizioni geometriche degli ioni nelle varie coordinazioni con i rispettivi numeri di coordinazione e, tra parentesi, il numero delle facce delle singole figure geometriche da cui deriva il nome della classe 4 (4) 8 (6) 6 (8) 12 (20)

con l’ossigeno il silicio assuma una coordinazione esclusivamente tetraedrica (perchè il rapporto del suo raggio ionico con quello dell’ossigeno è molto più vicino a 0, 225 che a 0, 414), l’alluminio, il litio, ferro trivalente, il magnesio, il ferro bivalente ed il manganese assumono coordinazione ottaedrica (perchè i rapporti dei loro raggi ionici con quello dell’ossigeno sono più vicini a 0, 414 che a 0, 225), il sodio ed il calcio assumono coordinazione esaedrica (perchè i valori dei rapporti dei loro raggi ionici con quello dell’ossigeno sono più vicini a 0, 732 che a 0, 414) Infine, il potassio ed il bario assumono coordinazione icosaedrica (perchè i valori dei rapporti dei loro raggi ionici con quello dell’ossigeno sono prossimi ad 1 che rappresenta il valore ideale).
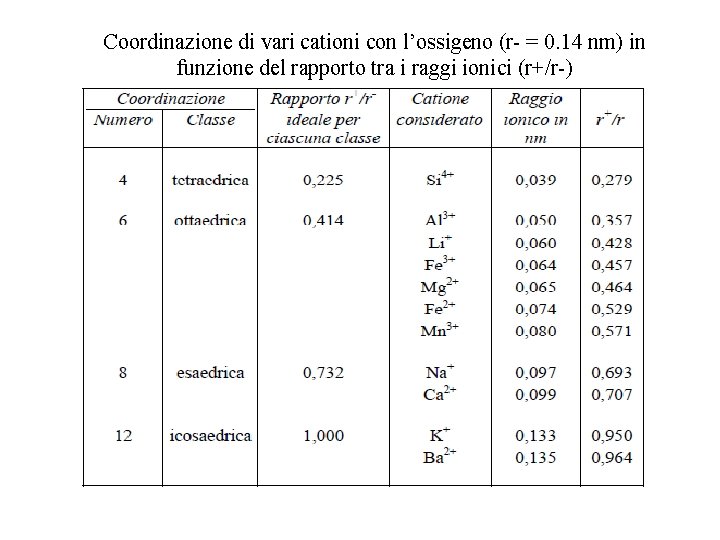
Coordinazione di vari cationi con l’ossigeno (r = 0. 14 nm) in funzione del rapporto tra i raggi ionici (r+/r )
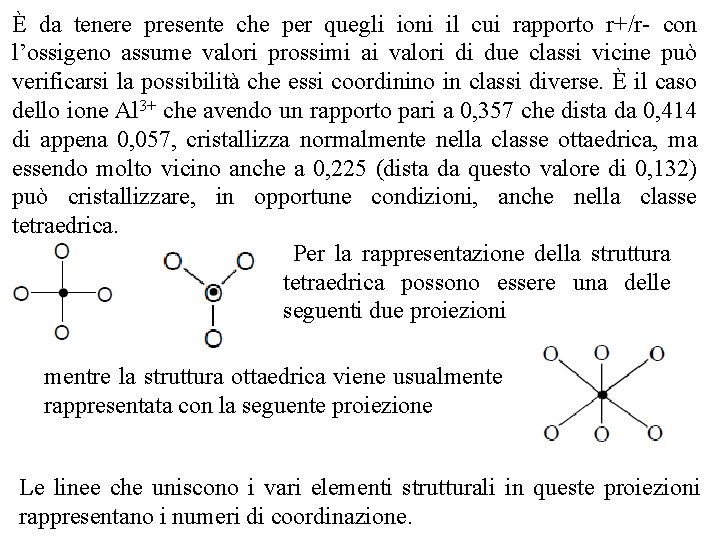
È da tenere presente che per quegli ioni il cui rapporto r+/r con l’ossigeno assume valori prossimi ai valori di due classi vicine può verificarsi la possibilità che essi coordinino in classi diverse. È il caso dello ione Al 3+ che avendo un rapporto pari a 0, 357 che dista da 0, 414 di appena 0, 057, cristallizza normalmente nella classe ottaedrica, ma essendo molto vicino anche a 0, 225 (dista da questo valore di 0, 132) può cristallizzare, in opportune condizioni, anche nella classe tetraedrica. Per la rappresentazione della struttura tetraedrica possono essere una delle seguenti due proiezioni mentre la struttura ottaedrica viene usualmente rappresentata con la seguente proiezione Le linee che uniscono i vari elementi strutturali in queste proiezioni rappresentano i numeri di coordinazione.
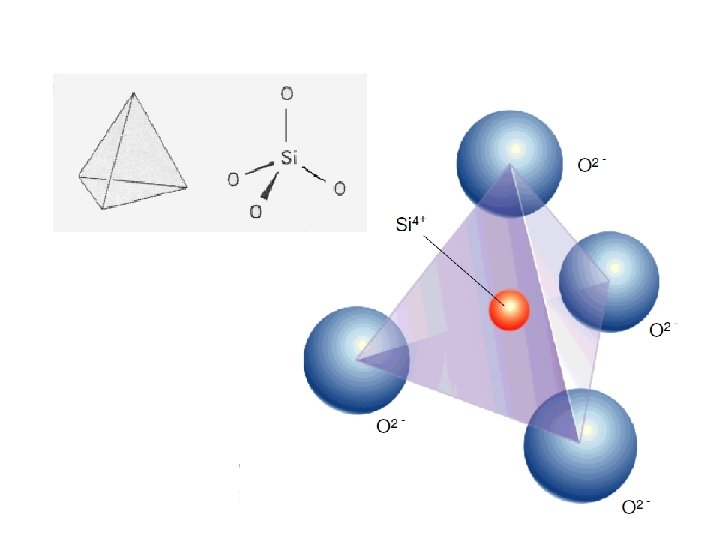
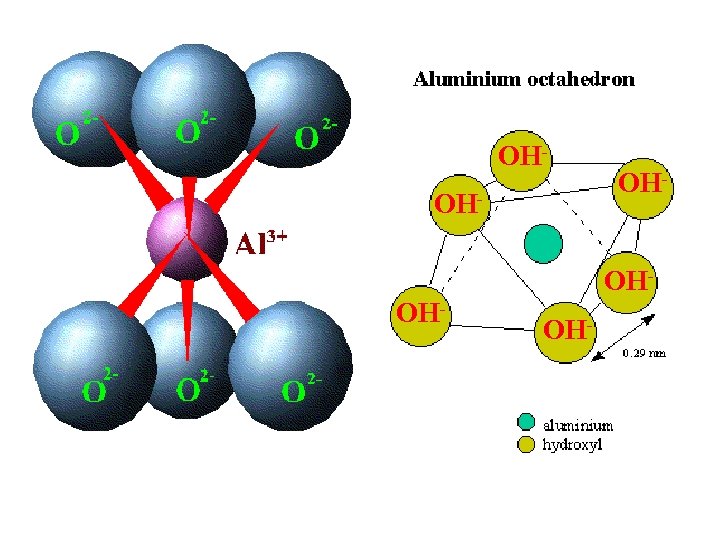
OHOH- OH-
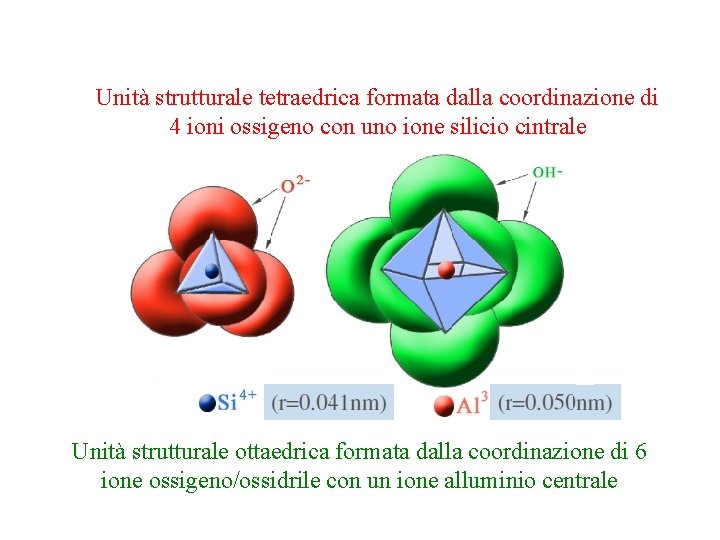
Unità strutturale tetraedrica formata dalla coordinazione di 4 ioni ossigeno con uno ione silicio cintrale Unità strutturale ottaedrica formata dalla coordinazione di 6 ione ossigeno/ossidrile con un ione alluminio centrale

I silicati vengono raggruppati in cinque classi (nesosilicati, sorosilicati, inosilicati, fillosilicati e tectosilicati) che differiscono per il modo con il quale i tetraedri si concatenano in seno al reticolo.
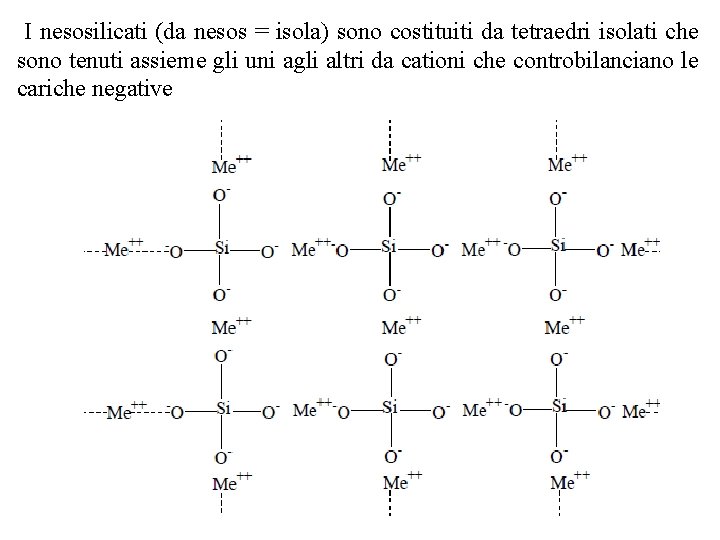
I nesosilicati (da nesos = isola) sono costituiti da tetraedri isolati che sono tenuti assieme gli uni agli altri da cationi che controbilanciano le cariche negative Si. O 44
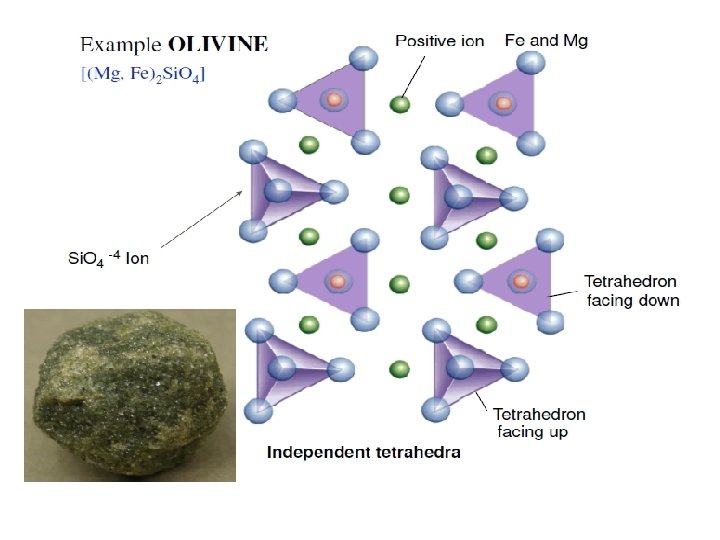
I costituenti più importanti di questa classe sono le olivine, costituite da miscele isomorfe di fosterite (Mg 2 Si. O 4) e fayalite (Fe 2 Si. O 4), i cui cationi che legano la struttura base Si. O 44 sono Mg++ e Fe++ ed i granati di formula generale R 32+ R 23+ (Si. O 4)3 con R 2+ = Ca 2+, Mg 2+, Fe 2+ e Mn 2+ e R 3+ = Al 3+, Fe 3+ e Cr 3+. I nesosilicati offrono resistenza molto diversa ai processi di alterazione chimica. Mentre le olivine sono fra i silicati meno stabili, i granati sono molto resistenti e rimangono inalterati tra i prodotti della decomposizione.
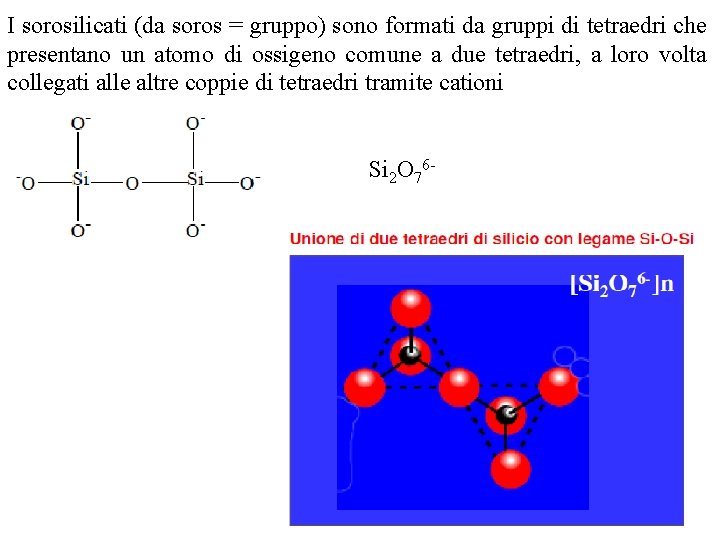
I sorosilicati (da soros = gruppo) sono formati da gruppi di tetraedri che presentano un atomo di ossigeno comune a due tetraedri, a loro volta collegati alle altre coppie di tetraedri tramite cationi Si 2 O 76
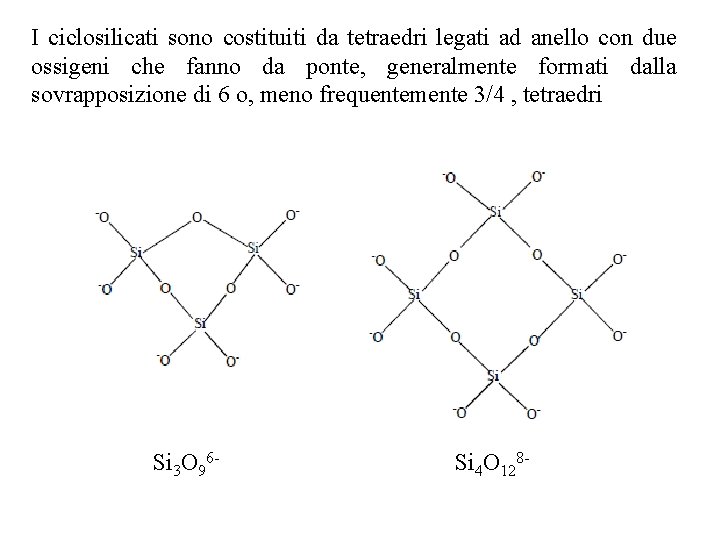
I ciclosilicati sono costituiti da tetraedri legati ad anello con due ossigeni che fanno da ponte, generalmente formati dalla sovrapposizione di 6 o, meno frequentemente 3/4 , tetraedri 6 12 Si O Si 6 O 3 189 Si 4 O 128
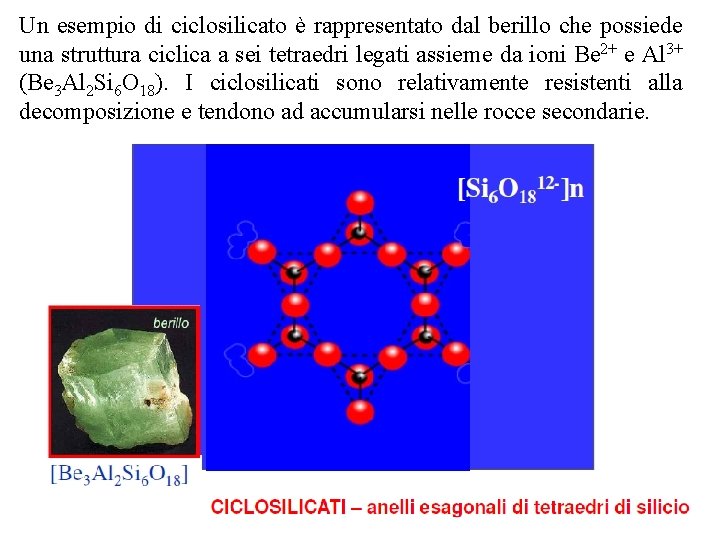
Un esempio di ciclosilicato è rappresentato dal berillo che possiede una struttura ciclica a sei tetraedri legati assieme da ioni Be 2+ e Al 3+ (Be 3 Al 2 Si 6 O 18). I ciclosilicati sono relativamente resistenti alla decomposizione e tendono ad accumularsi nelle rocce secondarie.
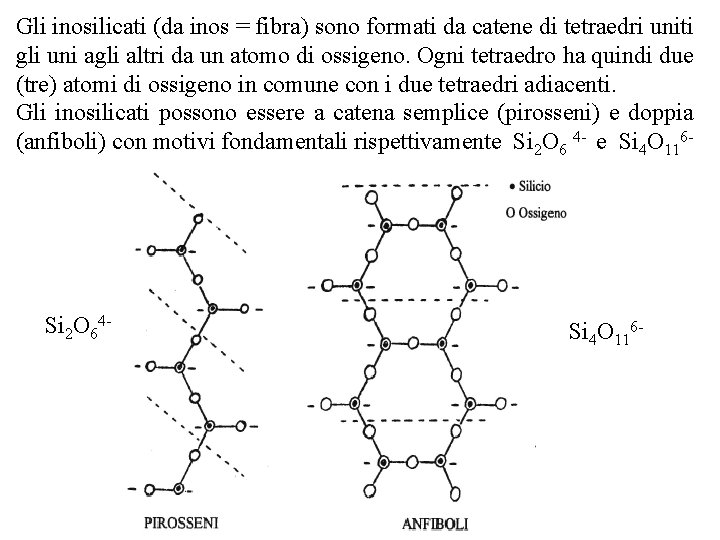
Gli inosilicati (da inos = fibra) sono formati da catene di tetraedri uniti gli uni agli altri da un atomo di ossigeno. Ogni tetraedro ha quindi due (tre) atomi di ossigeno in comune con i due tetraedri adiacenti. Gli inosilicati possono essere a catena semplice (pirosseni) e doppia (anfiboli) con motivi fondamentali rispettivamente Si 2 O 6 4 e Si 4 O 116 Si 2 O 64 Si 4 O 116
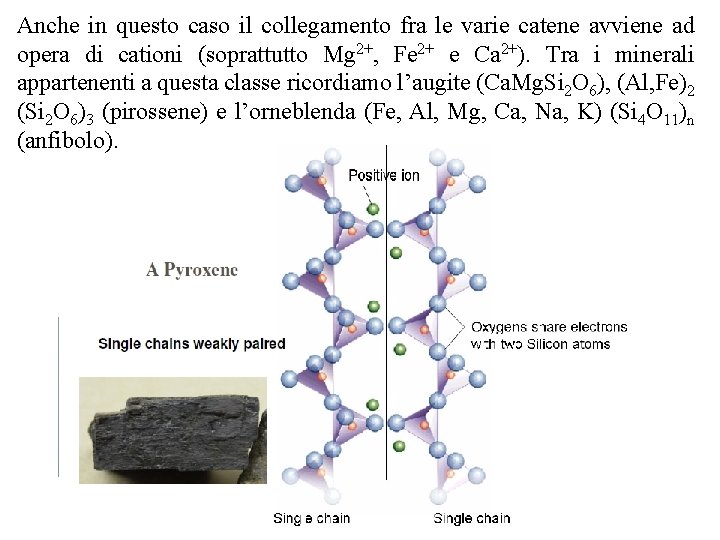
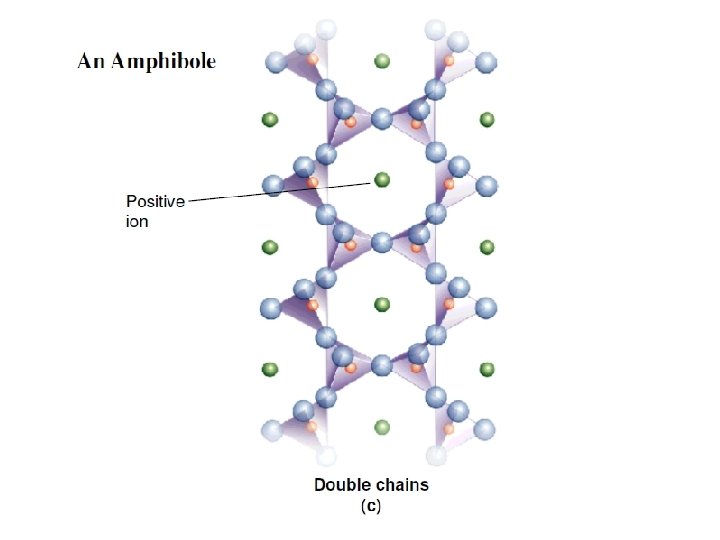
Anche in questo caso il collegamento fra le varie catene avviene ad opera di cationi (soprattutto Mg 2+, Fe 2+ e Ca 2+). Tra i minerali appartenenti a questa classe ricordiamo l’augite (Ca. Mg. Si 2 O 6), (Al, Fe)2 (Si 2 O 6)3 (pirossene) e l’orneblenda (Fe, Al, Mg, Ca, Na, K) (Si 4 O 11)n (anfibolo).
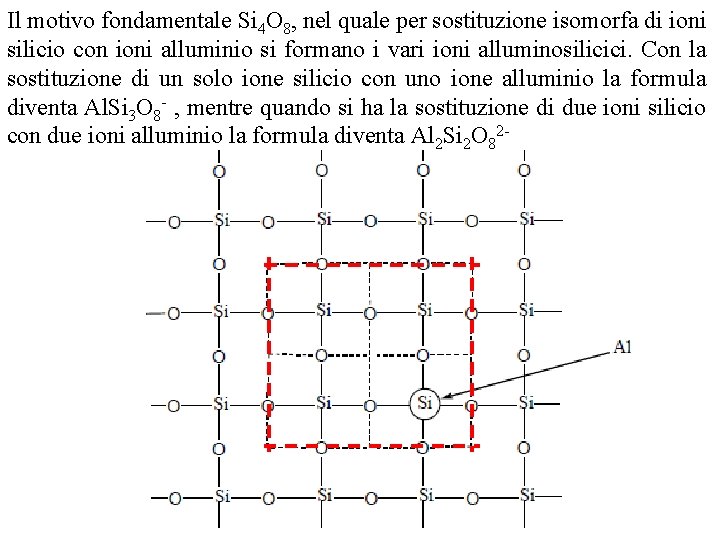
Il motivo fondamentale O 8, nel quale per sostituzione isomorfa ioni I tectosilicati (da tecton Si =4 edificio) si possono considerare derivatididalla silicio con 2 ioni formano i isomorfa vari ioni alluminosilicici. Conioni la silice (Si. O ) peralluminio parziale si sostituzione di ioni silicio con sostituzione di un struttura solo ionedella silicio con iuno alluminio la formula alluminio. Nella silice variione tetraedri di Si. O 4 sono diventa O 8 , per mentre quando si ha la sostituzione di tridimensionale due ioni silicio collegati. Al. Si fra 3 loro i vertici e assumono uno sviluppo 2 con due ioni alluminio la formulaciascun diventaatomo Al 2 Si 2 di O 8 ossigeno nel quale i tetraedri condividono Quarzo Si. O 2

Le cariche negative sono controbilanciate da cationi. Tipici rappresentanti della classe dei tectosilicati sono i feldspati e tra questi l’ortoclasio (KAl. Si 3 O 8), l’albite (Na. Al. Si 3 O 8) e l’anortite (Ca. Al 2 Si 2 O 8)
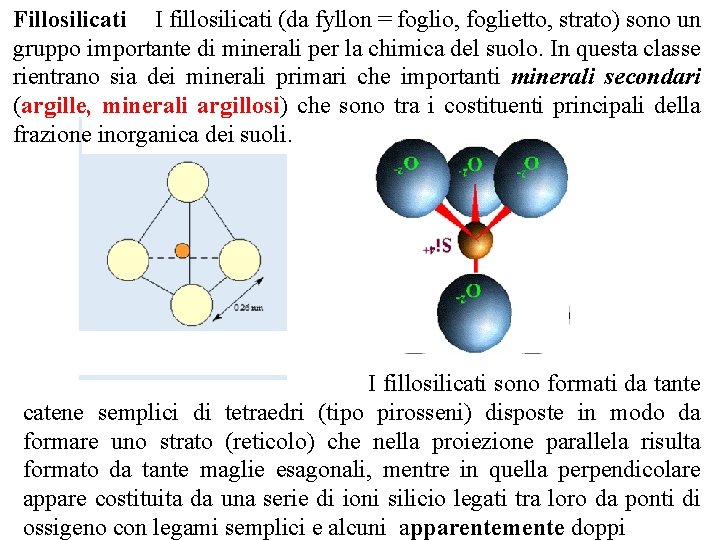
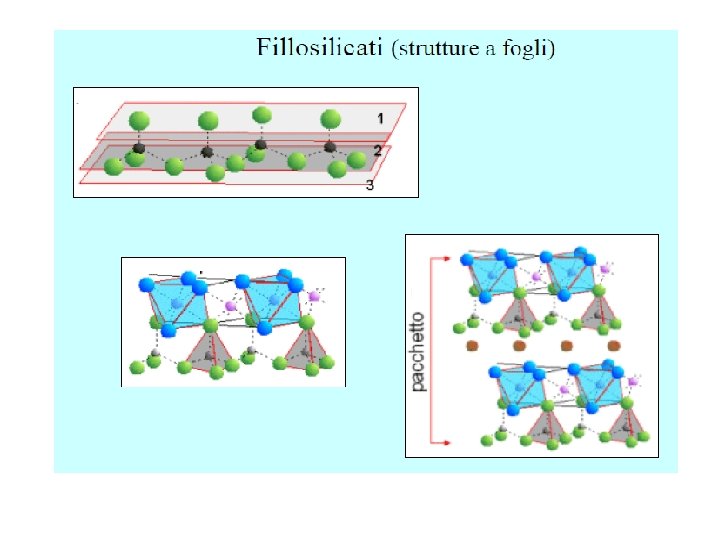
Fillosilicati I fillosilicati (da fyllon = foglio, foglietto, strato) sono un gruppo importante di minerali per la chimica del suolo. In questa classe rientrano sia dei minerali primari che importanti minerali secondari (argille, minerali argillosi) che sono tra i costituenti principali della frazione inorganica dei suoli. I fillosilicati sono formati da tante catene semplici di tetraedri (tipo pirosseni) disposte in modo da formare uno strato (reticolo) che nella proiezione parallela risulta formato da tante maglie esagonali, mentre in quella perpendicolare appare costituita da una serie di ioni silicio legati tra loro da ponti di ossigeno con legami semplici e alcuni apparentemente doppi
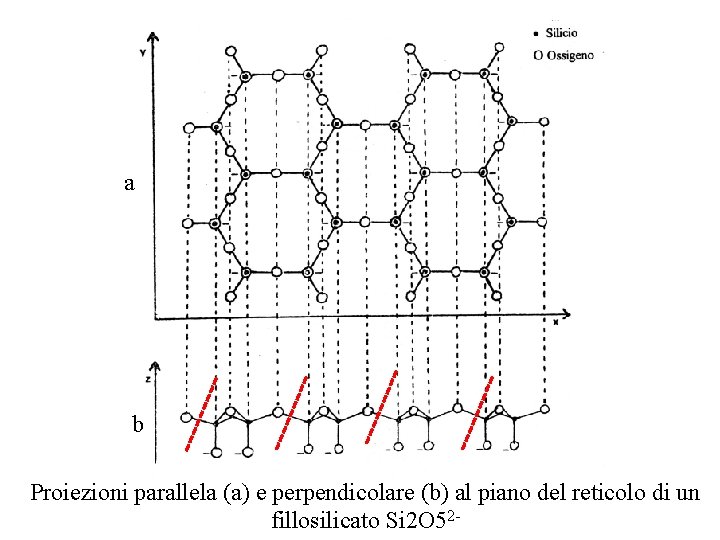
aa b Proiezioni parallela (a) e perpendicolare (b) al piano del reticolo di un fillosilicato Si 2 O 52
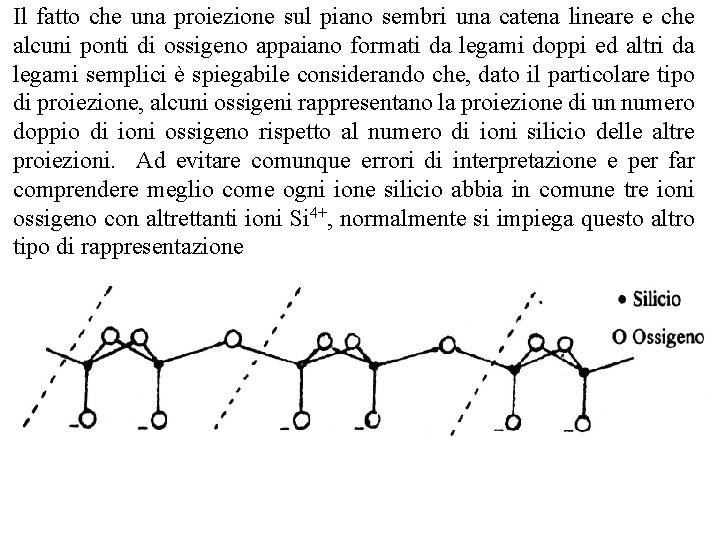
Il fatto che una proiezione sul piano sembri una catena lineare e che alcuni ponti di ossigeno appaiano formati da legami doppi ed altri da legami semplici è spiegabile considerando che, dato il particolare tipo di proiezione, alcuni ossigeni rappresentano la proiezione di un numero doppio di ioni ossigeno rispetto al numero di ioni silicio delle altre proiezioni. Ad evitare comunque errori di interpretazione e per far comprendere meglio come ogni ione silicio abbia in comune tre ioni ossigeno con altrettanti ioni Si 4+, normalmente si impiega questo altro tipo di rappresentazione
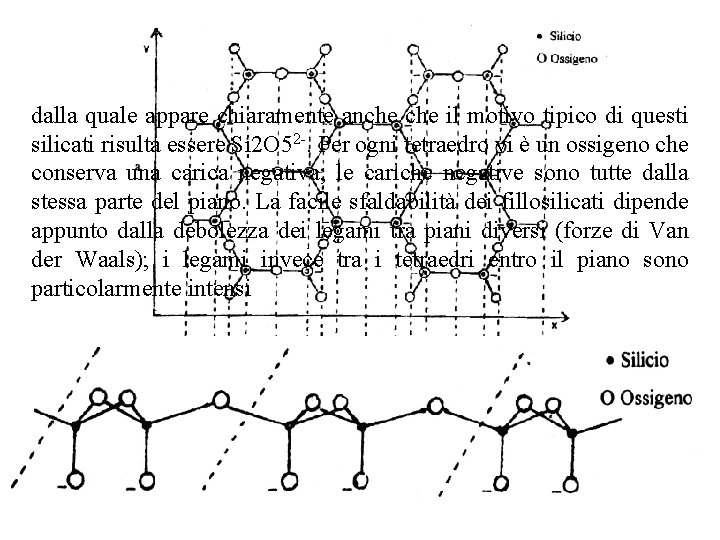
dalla quale appare chiaramente anche il motivo tipico di questi silicati risulta essere Si 2 O 52. Per ogni tetraedro vi è un ossigeno che conserva una carica negativa; le cariche negative sono tutte dalla stessa parte del piano. La facile sfaldabilità dei fillosilicati dipende appunto dalla debolezza dei legami tra piani diversi (forze di Van der Waals); i legami invece tra i tetraedri entro il piano sono particolarmente intensi
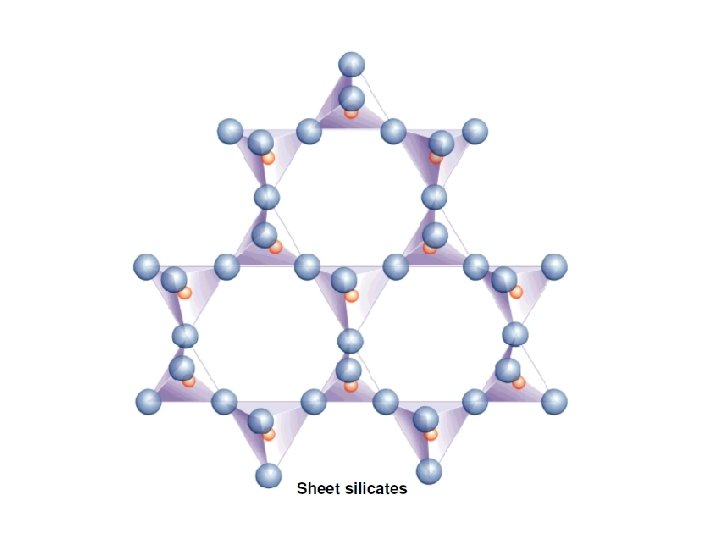
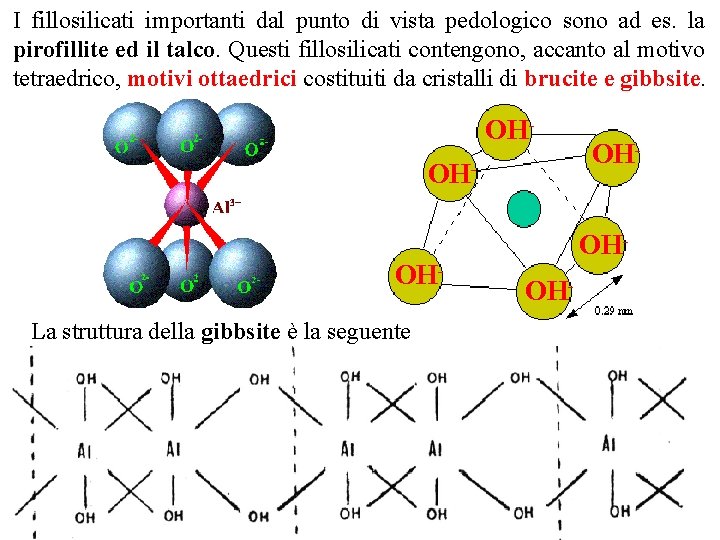
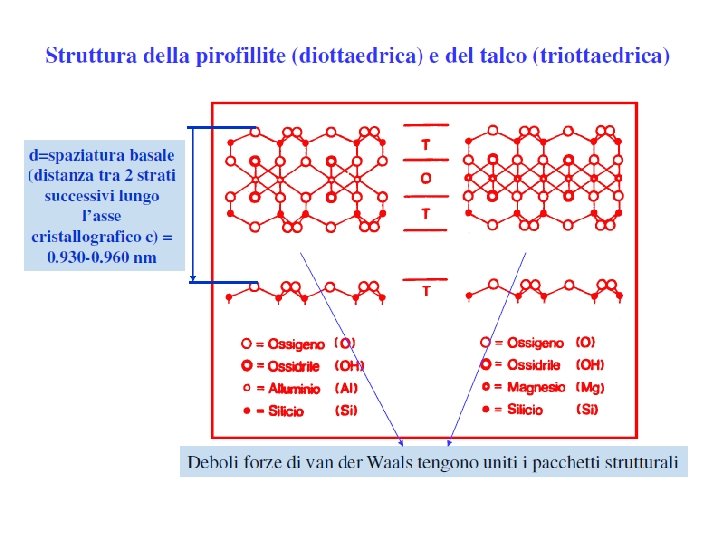
I fillosilicati importanti dal punto di vista pedologico sono ad es. la pirofillite ed il talco. Questi fillosilicati contengono, accanto al motivo tetraedrico, motivi ottaedrici costituiti da cristalli di brucite e gibbsite. OHOH- OHLa struttura della gibbsite è la seguente OHOH-
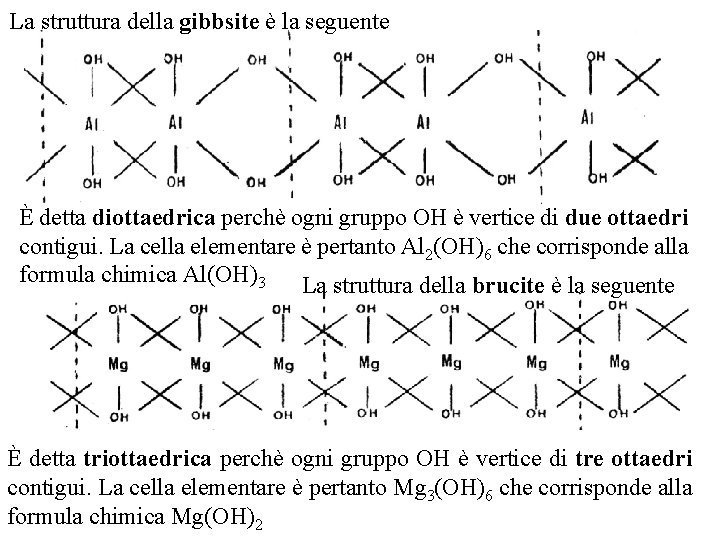
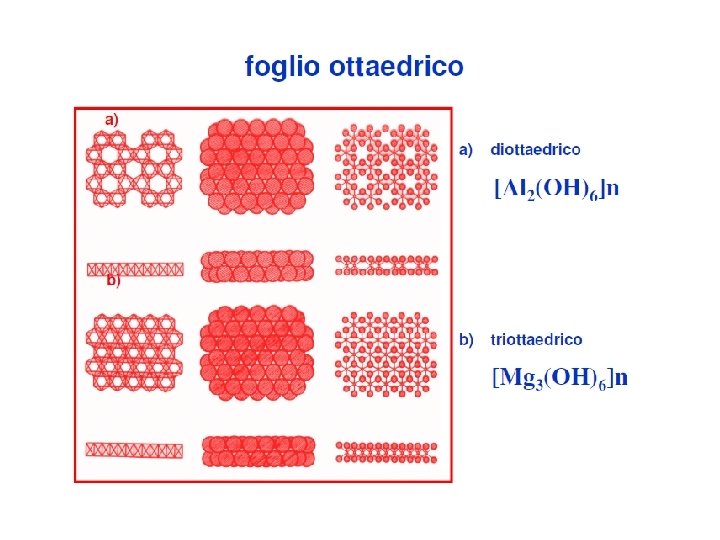
La struttura della gibbsite è la seguente È detta diottaedrica perchè ogni gruppo OH è vertice di due ottaedri contigui. La cella elementare è pertanto Al 2(OH)6 che corrisponde alla formula chimica Al(OH)3 La struttura della brucite è la seguente È detta triottaedrica perchè ogni gruppo OH è vertice di tre ottaedri contigui. La cella elementare è pertanto Mg 3(OH)6 che corrisponde alla formula chimica Mg(OH)2
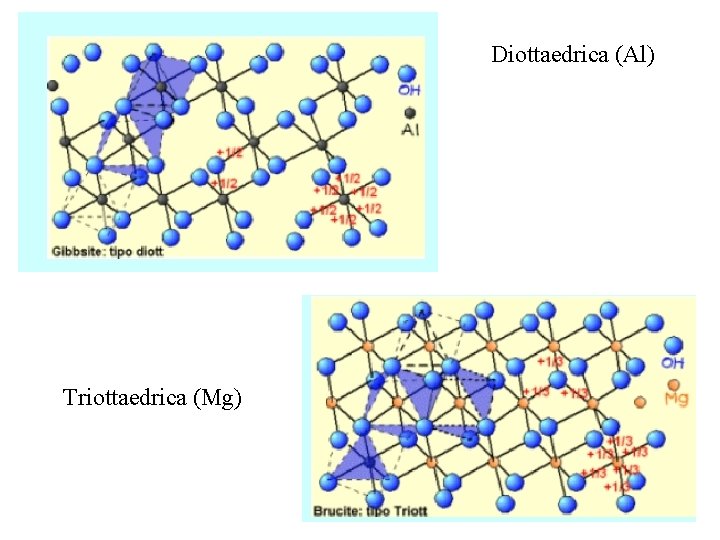
Diottaedrica (Al) Triottaedrica (Mg)
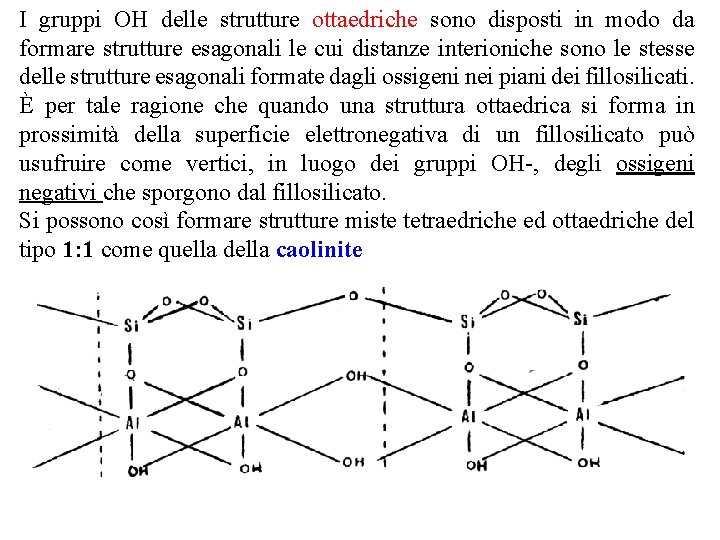
I gruppi OH delle strutture ottaedriche sono disposti in modo da formare strutture esagonali le cui distanze interioniche sono le stesse delle strutture esagonali formate dagli ossigeni nei piani dei fillosilicati. È per tale ragione che quando una struttura ottaedrica si forma in prossimità della superficie elettronegativa di un fillosilicato può usufruire come vertici, in luogo dei gruppi OH , degli ossigeni negativi che sporgono dal fillosilicato. Si possono così formare strutture miste tetraedriche ed ottaedriche del tipo 1: 1 come quella della caolinite
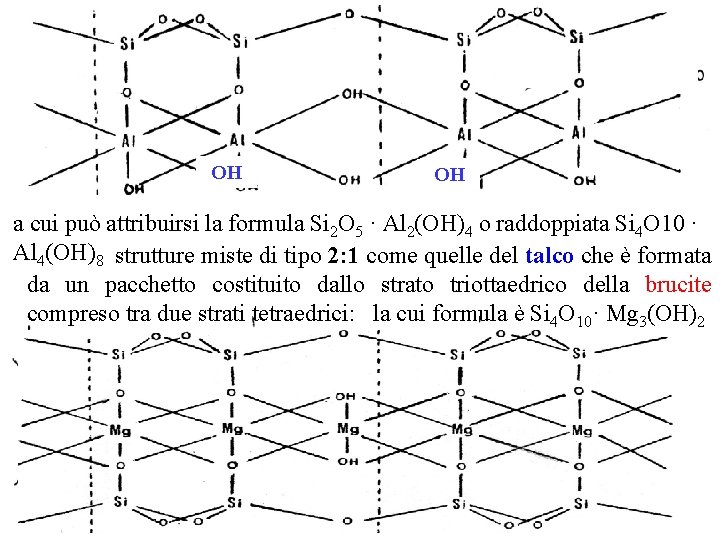
OH OH a cui può attribuirsi la formula Si 2 O 5 · Al 2(OH)4 o raddoppiata Si 4 O 10 · Al 4(OH)8 strutture miste di tipo 2: 1 come quelle del talco che è formata da un pacchetto costituito dallo strato triottaedrico della brucite compreso tra due strati tetraedrici: la cui formula è Si 4 O 10· Mg 3(OH)2
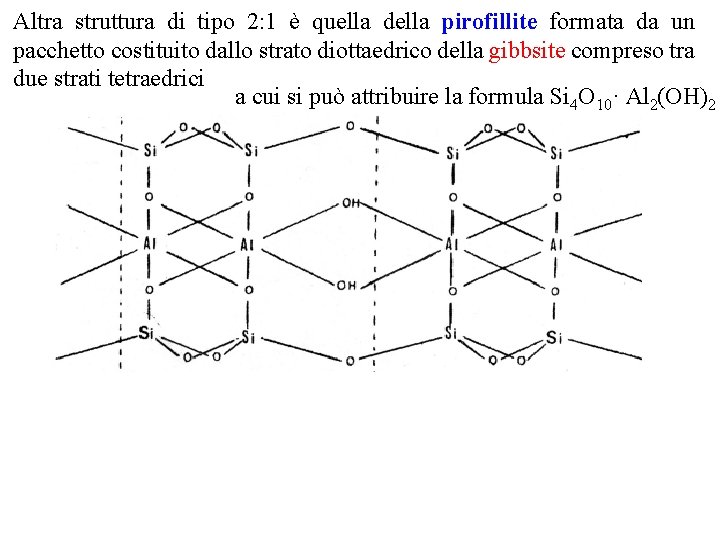
Altra struttura di tipo 2: 1 è quella della pirofillite formata da un pacchetto costituito dallo strato diottaedrico della gibbsite compreso tra due strati tetraedrici a cui si può attribuire la formula Si 4 O 10· Al 2(OH)2
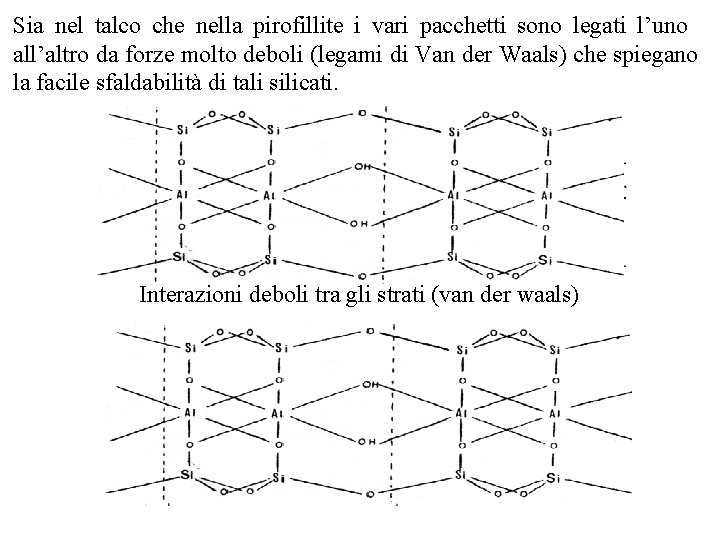
Sia nel talco che nella pirofillite i vari pacchetti sono legati l’uno all’altro da forze molto deboli (legami di Van der Waals) che spiegano la facile sfaldabilità di tali silicati. Interazioni deboli tra gli strati (van der waals)
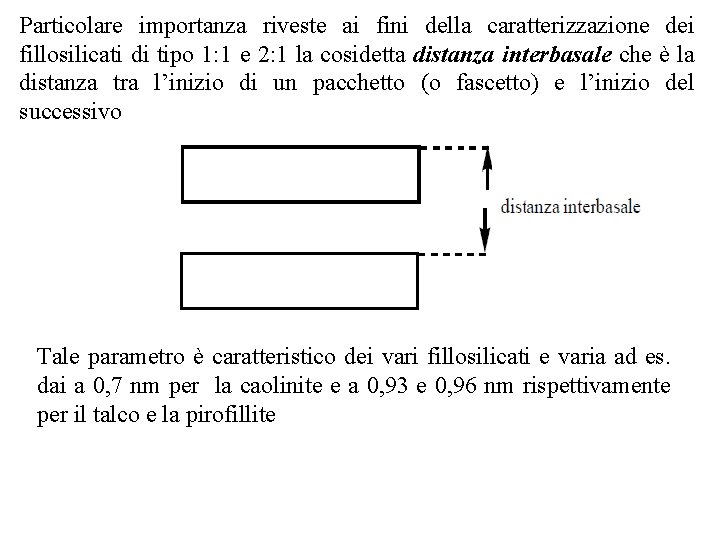
Particolare importanza riveste ai fini della caratterizzazione dei fillosilicati di tipo 1: 1 e 2: 1 la cosidetta distanza interbasale che è la distanza tra l’inizio di un pacchetto (o fascetto) e l’inizio del successivo Tale parametro è caratteristico dei vari fillosilicati e varia ad es. dai a 0, 7 nm per la caolinite e a 0, 93 e 0, 96 nm rispettivamente per il talco e la pirofillite
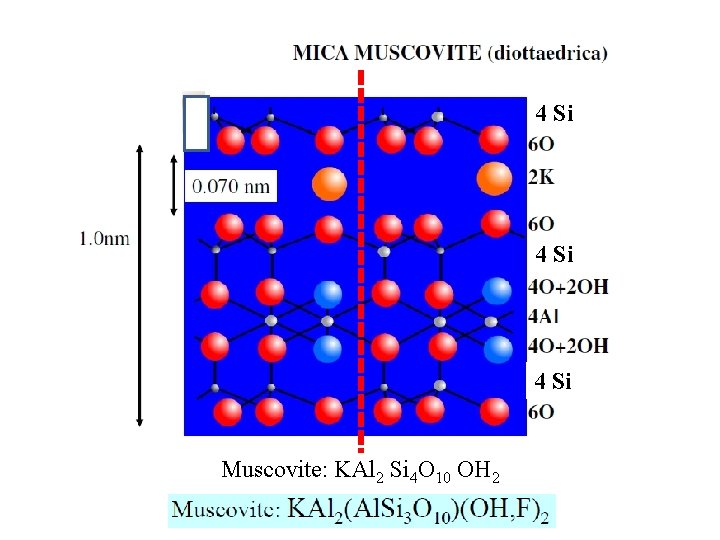
4 Si Muscovite: KAl 2 Si 4 O 10 OH 2
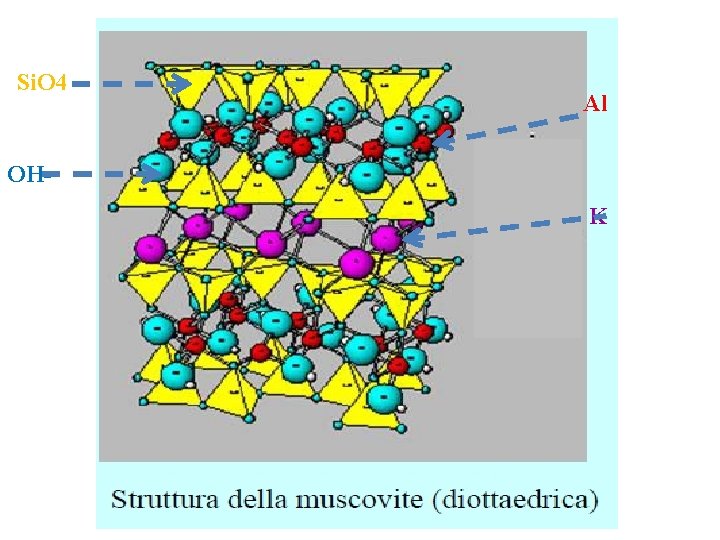
Si. O 4 Al OHK
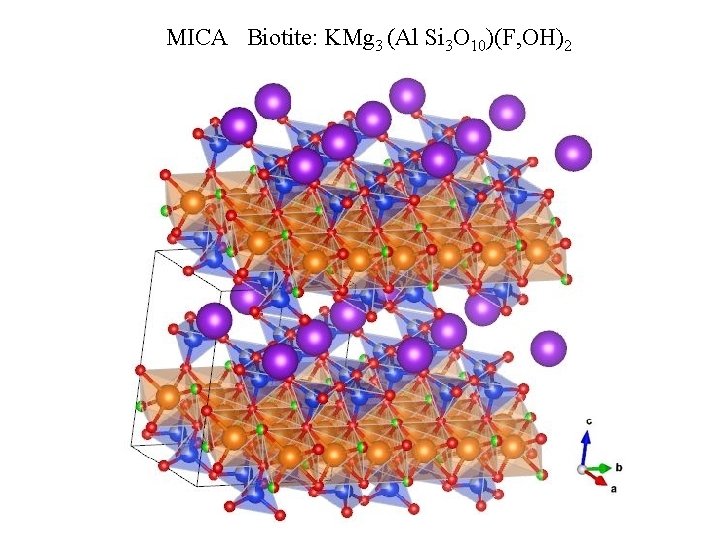
MICA Biotite: KMg 3 (Al Si 3 O 10)(F, OH)2
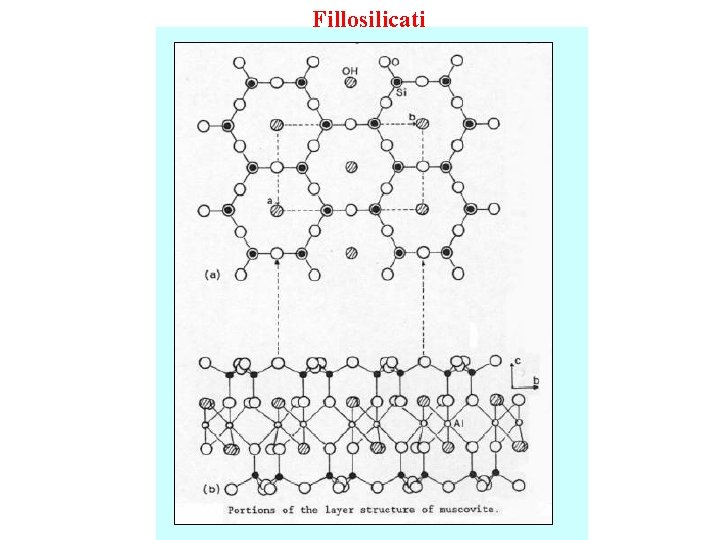
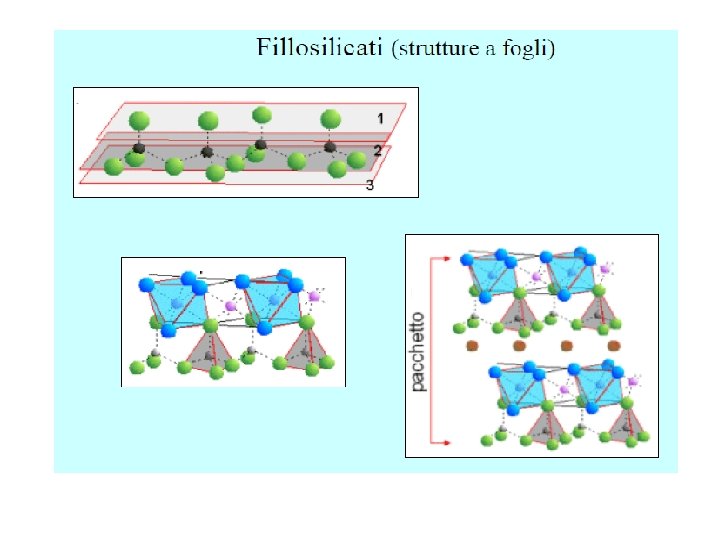
Fillosilicati



Ossidi e idrossidi Altri composti importanti ai fini pedogenetici per la formazione del suolo, oltre alla silice e ai silicati, sono gli ossidi ed idrossidi di alluminio e ferro. Gli ossidi sono una classe di minerali relativamente duri, alcuni molto duri, come il corindone, Al 2 O 3, che e’ il penultimo termine della scala di Mohs. Densi e refrattari, generalmente sono minerali accessori di rocce ignee e metamorfici e si rinvengono come minerali detritici, in particolare quelli resistenti all’alterazione superficiale dei sedimenti. Gli idrossidi sono meno duri e meno densi e sono minerali di alterazione secondaria o superficiale Col termine ossidi si intendono solidi con legami fortemente ionici di ioni O 2 e cationi metallici. Descrivibili anche attraverso l’impacchettamento compatto di ioni O 2 con i cationi che vanno a occupare cavità ottaedriche e tetraedriche
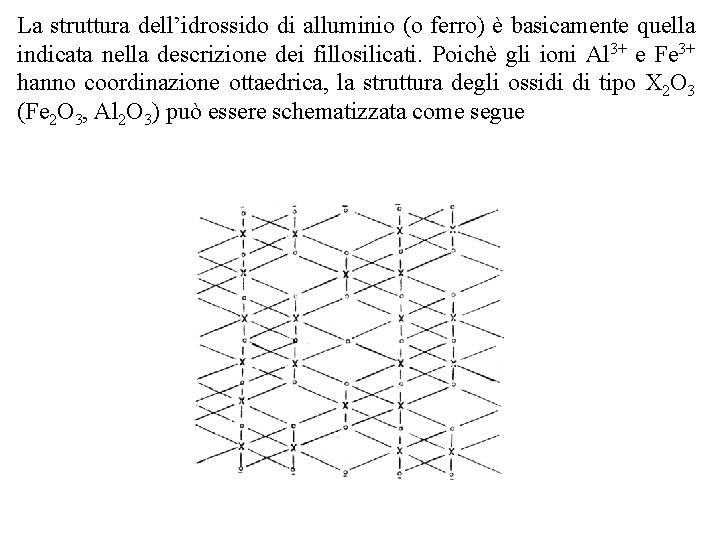
La struttura dell’idrossido di alluminio (o ferro) è basicamente quella indicata nella descrizione dei fillosilicati. Poichè gli ioni Al 3+ e Fe 3+ hanno coordinazione ottaedrica, la struttura degli ossidi di tipo X 2 O 3 (Fe 2 O 3, Al 2 O 3) può essere schematizzata come segue
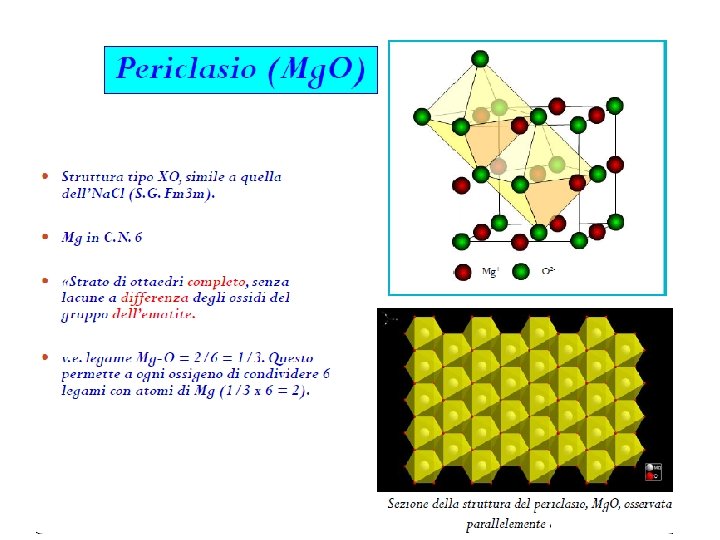
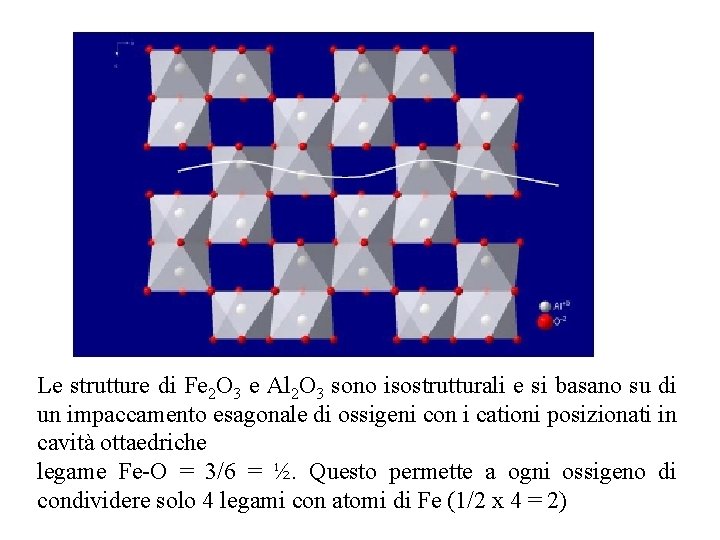
Le strutture di Fe 2 O 3 e Al 2 O 3 sono isostrutturali e si basano su di un impaccamento esagonale di ossigeni con i cationi posizionati in cavità ottaedriche legame Fe O = 3/6 = ½. Questo permette a ogni ossigeno di condividere solo 4 legami con atomi di Fe (1/2 x 4 = 2)
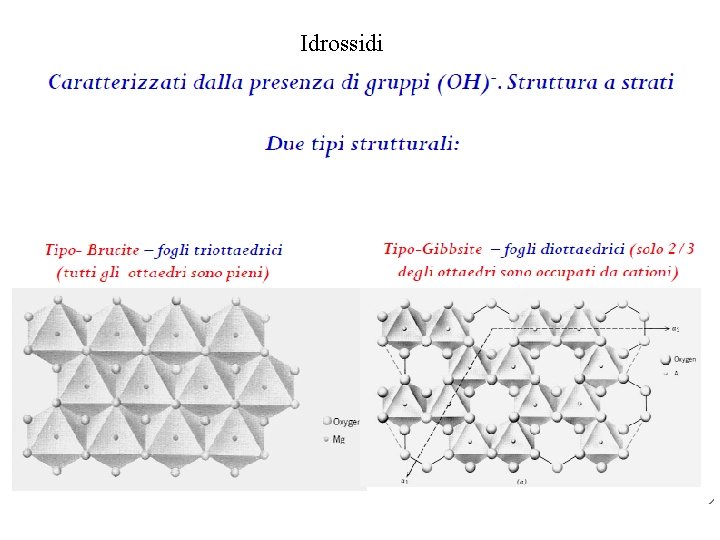
Idrossidi

- Slides: 98