Sminaire sur les Politiques Pharmaceutiques OMS Genve Suisse













- Slides: 18

Séminaire sur les Politiques Pharmaceutiques OMS, Genève, Suisse 09 au 13 May 2016 Autorités Nationales de Réglementation: Stratégie globale de l’OMS

2 2

Principales activités de RSS/Siège l Etablir le niveau de mise en oeuvre de la réglementation pharmaceutique dans les pays : Evaluation des autorités nationales de réglementation pharmaceutioque l Fournir un soutien aux autorités pour renforcer leurs capacités : Plan de développement institutionel l Fournir un soutien aux blocs économiques régionaux pour renforcer leurs capacités l Promouvoir l'harmonisation des pratiques parmi les autorités : Sur la base des normes et des lignes directrices élaborées par l'Organisation 3| ANRP, TBS 2016

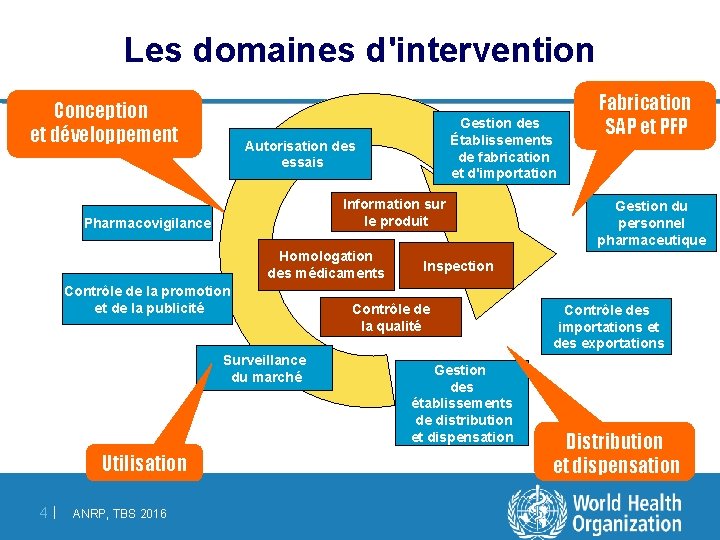
Les domaines d'intervention Conception et développement Autorisation des essais Information sur le produit Pharmacovigilance Homologation des médicaments Contrôle de la promotion et de la publicité Surveillance du marché Utilisation 4| ANRP, TBS 2016 Gestion des Établissements de fabrication et d'importation Fabrication SAP et PFP Gestion du personnel pharmaceutique Inspection Contrôle de la qualité Gestion des établissements de distribution et dispensation Contrôle des importations et des exportations Distribution et dispensation

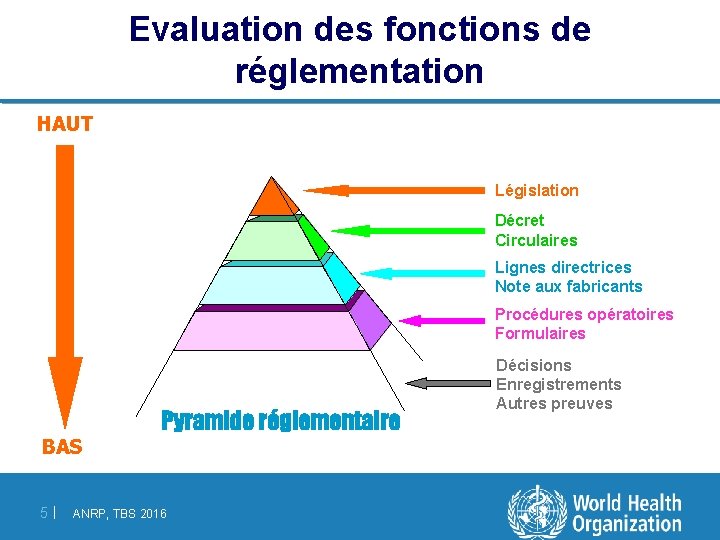
Evaluation des fonctions de réglementation HAUT Législation Décret Circulaires Lignes directrices Note aux fabricants Procédures opératoires Formulaires BAS 5| Pyramide réglementaire ANRP, TBS 2016 Décisions Enregistrements Autres preuves

Les étapes de l'évaluation de l'ANRP l Expression du besoin l Validation de la demande l Composition de l'équipe l Planification et préparation de la visite l Evaluation proprement dite – Réunion d'ouverture – Conduite de la visite – Réunion de clôture l Elaboration d'un rapport l Elaboration d'un plan de développement institutionnel 6| ANRP, TBS 2016

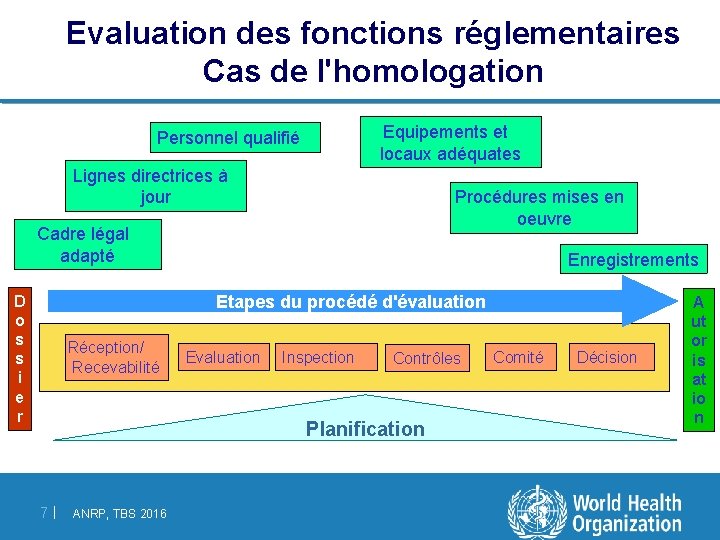
Evaluation des fonctions réglementaires Cas de l'homologation Equipements et locaux adéquates Personnel qualifié Lignes directrices à jour Procédures mises en oeuvre Cadre légal adapté Enregistrements Etapes du procédé d'évaluation D o s s i e r Réception/ Recevabilité Evaluation Inspection Contrôles Planification 7| ANRP, TBS 2016 Comité Décision A ut or is at io n

Evaluation de la structure institutionelle l Base légale de l'institution l Structure de gouvernance (DG, Président, Secrétaire général, etc…) l Organisation en place l Système de gestion de la qualité l Ressources financières l Gestion des ressources humaines 8| ANRP, TBS 2016

Evaluation de la structure institutionelle /2 l Indépendance et impartialité l Transparence et confidentialité l Gestion des comités et de l'expertise externe l Infrastructure et équipements l Modalités de surveillance et pour rendre compte l Gestion des technologies de l'information 9| ANRP, TBS 2016

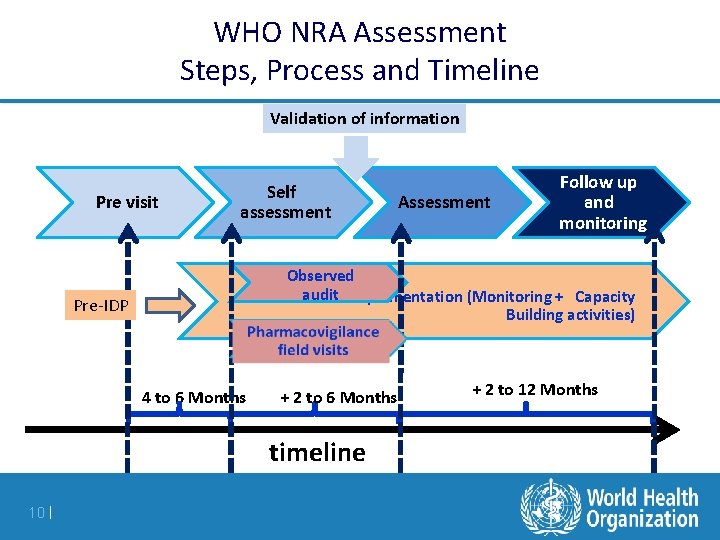
WHO NRA Assessment Steps, Process and Timeline Validation of information Pre visit Self assessment Observed IDPaudit implementation (Monitoring + Capacity Building activities) Pre-IDP 4 to 6 Months + 2 to 6 Months timeline 10 | Assessment Follow up and monitoring + 2 to 12 Months

Evaluation des ANRPs par l’OMS: 1997 11 |

Evaluation des ANRPs par l’OMS: 2014 12 |

Cartographie des outils d'évalutation Inside WHO – 8 tools (*PQ tool not included) 1 6 30 1 11 24 7 20 156 Rapid assessment -USP 1 10 33 RAST-SPS-MSH 4 14 41 PIC S 9 126 605 IMDRF 14 68 252 OMCL Network 9 67 164 BEMA 12 117 364 Medical Devices 9 74 594 PAHO Abbreviated 13 | 15 99 636 Harmonized Med. & Vac. Sub. Indicator* PAHO Indicator* 7 51 181 Medicine Vaccine Function Blood products Tools Outside WHO – 6 tools 6 79 44

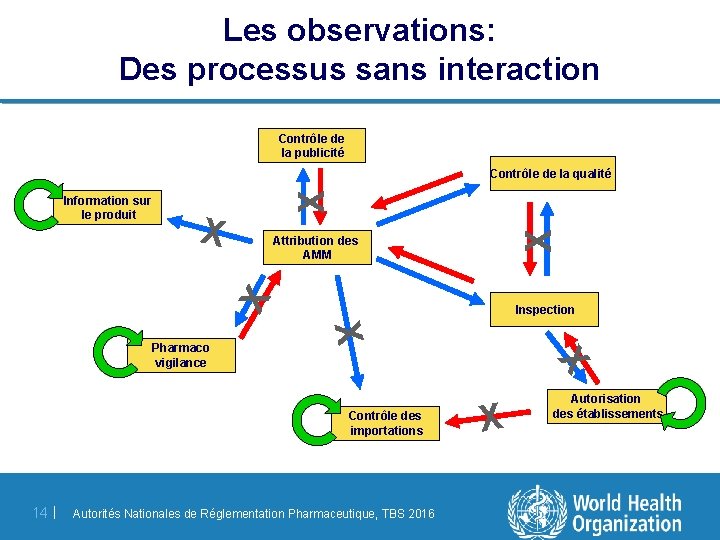
Les observations: Des processus sans interaction Contrôle de la publicité X X Attribution des AMM X Information sur le produit X Contrôle de la qualité X X Pharmaco vigilance Inspection Contrôle des importations 14 | Autorités Nationales de Réglementation Pharmaceutique, TBS 2016 X Autorisation des établissements

Exemples de déficiences observées : Cas de l'inspection l Ressources humaines – Absence de compétence technique des inspecteurs (ex : BPF) – Ressources humaines limitées au regard du nombre des établissements à inspecter – Pas de compétences judiciaires pour réaliser leurs missions. l Indépendance/Impartialité – Pas de code de conduite – Pas de mécanisme ou de ligne directrice pour gérer les conflits d'intérêt 15 | ANRP, TBS 2016

Exemples de déficiences observées : Cas de l'inspection / 2 l Equipement / Technologies de l'Information – Accès limité à internet, à des banques de données – Logistique inadéquate i. e. outils de communication, véhicules et ordinateurs l Organisation – Pas de coordination, de collaboration ou d'échange sur les programmes d'inspection et les établissements inspectés avec les inspecteurs régionaux – Pas de mécanisme pour démontrer que tous les inspecteurs suivent des procédures identiques sur l'ensemble du territoire l Enregistrements et données de sorties – Pas de listes consolidées des activités d'inspection 16 | ANRP, TBS 2016

La logique des activités de soutien Etablir ou réorganiser une structure Réglementation pharmaceutique Lignes directrices scientifiques et techniques Développer et mettre en oeuvre des procédures et formulaires Etude comparative de bonnes pratiques Activités de plaidoyer Diagnostic situationnel par évaluation des ANRP Activités de conseil Normes et guides développés par l'OMS Guide sur les systèmes qualité Procédures existantes développées par l'OMS ou la PQP Qualification à la fonction Nombreuses formations dispensées (inspection, homologation, vigilance) Gestion de l'information Système informatique OMS / SIAMED 17 | ANRP, TBS 2016

Merci