Sloen a struktura atomu Sloen a struktura atomu










![„řeka stability“[1] „řeka stability“[1]](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-12.jpg)






![jaderné přeměny nuklidů [2] jaderné přeměny nuklidů [2]](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-19.jpg)


![thoriová rozpadová řada [3] uranová rozpadová řada [4] aktiniová rozpadová řada [5] thoriová rozpadová řada [3] uranová rozpadová řada [4] aktiniová rozpadová řada [5]](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-23.jpg)






![Radioaktivita pohled do tokamaku [10] řetězová štěpná reakce [8] rozpad jádra uranu [9] Radioaktivita pohled do tokamaku [10] řetězová štěpná reakce [8] rozpad jádra uranu [9]](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-30.jpg)

![Radioaktivita – radiouhlíková metoda datování Ötzi – mumie eneolitického člověka [12] • sleduje obsah Radioaktivita – radiouhlíková metoda datování Ötzi – mumie eneolitického člověka [12] • sleduje obsah](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-32.jpg)

![Zdroje 9. 10. 11. 12. www. wikipedia. org, Nuclear fission [online]. 2010 -03 -03 Zdroje 9. 10. 11. 12. www. wikipedia. org, Nuclear fission [online]. 2010 -03 -03](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-34.jpg)
- Slides: 34

Složení a struktura atomu

Složení a struktura atomu • vývoj představ o složení hmoty – pojem atom poprvé použil Demokritos (5. st. př. n. l. ) • veškerá hmota je složena z malých neviditelných částic = atomů – atom je dále nedělitelný, nelze je vytvářet ani zničit – liší se navzájem tvarem, polohou a uspořádáním – poté byl atom na dlouho zapomenut

Složení a struktura atomu – v 19. století formuloval John Dalton Atomovou teorii • každý prvek se skládá ze stejných atomů – nelze je měnit ani ničit, jen různě uspořádat – Thompsonův (pudinkový) model – objevil přítomnost elektronů v atomu pudinkový model – atom je tvořen rovnoměrně nabitou kladnou hmotou, ve které jsou rozptýleny záporně nabité elektrony

Složení a struktura atomu – Rutherfordův (planetární) model • objevil přítomnost atomového jádra Bohrův model • záporně nabité elektrony krouží po kružnicích kolem velmi malého kladně nabitého jádra (jako planety kolem slunce) – Bohrův model • předpokládá existenci určitých vzdáleností, ve kterých mohou elektrony kolem jádra kroužit, aniž by se zřítili do jádra

Složení a struktura atomu – kvantově-mechanický model • elektrony se kolem jádra pohybují nahodile – pro elektrony lze určit, s jakou pravděpodobností se budou nacházet ve vybrané části prostoru » lze vymezit oblast, ve které se bude konkrétní elektron s největší pravděpodobností vyskytovat oblast výskytu elektronů - orbital

Složení a struktura atomu • Složení atomu – obsahuje 3 druhy částic – protony, neutrony a elektrony část atomu částice značka náboj hmotnost (kg) hmotnost (u) jádro proton p +1 1, 67· 10 -27 1 jádro neutron n 0 1, 67· 10 -27 1 obal elektron e -1 9. 10· 10 -31 0

Jádro atomu • nachází se ve středu atomu • je asi 100 000 x menší než celý atom – kdyby měl atom průměr 100 m, jádro by bylo velké jako zrnko máku • jádro tvoří prakticky celou hmotnost atomu – hmotnost elektronů je ve srovnání s hmotností protonů a neutronů zanedbatelná

Jádro atomu • v jádře nacházíme protony a neutrony – protonové číslo Z – počet protonů v jádře – neutronové číslo N – počet neutronů v jádře – nukleonové číslo A – počet nukleonů v jádře = počet jaderných částic A=Z+N

Jádro atomu • prvek • soubor atomů se stejným protonovým číslem (6 C, 8 O) • izotopy • atomy prvku s různým neutronovým číslem (12 C, 13 C) • nuklid • soubor atomů se stejným protonovým i neutronovým číslem ( 21 H, . . . )

Radioaktivita • jádra některých nuklidů jsou nestabilní a podléhají přeměnám • radioaktivita = proces, při kterém dochází ke změnám jader – je provázena vznikem neviditelného záření • radioaktivní záření

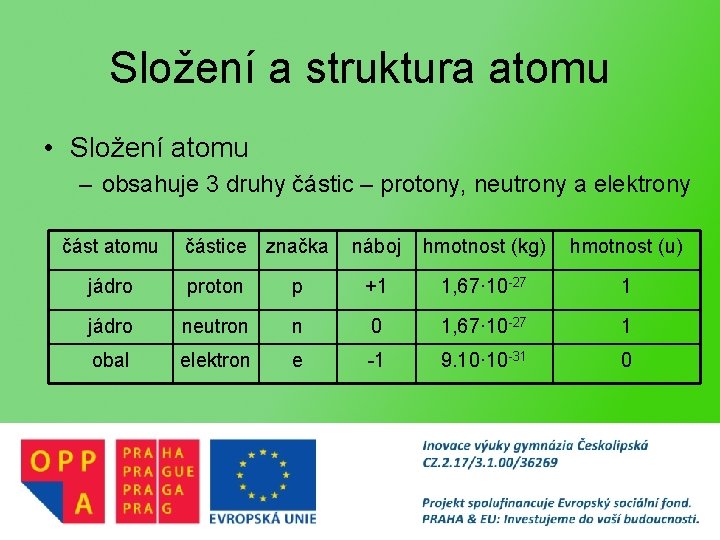
Radioaktivita – důležitým faktorem stability jádra je poměr počtu neutronů N a protonů Z • pro prvky s nižším protonovým číslem jsou nejstálejší nuklidy s poměrem 1 – 12 6 C, 16 8 O, . . . • pro prvky s vyšším protonovým číslem tento poměr narůstá až k hodnotě 1, 5 • „řeka stability“ – graf zakreslující stabilní nuklidy podle N a Z
![řeka stability1 „řeka stability“[1]](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-12.jpg)
„řeka stability“[1]

Radioaktivita – radioaktivní (jaderné) přeměny jsou spojeny s uvolňováním částic z jádra • záření α – je tvořeno částicemi α (jádra helia 42 He) – má velmi krátký dosah, je málo pronikavé • záření β – je tvořeno elektrony 0 -1 e (záření β-) nebo pozitrony 0+1 e (záření β+) – je pronikavější než α

Radioaktivita • záření γ – – elektromagnetické vlnění s vysokou energií podobá se rentgenovému záření má velmi vysokou pronikavost zpravidla doprovází záření β pronikavost záření

Radioaktivita • Radioaktivní rozpady – rozpad α • typický pro jádra těžkých prvků • z jádra se uvolní částice α (jádro 42 He) • vzniká jádro nového prvku chudšího o dva protony a dva neutrony (o 2 místa v periodické tabulce nalevo)

Radioaktivita – rozpad β • typický pro jádra s přebytkem neutronů (například 31 H) • přebytečný neutron se přemění na proton a elektron – proton zůstane v jádře • vzniklé jádro má o jeden proton více a jeden neutron méně (vzniká prvek ležící napravo v PSP)

Radioaktivita – rozpad β+ • typický pro jádra prvků obsahujících přebytek protonů • nadbytečný proton se přemění na neutron a pozitron – kladně nabitý elektron • vzniká prvek chudší o jeden proton a bohatší o jeden neutron (o jedno místo vlevo)

Radioaktivita – elektronový záchyt • přebytek protonů může vést i k záchytu elektronů – elektron z obalu je zachycen přebytečným protonem v jádře a vznikne neutron • vzniká prvek chudší o jeden proton a bohatší o jeden neutron (o jedno místo vlevo)
![jaderné přeměny nuklidů 2 jaderné přeměny nuklidů [2]](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-19.jpg)
jaderné přeměny nuklidů [2]

Radioaktivita – poločas rozpadu • čas, za který se rozpadne polovina jader radioaktivního nuklidu • nezáleží na množství atomů – pro daný nuklid je konstatní, nelze jej ovlivnit 212 Po 3. 10 -7 s 238 U 4, 5. 109 let 222 Rn 3, 82 dne

Radioaktivita

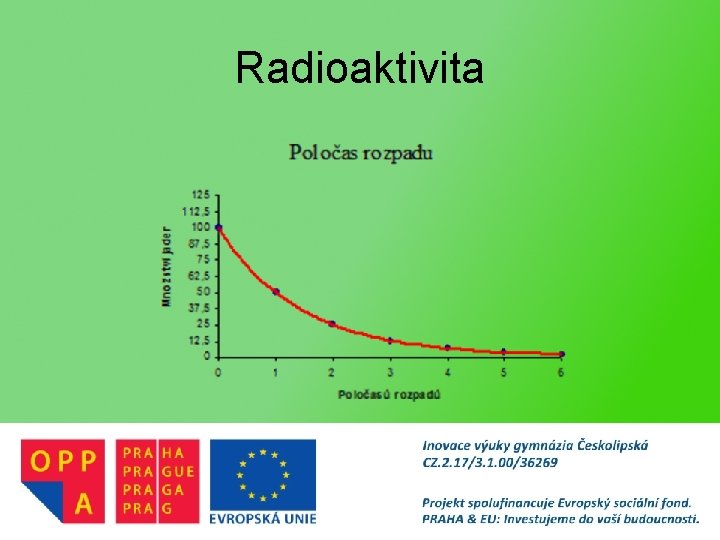
Radioaktivita – rozpadové řady • posloupnosti radioaktivních rozpadů • vycházejí z poměrně stálých nuklidů – 232 Th (t 1/2 = 13, 9 miliard let) – 238 U (t 1/2 = 710 milionů let) – 235 U (t 1/2 = 4, 5 miliard let) – následující rozpady jsou výrazně pomalejší » ustavilo se stálé množství meziproduktů v přírodě – všechny končí nuklidy olova, které jsou stabilní
![thoriová rozpadová řada 3 uranová rozpadová řada 4 aktiniová rozpadová řada 5 thoriová rozpadová řada [3] uranová rozpadová řada [4] aktiniová rozpadová řada [5]](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-23.jpg)
thoriová rozpadová řada [3] uranová rozpadová řada [4] aktiniová rozpadová řada [5]

• byla objevena i umělá rozpadová řada 237 Np → 209 Bi neptuniová rozpadová řada [6]

Radioaktivita • Jaderné reakce • uměle vyvolané jaderné přeměny • reakce atomového jádra s jinou částicí – prosté • jádro uvolňuje jednu nebo více lehkých částic • počet částic v jádře se mění jen málo 14 4 α → 17 O + 1 p N + 7 2 8 1 – zkrácený zápis 147 N (α, p) 178 O

Radioaktivita – takto připravené nuklidy jsou často nestálé a samovolně se rozpadají • umělá radioaktivita 27 Al + 4 α → 30 P + 1 n 15 13 2 0 30 P → 30 Si + 0 e 14 15 +1 – objevili ji manželé Joliot-Curie 1933 Frédéric a Irène Joliot-Curie [7]

Radioaktivita – štěpné • po srážce s jinou částicí (neutronem, . . . ) dochází k rozštěpení původního jádra, zpravidla na dvě menší • dochází k nim u těžkých atomů 235 U + 1 n → 93 Kr + 140 Ba + 3 1 n • častým produktem štěpných reakcí jsou další neutrony – ty mohou způsobit štěpení dalších jader » řetězová jaderná reakce

Radioaktivita – termojaderná fúze • při reakci dochází ke slučování lehkých jader více prvků za vzniku jádra těžšího prvku • probíhá za vysokých teplot (Slunce) 2 H + 2 H → 3 He + 1 n 2 H + 3 H → 4 He + 1 n 2 H + 6 Li → 7 Be + 1 n

Radioaktivita • Význam – jaderná energetika • štěpení 235 U v jaderných elektrárnách – je třeba regulovat množství neutronů » grafitové tyče, kyselina boritá • termojaderná fúze – zatím pouze experimentální reaktory » tokamaky – produkuje velké množství energie
![Radioaktivita pohled do tokamaku 10 řetězová štěpná reakce 8 rozpad jádra uranu 9 Radioaktivita pohled do tokamaku [10] řetězová štěpná reakce [8] rozpad jádra uranu [9]](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-30.jpg)
Radioaktivita pohled do tokamaku [10] řetězová štěpná reakce [8] rozpad jádra uranu [9]

Radioaktivita – lékařství • značení látek v těle pomocí některých radionuklidů • diagnostika zářením produkovaným radionuklidy – zbrojírenství • atomové bomby – neřízená řetezová štěpná reakce • vodíkové bomby jaderná bomba „Fat man“ [11] – termojaderná fúze je zahájena řetězovou jadernou reakcí
![Radioaktivita radiouhlíková metoda datování Ötzi mumie eneolitického člověka 12 sleduje obsah Radioaktivita – radiouhlíková metoda datování Ötzi – mumie eneolitického člověka [12] • sleduje obsah](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-32.jpg)
Radioaktivita – radiouhlíková metoda datování Ötzi – mumie eneolitického člověka [12] • sleduje obsah uhlíku 14 C ve vzorku rostlinných nebo živočišných tkání – ten je za života organismu stálý » rostliny jej získávají z atmosféry (CO 2), živočichové z rostlin – po úmrtí organismu dochází k pomalému rozpadu 14 C » poločas rozpadu je 5730 let • použitelná pro stáří od asi 100 do 50 000 let

Zdroje 1. 2. 3. 4. 5. 6. 7. 8. www. wikipedia. org, Isotopes and half-life [online]. 2009 -09 -26 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/8/80/Isotopes_and_half-life. svg www. wikipedia. org, Table isotopes en [online]. 2009 -05 -05 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/c/c 4/Table_isotopes_en. svg www. wikipedia. org, Decay chain(4 n, Thorium series) [online]. 2008 -12 -20 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/1/1 c/Decay_chain%284 n%2 CThorium_series%29. PNG www. wikipedia. org, Decay chain(4 n+2, Uranium series) [online]. 2008 -12 -20 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/a/a 1/Decay_chain%284 n%2 B 2%2 C_Uranium_series%29. PNG www. wikipedia. org, Aktiniová řada [online]. 2007 -09 -11 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/c/c 8/Aktiniova_rada. svg www. wikipedia. org, Decay chain(4 n+1, Neptunium series) [online]. 2008 -12 -20 [cit. 2013 -10 -02]. Dostupné z: http: //commons. wikimedia. org/wiki/File: Decay_chain%284 n%2 B 1, Neptunium_series%29. PNG www. wikipedia. org, Frederic and Irene Joliot-Curie [online]. 2012 -02 -14 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/3/39/Frederic_and_Irene_Joliot-Curie. jpg www. wikipedia. org, Fission chain reaction [online]. 2008 -01 -19 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/9/9 a/Fission_chain_reaction. svg
![Zdroje 9 10 11 12 www wikipedia org Nuclear fission online 2010 03 03 Zdroje 9. 10. 11. 12. www. wikipedia. org, Nuclear fission [online]. 2010 -03 -03](https://slidetodoc.com/presentation_image_h2/4a4f2a4b9c85f5befe4b1d637a92529c/image-34.jpg)
Zdroje 9. 10. 11. 12. www. wikipedia. org, Nuclear fission [online]. 2010 -03 -03 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/1/15/Nuclear_fission. svg www. wikipedia. org, Tcv int [online]. 2010 -10 -02 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/1/18/Tcv_int. jpg www. wikipedia. org, Fat man [online]. 2010 -01 -02 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/commons/1/1 a/Fat_man. png www. wikipedia. org, Oetzithe. Iceman 02 [online]. 2007 -05 -12 [cit. 2013 -10 -02]. Dostupné z: http: //upload. wikimedia. org/wikipedia/en/1/1 d/Oetzithe. Iceman 02. jpg