Skay i mineray Skay wapienne Skay gipsowe Hydraty











- Slides: 13

Skały i minerały Skały wapienne Skały gipsowe Hydraty (sole uwodnione) Krzemionka Zjawisko krasu

Minerały a skały v. Skorupa ziemska – zewnętrzna skalna warstwa Ziemi v. Minerały – to pierwiastki w stanie wolnym oraz związki chemiczne, które powstały w przyrodzie bez ingerencji człowieka v. Skały – naturalne skupiska minerałów, które powstały w wyniku procesów geologicznych v. Surowce mineralne – skały i minerały wydobywane i stosowane przez człowieka w różnych dziedzinach życia

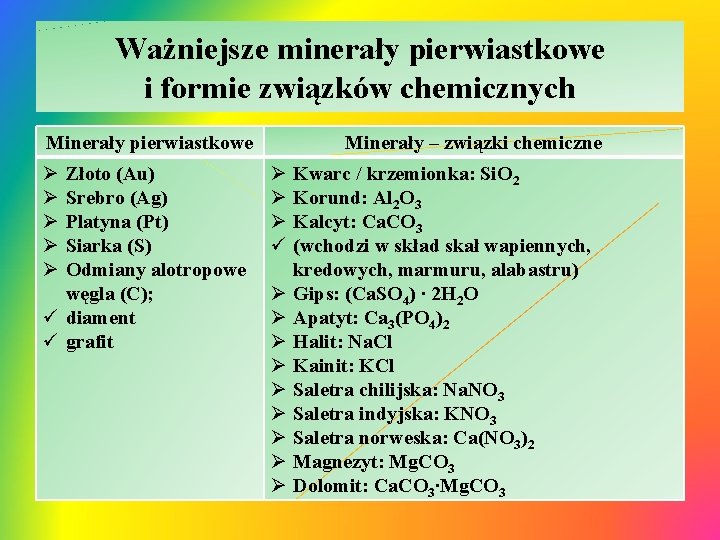
Ważniejsze minerały pierwiastkowe i formie związków chemicznych Minerały pierwiastkowe Ø Ø Ø Złoto (Au) Srebro (Ag) Platyna (Pt) Siarka (S) Odmiany alotropowe węgla (C); ü diament ü grafit Minerały – związki chemiczne Ø Ø Ø ü Ø Ø Ø Ø Ø Kwarc / krzemionka: Si. O 2 Korund: Al 2 O 3 Kalcyt: Ca. CO 3 (wchodzi w skład skał wapiennych, kredowych, marmuru, alabastru) Gips: (Ca. SO 4) ∙ 2 H 2 O Apatyt: Ca 3(PO 4)2 Halit: Na. Cl Kainit: KCl Saletra chilijska: Na. NO 3 Saletra indyjska: KNO 3 Saletra norweska: Ca(NO 3)2 Magnezyt: Mg. CO 3 Dolomit: Ca. CO 3∙Mg. CO 3

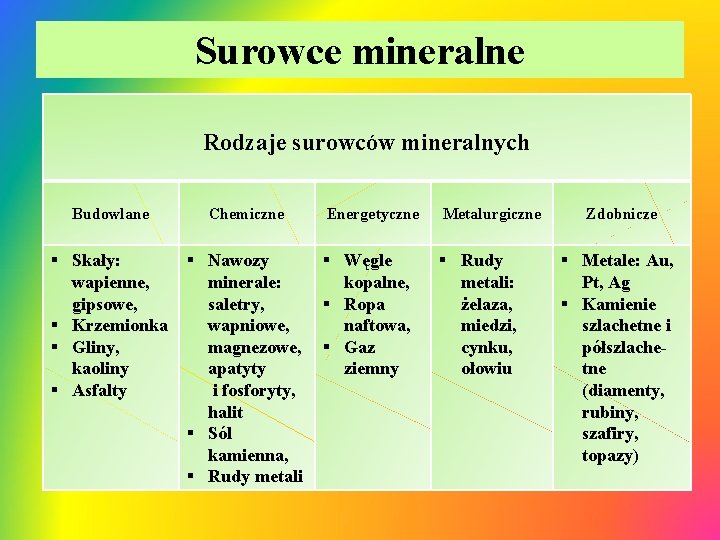
Surowce mineralne Rodzaje surowców mineralnych Budowlane Chemiczne § Skały: § Nawozy wapienne, minerale: gipsowe, saletry, § Krzemionka wapniowe, § Gliny, magnezowe, kaoliny apatyty § Asfalty i fosforyty, halit § Sól kamienna, § Rudy metali Energetyczne § Węgle kopalne, § Ropa naftowa, § Gaz ziemny Metalurgiczne § Rudy metali: żelaza, miedzi, cynku, ołowiu Zdobnicze § Metale: Au, Pt, Ag § Kamienie szlachetne i półszlachetne (diamenty, rubiny, szafiry, topazy)

Skały wapienne – kalcyt Węglan wapnia – Ca. CO 3 (kalcyt) wchodzi w skład skał: kreda, marmur, wapień Wykrywanie kalcytu – kwas węglowy jest kwasem słabym i nietrwałym, wypierany jest z soli przez kwasy mocniejsze: Ø Ca. CO 3 + 2 HCl Ca. Cl 2 + H 2 O + CO 2↑ ØCa. CO 3 + 2 H+ + 2 Cl- Ca 2+ + 2 Cl- + H 2 O + CO 2↑ : wydziela się bezbarwny, bezwonny gaz i rozpuszczalny w wodzie chlorek wapnia ØCa. CO 3 + H 2 SO 4 Ca. SO 4+ H 2 O + CO 2↑ ØCa. CO 3 + 2 H+ + SO 42 - Ca. SO 4 + H 2 O + CO 2↑ : wydziela się bezbarwny, bezwonny gaz i trudno rozpuszczalny w wodzie siarczan(VI) wapnia Ø 3 Ca. CO 3 + 2 H 3 PO 4 Ca 3(PO 4)2 + 3 H 2 O + 3 CO 2↑ Ø 3 Ca. CO 3 + 6 H+ + 2 PO 43 - Ca 3(PO 4)2 + 3 H 2 O + 3 CO 2↑ : wydziela się bezbarwny, bezwonny gaz i trudno rozpuszczalny w wodzie ortofosforan(V) wapnia ØCa. CO 3 + 2 HNO 3 Ca(NO 3)2 + H 2 O + CO 2↑ ØCa. CO 3 + 2 H+ + NO 3 - Ca 2+ + 2 NO 3 - + H 2 O + CO 2↑ : wydziela się bezbarwny, bezwonny gaz i rozpuszczalny w wodzie azotan(V) wapnia

Skały wapienne – kalcyt v Identyfikacja CO 2: Ca(OH)2 + CO 2 Ca. CO 3↓ + H 2 O; Ca 2+ + 2 OH- + CO 2 Ca. CO 3↓ + H 2 O v Minerały krzemionka, gips (anhydryt), skały (granit) nie reagują z kwasem chlorowodorowym co umożliwia wykrywanie minerałów, skał i soli węglanowych (Ca. CO 3, Mg. CO 3) § Anhydryt reaguje z kwasem siarkowym(VI), powstaje wodorosiarczan(VI) wapnia rozpuszczalny w wodzie , lecz nie wydziela się gaz ü Ca. SO 4 + H 2 SO 4 Ca 2+ + HSO 4 - ; Ca. SO 4 + HCl r. nie zachodzi § Krzemionka nie reaguje z kwasami (wyjątek HF(aq)), natomiast reaguje z wodnymi roztworami mocnych zasad, powstają rozpuszczalne w wodzie sole kwasu krzemowego(IV) ü Si. O 2 + HCl r. nie zachodzi ü Si. O 2 + 4 HF Si. F 4↑ + 2 H 2 O ü Si. O 2 + 2 Na. OH Na 2 Si. O 3 + H 2 O ü Si. O 2 + 2 Na+ + 2 OH- 2 Na+ + Si. O 32 - + H 2 O

Skały wapienne i ich zastosowanie Wapień – Ca. CO 3 Ø Skała osadowa Ø Barwa biała lub beżowa, z domieszkami barwy czerwonawej, zielonkawej lub brunatnej Ø Produkcja wapna palonego, odkwaszający nawóz, produkcja szkła Kreda – do 70% Ca. CO 3 Ø Skała osadowa Ø Barwa biała lub szara Ø Biały pigment farb, Ø Wyrób kredy do pisania, past do zębów, kitów, nawóz odkwaszający Marmur i alabaster Ca. CO 3 Ø Skała metamorficzna, utworzona z wapieni pod wpływem wysokich temp. i ciśnienia Ø Budowa krystaliczna Ø Barwa białej, różowej, zielonkawej Ø Materiał budowlany, rzeźbiarski

Skały gipsowe Anhydryt Ca. SO 4 Gips Ca. SO 4 ∙ 2 H 2 O § Budowa krystaliczna, barwy § Budowa niebieskoszarej, rzadko białej drobnokrystaliczna, lub kremowej, łatwo chłonie półprzezroczysta, wodę zwiększając objętość do plastyczna i miękka, 60% z jednoczesnym pękaniem i słabo rozpuszczalna rozwarstwieniem w wodzie zimnej, lepiej § Stosowany w budownictwie, w ciepłej przemyśle cementowym, § Stosowany jubilerstwie w budownictwie, medycynie, w rzeźbiarstwie

Hydraty – sole uwodnione v Hydraty – sole, które w stanie stałym mają wbudowane w sieć krystaliczną cząsteczki wody – tzw. wodę krystaliczną: Ø Cu. SO 4 – siarczan(VI) miedzi(II); bezbarwny Ø Cu. SO 4 ∙ 5 H 2 O – siarczan(VI) miedzi(II) – woda (1/5) (odczyt woda 1 do 5); barwa niebieska Ø Ca. SO 4 – siarczan(VI) wapnia / anhydryt Ø Ca. SO 4 ∙ 2 H 2 O – siarczan(VI) wapnia – woda (1/2) / gips Ø (Ca. SO 4)2 ∙ H 2 O – siarczan(VI) wapnia – woda (2/1) / gips palony Ø Ca. SO 4 ∙ H 2 O siarczan(VI) wapnia – woda (1/1) Ø Co. Cl 2 – chlorek kobaltu(II); barwa niebieska Ø Co. Cl 2 ∙ 2 H 2 O – chlorek kobaltu(II) – woda (1/2); barwa różowa, Ø Co. Cl 2 ∙ 6 H 2 O – chlorek kobaltu(II) woda (1/6): barwa intensywnie różowa v Wodę krystaliczną można usunąć przez prażenie hydratów

Skala twardości Mohsa Skala 1 2 3 4 5 6 7 8 9 10 Przykłady minerałów talk, (paznokieć 2, 5) / gips, grafit, sól kamienna kalcyt fluoryt (stal noża – 5, 5) / apatytyt szkło okienne / ortoklaz kwarc topaz korund diament

Krzemionka / kwarc Kwarc – minerał wchodzący w skład skał (piasek, żwir, piaskowce, granit, gnejs) – jest tlenkiem krzemu(IV) Si. O 2 Właściwości fizyczne § § Budowa krystaliczna Bez domieszek jest bezbarwny Twardy ale kruchy Gęstość 2, 65 g/cm 3 Właściwości chemiczne § Mało reaktywny chemicznie § Reaguje z kwasem HF i wodnymi roztworami mocnych zasad § Tp = 1723 o. C, Tw = 2230 o. C üSi. O 2 + HCl/H 2 SO 4/HNO 3 r. nie zachodzi üSi. O 2 + 4 HF Si. F 4↑ + 2 H 2 O üSi. O 2 + 2 Na. OH Na 2 Si. O 3 + H 2 O üSi. O 2 + 2 Na+ + 2 OH- 2 Na 2+ + Si. O 32 - + H 2 O üSi. O 2 + 4 KOH K 4 Si. O 4 + 2 H 2 O üSi. O 2 + 4 K+ + 4 OH- 4 K+ + Si. O 44 - + 2 H 2 O

Krzemionka / kwarc Odmiany kwarcu Kryształ górski – bezbarwny, Ametyst – fioletowa barwa o silnym połysku jest efektem domieszek tlenków żelaza Agat – mikrokrystaliczna struktura, bardzo twardy Tygrysie oczko – nieprzezroczysta odm. , barwy żółtej lub brunatnej

Zjawisko krasu v Kras – procesy chemicznej erozji skał i minerałów pod wpływem czynników środowiska: Ø wody, Ø tlenków kwasowych (CO 2, SO 2, NO 2) Ø kwaśnych opadów v Węglany – sole kwasu węglowego przechodzą w wodorowęglany (wapnia, magnezu) rozpuszczalne w wodzie, w wyniku rozpuszczania powstają jaskinie krasowe z stalaktytami i stalagmitami Ø Ca. CO 3 + CO 2 + H 2 O ↔Ca 2+ + 2 HCO 3Ø Mg. CO 3 + CO 2 + H 2 O ↔ Mg 2+ + 2 HCO 3 v Przechodzące do roztworu kationy wapnia i magnezu nadają wodzie twardość węglanową (przemijającą)