Sistemas Conjugados Simetria de Orbitales y Espectroscopia UV

Sistemas Conjugados, Simetria de Orbitales, y Espectroscopia UV

Definiciones • Dobles enlaces conjugados son separados por simple enlace. Ejemplo: 1, 3 -pentadieno. • Dobles enlaces insaturados son separados por dos o mas simples enlaces. 1, 4 pentadieno. • Dobles enlaces acumulados estan sobre carbonos adyacentes. Ejemplo: 1, 2 pentadieno. => EHCH 2

Energia de Resonancia • Calor de hidrogenación de trans-1 , 3 pentadieno es menos de lo esperado. • H para 1 -penteno es 30. 0 kcal/mol y para trans-2 -penteno es 27. 4 kcal/mol, 57, 4 kcal para trans-1 , 3 -pentadieno • Actual H es 53. 7 kcal, por lo tanto el dieno conjugado es mas estable. • Diferencia, (57. 4 – 53. 7) 3. 7 kcal/mol, es la resonancia energetica. EHCH 3 =>
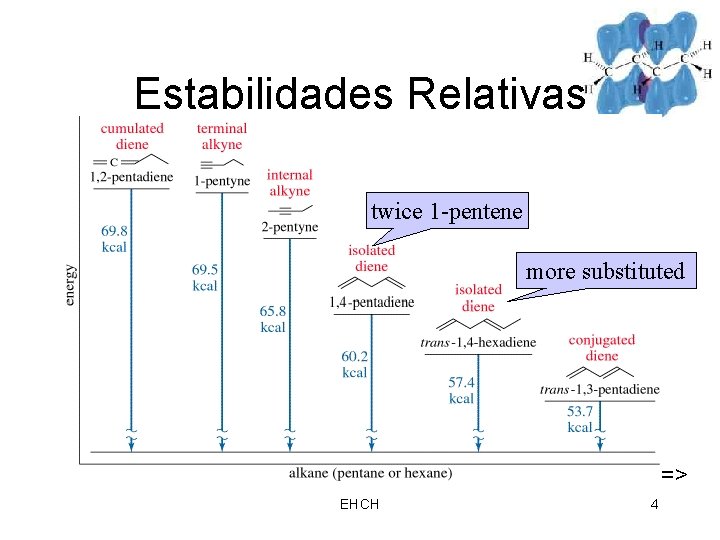
Estabilidades Relativas twice 1 -pentene more substituted => EHCH 4
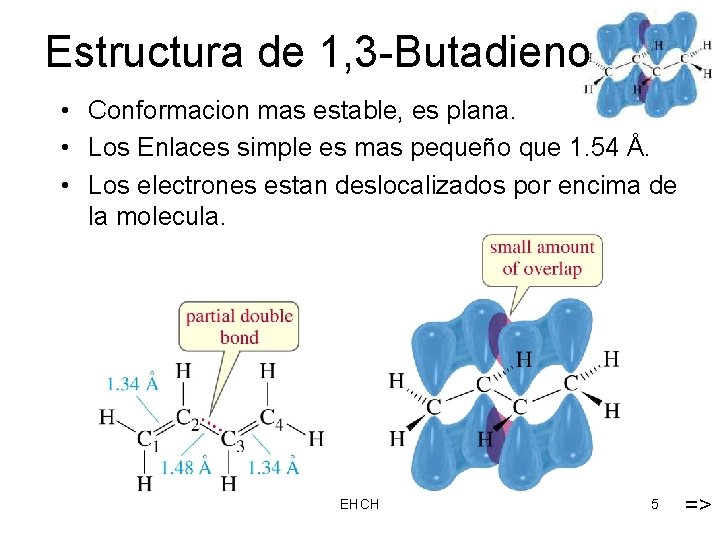
Estructura de 1, 3 -Butadieno • Conformacion mas estable, es plana. • Los Enlaces simple es mas pequeño que 1. 54 Å. • Los electrones estan deslocalizados por encima de la molecula. EHCH 5 =>

Construccion de Orbitales Moleculares • Los orbitales moleculares Pi son de lado de las superposiciones de orbitales p. • Los orbitales p tienen 2 lobulos. Mas (+) y menos (-) indicar las fases contrarias de la función de onda, no carga electrica. • Cuando los lobulos construyen superposicion, (+ y +, o - y -) un enlace MO es formado. • Cuando los lobulos + y – se sobreponen, se cancela la onda y un node forma; antienlace MO. => EHCH 6
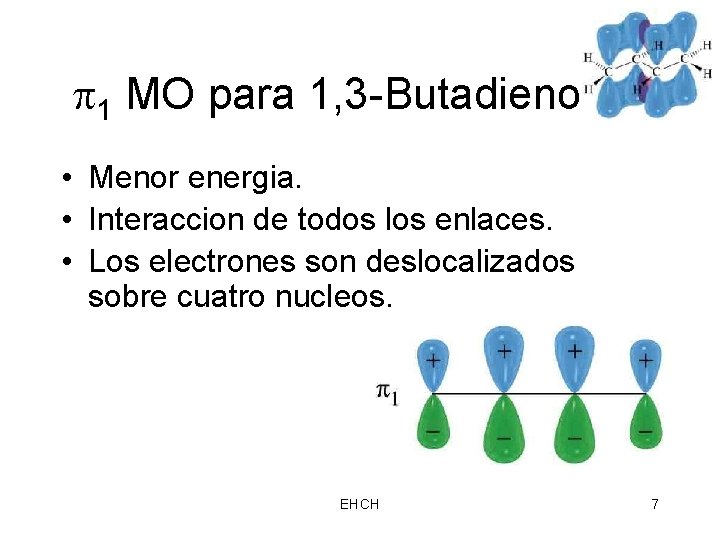
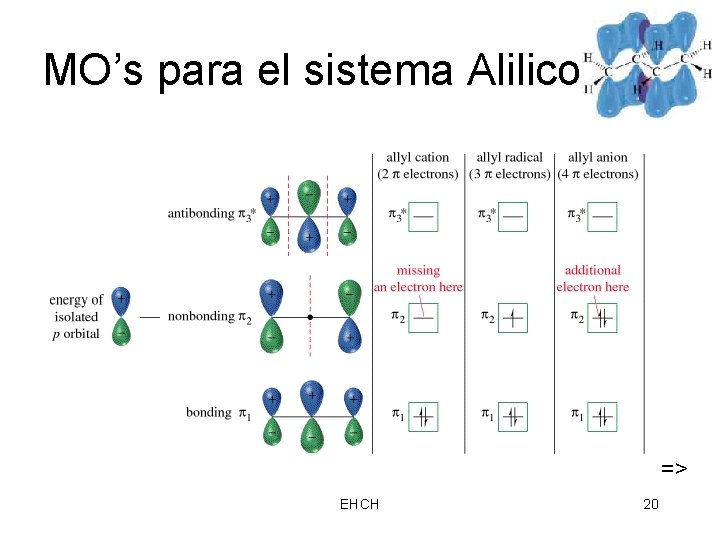
1 MO para 1, 3 -Butadieno • Menor energia. • Interaccion de todos los enlaces. • Los electrones son deslocalizados sobre cuatro nucleos. => EHCH 7
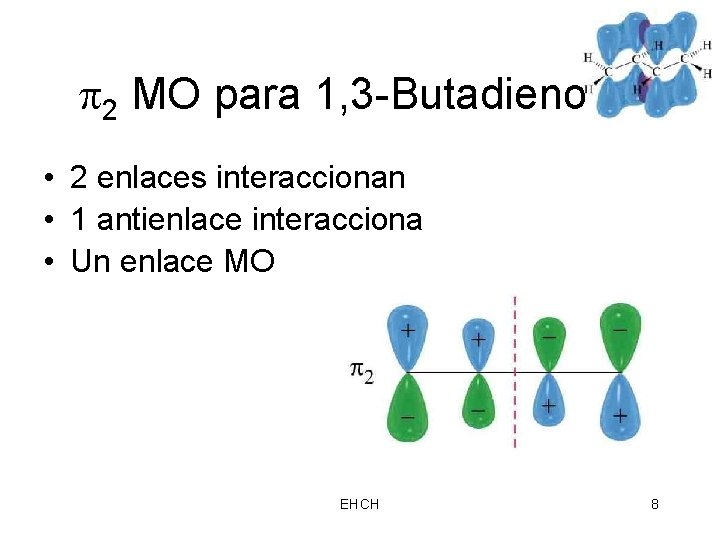
2 MO para 1, 3 -Butadieno • 2 enlaces interaccionan • 1 antienlace interacciona • Un enlace MO => EHCH 8
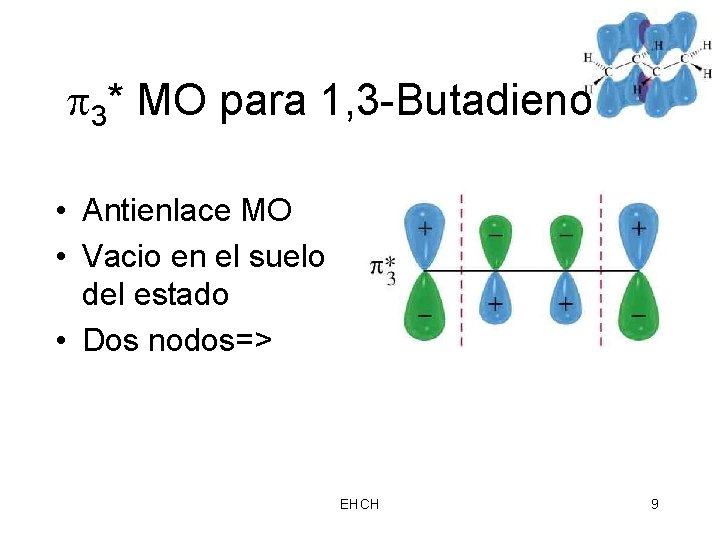
3* MO para 1, 3 -Butadieno • Antienlace MO • Vacio en el suelo del estado • Dos nodos=> EHCH 9
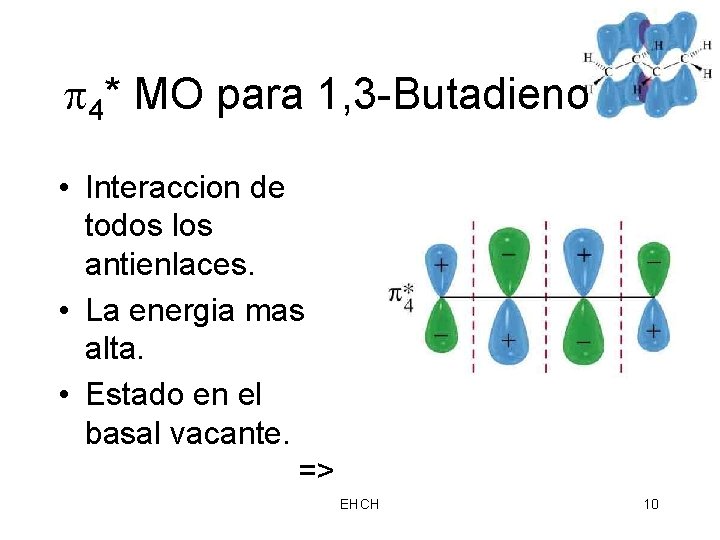
4* MO para 1, 3 -Butadieno • Interaccion de todos los antienlaces. • La energia mas alta. • Estado en el basal vacante. => EHCH 10
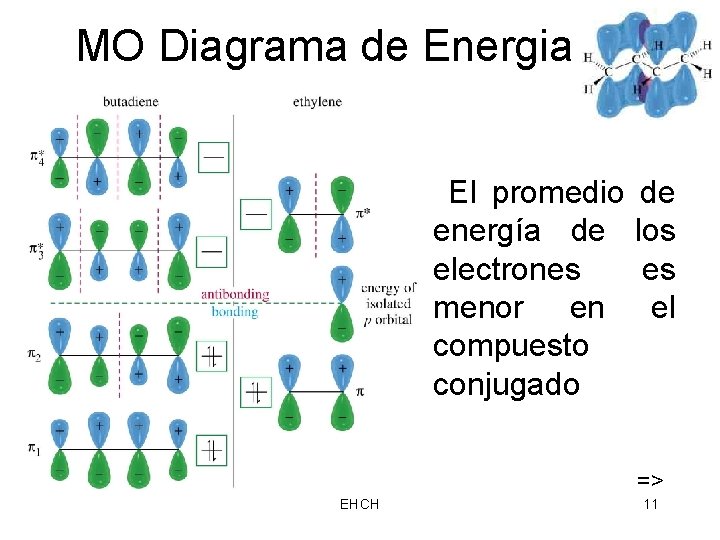
MO Diagrama de Energia El promedio energía de electrones menor en compuesto conjugado de los es el => EHCH 11
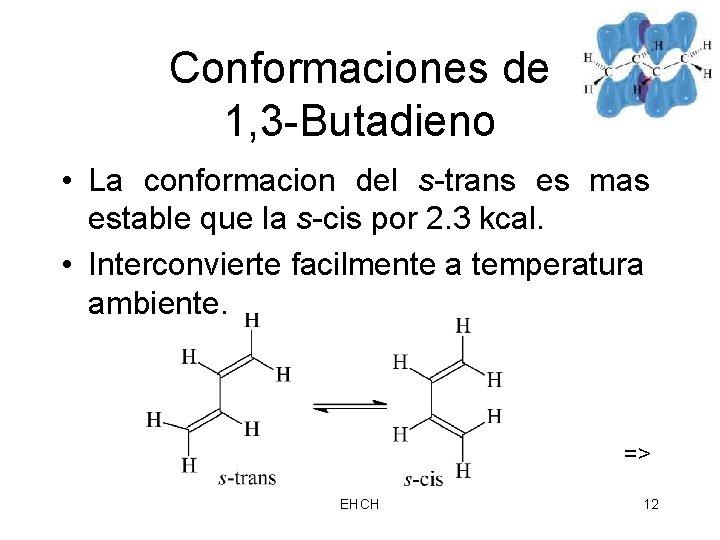
Conformaciones de 1, 3 -Butadieno • La conformacion del s-trans es mas estable que la s-cis por 2. 3 kcal. • Interconvierte facilmente a temperatura ambiente. => EHCH 12
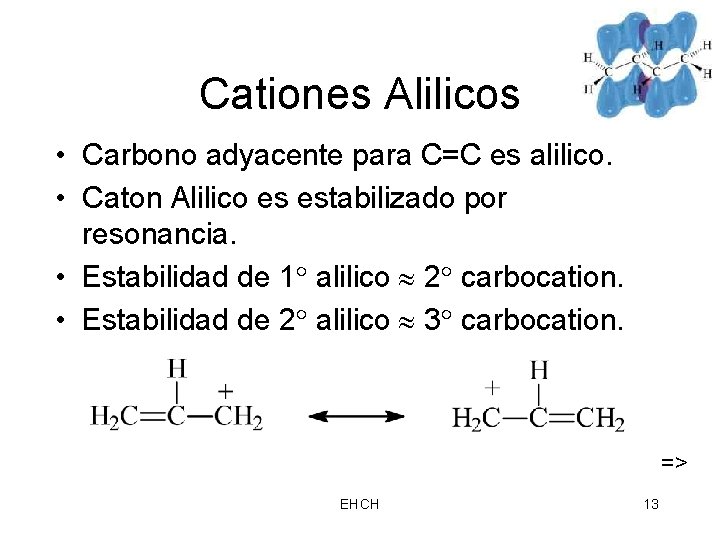
Cationes Alilicos • Carbono adyacente para C=C es alilico. • Caton Alilico es estabilizado por resonancia. • Estabilidad de 1 alilico 2 carbocation. • Estabilidad de 2 alilico 3 carbocation. => EHCH 13

1, 2 - y 1, 4 -Adicion para Dienos Conjugados • Adicion electrofilica para el doble enlace produce el intermediario mas estable • Para dienos conjugados, la resonancia estabilizada es por un cation alilico • Nucleofilo agrega a cualquiera de los carbonos 2 o 4, que tienen la carga positiva deslocalizadas => EHCH 14
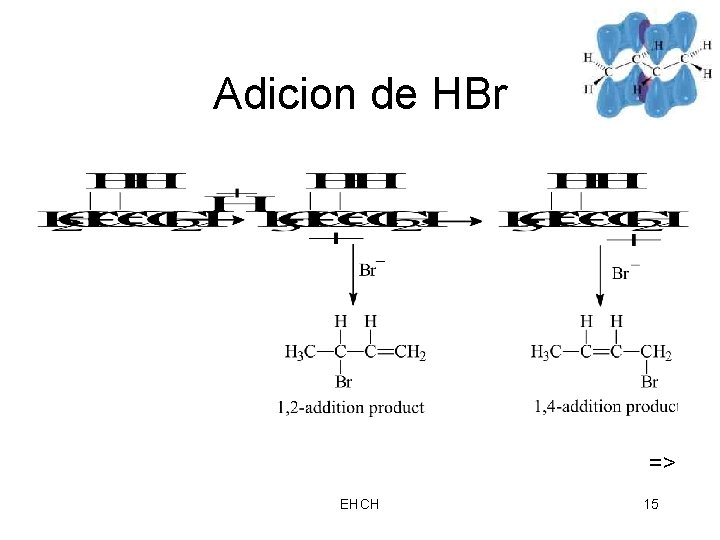
Adicion de HBr => EHCH 15
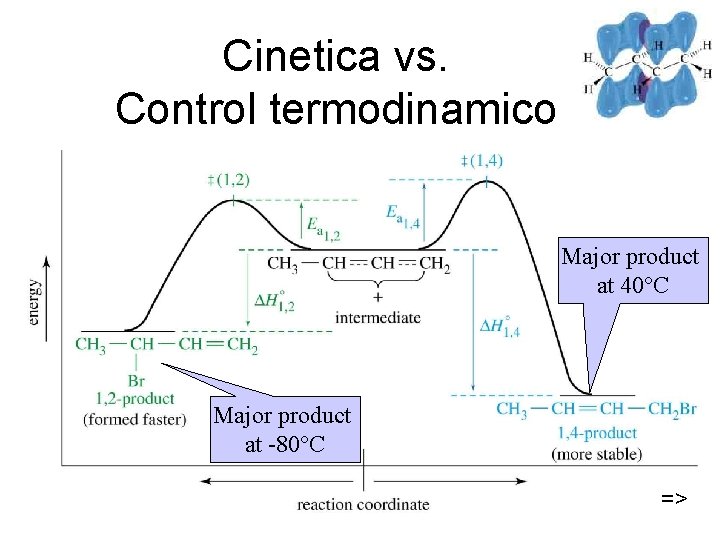
Cinetica vs. Control termodinamico Major product at 40 C Major product at -80 C Chaper 15 16 =>

Radicales Alilicos • Estabilizados por resonancia. • Radicales estables: 1 < 2 < 3 < 1 alilicos. • Substitucion en la posicion alilica compite con adicion de doble enlace. • Para fomentar la sustitución, utilice una baja concentración de reactivo con la luz, el calor, o peróxidos para iniciar la formación de radicales libres. =>17 EHCH
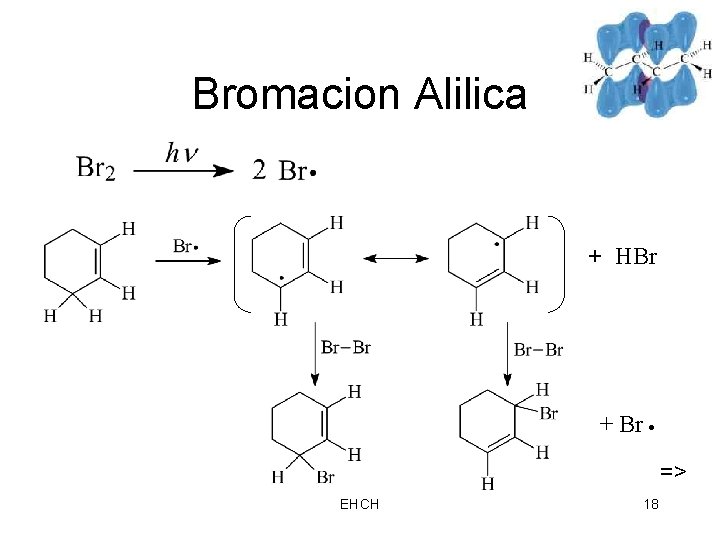
Bromacion Alilica + HBr + Br => EHCH 18
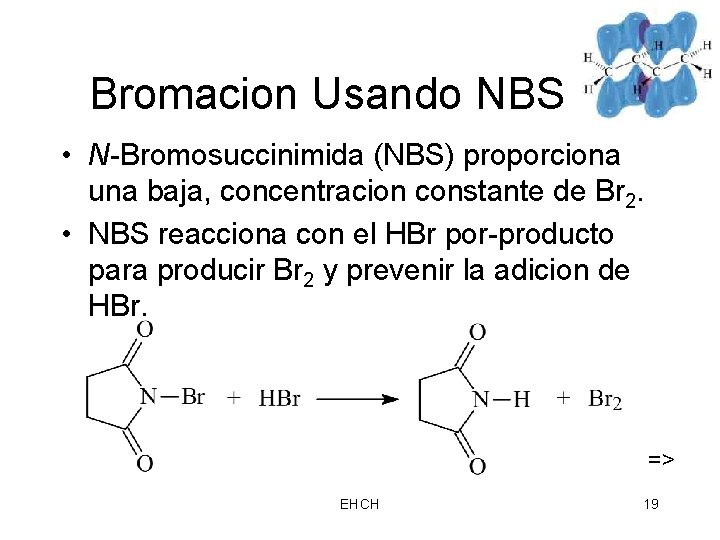
Bromacion Usando NBS • N-Bromosuccinimida (NBS) proporciona una baja, concentracion constante de Br 2. • NBS reacciona con el HBr por-producto para producir Br 2 y prevenir la adicion de HBr. => EHCH 19
MO’s para el sistema Alilico => EHCH 20
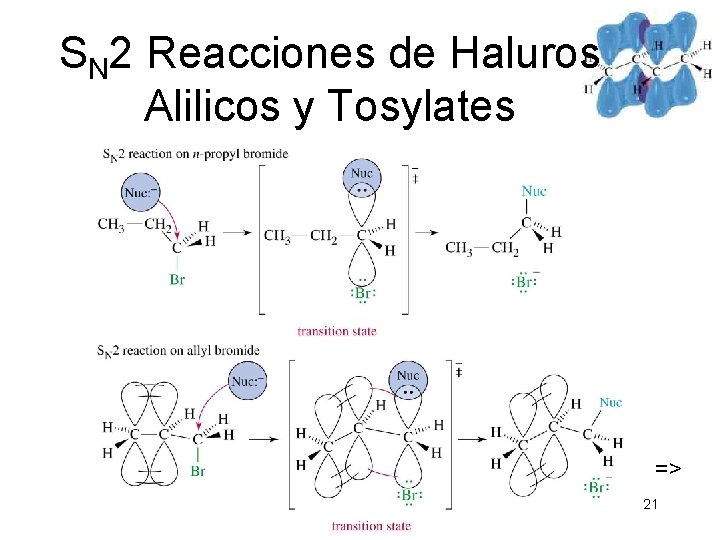
SN 2 Reacciones de Haluros Alilicos y Tosylates => Chaper 15 21
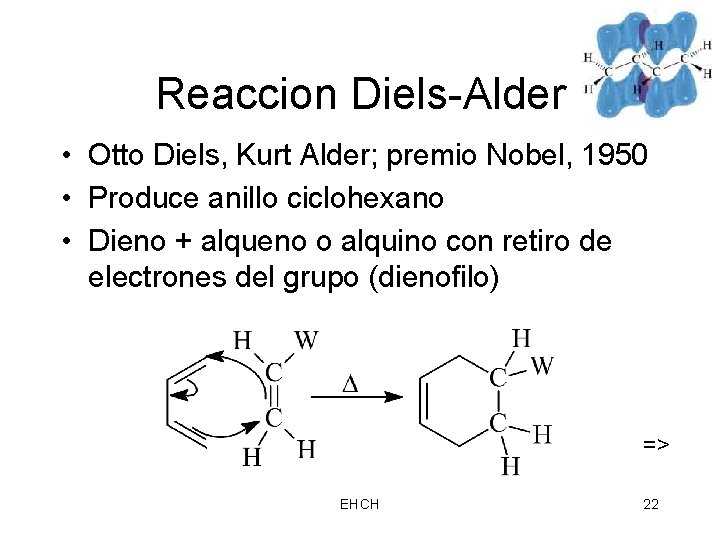
Reaccion Diels-Alder • Otto Diels, Kurt Alder; premio Nobel, 1950 • Produce anillo ciclohexano • Dieno + alqueno o alquino con retiro de electrones del grupo (dienofilo) => EHCH 22
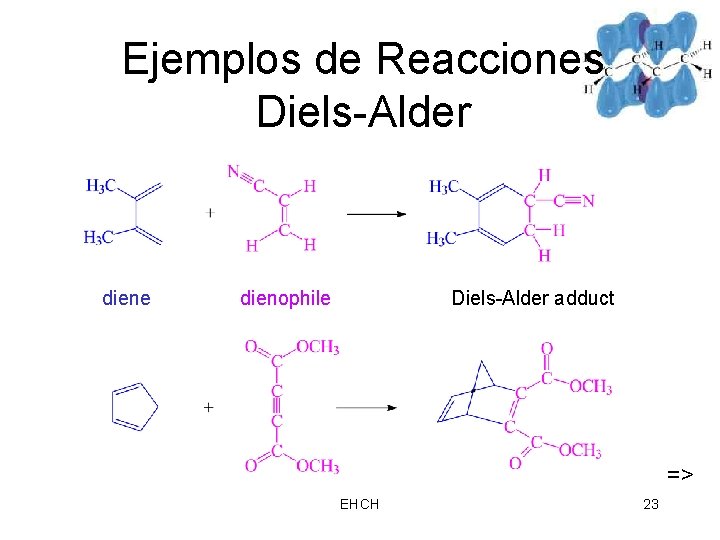
Ejemplos de Reacciones Diels-Alder diene dienophile Diels-Alder adduct => EHCH 23

Requisitos Estereoquimicos • Dieno debe ser en conformacion s-cis. • Dieno’s C 1 y C 4 deben sobreponer orbitales p con dienofilos de orbitales p para formar nuevos enlaces sigma. • Ambos enlaces sigma estan en la misma cara del dieno: sintesis estereoqumica. => EHCH 24
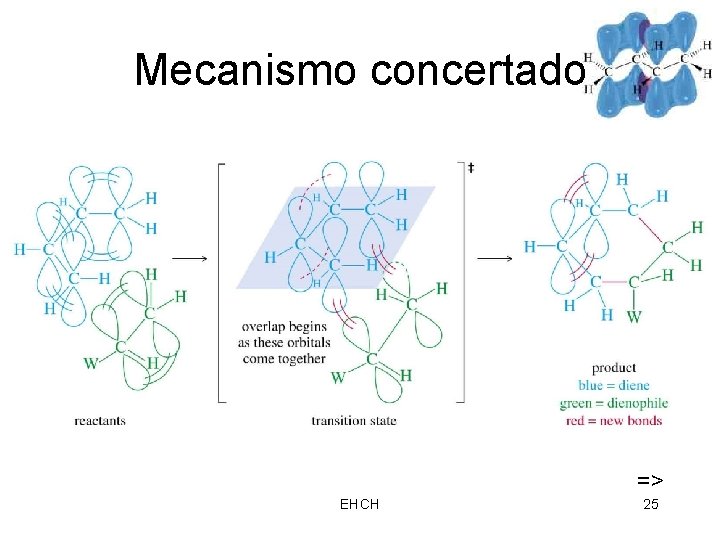
Mecanismo concertado => EHCH 25
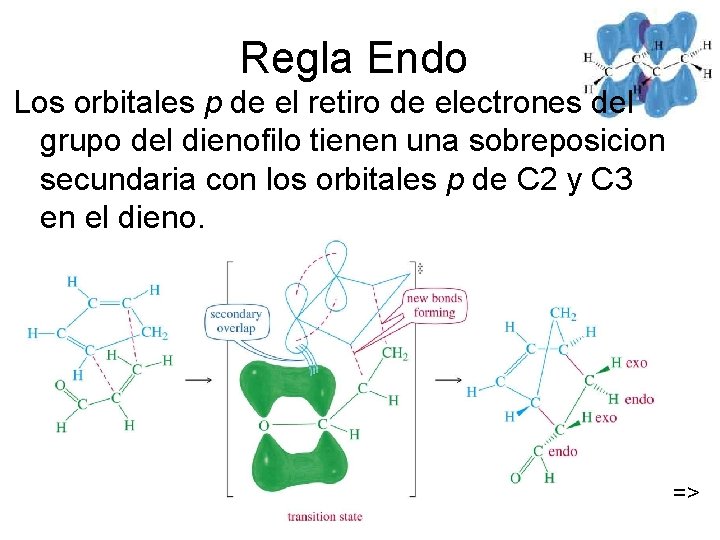
Regla Endo Los orbitales p de el retiro de electrones del grupo del dienofilo tienen una sobreposicion secundaria con los orbitales p de C 2 y C 3 en el dieno. Chaper 15 26 =>
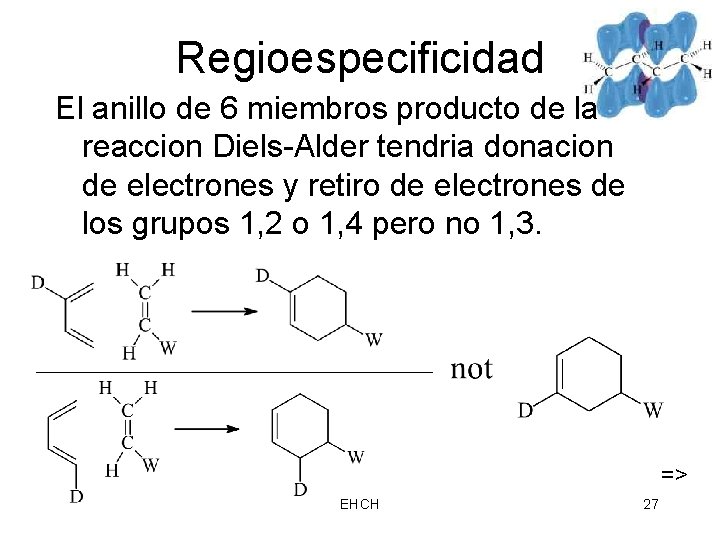
Regioespecificidad El anillo de 6 miembros producto de la reaccion Diels-Alder tendria donacion de electrones y retiro de electrones de los grupos 1, 2 o 1, 4 pero no 1, 3. => EHCH 27
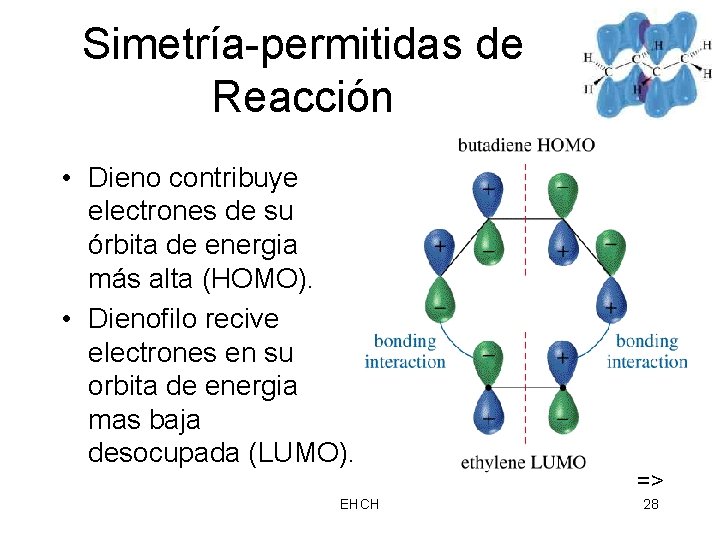
Simetría-permitidas de Reacción • Dieno contribuye electrones de su órbita de energia más alta (HOMO). • Dienofilo recive electrones en su orbita de energia mas baja desocupada (LUMO). EHCH => 28
![Cicloadicion “Prohibida” [2 + 2] cicloadicion de dos etilenos para formar ciclobuteno tiene anti-enlaces Cicloadicion “Prohibida” [2 + 2] cicloadicion de dos etilenos para formar ciclobuteno tiene anti-enlaces](http://slidetodoc.com/presentation_image_h2/71e496fceb4fd53f17466da5a31267d0/image-29.jpg)
Cicloadicion “Prohibida” [2 + 2] cicloadicion de dos etilenos para formar ciclobuteno tiene anti-enlaces sobrepuestos de HOMO y LUMO EHCH => 29
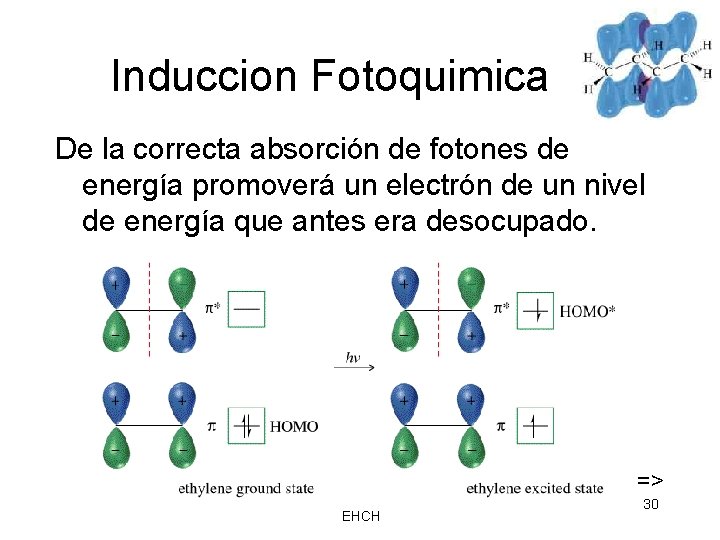
Induccion Fotoquimica De la correcta absorción de fotones de energía promoverá un electrón de un nivel de energía que antes era desocupado. => EHCH 30
![[2 + 2] Cicloadicion Fotoquímicamente permitido, pero térmicamente prohibido => EHCH 31 [2 + 2] Cicloadicion Fotoquímicamente permitido, pero térmicamente prohibido => EHCH 31](http://slidetodoc.com/presentation_image_h2/71e496fceb4fd53f17466da5a31267d0/image-31.jpg)
[2 + 2] Cicloadicion Fotoquímicamente permitido, pero térmicamente prohibido => EHCH 31

Espectroscopia Ultravioleta • 200 -400 nm fotones excitan los electrones de una union de orbitales a un antienlace de orbitales * • Dienos conjugados tienen MO’s que estan mas cerca de la energia • Un compuesto que tiene una cadena larga de dobles enlaces absorbe luz en una gran longitud de onda. => EHCH 32
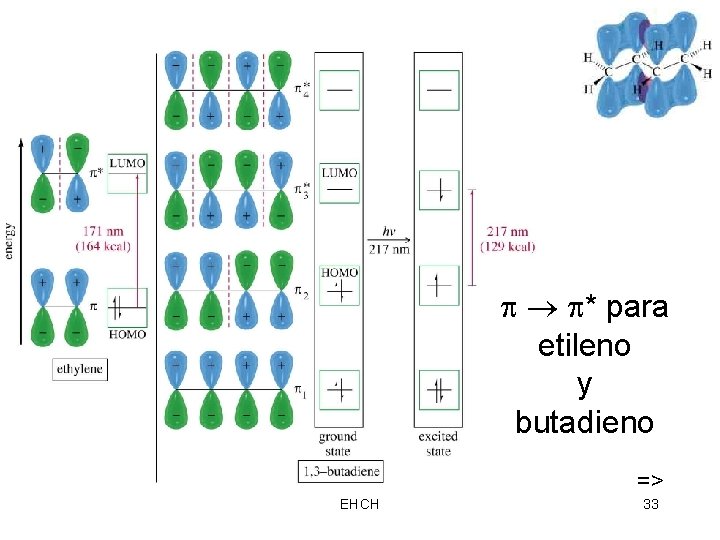
* para etileno y butadieno => EHCH 33

Obtencion de un Espectro UV • El espectrómetro mide la intensidad de un haz de referencia sólo a través de disolvente (Ir) y la intensidad de un haz a través de una solución de la muestra (Is). • La absorbancia es el log del radio • La grafica es absorbancia vs longitud de onda. => EHCH 34

El Espectro UV • Por lo general, muestra picos. • Lee max de la grafica. • Absorbancia, A, demuestra la ley de Beer’s: A = cl donde es la absortividad molar, c es la concentracion de la muestra en moles por litro, y l es la longitud de la trayectoria de la luz en centimetros. EHCH 35
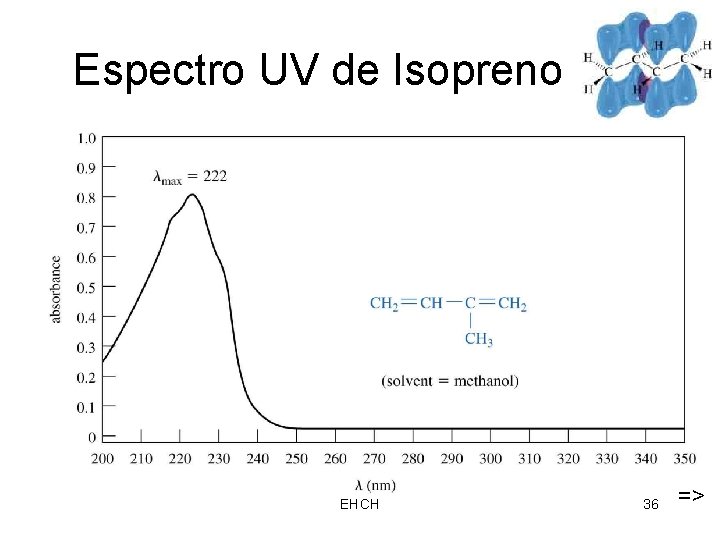
Espectro UV de Isopreno EHCH 36 =>
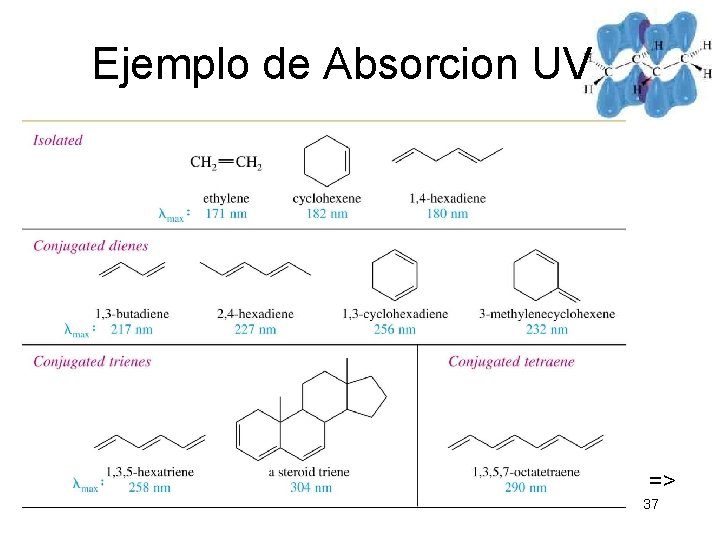
Ejemplo de Absorcion UV => Chaper 15 37

Reglas Woodward-Fieser => Chaper 15 38

EHCH 39
- Slides: 39