Sistema peridico y enlace 1 Sabiendo que el

Sistema periódico y enlace

1 • Sabiendo que el átomo de cloro tiene 17 electrones y 18 neutrones, a) ¿Cuál es su número atómico? ¿Y su número másico? b) Escribe la representación del átomo. a) Z=17; A=35. b) 35 17 Cl

2 • Dado el elemento químico de número atómico 12 y número másico 25 (Mg) determina: a) La constitución de su núcleo. b) La distribución de los electrones en el átomo neutro. c) El número de protones, neutrones y electrones que tiene el ion estable que forma. a) 12 protones y 13 neutrones. b) (2, 2, 6, 2). c) Mg 2+ tendría 12 protones, 13 neutrones y 10 electrones (2, 2, 6).
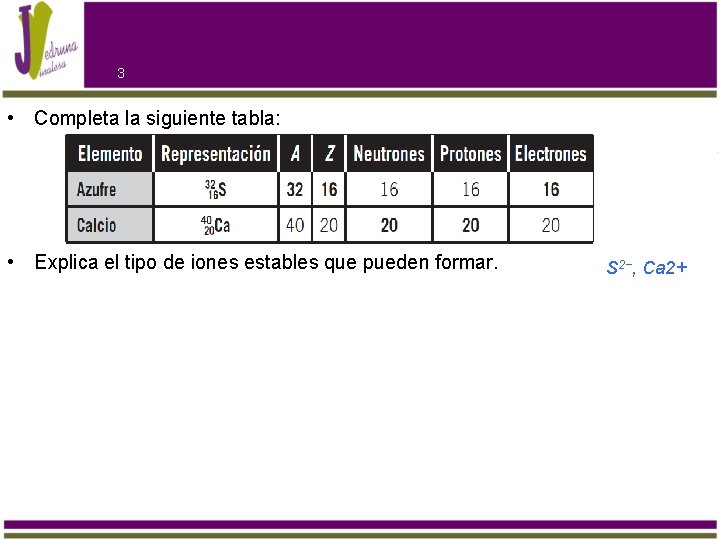
3 • Completa la siguiente tabla: • Explica el tipo de iones estables que pueden formar. S 2−, Ca 2+
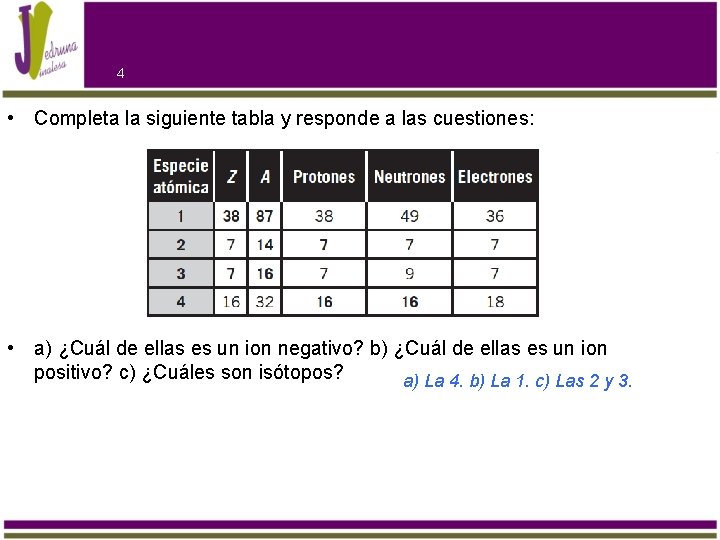
4 • Completa la siguiente tabla y responde a las cuestiones: • a) ¿Cuál de ellas es un ion negativo? b) ¿Cuál de ellas es un ion positivo? c) ¿Cuáles son isótopos? a) La 4. b) La 1. c) Las 2 y 3.
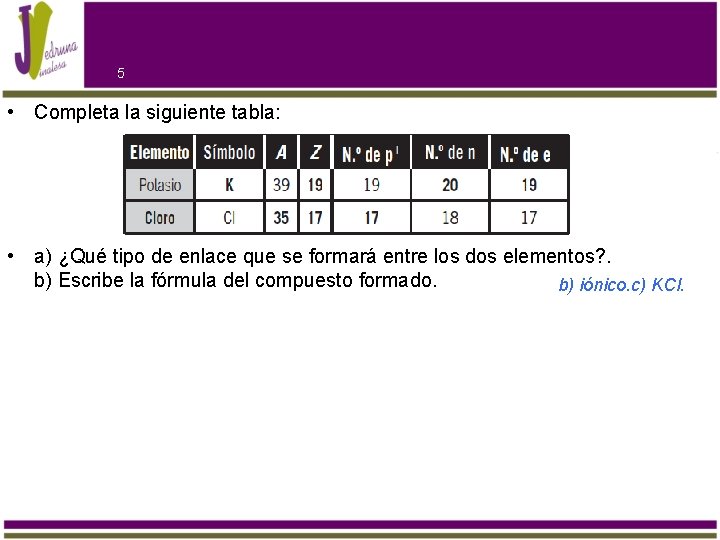
5 • Completa la siguiente tabla: • a) ¿Qué tipo de enlace que se formará entre los dos elementos? . b) Escribe la fórmula del compuesto formado. b) iónico. c) KCl.
6 • Establece el tipo de enlace entre átomos que aparecerá en los siguientes compuestos: a) KF: enlace iónico. a) Fluoruro de potasio. b) Al: enlace metálico. b) Aluminio. c) Si. O 2: enlace covalente. c) Dióxido de silicio. d) Br 2: enlace covalente. • d) Bromo. e) H 2 O: enlace covalente. e) Agua.

7 • Dados los iones siguientes: O 2−, F−, Ca 2+, K+. a) Indica el número de protones y electrones de cada uno. b) Escribe su distribución electrónica. c) ¿qué tienen en común todos ellos? . (Dato: números atómicos: O = 8; F = 9; Ca = 20; K=19. ) a) O 2−: 8 protones y 10 electrones. F−: 9 protones y 10 electrones. Ca 2+: 20 protones y 18 electrones. K+: 19 protones y 18 electrones. b) O 2−: (2, 8). F−: (2, 8). Ca 2+: (2, 8, 8). K+: (2, 8, 8). c) Todos tienen su último nivel de energía completo con 8 electrones

8 • Dado el átomo 27 13 Al, expresa toda la información acerca de su estructura y sus propiedades que puedes sacar con esta representación Z = 13 y A = 27; tiene 13 protones, 14 neutrones y 13 electrones. Es un metal con tendencia a perder 3 electrones y formar el ion Al 3+.
9 • Explica el tipo de enlace que aparece en las siguientes sustancias y escribe su fórmula: a) Li. Cl: enlace iónico. a) Cloruro de litio. b) H 2: enlace covalente. b) Hidrógeno. c) CCl 4: enlace covalente. c) Tetracloruro de carbono.
10

1 11 • Describe las partículas fundamentales constituyentes del átomo e indica el número de partículasque hay en el átomo representado por 190 Os. 76 76 protones, 76 electrones y 114 neutrones.
12 • Determina el número de partículas de cada tipo que hay en los siguientes 133 átomos: a) 200 Hg. b) 55 Cs 80 a) 80 protones, 120 neutrones y 80 electrones; b) 55 protones, 78 neutrones y 55 electrones
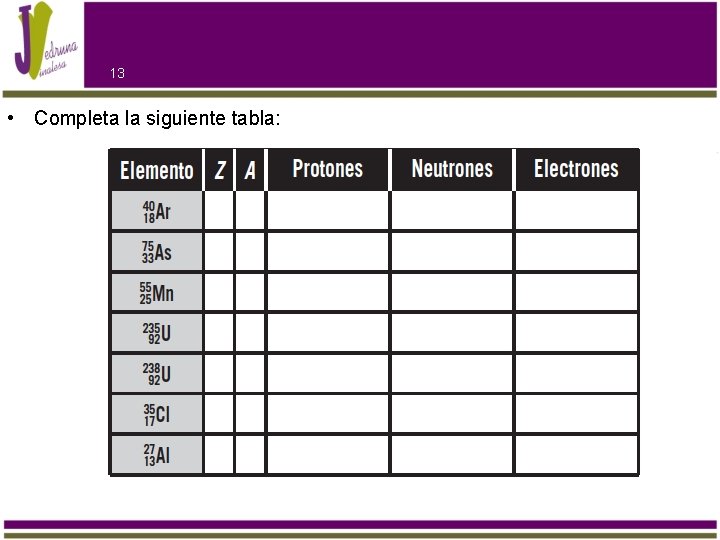
13 • Completa la siguiente tabla:
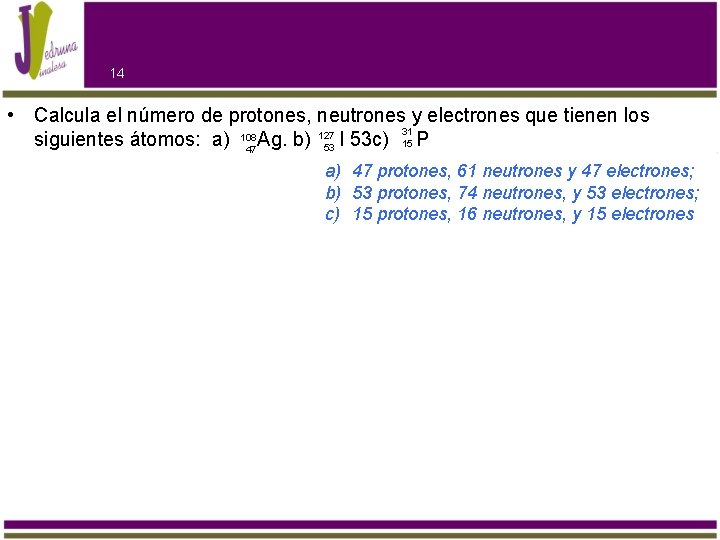
14 • Calcula el número de protones, neutrones y electrones que tienen los 31 127 siguientes átomos: a) 108 Ag. b) I 53 c) 15 P 53 47 a) 47 protones, 61 neutrones y 47 electrones; b) 53 protones, 74 neutrones, y 53 electrones; c) 15 protones, 16 neutrones, y 15 electrones

2 15 • Completa la siguiente tabla: y ordena de mayor a menor la energía de ionización (energía necesaria para arrancar un electrón) de los elementos anteriores. Ne > S > Ca
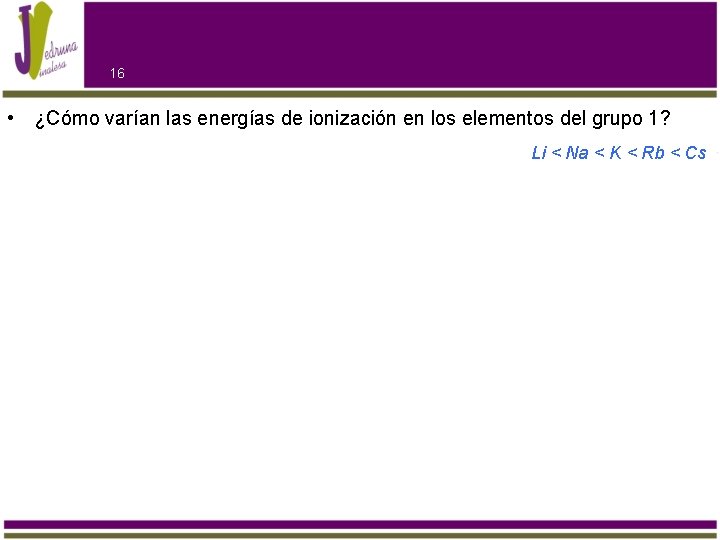
16 • ¿Cómo varían las energías de ionización en los elementos del grupo 1? Li < Na < K < Rb < Cs
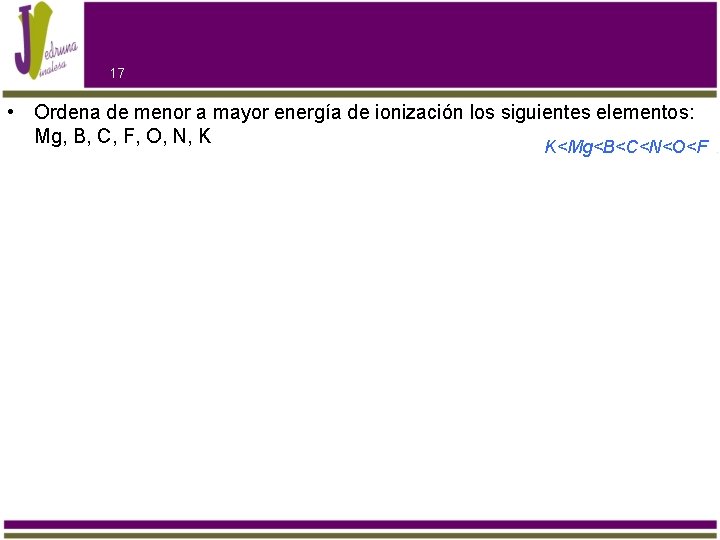
17 • Ordena de menor a mayor energía de ionización los siguientes elementos: Mg, B, C, F, O, N, K K<Mg<B<C<N<O<F

3 18 • La estructura electrónica de un elemento es (2, 5). a) ¿Cuál es su número atómico? b) ¿Qué posición ocupa en el sistema periódico? c) ¿Es un metal o un no metal? d) ¿De qué elemento se trata? e) Nombra otros elementos que pertenezcan al mismo grupo. f) Supón que gana un electrón. Completa la siguiente tabla: a) 7; b) pertenecerá al grupo 15; c) es un no metal; d) Es el N. e) P, As, Sb y Bi
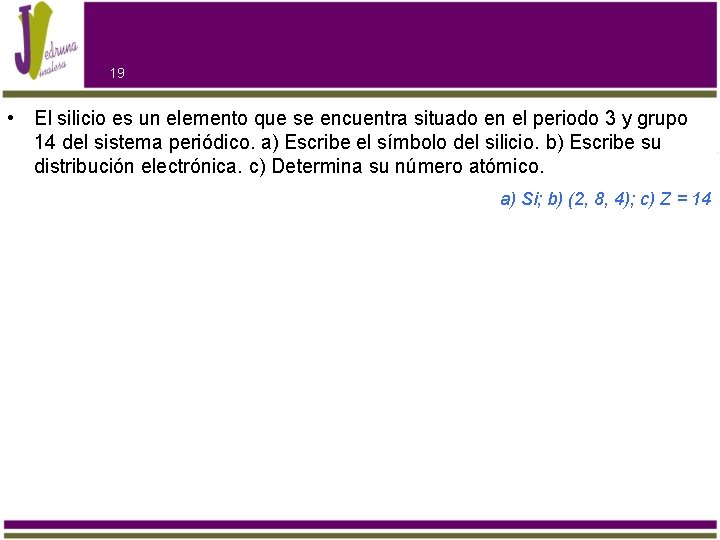
19 • El silicio es un elemento que se encuentra situado en el periodo 3 y grupo 14 del sistema periódico. a) Escribe el símbolo del silicio. b) Escribe su distribución electrónica. c) Determina su número atómico. a) Si; b) (2, 8, 4); c) Z = 14
20 • Un elemento X está situado en el periodo 3 y grupo 17 del sistema periódico. a) ¿Cuál es su distribución electrónica? b) ¿Cuál es su número atómico? c) ¿Qué elemento es? a) (2, 8, 7); b) Z = 17; c) Cloro, Cl

4 21 • Con el fin de determinar el tipo de enlace que une a los átomos en tres sustancias desconocidas A, B y C, se han realizado los siguientes ensayos, cuyos resultados aparecen en la siguiente tabla: Justifica el tipo de enlace que cabe esperar en las sustancias A, B y C. La sustancia A es un compuesto iónico. La sustancia B es un metal. La sustancia C es un compuesto covalente.
22 • Dados los átomos 73 Li, 168 O, 35 17 Cl. a) Explica el tipo de enlace que aparece cuando se combina el litio con el oxígeno. b) Explica el tipo de enlace que aparece cuando se combina el cloro con el oxígeno. a) iónico; b) covalente
23 • Clasifica las siguientes sustancias por el enlace químico que presentan: Na. Cl, H 2 O, N 2, Fe, SO 2 Iónico, covalente, metálico, covalente
24 • Indica razonadamente el tipo de enlace existente en las siguientes sustancias: Cl 2, Fe. Cl 2, Na. Br, SO 3, Mg y C Covalente, iónico, covalente, metálico y covalente

25 • Ordena las siguientes sustancias en orden creciente de sus puntos de fusión (atendiendo al enlace que presentan): N 2, Cu, CO 2 y H 2 O N 2 < CO 2 < H 2 O < Cu
26 • El magnesio se une al bromo para formar el bromuro de magnesio. a) ¿Con qué tipo de enlace se unen? b) ¿Qué propiedades cabe esperar para el compuesto bromuro de magnesio? a) Iónico; b) Propiedades de los compuestos iónicos

27 • Escribe la configuración electrónica de todos los elementos del grupo de los halógenos. ¿Qué tienen todos ellos en común? Flúor. 1 s 2 2 p 5 Cloro. 1 s 2 2 p 6 3 s 2 3 p 5 Bromo. 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 5 Yodo. 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 6 5 s 2 4 d 10 5 p 5 Astato. 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 10 4 p 6 5 s 2 4 d 10 5 p 6 6 s 2 5 d 10 6 p 5 Todos tienen la misma estructura en el último nivel: 5 p 5

CONFIGURACIÓN ELECTRÓNICA ABREVIADA 28 • Escribe la configuración electrónica abreviada de: a) Arsénico. b) Un elemento que contiene 25 electrones. c) Silicio. d) El elemento número 53. e) Sodio. f) Ion cadmio, Cd 2+. [Ar] 4 s 2 3 d 10 4 p 3 [Ar] 4 s 2 3 d 5 [Ne] 3 s 2 3 p 2 [Kr] 5 s 2 4 d 10 5 p 5 [Ne] 3 s 1 [Kr] 4 d 10
- Slides: 29