Sistema de Barreira Estril e rastreamento para processos

Sistema de Barreira Estéril e rastreamento para processos de esterilização Artigos: 38, 77 a 85 Resolução RDC 15 – Última Chamada Maria Águida Cassola Outubro 2013

Artigos RDC 15 Art. 38 As leitoras de indicadores biológicos e as seladoras térmicas devem ser calibradas, no mínimo, anualmente. Art. 77 O CME e a empresa processadora devem utilizar embalagens que garantam a manutenção da esterilidade do conteúdo, bem como a sua transferência sob técnica asséptica. Art. 78 As embalagens utilizadas para a esterilização de produtos para saúde devem estar regularizadas junto à Anvisa, para uso especifico em esterilização. Art. 79 Não é permitido o uso de embalagens de papel kraft, papel toalha, papel manilha, papel jornal e lâminas de alumínio, assim como as embalagens tipo envelope de plástico transparente não destinadas ao uso em equipamentos de esterilização. Art. 80 A selagem de embalagens tipo envelope deve ser feita por termoseladora ou conforme orientação do fabricante. Art. 81 Não é permitido o uso de caixas metálicas sem furos para esterilização de produtos para saúde. Art. 82 O CME que utiliza embalagem de tecido de algodão, deve possuir um plano contendo critérios de aquisição e substituição do arsenal de embalagem de tecido mantendo os registros desta movimentação. Parágrafo único. Não é permitido o uso de embalagens de tecido de algodão reparadas com remendos ou cerzidas e sempre que for evidenciada a presença de perfurações, rasgos, desgaste do tecido ou comprometimento da função de barreira, a embalagem deve ter sua utilização suspensa. Art. 83 É obrigatória a identificação nas embalagens dos produtos para saúde submetidos à esterilização por meio de rótulos ou etiquetas. Art. 84 O rótulo dos produtos para saúde processados deve ser capaz de se manter legível e afixado nas embalagens durante a esterilização, transporte, armazenamento, distribuição e até o momento do uso. Art. 85 O rótulo de identificação da embalagem deve conter: I - nome do produto; II - número do lote; III - data da esterilização; IV - data limite de uso; V - método de esterilização; VI - nome do responsável pelo preparo.

EMBALAGEM SISTEMA DE BARREIRA ESTÉRIL (SBE) Direitodeconsumirwordpress. com

Registro de Embalagens Requerimentos Anvisa ◦ ◦ ◦ Nome comercial produto Instruções Uso Especificações Técnicas, Dimensões, Volumes Foto do produto Rótulo ( contendo lote, validade - na menor unidade de venda) ◦ Estudo de Estabilidade para det. prazo de validade ◦ Documentação fabricante e importador

“EMBALAGENS” MÉDICAS Sistema de Barreira Estéril ( SBE/SBS) Instituições de Saúde e Fabricantes de Artigos Médicos Legislação: ◦ ◦ ISO 11607 (Partes 1 e 2) EN 868 ( Partes 1 a 5) ABNT 14990 ISO 16775 -Guias de Uso de Normas (em desenvolvimento)

ISO 11607 -1 e 2 Principais pontos de esclarecimento: ◦ 4. 1. 1 – Quality System - The activities described within and subsequent clauses of this International Standard shal be carried out within a formal quality system. Note: It´s not necessary to obtain third party certification of the quality system to fullfil the requirements of this International Standard. ◦ 4. 1. 2 – Sampling – The sampling plans used for selection and testing of packaging materials shall be chosen by agreement between involved parts. ◦ 4. 1. 3. 5 – The following material properties shall be evaluated with appropriate test methods agreed by producer and manufacturer: Microbial barrier Toxicological attributes Physical and chemical properties Compatiblity with Sterilization process Compatibility with forming and sealing process Shelf life limitations for presterilzation and poststerilzation storage (Part 2 – Validation requirements forming, sealing and assembly processes)

ISO 11607 -1 e 2 Principais pontos de esclarecimento: ◦ 4. 1. 8. Responsibilities ◦ 4. 1. 8. 1 It shall be the responsibility of manufacturer to ensure that the final package is validated in accordance with this International Standard ◦ 4. 1. 8. 2 The responsibility for conducting compliance qualification tests on materials shall rest to the producer ◦ 4. 1. 8. 3. The responsability for conducting performance qualification tests shall rest with the manufacturer. Definições: Producer – fabricante material da embalagem Manufacturer – relacionado à esterilização do produto
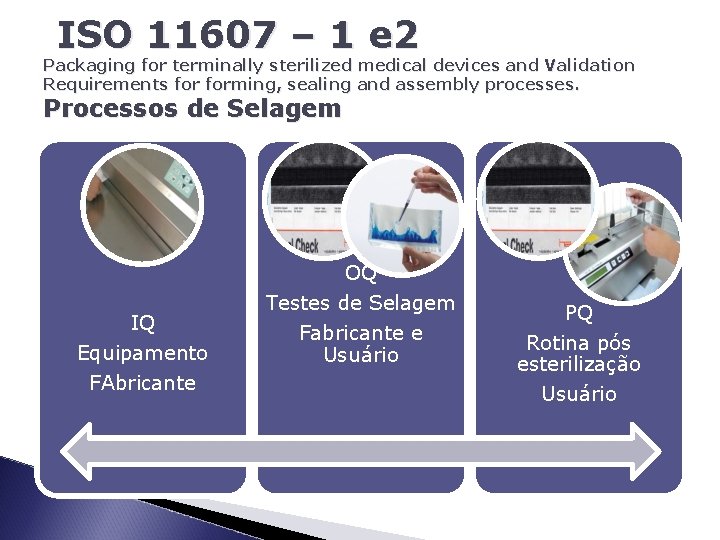
ISO 11607 – 1 e 2 Packaging for terminally sterilized medical devices and Validation Requirements forming, sealing and assembly processes. Processos de Selagem IQ Equipamento FAbricante OQ Testes de Selagem Fabricante e Usuário PQ Rotina pós esterilização Usuário

IQ – Equipamento de Selagem “Documentação que evidencia que o equipamento foi fornecido e instalado de acordo com especificação” Características de projeto e fabricação do equipamento Habilidade de controlar e monitorar parâmetros críticos de processo ( P, T , V) Segurança Lista de partes e peças Alarmes ou outros sistemas que demonstrem falhas do sistema Especificações de Calibração escritas pelo Fabricante Agenda de limpeza e manutenção preventiva Mecanismos de controle que “ avisam “ falhas de processo. Treinamento de usuários documentado Conexão com softwares de documentação ou controle devem ser validados. Ex. Simulação de entrada de dados corretos e incorretos ou queda de energia para detectar confiabilidade e rastreabilidade de dados.

Calibração de Fábrica Verificar documentação enviada pelo fabricante. Montar um plano de calibração anual ou de acordo com especificação do fabricante. Art. 38 As leitoras de indicadores biológicos e as seladoras térmicas devem ser calibradas, no mínimo, anualmente.

Calibração de Seladoras Sensor Temperatura (calibrar temperatura de selagem) DMS (calibrar pressão de selagem) Tacômetro (calibrar velocidade de selagem)

OQ – Embalagem + Seladora “Documentos que evidenciam que o equipamento opera de acordo com limites prédeterminados, quando usado de acordo com procedimentos operacionais” Peeling test (VISUAL) ◦ Deve ser feita por um inspetor com acuidade visual normal ◦ Delaminação permitida até 10 mm ◦ Caso haja desvios, os mesmos devem ser corrigidos Deve-se verificar também: ◦ ◦ Presença de material estranho Dimensão ( 30 mm da borda e do artigo médico) Integridade da selagem ( seal check ou similar) Presença de umidade ou manchas

OQ – SBE + Seladora Propriedades de Qualidade Selagem: ◦ Continuidade da Selagem para uma largura pré-definida ( min 6 mm de acordo com ABNT 14990 – 7 e EN 868 -5) ◦ Nenhuma abertura ◦ Sem vincos ou dobras ◦ Sem delaminação ou separação do material Indicadores de Selagem ◦ Determinação Parâmetros da selagem

OQ – SBE + Seladora Set a seladora nas temperaturas mínimas e máximas indicadas pelo fabricante da embalagem e sele-as sem o uso de seal check.

Fazendo o teste

OQ – SBE + Seladora Checar se a selagem está intacta com teste visual e seal check ü

OQ – SBE + Seladora Definir a temperatura de selagem ( média entre mínima e máxima). Nesse caso é de 188 graus C.

Uso de Indicadores de Selagem – OQ e Rotina

Exemplos Seal Check Resultado Seal Check Visualização Normal
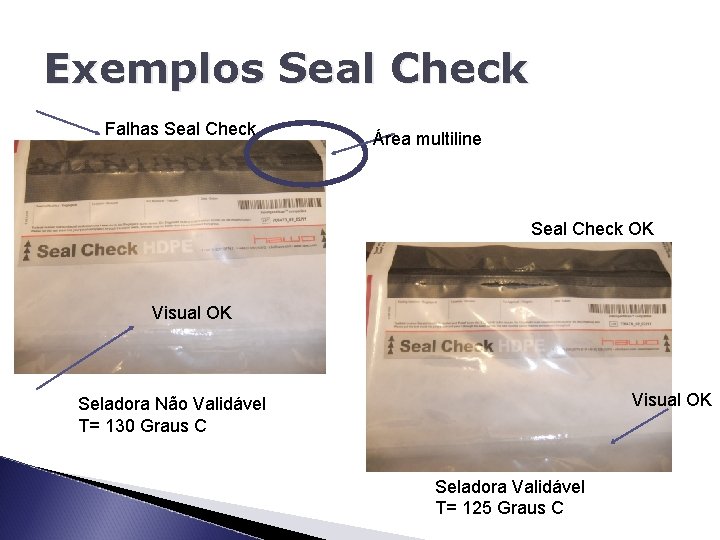
Exemplos Seal Check Falhas Seal Check Área multiline Seal Check OK Visual OK Seladora Não Validável T= 130 Graus C Seladora Validável T= 125 Graus C

PQ – Rotinas “ Documentos que evidenciam que o equipamento consistentemente desempenha de acordo com critérios pré –estabelecidos atingindo a especificação do produto” Força tensil para cada processo de esterilização ◦ ◦ 5 a 10 amostras por processo Resultado: > 1, 5 N/15 mm – EN 868 -5 Análise de desvios e ações corretivas Análise anual ou em revalidações Parâmetros críticos devem ser monitorados e documentados rotineiramente Vários métodos- Força Tensil ou Explosão e Ruptura (EN 868 -5 - annex D ou ASTM F 88)

Equipamento – Teste força tensil pós esterilização

EM 868 -5 EN 868 -5 Annex D
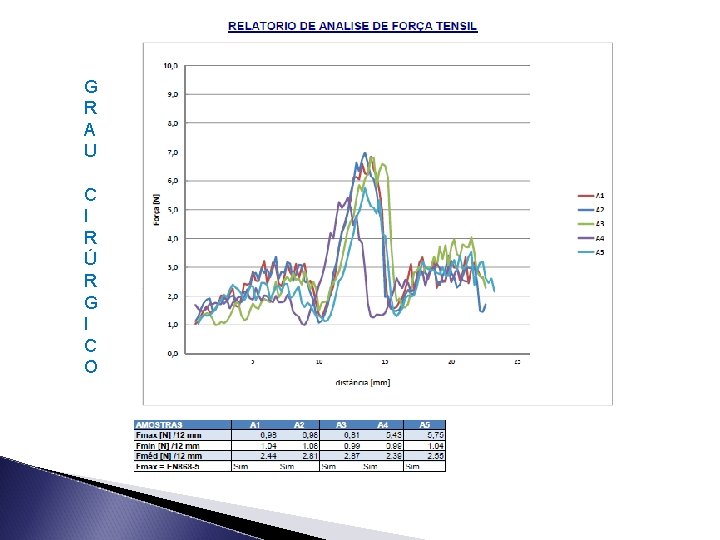
G R A U C I R Ú R G I C O

Outros materiais Embalagens não seláveis Validação baseada em IQ/OQ/PQ ( quando existe um equipamento) Verificação baseada em: ◦ 4. 1. 3. 5 – The following material properties shall be evaluated with appropriate test methods agreed by producer and manufacturer: Microbial barrier Toxicological attributes Physical and chemical properties Compatiblity with Sterilization process Compatibility with forming and sealing process Shelf life limitations for presterilzation and poststerilzation storage (Part 2 – Validation requirements forming, sealing and assembly processes)

Sistemas de Barreira Estéril

Sistemas de Barreira Estéril Embalagem Rígida Embalagem Flexível

Sistemas de Barreira ? ? ? Estéril X
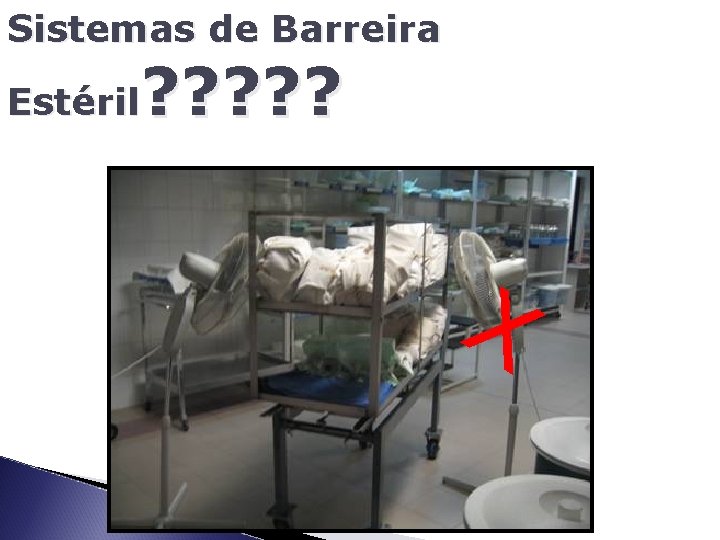
Sistemas de Barreira ? ? ? Estéril X

Sistemas de Barreira ? ? ? Estéril X Estudo da Universidade de Tubingen ( Alemanha) encontrou mais de 30% de falhas em embalagens Auto-selantes.

Impressão e Rotulagem

Rotulagem Área de Produção SBE

Impressões e Rotulagem Sistemas inteligentes- Definição parâmetros Identificação Impressão Rastreabilidade

Rotulagem

Revalidações Lista de variáveis que podem afetar o status do processo validado: ◦ ◦ Mudanças na matéria prima Nova peça instalada no equipamento Mudança do local de instalação Mudança nos parâmetros do processo de esterilização ◦ Tendência negativa na qualidade ou indicadores de processo

Referências ISO 11607 - 1 e 2 - Packaging for terminally sterilized devices ABNT NBR 14990 – Sistemas e materiais de embalagem para esterilização Zentral Sterilisation – Guideline for the Validation of the Sealing Process According to EN ISO 11607 -2 – A. Carter (German Society for Sterilization Supply, DGSV) – Vol 16, 2008. Validação do Processo de Selagem em Embalagens de Produtos Reprocessados na Central de Esterilização – Maria Águida Cassola - Revista Sobecc – Ano 17 Número 2, Abr/Jun 2012

“ We can not change the human condition, but we can change the conditions under which humans work” by Dr. James Reason “ Não podemos mudar a condição humana, mas podemos mudar as condições nas quais os humanos trabalham” OBRIGADA! aguidacassola@terra. com. br 11 9 9798 1024
- Slides: 37