SINH KH DNG V TNG NG SINH HC
























- Slides: 29

SINH KHẢ DỤNG VÀ TƯƠNG ĐƯƠNG SINH HỌC TỔNG QUAN Phùng Thị Vinh

Nội dung n Khái niệm n n Thuốc mới, generic, inovator Sinh khả dụng, tương đương sinh học Ý nghĩa của TĐSH Yêu cầu chứng minh TĐSH 2

3

4

5

6

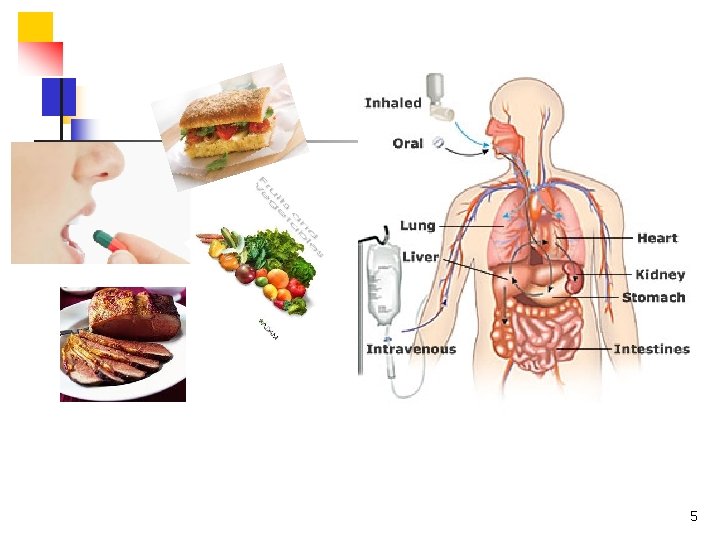
… ? ? ? n n n Thuốc được hấp thu vào cơ thể ? Chuyển hóa, phân bố thuốc/ cơ thể ? Yếu tổ ảnh hưởng (thức ăn) ? Đối tượng sử dụng (người lớn, trẻ em, người già, suy giảm chức năng) ? Một loại thuốc (dược chất, dạng bào chế giống nhau; NSX khác nhau Hiệu quả có giống nhau không ? 7

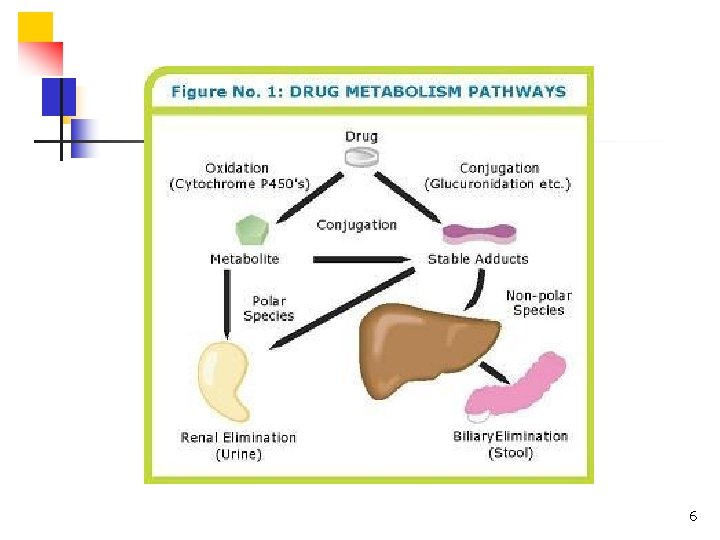
Câu trả lời ? n n n Chất lượng có giống nhau ? Tác động của thuốc trong cơ thể ? (sinh khả dụng) Có thay thế cho nhau được không ? (tương đương sinh học) 8

KHÁI NiỆM 9

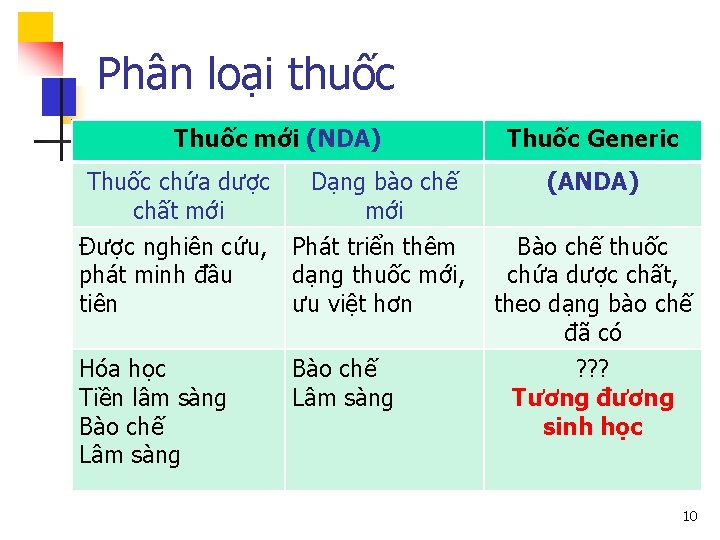
Phân loại thuốc Thuốc mới (NDA) Thuốc Generic Thuốc chứa dược chất mới Dạng bào chế mới (ANDA) Được nghiên cứu, phát minh đầu tiên Phát triển thêm dạng thuốc mới, ưu việt hơn Hóa học Tiền lâm sàng Bào chế Lâm sàng Bào chế thuốc chứa dược chất, theo dạng bào chế đã có ? ? ? Tương đương sinh học 10

KHÁI NIỆM n Tương đương bào chế n n Dược chất giống nhau Cùng dạng bào chế, hàm lượng Đạt cùng mức tiêu chuẩn chất lượng Thế phẩm bào chế n n Chứa cùng dược chất, dược chất có thể dưới dạng khác nhau (muối, este) Dạng bào chế, hàm lượng có thể khác 11

KHÁI NIỆM n Thuốc đối chứng (dùng trong NC so sánh SKD/ đánh giá TĐSH) n Thuốc phát minh n Chế phẩm có uy tín nhất trên thị trường n Chế phẩm đã được cấp phép, được cơ quan quản lý chấp thuận n Đáp ứng nguyên tắc lựa chọn (khu vực, quốc gia) 12

KHÁI NIỆM n n Dược động học: Quá trình thuốc hấp thu vào cơ thể thải trừ ra khỏi n Cmax , AUC, Tmax; Cmin, Cav/ Css n T 1/2 ; kel; Vd; Clr Sinh khả dụng (bioavailability): n Tốc độ, mức độ hấp thu của dược chất/ chất có tác dụng; Sẵn có ở nơi tác dụng n F% (AUC), Tmax; Cmax 13

KHÁI NIỆM n n Tương đương sinh học (bioequivalence): n Tương đương bào chế/ thế phẩm bào chế n Sinh khả dụng (tốc độ và mức độ hấp thu) khác nhau không đáng kể n Cùng mức liều; Cùng điều kiện thử nghiệm. FDA mở rộng: Tốc độ (Tmax) khác nhau có chủ ý được coi là TĐSH 14

KHÁI NIỆM n n Sinh khả dụng: là đặc tính biểu thị tốc độ và mức độ hấp thu của dược chất hoặc chất có tác dụng vào tuần hoàn chung và sẵn có ở nơi tác dụng; Hoặc một cách đầy đủ hơn là: sinh khả dụng biểu thị mức độ và tốc độ dược chất hoặc chất có tác dụng giải phóng ra khỏi dạng bào chế và sẵn có ở tuần hoàn chung. Tương đương sinh học: là thuật ngữ chỉ hai thuốc tương đương bào chế hoặc thế phẩm bào chế có sinh khả dụng của cùng một mức liều tương tự nhau, trong cùng điều kiện thử nghiệm. 15

KHÁI NIỆM n Nghiên cứu dược động học: NC xác định các thông số DĐH (động vật TN/ người) n Nghiên cứu sinh khả dụng: Xác định các thông số DĐH, các yếu tố ảnh hưởng, các đối tượng khác nhau (người già, trẻ em…) n Đánh giá TĐSH: So sánh 2 chế phẩm trong điều kiện sinh học như nhau bằng phương pháp chuẩn hóa 16

Ý NGHĨA CỦA DỮ LiỆU SKD & TĐSH 17

% BE ? trong cấu thành hiệu quả thuốc "Bánh Trung thu " Sử dụng Nghiên cứu phát triển Phân phối Đánh giá chất lượng (QC & BE) Sản xuất 18

Ý nghĩa về khoa học (SKD) n Cho biết đặc tính sinh học của thuốc: n n Thông số dược động học chung Đặc tính DĐH của thuốc trong các điều kiện sinh học khác nhau (trạng thái no, đói, sinh lý già/ trẻ, nam/ nữ; bệnh lý)… n Dự đoán hiệu quả điều trị thông qua đặc tính sinh khả dụng so sánh (tốt hơn/ kém chế phẩm so sánh) n Theo dõi điều trị (điều chỉnh liều) 19

Ý nghĩa về khoa học … n n n Khả năng so sánh chất lượng của thuốc Bằng chứng về mức độ TĐSH của chế phẩm nghiên cứu so với thuốc đối chứng. Khả năng thay thế các thuốc đối chứng (thuốc phát minh, đắt tiền) bằng các thuốc generic đã được chứng minh TĐSH (inter-changeable/ inter-changeability) 20

Ý nghĩa về thực tiễn n Sản xuất (nghiên cứu phát triển): Tối ưu hóa công thức/kỹ thuật bào chế thuốc có SKD cao n Quản lý: Xét cấp phép lưu hành; n Công bố thuốc chứng minh TĐSH. n n Sử dụng, điều trị: Lựa chọn thuốc có chất lượng trong điều trị (“thầu”) 21

Ý nghĩa khác … n Doanh nghiệp: Chiến lược phát triển sản phẩm, xây dựng thương hiệu, cạnh tranh lành mạnh. n Quốc gia: Xây dựng hàng rào kỹ thuật trong hội nhập kinh tế toàn cầu, khu vực. n Xã hội: Góp phần đảm bảo công bằng và lợi ích cho người bệnh trong điều trị 22

Yêu cầu dữ liệu SKD/TĐSH Theo qui định của từng quốc gia. Nguyên tắc chung: n Không cần thiết với tất cả các dạng bào chế n Không thể thực hiện với tất cả các loại thuốc n Qui định chung, và xem xét trên trường hợp cụ thể n 23

Một số qui định chung: n Thuốc uống dạng rắn: Viên nén, viên nang, thuốc bột. . . n Thuốc có khoảng điều trị hẹp; n Thuốc tác dụng kéo dài (phóng thích chậm, có kiểm soát) Một số dạng bào chế khác: qua da, trực tràng, dạng thuốc đặc biệt Không bắt buộc với: thuốc tiêm TM, tiêm bắp, thuốc tác dụng tại chỗ, thuốc nhỏ mắt, mũi, xông, hít. . . (dạng dung dịch/ nước) n n n 24

Thế giới ? ? n n Dữ liệu để cấp phép lưu hành (qui chế đăng ký thuốc): Hầu hết các quốc gia có qui định Danh mục các thuốc bắt buộc phải có dữ liệu TĐSH khác nhau ở các quốc gia n n n Tất cả thuốc Thuốc kê đơn Một số theo danh mục, tăng dần. 25

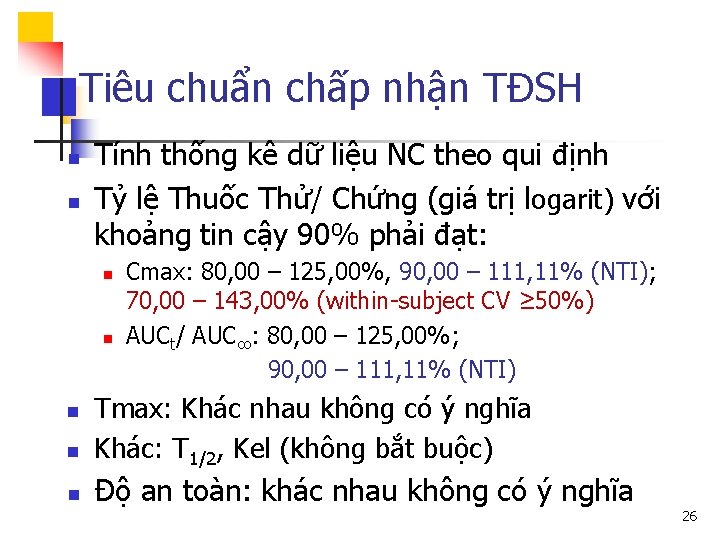
Tiêu chuẩn chấp nhận TĐSH n n Tính thống kê dữ liệu NC theo qui định Tỷ lệ Thuốc Thử/ Chứng (giá trị logarit) với khoảng tin cậy 90% phải đạt: n n Cmax: 80, 00 – 125, 00%, 90, 00 – 111, 11% (NTI); 70, 00 – 143, 00% (within-subject CV ≥ 50%) AUCt/ AUC∞: 80, 00 – 125, 00%; 90, 00 – 111, 11% (NTI) n Tmax: Khác nhau không có ý nghĩa Khác: T 1/2, Kel (không bắt buộc) n Độ an toàn: khác nhau không có ý nghĩa n 26

Xem xét trên kq TĐSH ? Thuốc mới Dược chất mới Nghiên cứu hóa học Tiền lâm sàng Bào chế Lâm sàng Thuốc Generic Dạng bào chế mới Bào chế Lâm sàng - Tương đương sinh học OK - Không tương đương sinh học ? Thay đổi bào chế Thử lâm sàng để chứng minh 27

Tài liệu tham khảo (Guidelines) n Tra cứu: “SEARCH” / Google n BEBAC. Consultancy services for bioequivalence - Guidelines n Mỹ: http: //www. fda. gov; http: //www. fda. gov/cder/guidance; n Châu u (http: //www. emea. europa. eu n WHO: http: //www. who. int n Việt nam – Cục QL Dược (http: //www. dav. gov. vn) 28

Dừng bước ? 29