Simpozij o istraivanju i bolestima mozga 16 oujka

Simpozij o istraživanju i bolestima mozga 16. ožujka 2016. Preporodna dvorana HAZU, Opatička 18, Zagreb Epigenomika Alzheimerove bolesti Prof. dr. sc. Goran Šimić, dr. med. Zavod za neuroznanost Hrvatski institut za istraživanje mozga, Šalata 12 Medicinski fakultet Sveučilišta u Zagrebu ZAGREB 10000, REPUBLIKA HRVATSKA Hrvatska zaklada za znanost Projekt IP-2014 -09 -9730 (2015 -2019) Croatian Science Foundation
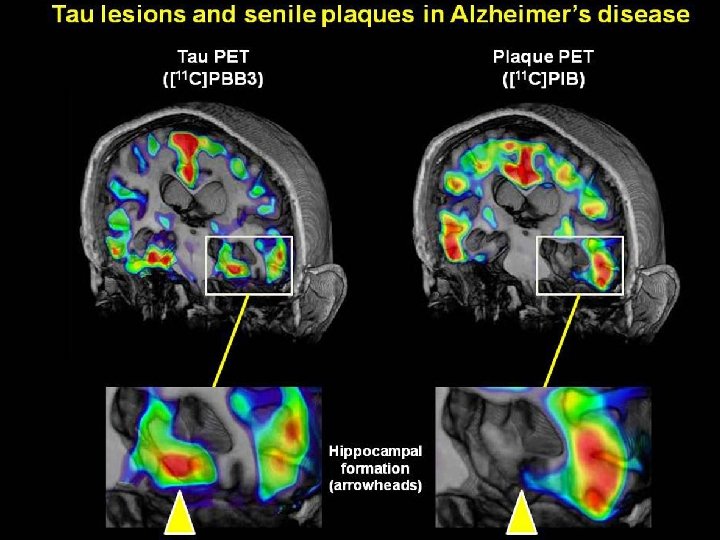
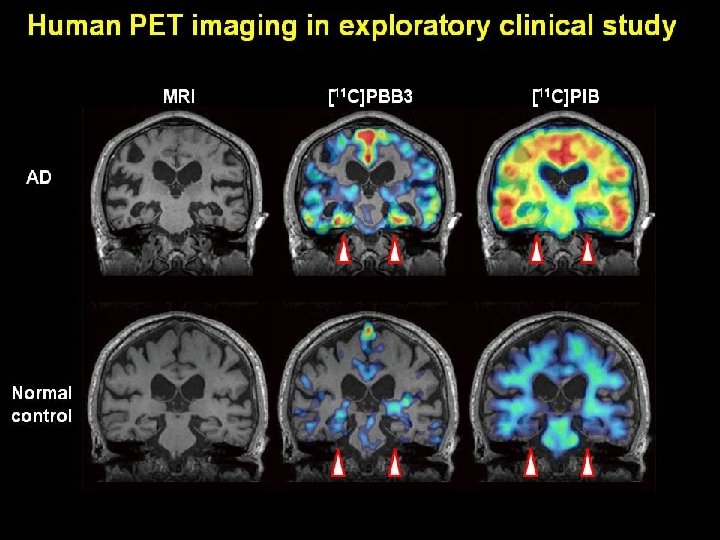

18 F-AV-1451 PET Schöll et al. , PET imaging of tau deposition in the aging human brain. Neuron 2016 nakupljanje patoloških tau proteina u obliku sparenih uzvojitih filamenata (PHF) u starijih osoba se vidi samo u sljepoočnom dijelu sljepoočnog režnja i povezano je s neprogresivnim oštećenjem epizodičkog deklarativnog pamćenja (strelica) (PART), a za ostala područja podrazumijeva prisutnost A i dobro korelira s općim stupnjem propadanja spoznajnih sposobnosti (demencijom); taj nalaz potvrđuje in vitro i in vivo zapažanja da reduciranje količine endogenog tau proteina sprječava štetno djelovanje A (Roberson et al. , Science 2007); A je u AD katalizator patoloških promjena tau proteina

Oblici Alzheimerove bolesti AB s ranim početkom (EOAD, obiteljska): prije 60. /65. godine života): 1/6% svih oboljelih 61% svih oboljelih od AB mlađih od 60 godina života ima poz. obiteljsku anamnezu, a od njih 13% (tj. sveukupno 7, 93% mlađih od 60 godina) zadovoljava striktne kriterije za autosomno dominantno nasljeđivanje (dokumentirana bolest u 3 generacije) nastaje uslijed obiteljskih mutacija 3 gena: 1. gena za prekursorni protein amiloida, APP (na 21. kromosomu) - do sada otkrivene 34 mutacije koje uzrokuju bolest 2. presenilina 1, PS-1 (na 14. kromosomu) - do sada otkriveno 185 mutacija koje uzrokuju bolest 3. presenilina 2, PS-2 (na 1. kromosomu) - do sada otkriveno 13 mutacija koje uzrokuju bolest AB s kasnim početkom (LOAD, sporadična): 94 -99% svih oboljelih Bird, Genet. Med. , 2008
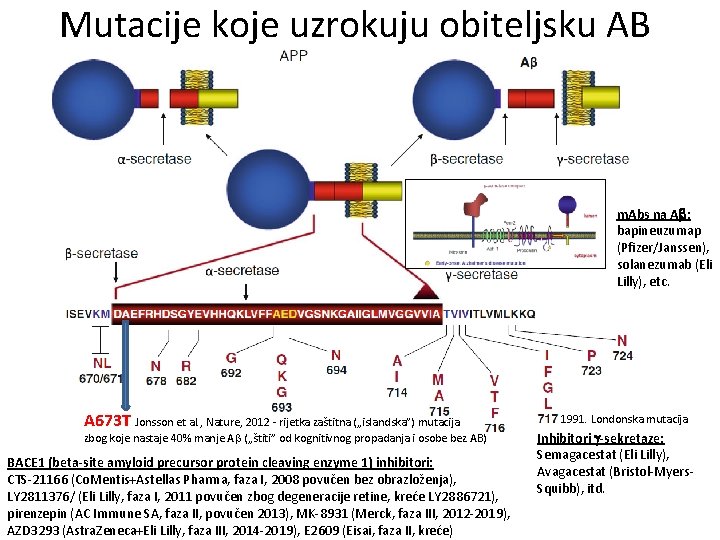
Mutacije koje uzrokuju obiteljsku AB m. Abs na A : bapineuzumap (Pfizer/Janssen), solanezumab (Eli Lilly), etc. A 673 T Jonsson et al. , Nature, 2012 - rijetka zaštitna („islandska”) mutacija zbog koje nastaje 40% manje A („štiti” od kognitivnog propadanja i osobe bez AB) BACE 1 (beta-site amyloid precursor protein cleaving enzyme 1) inhibitori: CTS-21166 (Co. Mentis+Astellas Pharma, faza I, 2008 povučen bez obrazloženja), LY 2811376/ (Eli Lilly, faza I, 2011 povučen zbog degeneracije retine, kreće LY 2886721), pirenzepin (AC Immune SA, faza II, povučen 2013), MK-8931 (Merck, faza III, 2012 -2019), AZD 3293 (Astra. Zeneca+Eli Lilly, faza III, 2014 -2019), E 2609 (Eisai, faza II, kreće) 1991. Londonska mutacija Inhibitori -sekretaze: Semagacestat (Eli Lilly), Avagacestat (Bristol-Myers. Squibb), itd.
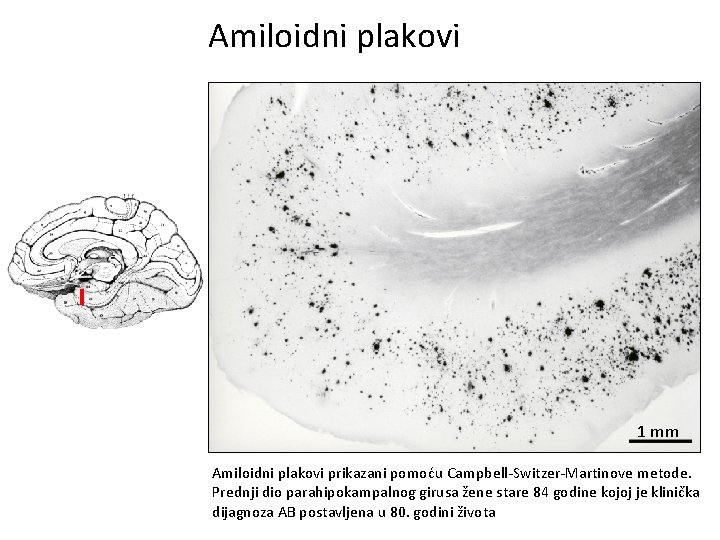
Amiloidni plakovi 1 mm Amiloidni plakovi prikazani pomoću Campbell-Switzer-Martinove metode. Prednji dio parahipokampalnog girusa žene stare 84 godine kojoj je klinička dijagnoza AB postavljena u 80. godini života

Polimorfizmi gena koji povećavaju rizik za nastanak sporadične AB Na temelju 320 meta-analiza 1395 istraživanja u kojima je proučavano 695 gena i njihovih 2973 polimorfizama, više od 30 gena pokazalo je pozitivnu povezanost, a najveću (s pripadajućim Bayesovim čimbenikom) imaju: • • • BF > 50 APOE apolipoprotein E - različiti APOE genotipovi povezani su s različitom sposobnošću čišćenja A iz mozga 23. 4 BIN 1 - kodira za nukleoplazmatski adaptorski protein 20. 1 CLU - kodira za apolipoprotein J 18. 8 ABCA 7 - kodira za protein koji se veže za adenozin-trifosfat (ATP) 18. 1 CR 1 - kodira za komponentu receptora za komplement 17. 3 PICALM - kodira za klatrinski protein koji se veže za fosfatidilinozitol 8. 7 MS 4 A 6 A - kodira za transmembranski protein hematopoetskih stanica 7. 7 CD 33 - kodira za transmembranski receptor stanica mijeloidne linije 6. 9 MS 4 A 4 E kodira za transmembranski protein hematopoetskih stanica 6. 6 CD 2 AP kodira za molekulu uključenu u regulaciju aktinskog citoskeleta Nedavno su otkrivena su još dva gena čije mutacije povećavaju rizik za obolijevanje od AB s kasnim početkom: TREM 2 – kodira za receptor na mikroglija stanicama i PLD 3 – kodira za receptor na lizosomima
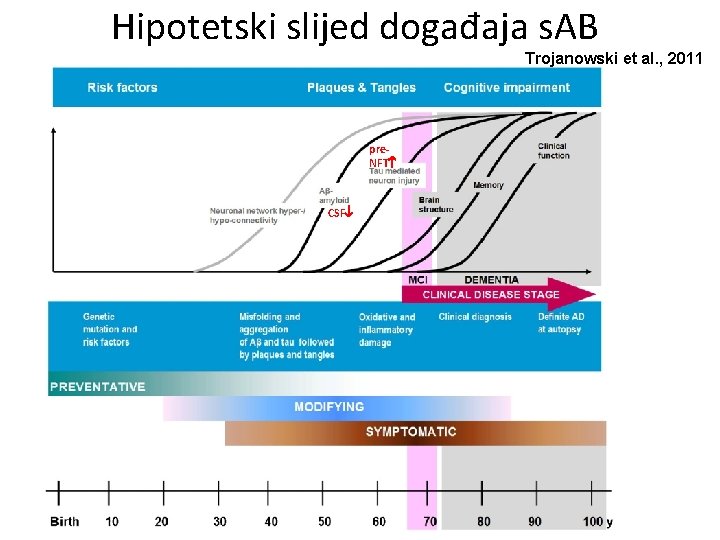
Hipotetski slijed događaja s. AB Trojanowski et al. , 2011 pre. NFT CSF

Neka nerazjašnjena pitanja u svezi s A • Zašto su amiloidni plakovi varijabilne veličine? • Što utječe na pretvorbu difuznih depozita (koje imaju i kognitivno normalne, zdrave osobe) u fibrile amiloida (koji se smatraju patološkima? • Curi li amiloid u moždanu koru iz aferentnih 5 -HT vlakana tipa D (nemaju sinapse, nego otpuštaju 5 -HT difuzno, putem volumske transmisije? • Služi li A služi kao zaptivač (sealant) nakon mikrokrvarenja (APP se veže za koagulacijski čimbenik XIa), zbog čega nastaje amiloidna angiopatija (CAA) • Kako to da 2 genotip APOE gena povećava rizik za moždani udar a 4 genotip APOE za Alzheimerovu bolest (što više protutijelima in vivo otplavimo A , to se više povećava vjerojatnost za moždani udar) • Najvažnije – kako A utječe na post-translacijske i ostale promjene tau proteina?
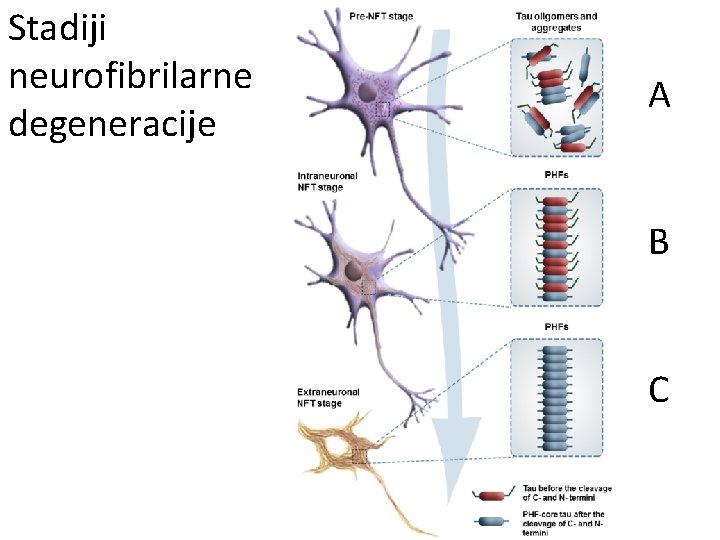
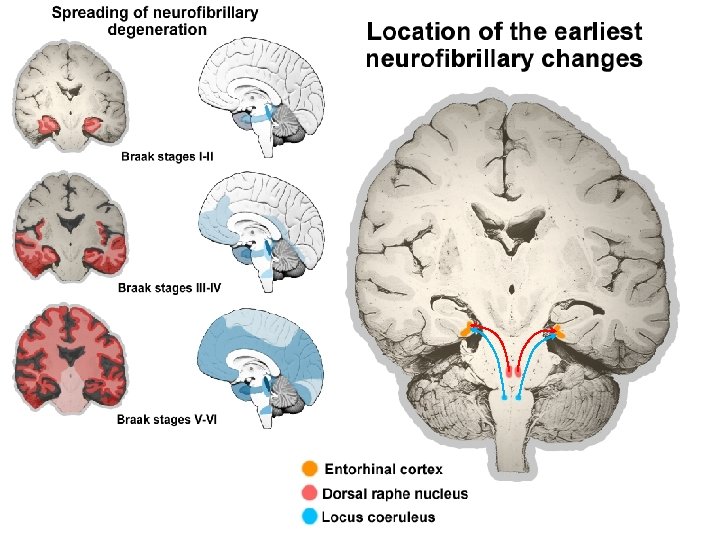
Stadiji neurofibrilarne degeneracije A B C
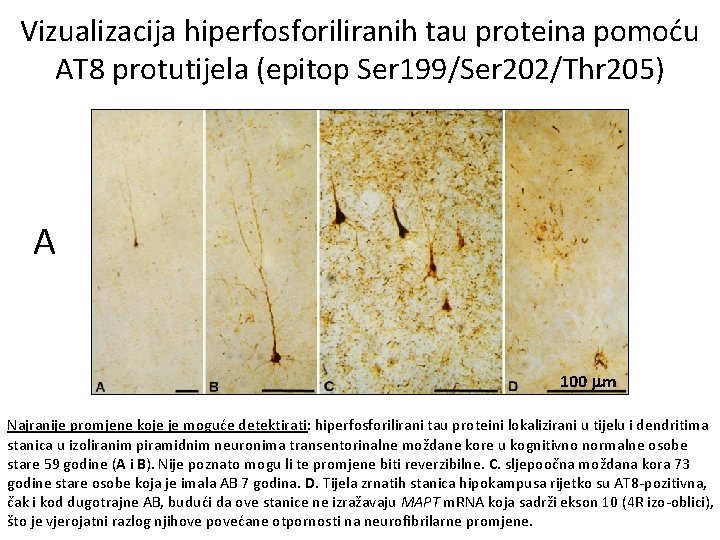
Vizualizacija hiperfosforiliranih tau proteina pomoću AT 8 protutijela (epitop Ser 199/Ser 202/Thr 205) A 100 m Najranije promjene koje je moguće detektirati: hiperfosforilirani tau proteini lokalizirani u tijelu i dendritima stanica u izoliranim piramidnim neuronima transentorinalne moždane kore u kognitivno normalne osobe stare 59 godine (A i B). Nije poznato mogu li te promjene biti reverzibilne. C. sljepoočna moždana kora 73 godine stare osobe koja je imala AB 7 godina. D. Tijela zrnatih stanica hipokampusa rijetko su AT 8 -pozitivna, čak i kod dugotrajne AB, budući da ove stanice ne izražavaju MAPT m. RNA koja sadrži ekson 10 (4 R izo-oblici), što je vjerojatni razlog njihove povećane otpornosti na neurofibrilarne promjene.
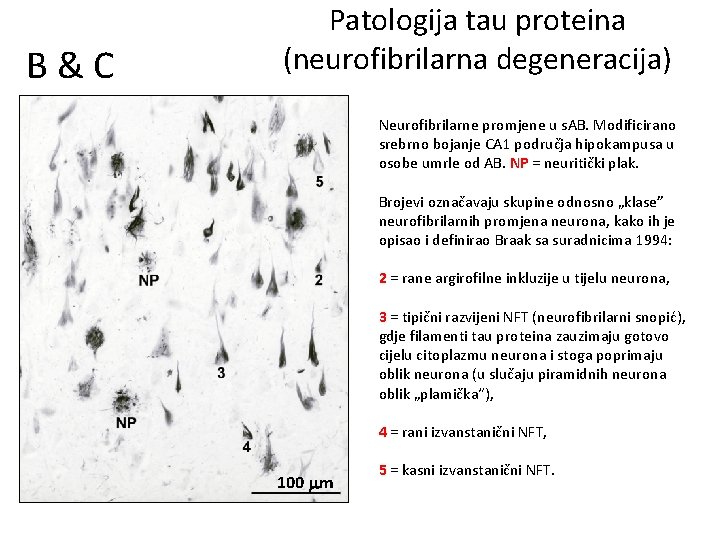
B&C Patologija tau proteina (neurofibrilarna degeneracija) Neurofibrilarne promjene u s. AB. Modificirano srebrno bojanje CA 1 područja hipokampusa u osobe umrle od AB. NP = neuritički plak. Brojevi označavaju skupine odnosno „klase” neurofibrilarnih promjena neurona, kako ih je opisao i definirao Braak sa suradnicima 1994: 2 = rane argirofilne inkluzije u tijelu neurona, 3 = tipični razvijeni NFT (neurofibrilarni snopić), gdje filamenti tau proteina zauzimaju gotovo cijelu citoplazmu neurona i stoga poprimaju oblik neurona (u slučaju piramidnih neurona oblik „plamička“), 4 = rani izvanstanični NFT, 100 m 5 = kasni izvanstanični NFT.

Najranije NF promjene u dorzalnoj raphe jezgri 100 m Bielschowsky srebrno bojenje (lijevo) i bojanje srebrnim jodidom po Gallyasu (desno) u 69 godina stare ženske osobe s blagim kognitivnim poremećajem (mild cognitive impairment - MCI, mali neurokognitivni poremećaj prema DSM 5), koja je također imala i BPSD. Vide se NFT i degenerirani neuriti.
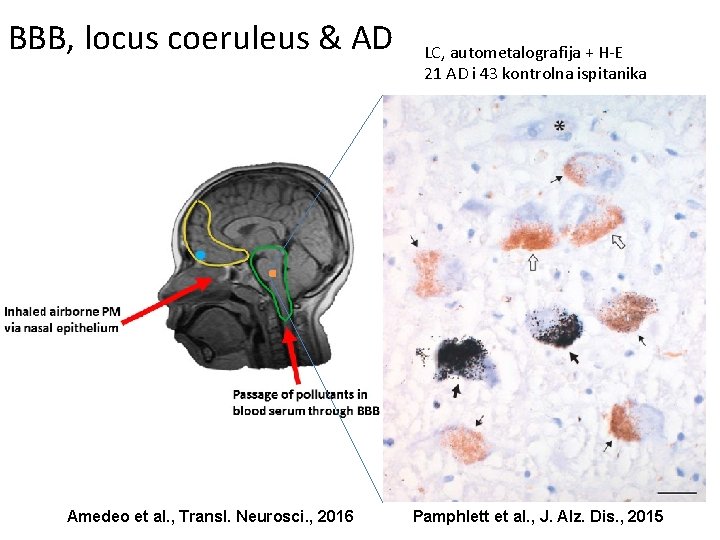
BBB, locus coeruleus & AD Amedeo et al. , Transl. Neurosci. , 2016 LC, autometalografija + H-E 21 AD i 43 kontrolna ispitanika Pamphlett et al. , J. Alz. Dis. , 2015
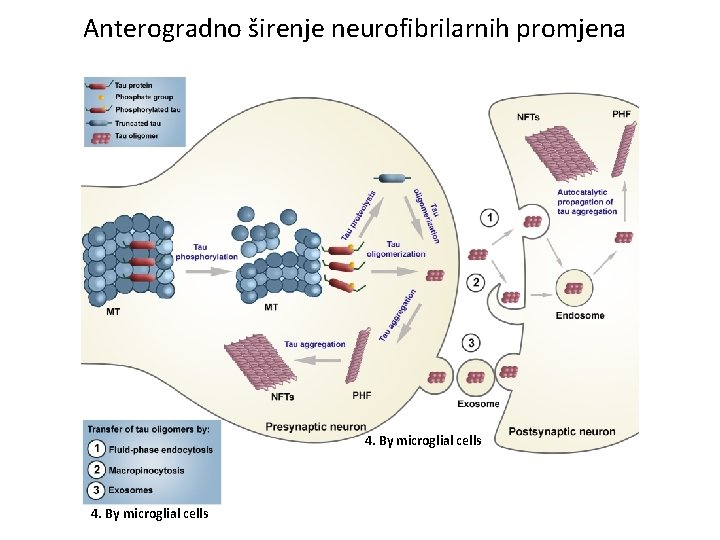
Anterogradno širenje neurofibrilarnih promjena 4. By microglial cells
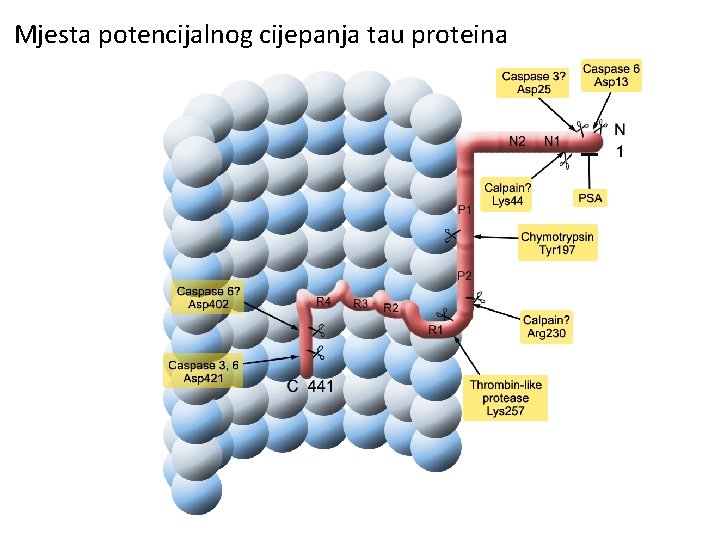
Mjesta potencijalnog cijepanja tau proteina
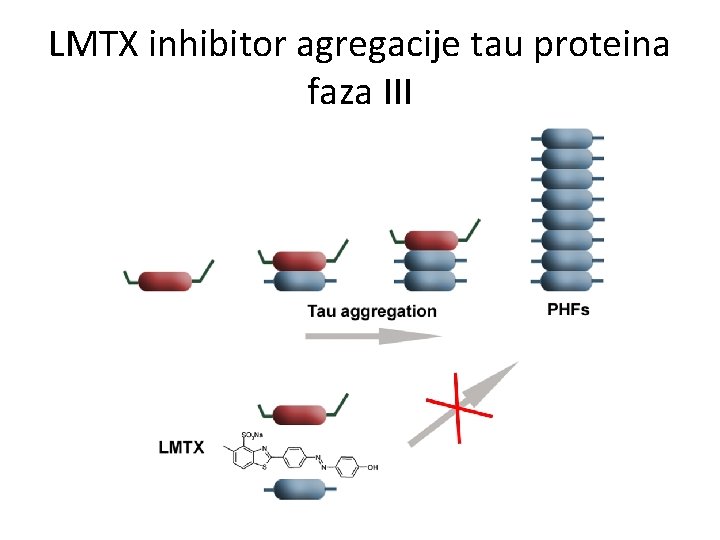
LMTX inhibitor agregacije tau proteina faza III

Neka nerazjašnjena pitanja povezana s tau proteinom • Događa li je najprije hiperfosforilacija, pa cijepanje tau proteina ili obrnuto? • Je li se tau odvojen od mikrotubula lakše ili teže hiperfosforilira? • Može li C 3 fragment (R 1 -R 4) pomoću kojega tau stabilizira mikrotubule poslužiti kao predložak (šablona, template) za oligomerizaciju i agregaciju kad se prenese transinaptički, egzo- ili ektosomski, ili mikroglijom u postsinaptički neuron? • Koje posttranslacijske promjene (i gdje) pospješuju navedeni slijed patoloških promjena tau proteina (fosforilacija, acetilacija, O-glikozilacija)? • Koja su dodatna obilježja pojedinih populacija neurona (glutamatergičkih, monoaminergičkih) za povećanu vulnerabilnost na neurofibrilarnu degeneraciju? • Putem kojih biokemijskih promjena nastaju druge primarne i sekundarne tauopatije (progresivna supranuklearna kljenut, PSP, bolest argirofilnih zrnaca, Ag. D, i kortikobazalna degeneracija, CBD)?

Epigenetske promjene • Su sve promjene u izraženosti gena koje nisu posljedica promjene u DNA slijedu: - Metilacija DNA (između svega ostaloga, odgovorna je i za genomski utisak – genomic imprinting, inaktivaciju drugog X kromosoma, promjene povezane sa starenjem, itd. ) - Modifikacija histona - Ne-kodirajuće duge RNA (lnc. RNA, više od 200 nukleotida) - Nekodirajuće male RNA, npr. mikro. RNA (mi. RNA, obično 22 nukleotida) Epigenetske promjene smatraju se najvažnijim činiteljima povezanim sa starenjem, bolestima koje se javljaju sa starenjem i nastankom tumora
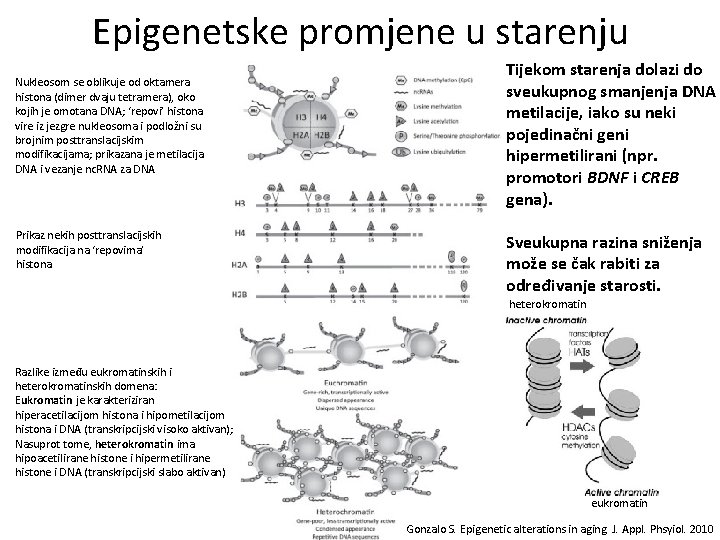
Epigenetske promjene u starenju Nukleosom se oblikuje od oktamera histona (dimer dvaju tetramera), oko kojih je omotana DNA; ‘repovi’ histona vire iz jezgre nukleosoma i podložni su brojnim posttranslacijskim modifikacijama; prikazana je metilacija DNA i vezanje nc. RNA za DNA Prikaz nekih posttranslacijskih modifikacija na ‘repovima’ histona Tijekom starenja dolazi do sveukupnog smanjenja DNA metilacije, iako su neki pojedinačni geni hipermetilirani (npr. promotori BDNF i CREB gena). Sveukupna razina sniženja može se čak rabiti za određivanje starosti. heterokromatin Razlike između eukromatinskih i heterokromatinskih domena: Eukromatin je karakteriziran hiperacetilacijom histona i hipometilacijom histona i DNA (transkripcijski visoko aktivan); Nasuprot tome, heterokromatin ima hipoacetilirane histone i hipermetilirane histone i DNA (transkripcijski slabo aktivan) eukromatin Gonzalo S. Epigenetic alterations in aging. J. Appl. Phsyiol. 2010
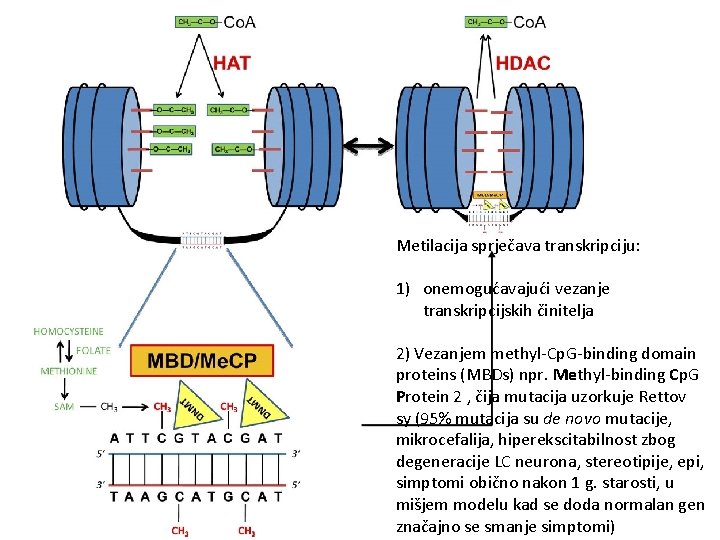
Metilacija sprječava transkripciju: 1) onemogućavajući vezanje transkripcijskih činitelja 2) Vezanjem methyl-Cp. G-binding domain proteins (MBDs) npr. Methyl-binding Cp. G Protein 2 , čija mutacija uzorkuje Rettov sy (95% mutacija su de novo mutacije, mikrocefalija, hiperekscitabilnost zbog degeneracije LC neurona, stereotipije, epi, simptomi obično nakon 1 g. starosti, u mišjem modelu kad se doda normalan gen značajno se smanje simptomi)
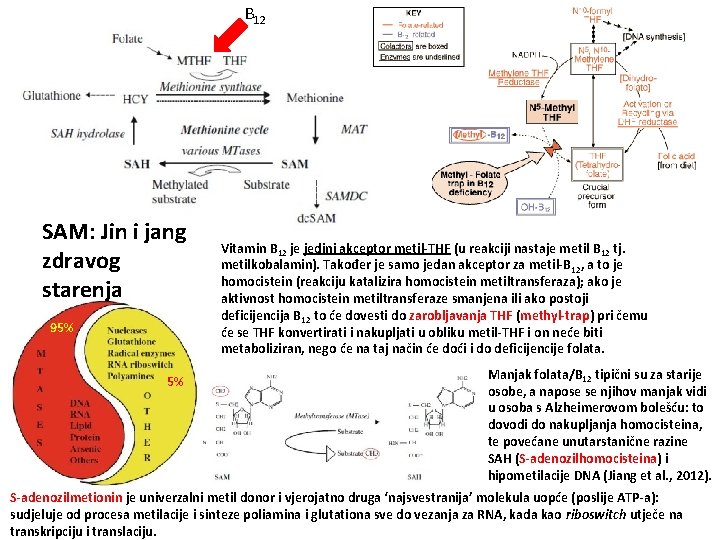
B 12 SAM: Jin i jang zdravog starenja 95% 5% Vitamin B 12 je jedini akceptor metil-THF (u reakciji nastaje metil B 12 tj. metilkobalamin). Također je samo jedan akceptor za metil-B 12, a to je homocistein (reakciju katalizira homocistein metiltransferaza); ako je aktivnost homocistein metiltransferaze smanjena ili ako postoji deficijencija B 12 to će dovesti do zarobljavanja THF (methyl-trap) pri čemu će se THF konvertirati i nakupljati u obliku metil-THF i on neće biti metaboliziran, nego će na taj način će doći i do deficijencije folata. Manjak folata/B 12 tipični su za starije osobe, a napose se njihov manjak vidi u osoba s Alzheimerovom bolešću: to dovodi do nakupljanja homocisteina, te povećane unutarstanične razine SAH (S-adenozilhomocisteina) i hipometilacije DNA (Jiang et al. , 2012). S-adenozilmetionin je univerzalni metil donor i vjerojatno druga ‘najsvestranija’ molekula uopće (poslije ATP-a): sudjeluje od procesa metilacije i sinteze poliamina i glutationa sve do vezanja za RNA, kada kao riboswitch utječe na transkripciju i translaciju.
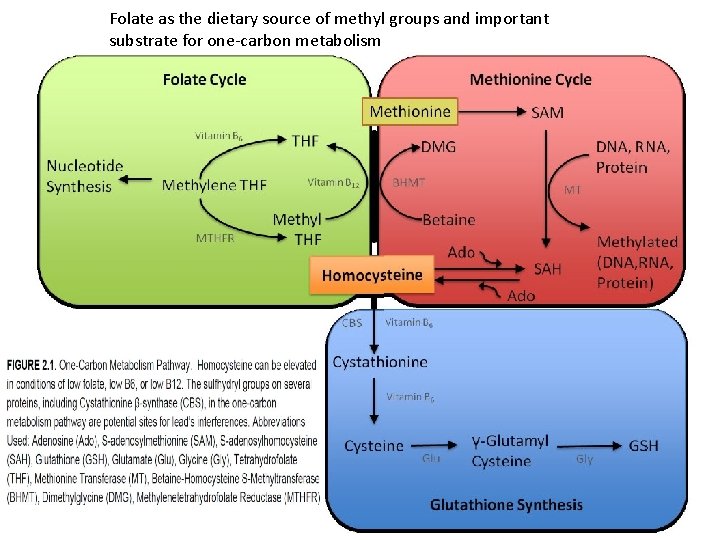
Folate as the dietary source of methyl groups and important substrate for one-carbon metabolism

U usporedbi s monogenskim bolestima, LOAD je karakteriziran brojnim anomalijama koje ukazuju na epigenetsku komponentu u nastanku bolesti, kao što su: 1) 2) 3) 4) Dominacija sporadičnih slučajeva nad obiteljskima Niska konkordancija jednojajčanih blizanaca Kasna dob nastupa bolesti Niske razine folata i visoke razine homocisteina (neovisni rizični činitelj i za Va. D odnosno moždani udar)

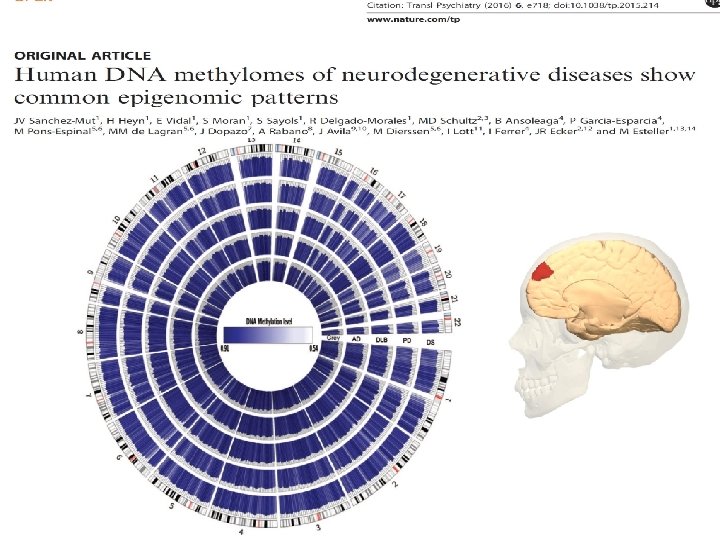
Epigenetske promjene u AD Kwok et al. , 2010
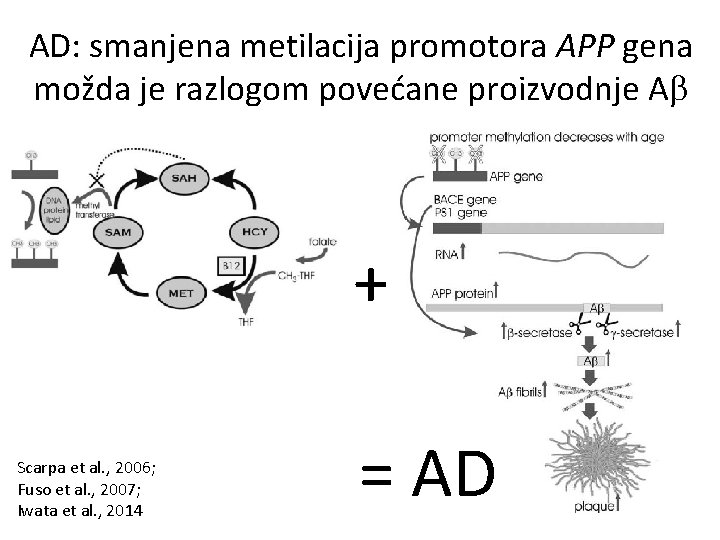
AD: smanjena metilacija promotora APP gena možda je razlogom povećane proizvodnje A + Scarpa et al. , 2006; Fuso et al. , 2007; Iwata et al. , 2014 = AD
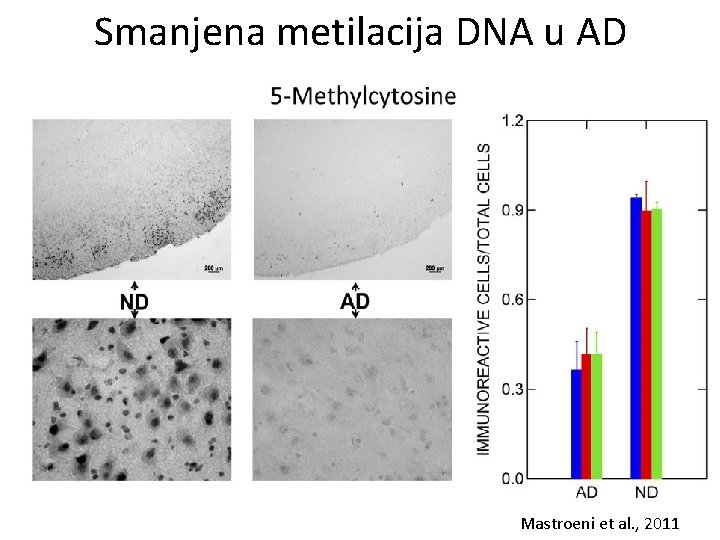
Smanjena metilacija DNA u AD Mastroeni et al. , 2011
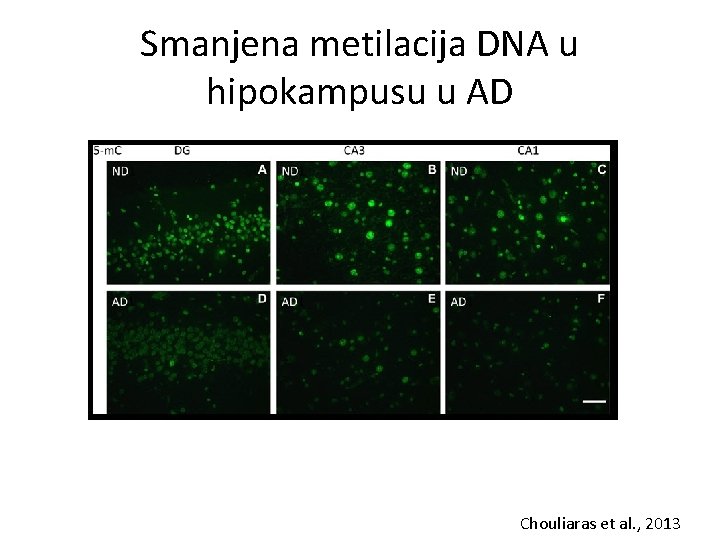
Smanjena metilacija DNA u hipokampusu u AD Chouliaras et al. , 2013
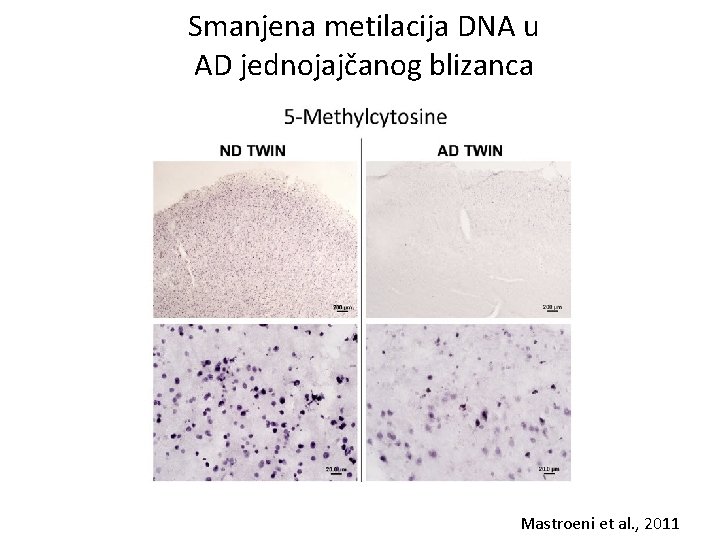
Smanjena metilacija DNA u AD jednojajčanog blizanca Mastroeni et al. , 2011
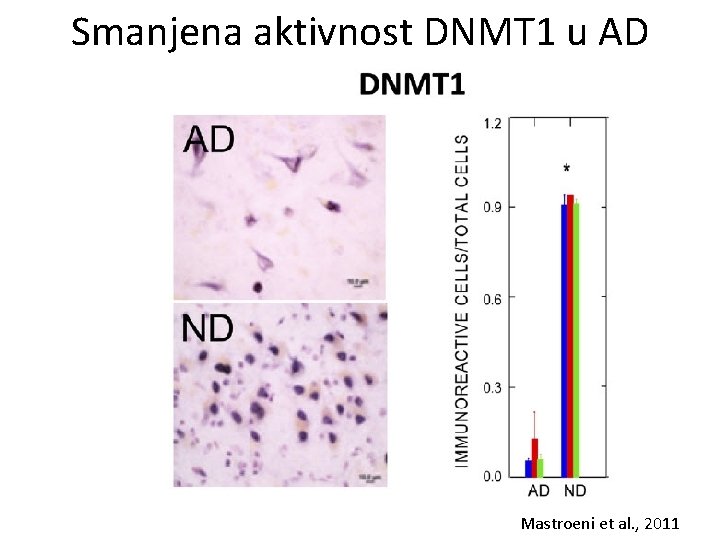
Smanjena aktivnost DNMT 1 u AD Mastroeni et al. , 2011
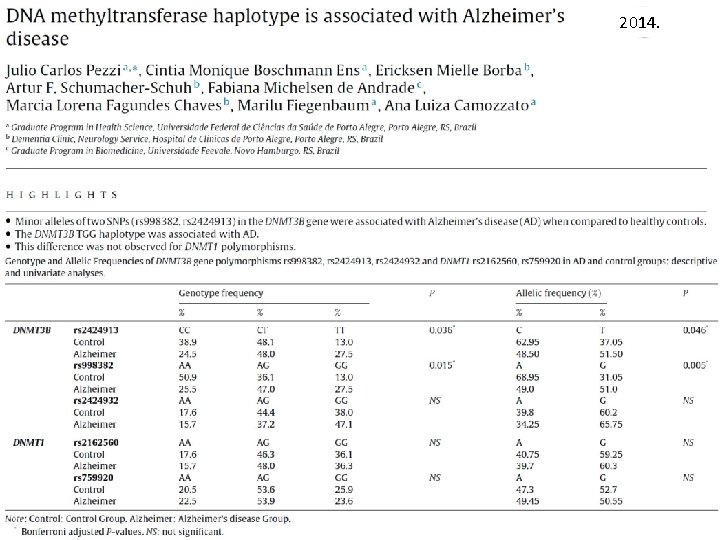
2014.

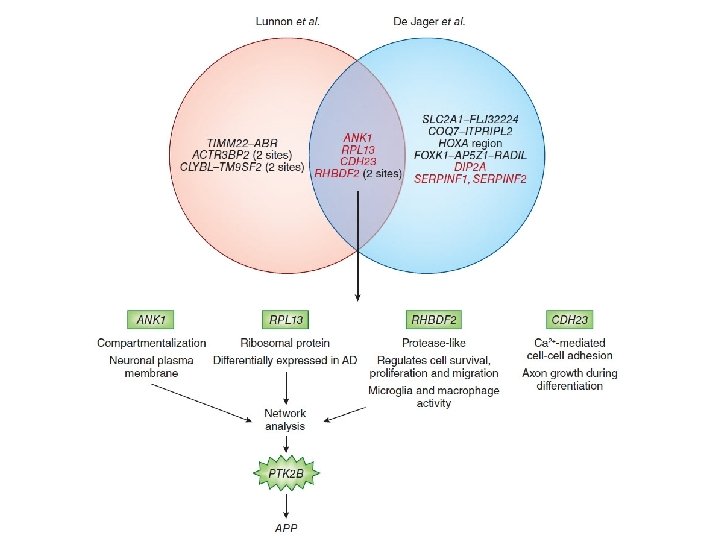
Metilacija ANK 1, CDH 23, DIP 2 A, RHBDF 2, RPL 13, SERPINF 1 i SERPINF 2 u AD Zeleno = Cp. G otoci Plavo = stupanj DNA metilacije Unutrašnje crveno = m. RNA izraženost gena povezana s dijagnozom AD Jager et al. , 2014
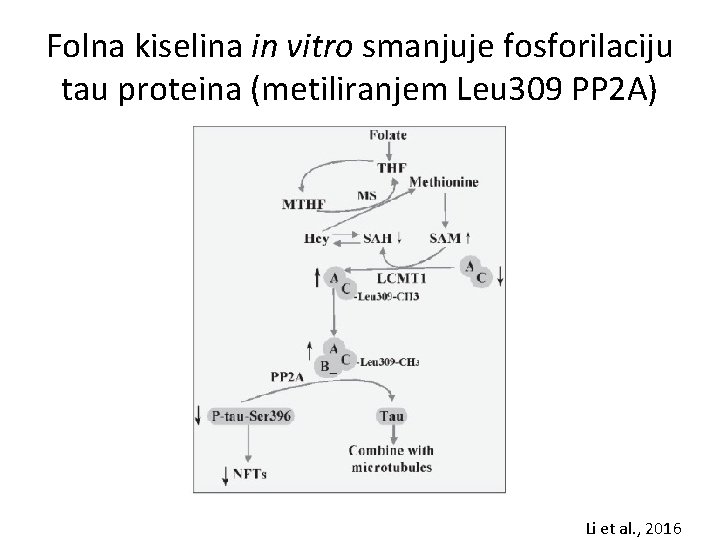
Folna kiselina in vitro smanjuje fosforilaciju tau proteina (metiliranjem Leu 309 PP 2 A) Li et al. , 2016
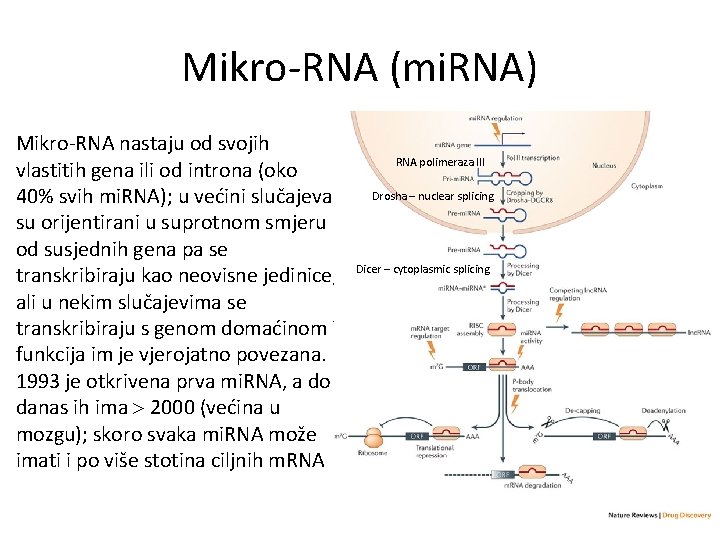
Mikro-RNA (mi. RNA) Mikro-RNA nastaju od svojih vlastitih gena ili od introna (oko 40% svih mi. RNA); u većini slučajeva su orijentirani u suprotnom smjeru od susjednih gena pa se transkribiraju kao neovisne jedinice, ali u nekim slučajevima se transkribiraju s genom domaćinom i funkcija im je vjerojatno povezana. 1993 je otkrivena prva mi. RNA, a do danas ih ima 2000 (većina u mozgu); skoro svaka mi. RNA može imati i po više stotina ciljnih m. RNA polimeraza III Drosha – nuclear splicing Dicer – cytoplasmic splicing
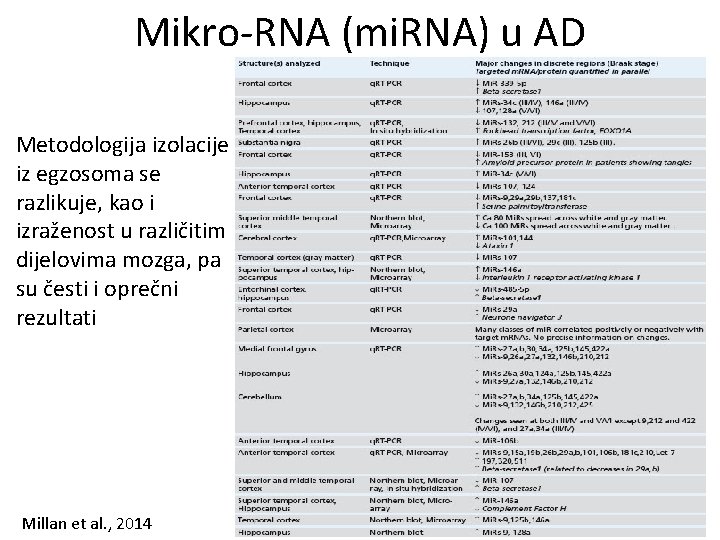
Mikro-RNA (mi. RNA) u AD Metodologija izolacije iz egzosoma se razlikuje, kao i izraženost u različitim dijelovima mozga, pa su česti i oprečni rezultati Millan et al. , 2014
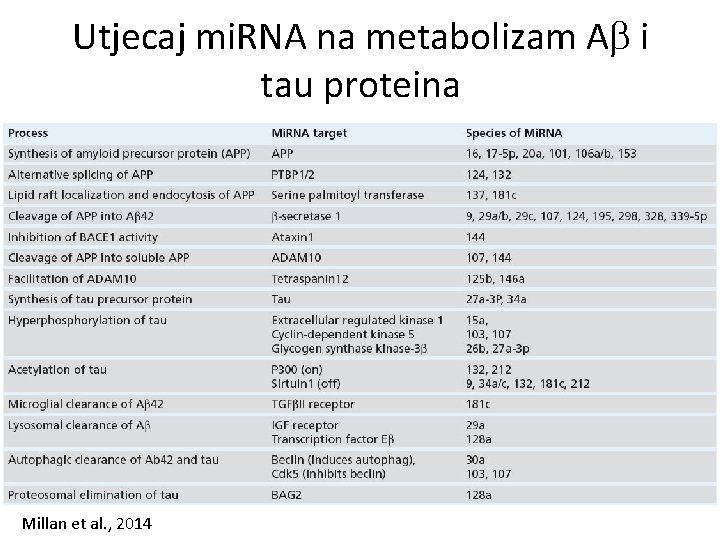
Utjecaj mi. RNA na metabolizam A i tau proteina Millan et al. , 2014

Epigenetska regulacija mt. DNA u AD • Usprkos inicijalnim kontroverznim rezultatima i 5 metilcitozin i 5 -hidroksimetilcitozin su potvrđeni u mt • Mt. DNA nije čvrsto omotana oko histona kao nuklearna, DNMT 1 se veže za mt genom i utječe na izraženost mt gena • Metilacija mt. DNA događa je i na Cp. G dinukleotidina i na ne. Cp. G mjestima u mt genomu • Smanjene razine mt. DNA 5 -hm. C i povećana izraženost nekih mt gena dokazana je u prefrontalnoj moždanoj kori starog miša

Ireverzibilni DNMT inhibitor 5 -azacitidin • Inicijalno je odobren od FDA za mijelodisplastičke sindrome (kojima je uzrok hipermetilacija tumorsupresorskih gena), a zatim su mu proširene indikacije 2009, 2012 i 2014 za liječenje različitih zloćudnih tumora • Time je otvoren put za istraživanje i registraciju i drugih spojeva koji djeluju na epigenetske mehanizme u drugim bolestima i stanjima, možda jednog dana sprečavanjem hipometilacije i za prevenciju ne samo AD nego i samog procesa starenja!

Zaključci • Epigenetska regulacija odvija se i na transkripcijskoj i posttranskripcijskoj razini • Proces starenja svih stanica i tkiva uključuje široko rasprostranjene epigenetske promjene • Gotovo sve neurodegenerativne bolesti, napose AD, povezane su s poremećenom epigenetskom regulacijom • Reverzibilna narav epigenetskih promjena obećavajući je terapijski cilj • Za bolje razumijevanje epigenetskih procesa trenutno su najveća prepreka metodološki problemi (skupoća opreme i nestandardiziranost postupaka)

Hvala na pažnji Zahvaljujem suradnicima na pomoći Hrvatska zaklada za znanost Projekt IP-2014 -09 -9730 (2015 -2019) Hiperfosforilacija, agregacija i transsinaptički prijenos tau proteina u Alzheimerovoj bolesti: analiza cerebrospinalne tekućine i ispitivanje potencijalnih neuroprotektivnih spojeva Croatian Science Foundation Mirta Boban
- Slides: 44