Siguen siendo las antraciclinas necesarias para el tratamiento
















- Slides: 38

¿Siguen siendo las antraciclinas necesarias para el tratamiento del cáncer de mama? CONCLUSIONES Agustí Barnadas Molins Barcelona

Las antraciclinas como…………

Las antraciclinas como generadoras de…


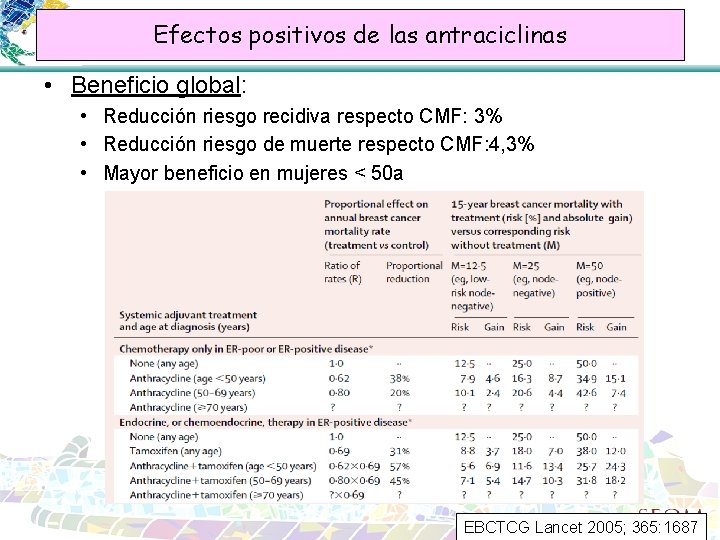
Efectos positivos de las antraciclinas • Beneficio global: • Reducción riesgo recidiva respecto CMF: 3% • Reducción riesgo de muerte respecto CMF: 4, 3% • Mayor beneficio en mujeres < 50 a EBCTCG Lancet 2005; 365: 1687

Efectos negativos de las antraciclinas • Toxicidad cardiaca: • Aguda • Tardía • Mielotoxicidad • Anemia • Neutropenia • Toxicidad emetógena • Mucositis • Riesgo inducción segundas neoplasias: • Leucemias • Síndromes mielodisplásicos

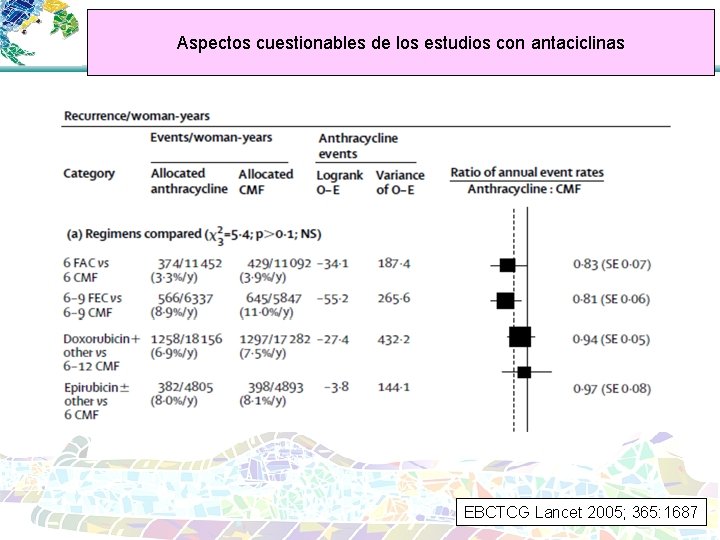
Aspectos cuestionables de los estudios con antaciclinas EBCTCG Lancet 2005; 365: 1687

Aspectos cuestionables de los estudios con antraciclinas • Estudios incluidos en el meta-análisis no son homogéneos • • Dosis Número de ciclos ¿Cuál de los esquemas es el estándar? Reducciones de dosis – intensidad de dosis • ¿Cuáles son las pacientes que más se benefician? • ¿Disponemos de variables predictivas de respuesta/efecto?

¿Evidencias para poder obviar las antraciclinas? v Estudios aleatorizados con taxanos sin antraciclinas § HER 2 +/US Oncology 9735 Adriamicina-ciclofosfamida (AC) x 4 Docetaxel-ciclofosfamida (AT) x 4 § HER 2 positivos BCIRG 006 Adriamicina-ciclofosfamida x 4 ---- docetaxel x 4 (AC-T) Adriamicina-ciclofosfamida x 4 ---- docetaxel x 4 + trastuzumab (AC-TH) Docetaxel-sales de platino x 6 + trastuzumab (TCH)

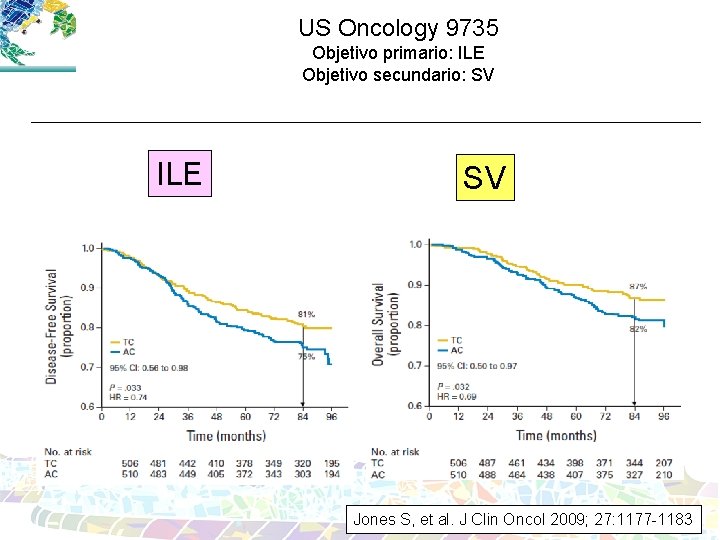
US Oncology 9735 Objetivo primario: ILE Objetivo secundario: SV ILE SV Jones S, et al. J Clin Oncol 2009; 27: 1177 -1183

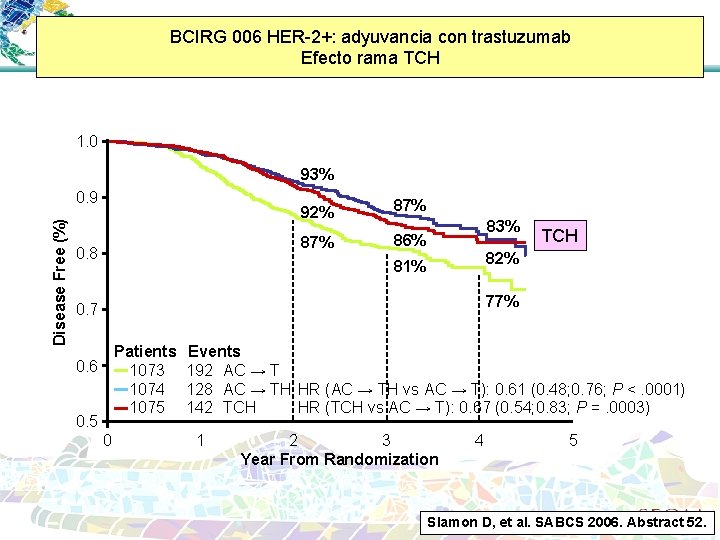
BCIRG 006 HER-2+: adyuvancia con trastuzumab Efecto rama TCH 1. 0 93% Disease Free (%) 0. 9 0. 8 92% 87% 86% 83% TCH 82% 81% 77% 0. 7 Patients 1073 1074 1075 0. 6 0. 5 0 Events 192 AC → T 128 AC → TH HR (AC → TH vs AC → T): 0. 61 (0. 48; 0. 76; P <. 0001) 142 TCH HR (TCH vs AC → T): 0. 67 (0. 54; 0. 83; P =. 0003) 1 2 3 Year From Randomization 4 5 Slamon D, et al. SABCS 2006. Abstract 52.

Reflexiones referentes al estudio US Oncology 9735 • ¿Se puede considerar un esquema estándar y óptimo 4 ciclos de AC? • El esquema AC demostró ser equivalente a CMF x 6 estudio NSABP B-15 • Los esquemas FEC/FAC o secuenciales ADR— CMF han demostrado superioridad a CMF • Los esquemas secuenciales de antraciclinas y taxanos han mostrado ser superiores a ACx 4 en el tratamiento primario y en la adyuvancia • ¿Tenemos bien definida la dosis óptima de adriamicina? • ¿Son suficientes 4 ciclos de AT?

Estudios pendientes de publicación…. . § BIG 02 -98 § Tratamiento secuencial Dox (75 mg/m 2) Docetaxel (100 mg/m 2) § Concomitante Dox (50 mg/m 2) Docetaxel (75 mg/m 2) § BCIRG-005 § TAC vs AC Docetaxel Población G+ HER-2 negativo

¿Disponemos de Marcadores moleculares para la selección de tratamiento? • Papel del HER-2 • Papel de la Topoisomerasa II-alfa • ¿otros?

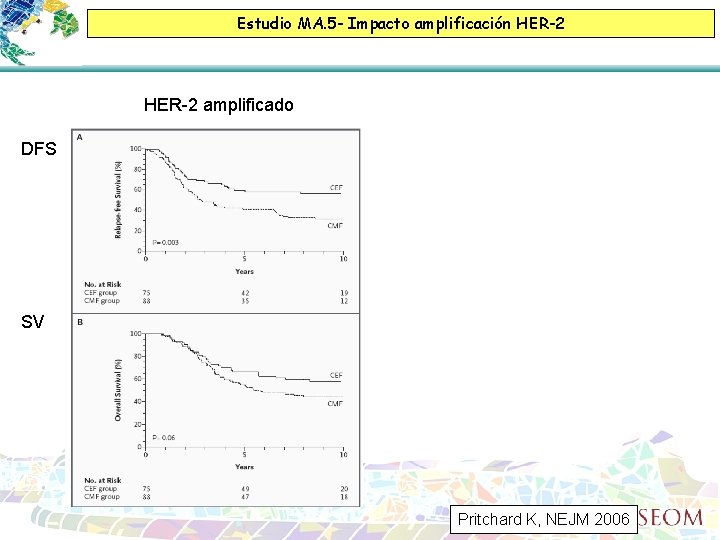
Estudio MA. 5 - Impacto amplificación HER-2 amplificado DFS SV Pritchard K, NEJM 2006

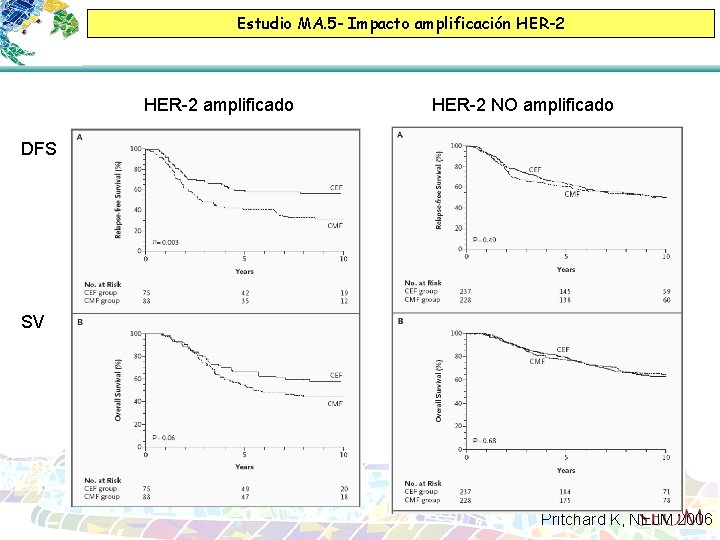
Estudio MA. 5 - Impacto amplificación HER-2 amplificado HER-2 NO amplificado DFS SV Pritchard K, NEJM 2006

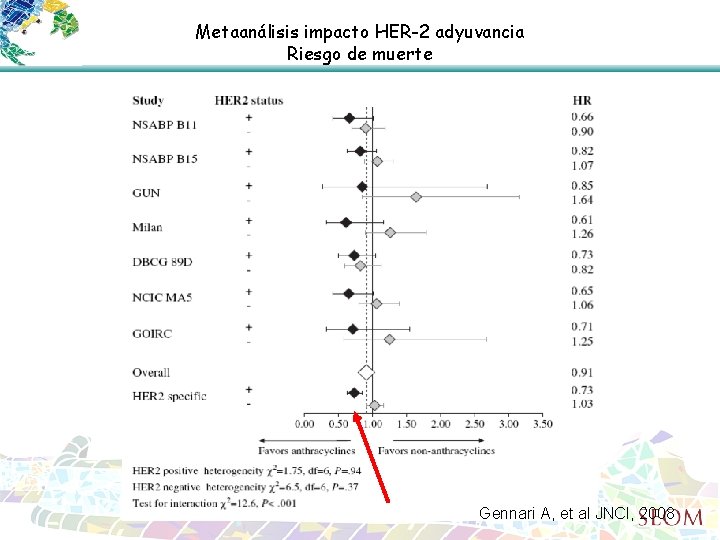
Metaanálisis impacto HER-2 adyuvancia Riesgo de muerte Gennari A, et al JNCI, 2008

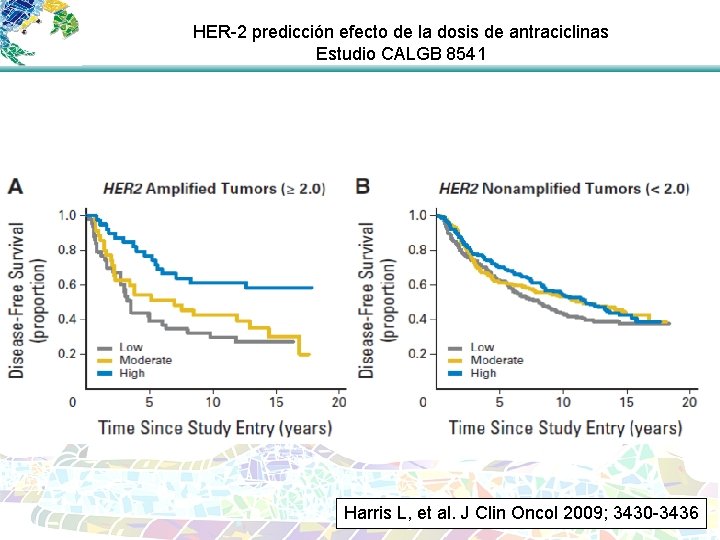
HER-2 predicción efecto de la dosis de antraciclinas Estudio CALGB 8541 Harris L, et al. J Clin Oncol 2009; 3430 -3436

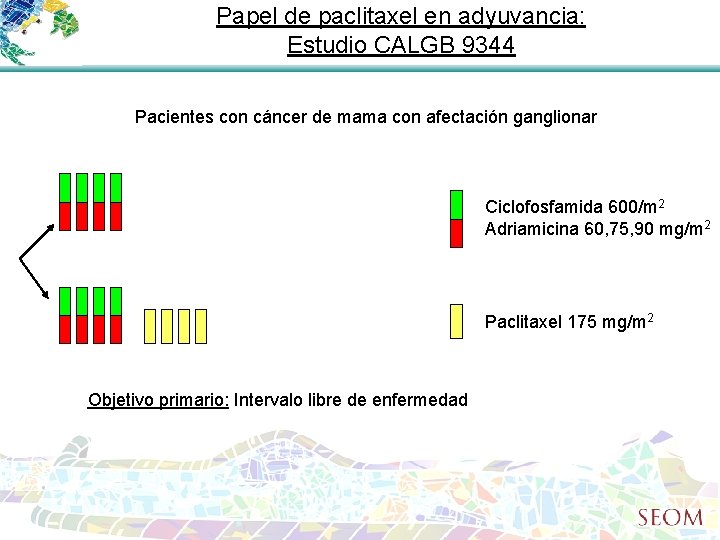
Papel de paclitaxel en adyuvancia: Estudio CALGB 9344 Pacientes con cáncer de mama con afectación ganglionar Ciclofosfamida 600/m 2 Adriamicina 60, 75, 90 mg/m 2 Paclitaxel 175 mg/m 2 Objetivo primario: Intervalo libre de enfermedad

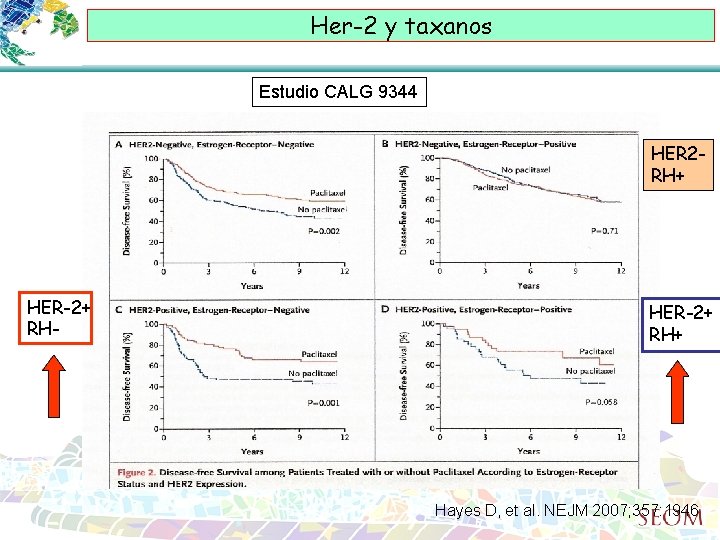
Her-2 y taxanos Estudio CALG 9344 HER 2 RH+ HER-2+ RH- HER-2+ RH+ Hayes D, et al. NEJM 2007; 357: 1946

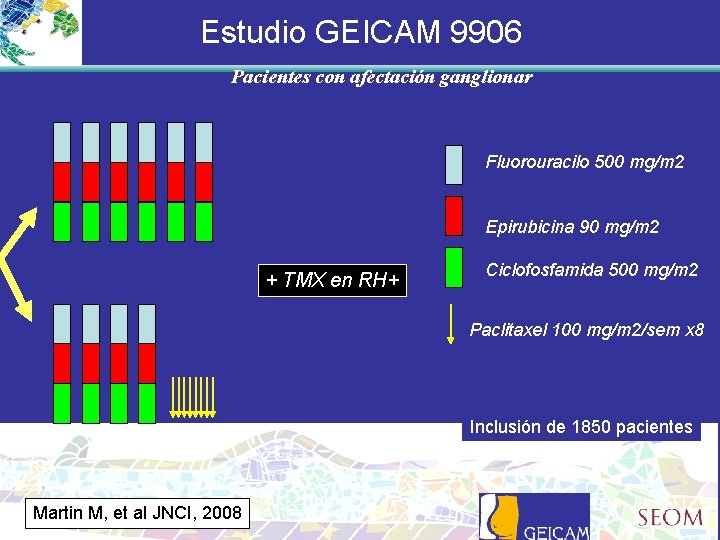
Estudio GEICAM 9906 Pacientes con afectación ganglionar Fluorouracilo 500 mg/m 2 Epirubicina 90 mg/m 2 + TMX en RH+ Ciclofosfamida 500 mg/m 2 Paclitaxel 100 mg/m 2/sem x 8 Inclusión de 1850 pacientes Martin M, et al JNCI, 2008

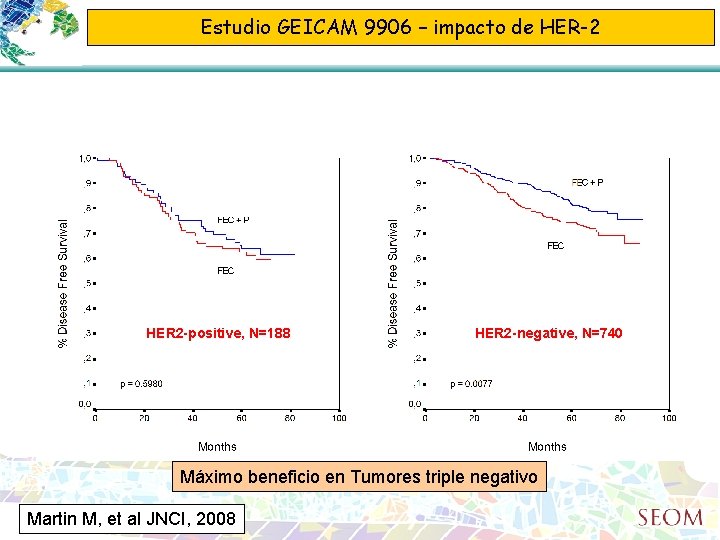
Estudio GEICAM 9906 – impacto de HER-2 HER 2 -positive, N=188 HER 2 -negative, N=740 Máximo beneficio en Tumores triple negativo Martin M, et al JNCI, 2008

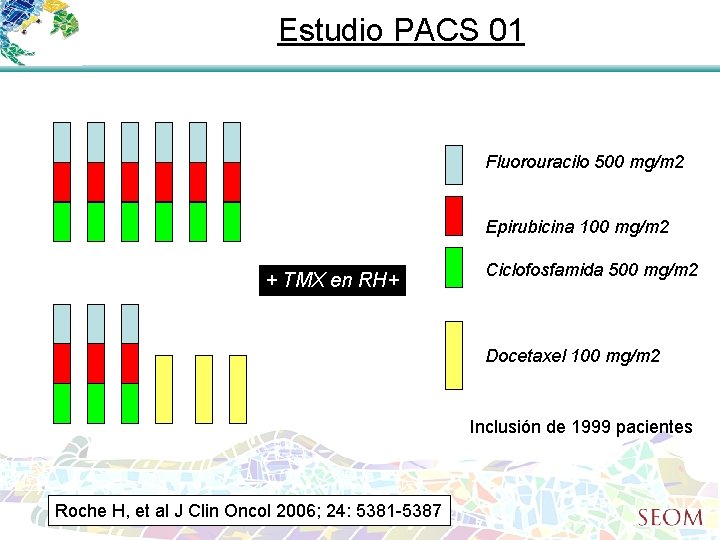
Estudio PACS 01 Fluorouracilo 500 mg/m 2 Epirubicina 100 mg/m 2 + TMX en RH+ Ciclofosfamida 500 mg/m 2 Docetaxel 100 mg/m 2 Inclusión de 1999 pacientes Roche H, et al J Clin Oncol 2006; 24: 5381 -5387

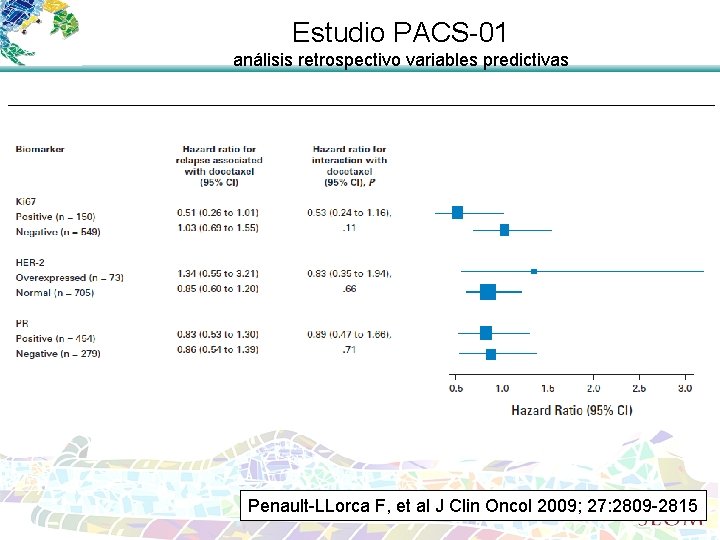
Estudio PACS-01 análisis retrospectivo variables predictivas Penault-LLorca F, et al J Clin Oncol 2009; 27: 2809 -2815

Topoisomerasa-II alfa

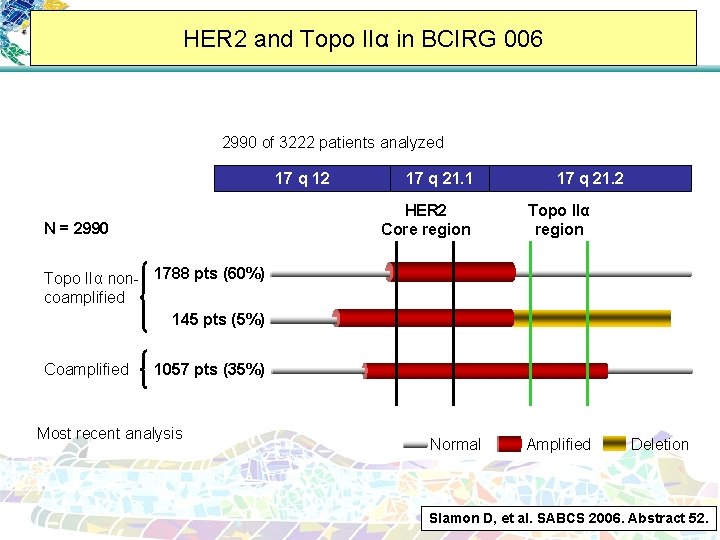
HER 2 and Topo IIα in BCIRG 006 2990 of 3222 patients analyzed 17 q 12 17 q 21. 1 HER 2 Core region N = 2990 17 q 21. 2 Topo IIα region Topo IIα non- 1788 pts (60%) coamplified 145 pts (5%) Coamplified 1057 pts (35%) Most recent analysis Normal Amplified Deletion Slamon D, et al. SABCS 2006. Abstract 52.

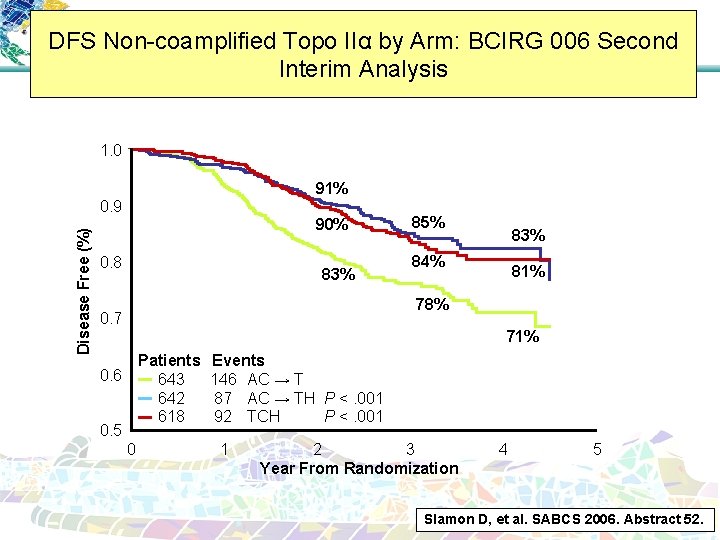
DFS Non-coamplified Topo IIα by Arm: BCIRG 006 Second Interim Analysis 1. 0 91% Disease Free (%) 0. 9 90% 0. 8 83% 85% 83% 84% 81% 78% 0. 7 71% Patients 643 642 618 0. 6 0. 5 0 Events 146 AC → T 87 AC → TH P <. 001 92 TCH P <. 001 1 2 3 Year From Randomization 4 5 Slamon D, et al. SABCS 2006. Abstract 52.

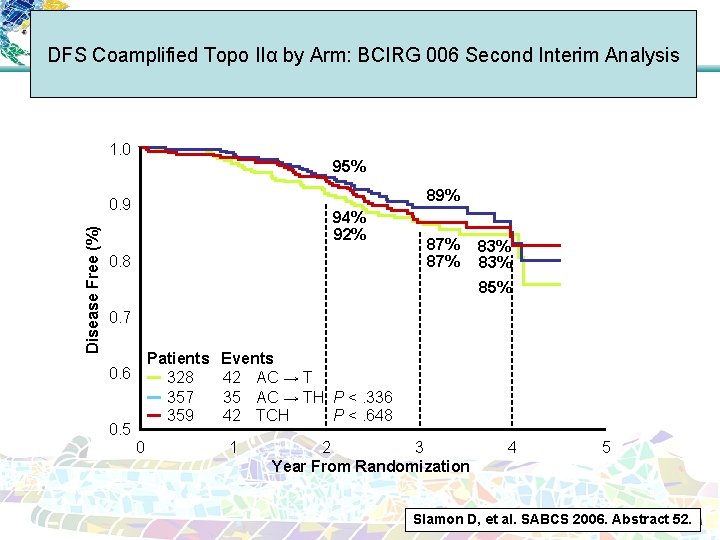
DFS Coamplified Topo IIα by Arm: BCIRG 006 Second Interim Analysis 1. 0 95% 89% Disease Free (%) 0. 9 94% 92% 0. 8 87% 83% 85% 0. 7 Patients 328 357 359 0. 6 0. 5 0 Events 42 AC → T 35 AC → TH P <. 336 42 TCH P <. 648 1 2 3 Year From Randomization 4 5 Slamon D, et al. SABCS 2006. Abstract 52.

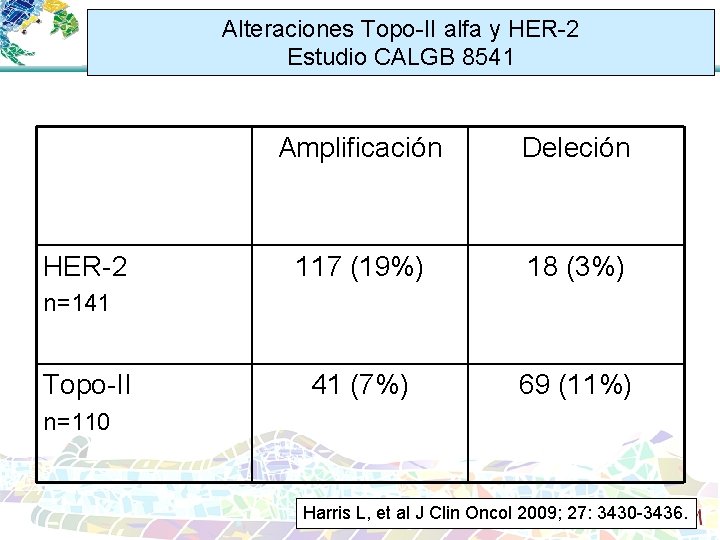
Alteraciones Topo-II alfa y HER-2 Estudio CALGB 8541 HER-2 Amplificación Deleción 117 (19%) 18 (3%) 41 (7%) 69 (11%) n=141 Topo-II n=110 Harris L, et al J Clin Oncol 2009; 27: 3430 -3436.

Coincidencias Topo-II/HER-2 Estudio CALGB 8541 n= 624 Topo-II amplificada HER-2 amplificado HER-2 no amplificado 39 2 N=41 33% de todos los casos HER-2 + Topo-II deleccionada 30 22 HER-2 deleción 17 n=61 Harris L, et al J Clin Oncol 2009; 27: 3430 -3436.

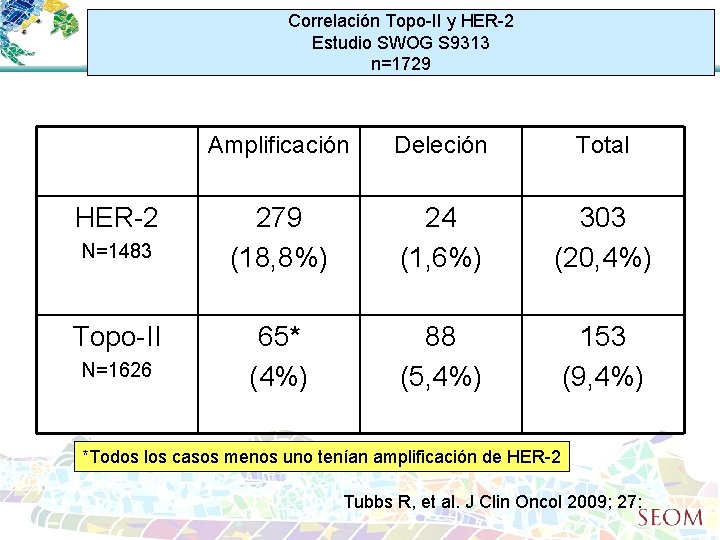
Correlación Topo-II y HER-2 Estudio SWOG S 9313 n=1729 HER-2 N=1483 Topo-II N=1626 Amplificación Deleción Total 279 (18, 8%) 24 (1, 6%) 303 (20, 4%) 65* (4%) 88 (5, 4%) 153 (9, 4%) *Todos los casos menos uno tenían amplificación de HER-2 Tubbs R, et al. J Clin Oncol 2009; 27:

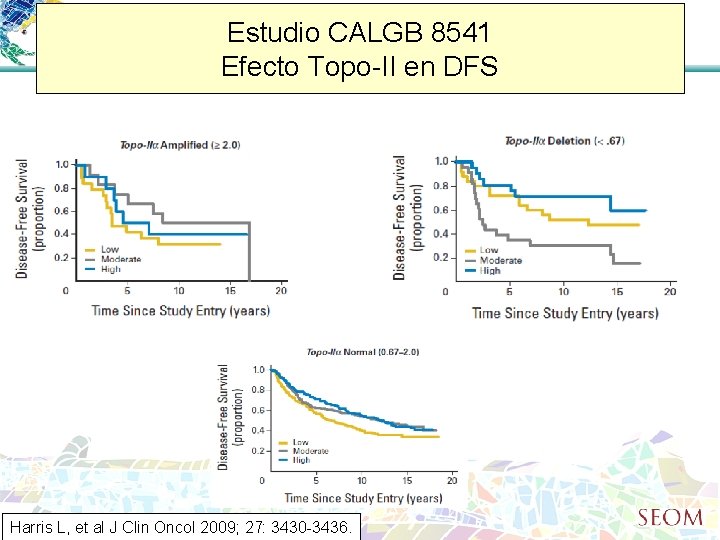
Estudio CALGB 8541 Efecto Topo-II en DFS Harris L, et al J Clin Oncol 2009; 27: 3430 -3436.

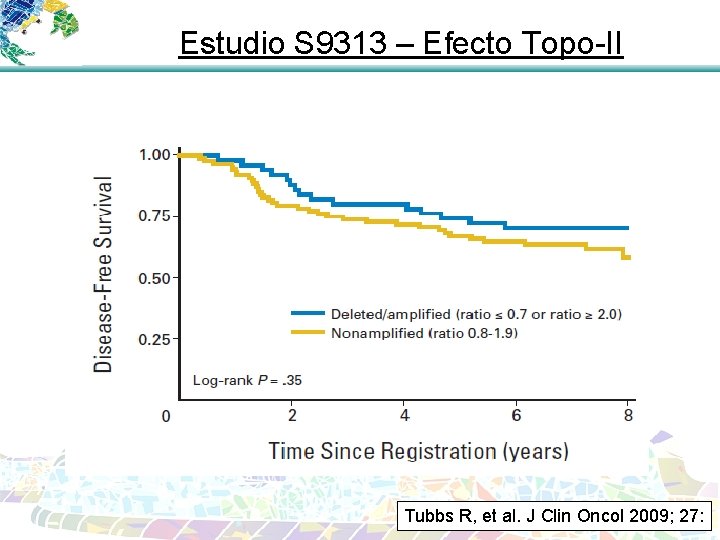
Estudio S 9313 – Efecto Topo-II Tubbs R, et al. J Clin Oncol 2009; 27:

Relación HER-2/Topo-II • A pesar de hallarse en el mismo cromosoma, la amplificación de Topo-II se asocia con amplificación de HER-2 en un 30% de casos. • La amplificación de Topo-II no permite distinguir un mayor beneficio de la administración de antraciclinas, ni del incremento de la dosis de las mismas • En los casos HER-2, la presencia de amplificación de Topo-II sugiere que el beneficio podría obtenerse, únicamente con antraciclinas sin trastuzumab, o por el contrario con trastuzumab sin antraciclinas • No existen estudios prospectivos que estratifiquen a las pacientes según estas variables • No disponemos de un marcador molecular que permita individualizar el tratamiento con antraciclinas

¿Siguen siendo las antraciclinas necesarias para el tratamiento del cáncer de mama? • A la espera de los estudios que están en marcha, en especial US Oncology TCx 6 vs TAC x 6, se deberá continuar recomendando la administración de antraciclinas en la adyuvancia • En casos seleccionados y para minimizar el riesgo de toxicidad cardiaca es posible evitar las antraciclinas, utilizando esquemas como el TC pero hasta el momento solo se dispone de evidencia con la administración de 4 ciclos • • Segundas neoplasias FEVI en el límite inferior de la normalidad RDT previa Pacientes con edad superior a 65 años? • En los casos HER-2 positivo y sin amplificación de Topo-II se podría evitar la antraciclina, y utilizar el esquema TCH con igual eficacia. En este esquema el trastuzumab se administra desde el principio del tratamiento. No obstante, el estudio BCIRG 006 no planteó la comparación AC-TH vs TCH • No se dispone de ningún marcador predictivo de respuesta para seleccionar de forma conveniente a las enfermas



¿ANTRACICLINAS SI? s a d ca i f i t s u s j a l n o é st ránd e ue inist q s m a l d a n r e a s u e t tin n n e i o ac os c p s m a l e r n e E deb ¿ANTRACICLINAS NO?