SIGNALISATION DANS LE TISSU OSSEUX IMPLICATION DANS LE


![La matrice osseuse matrice minérale : hydroxyapatite + [Ca 10(PO 4)6(OH)2] et carbonate de La matrice osseuse matrice minérale : hydroxyapatite + [Ca 10(PO 4)6(OH)2] et carbonate de](https://slidetodoc.com/presentation_image/10f62577c0f99ba2c592f3564ef7367f/image-8.jpg)

- Slides: 28

SIGNALISATION DANS LE TISSU OSSEUX : IMPLICATION DANS LE REMODELAGE DES OS

LE TISSU OSSEUX Tissu conjonctif solide et calcifié assurant 3 fonctions essentielles dans l’organisme: 1) mécanique & protectrice (adaptation aux contraintes mécaniques) 2) métabolique (équilibre phosphocalcique) 3) hématopoiétique (support structural et fonctionnel aux cellules hématopoiétiques)

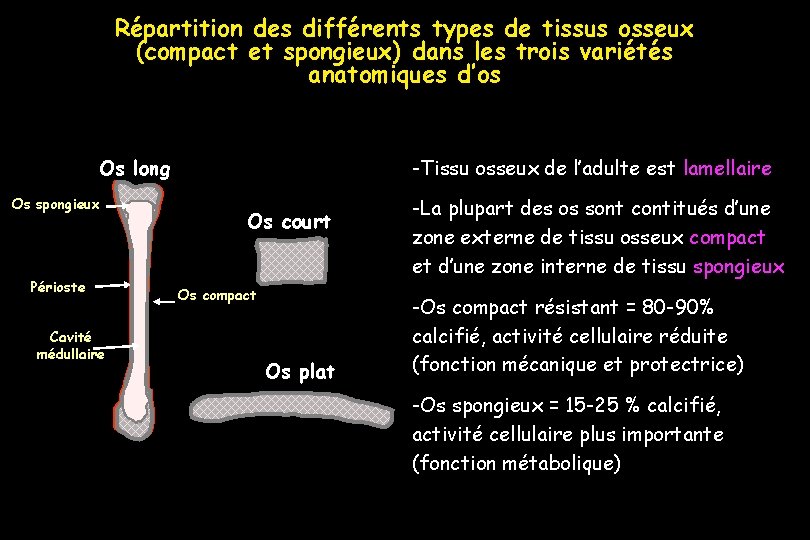
Répartition des différents types de tissus osseux (compact et spongieux) dans les trois variétés anatomiques d’os -Tissu osseux de l’adulte est lamellaire Os long Os spongieux Périoste Cavité médullaire Os court Os compact Os plat -La plupart des os sont contitués d’une zone externe de tissu osseux compact et d’une zone interne de tissu spongieux -Os compact résistant = 80 -90% calcifié, activité cellulaire réduite (fonction mécanique et protectrice) -Os spongieux = 15 -25 % calcifié, activité cellulaire plus importante (fonction métabolique)

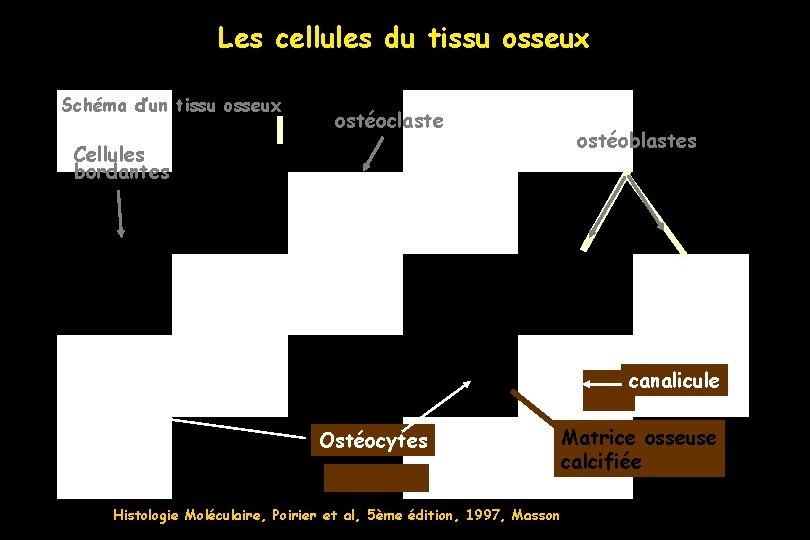
Les cellules du tissu osseux Schéma d’un tissu osseux ostéoclaste Cellules bordantes ostéoblastes canalicule Ostéocytes Histologie Moléculaire, Poirier et al, 5ème édition, 1997, Masson Matrice osseuse calcifiée

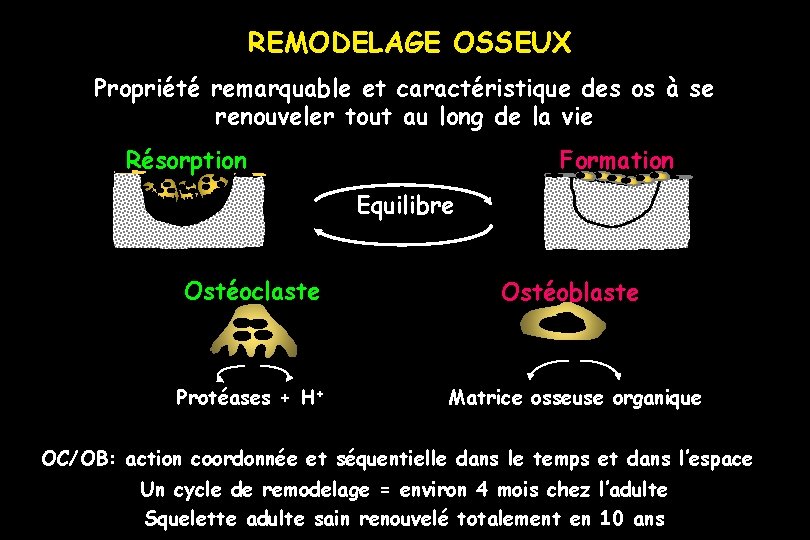
REMODELAGE OSSEUX Propriété remarquable et caractéristique des os à se renouveler tout au long de la vie Résorption Formation Equilibre Ostéoclaste Ostéoblaste Protéases + H+ Matrice osseuse organique OC/OB: action coordonnée et séquentielle dans le temps et dans l’espace Un cycle de remodelage = environ 4 mois chez l’adulte Squelette adulte sain renouvelé totalement en 10 ans

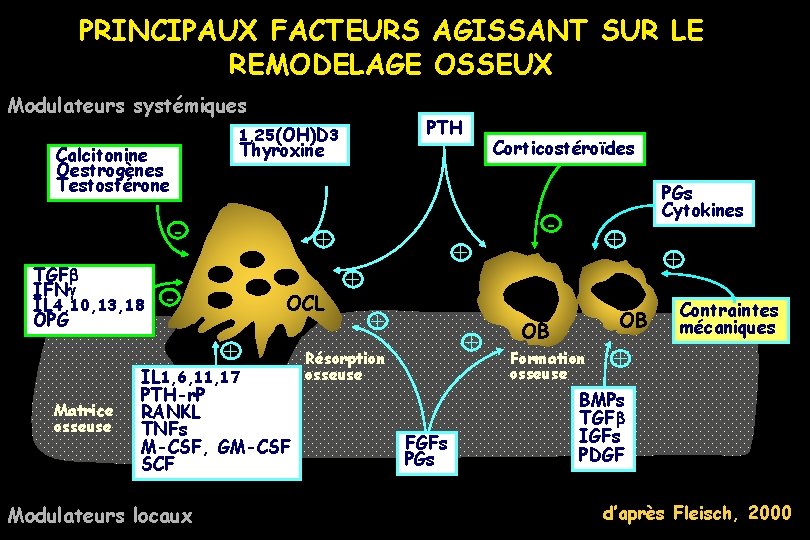
PRINCIPAUX FACTEURS AGISSANT SUR LE REMODELAGE OSSEUX Modulateurs systémiques Thyroxine Calcitonine Oestrogènes Testostérone TGFb IFN IL 4, 10, 13, 18 OPG - OCL IL 1, 6, 11, 17 PTH-r. P RANKL TNFs M-CSF, GM-CSF SCF Modulateurs locaux Corticostéroïdes PGs Cytokines - + + Matrice osseuse PTH 1, 25(OH)D 3 + + + Résorption osseuse FGFs PGs OB OB Formation osseuse + Contraintes mécaniques + BMPs TGFb IGFs PDGF d’après Fleisch, 2000

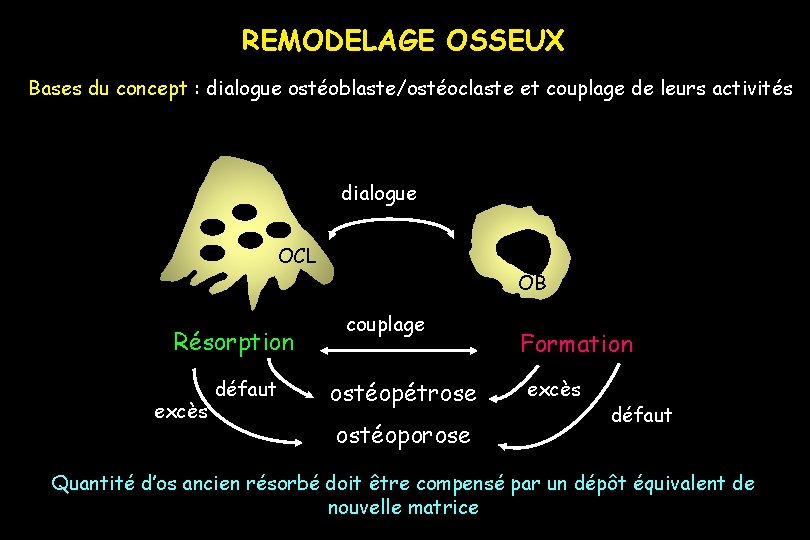
REMODELAGE OSSEUX Bases du concept : dialogue ostéoblaste/ostéoclaste et couplage de leurs activités dialogue OCL Résorption excès défaut OB couplage ostéopétrose ostéoporose OB Formation excès défaut Quantité d’os ancien résorbé doit être compensé par un dépôt équivalent de nouvelle matrice
![La matrice osseuse matrice minérale hydroxyapatite Ca 10PO 46OH2 et carbonate de La matrice osseuse matrice minérale : hydroxyapatite + [Ca 10(PO 4)6(OH)2] et carbonate de](https://slidetodoc.com/presentation_image/10f62577c0f99ba2c592f3564ef7367f/image-8.jpg)
La matrice osseuse matrice minérale : hydroxyapatite + [Ca 10(PO 4)6(OH)2] et carbonate de calcium matrice organique: -85 % collagène (type I, traces types X, III, V) organisé en triple hélice a -15 % protéines non-collagéniques (substance fondamentale) Composition substance fondamentale Protéines osseuses non-collagéniques Ostéocalcine Protéine matricielle Gla Glycoprotéines : Phosphatase alcaline Thrombospondine, ostéonectine, fibronectine, vitronectine Tetranectine Sialoprotéines: Ostéopontine, bone sialoprotéine Protéoglycannes: versican, décorine, biglycan, fibromoduline, ostéoadhérine Facteurs de croissance: (IGFs, TGFsb, PDGF) Interleukines (IL-1, IL-6, IFNs- , TNFs) Chimiokines (MCP-1) Protéines plasmatiques Glycoprotéine a 2 HS Albumine, immunoglobulines hormones 15 -25 % 2% 9% 15 -25% 10% 4% - de 1% 5 -10% 3% - de 1%

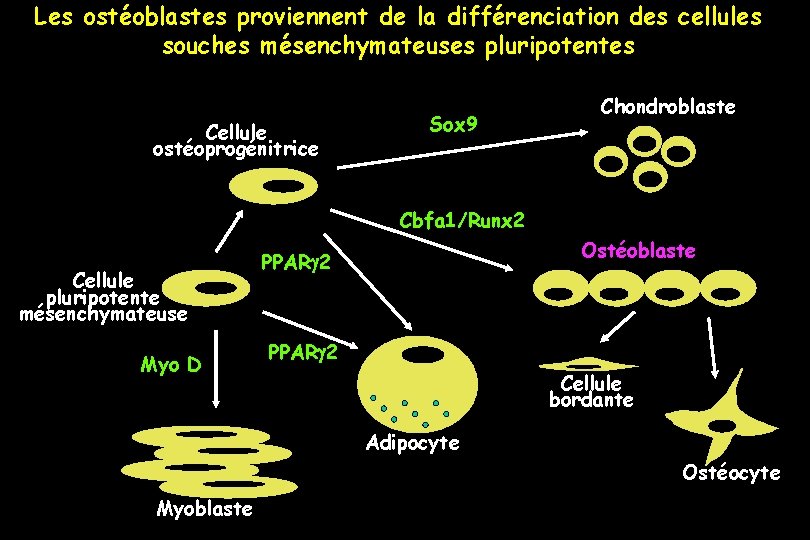
Les ostéoblastes proviennent de la différenciation des cellules souches mésenchymateuses pluripotentes Cellule ostéoprogénitrice Sox 9 Chondroblaste Cbfa 1/Runx 2 Cellule pluripotente mésenchymateuse Myo D Ostéoblaste PPAR 2 Cellule bordante Adipocyte Ostéocyte Myoblaste

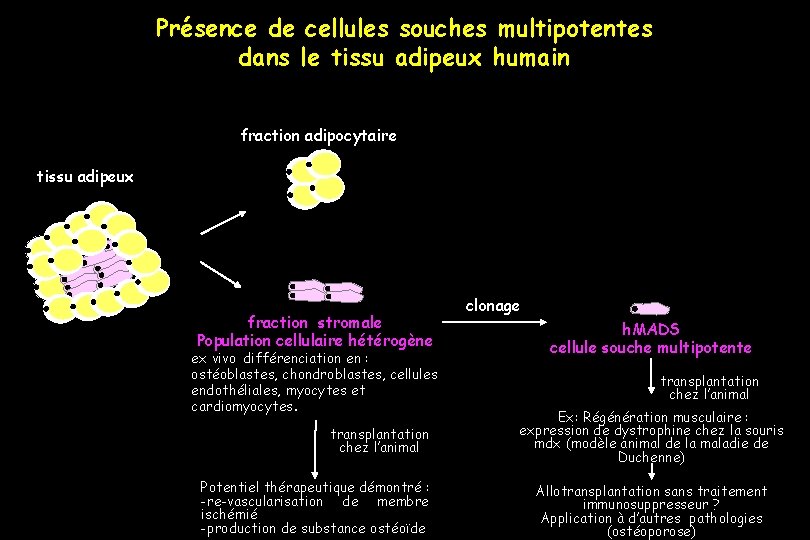
Présence de cellules souches multipotentes dans le tissu adipeux humain fraction adipocytaire tissu adipeux fraction stromale Population cellulaire hétérogène ex vivo différenciation en : ostéoblastes, chondroblastes, cellules endothéliales, myocytes et cardiomyocytes. transplantation chez l’animal Potentiel thérapeutique démontré : -re-vascularisation de membre ischémié -production de substance ostéoïde clonage h. MADS cellule souche multipotente transplantation chez l’animal Ex: Régénération musculaire : expression de dystrophine chez la souris mdx (modèle animal de la maladie de Duchenne) Allotransplantation sans traitement immunosuppresseur ? Application à d’autres pathologies (ostéoporose)

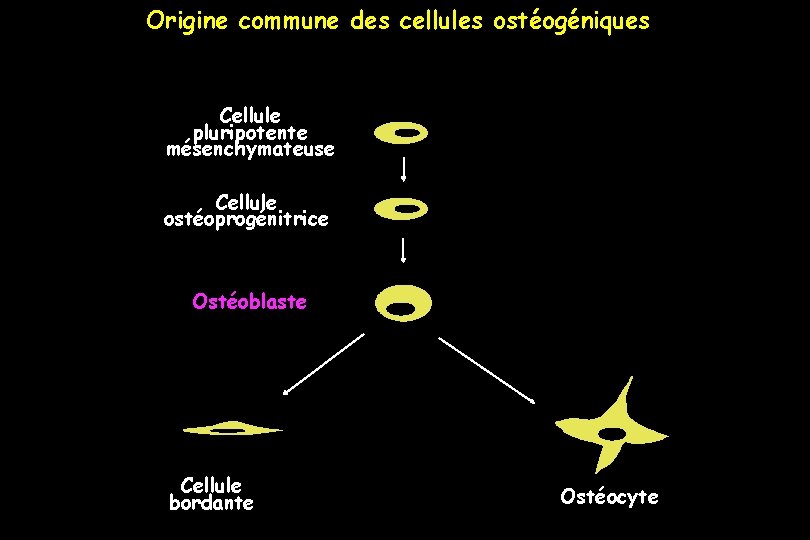
Origine commune des cellules ostéogéniques Cellule pluripotente mésenchymateuse Cellule ostéoprogénitrice Ostéoblaste Cellule bordante Ostéocyte

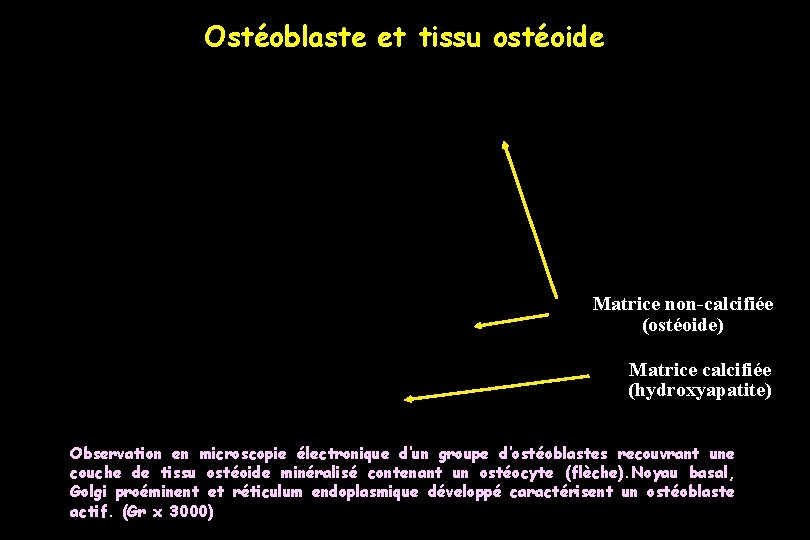
Ostéoblaste et tissu ostéoide N OB 1 N N OB 2 OB 3 Matrice non-calcifiée (ostéoide) Matrice calcifiée (hydroxyapatite) Observation en microscopie électronique d’un groupe d’ostéoblastes recouvrant une couche de tissu ostéoide minéralisé contenant un ostéocyte (flèche). Noyau basal, Golgi proéminent et réticulum endoplasmique développé caractérisent un ostéoblaste actif. (Gr x 3000)

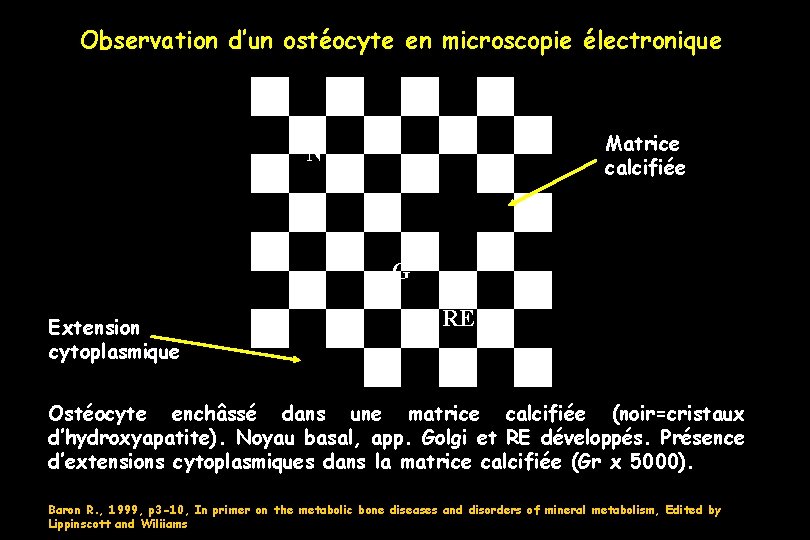
Observation d’un ostéocyte en microscopie électronique Matrice calcifiée N G Extension cytoplasmique RE Ostéocyte enchâssé dans une matrice calcifiée (noir=cristaux d’hydroxyapatite). Noyau basal, app. Golgi et RE développés. Présence d’extensions cytoplasmiques dans la matrice calcifiée (Gr x 5000). Baron R. , 1999, p 3 -10, In primer on the metabolic bone diseases and disorders of mineral metabolism, Edited by Lippinscott and Wiliiams

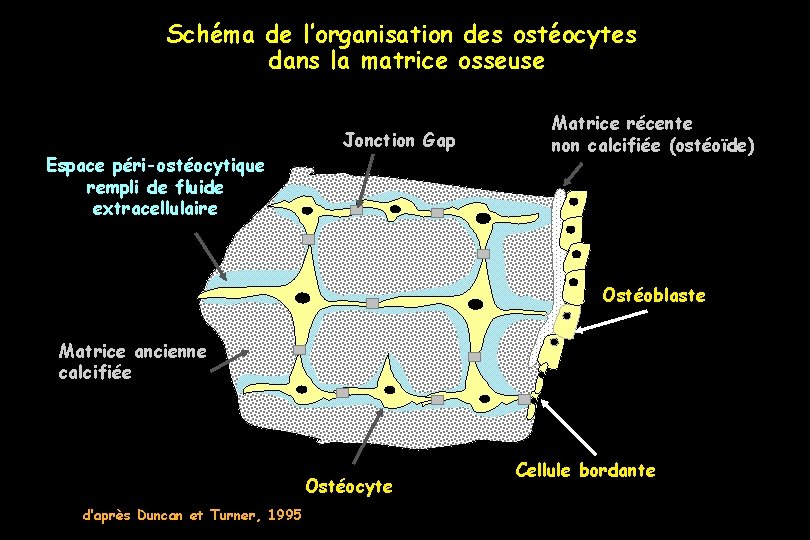
Schéma de l’organisation des ostéocytes dans la matrice osseuse Jonction Gap Espace péri-ostéocytique rempli de fluide extracellulaire Matrice récente non calcifiée (ostéoïde) Ostéoblaste Matrice ancienne calcifiée Ostéocyte d’après Duncan et Turner, 1995 Cellule bordante

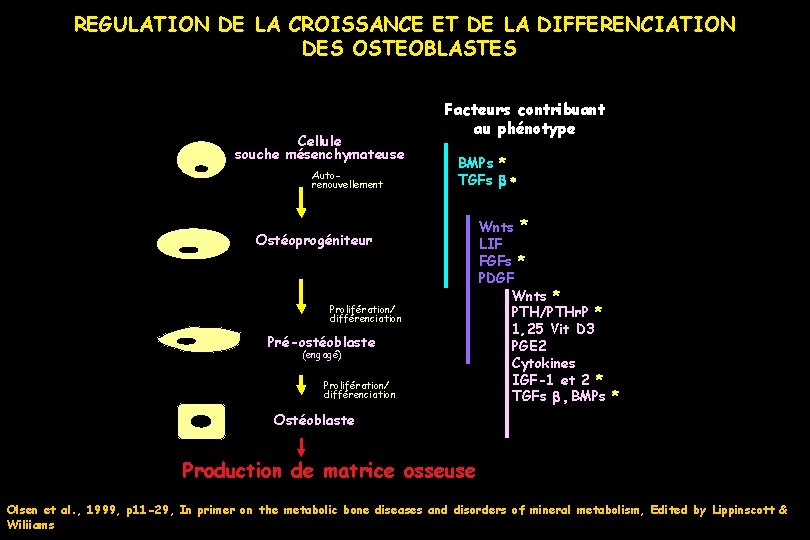
REGULATION DE LA CROISSANCE ET DE LA DIFFERENCIATION DES OSTEOBLASTES Cellule souche mésenchymateuse Autorenouvellement Facteurs contribuant au phénotype BMPs * TGFs b Ostéoprogéniteur Prolifération/ différenciation Pré-ostéoblaste (engagé) Prolifération/ différenciation Wnts * LIF FGFs * PDGF Wnts * PTH/PTHr. P * 1, 25 Vit D 3 PGE 2 Cytokines IGF-1 et 2 * TGFs b BMPs * Ostéoblaste Production de matrice osseuse Olsen et al. , 1999, p 11 -29, In primer on the metabolic bone diseases and disorders of mineral metabolism, Edited by Lippinscott & Wiliiams

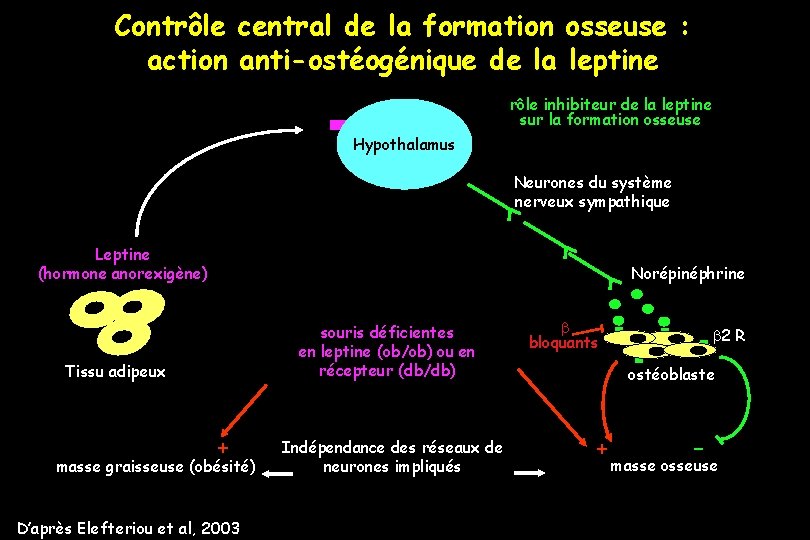
Contrôle central de la formation osseuse : action anti-ostéogénique de la leptine rôle inhibiteur de la leptine sur la formation osseuse Hypothalamus Neurones du système nerveux sympathique Leptine (hormone anorexigène) Norépinéphrine souris déficientes en leptine (ob/ob) ou en récepteur (db/db) Tissu adipeux + masse graisseuse (obésité) D’après Elefteriou et al, 2003 Indépendance des réseaux de neurones impliqués b bloquants b 2 R ostéoblaste + - masse osseuse

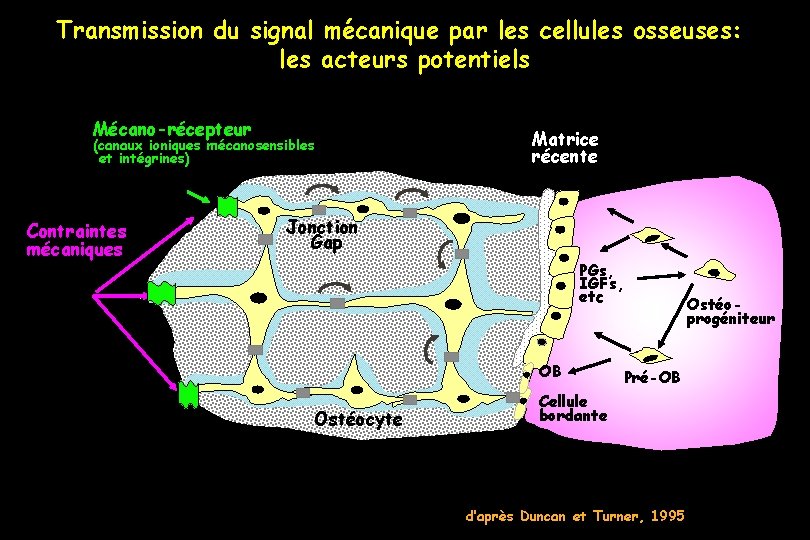
Transmission du signal mécanique par les cellules osseuses: les acteurs potentiels Mécano-récepteur (canaux ioniques mécanosensibles et intégrines) Contraintes mécaniques Matrice récente Jonction Gap PGs, IGFs, etc OB Ostéocyte Ostéoprogéniteur Pré-OB Cellule bordante d’après Duncan et Turner, 1995 moelle

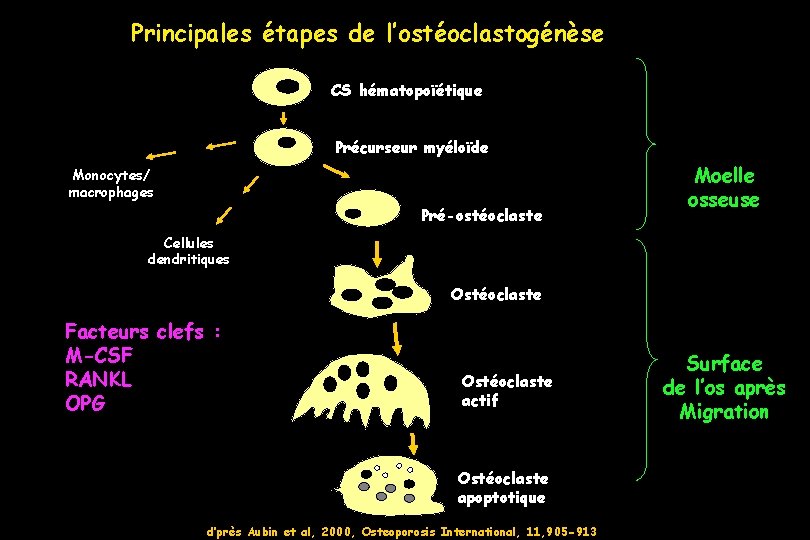
Principales étapes de l’ostéoclastogénèse CS hématopoïétique Précurseur myéloïde Monocytes/ macrophages Pré-ostéoclaste Moelle osseuse Cellules dendritiques Ostéoclaste Facteurs clefs : M-CSF RANKL OPG Ostéoclaste actif Ostéoclaste apoptotique d’près Aubin et al, 2000, Osteoporosis International, 11, 905 -913 Surface de l’os après Migration

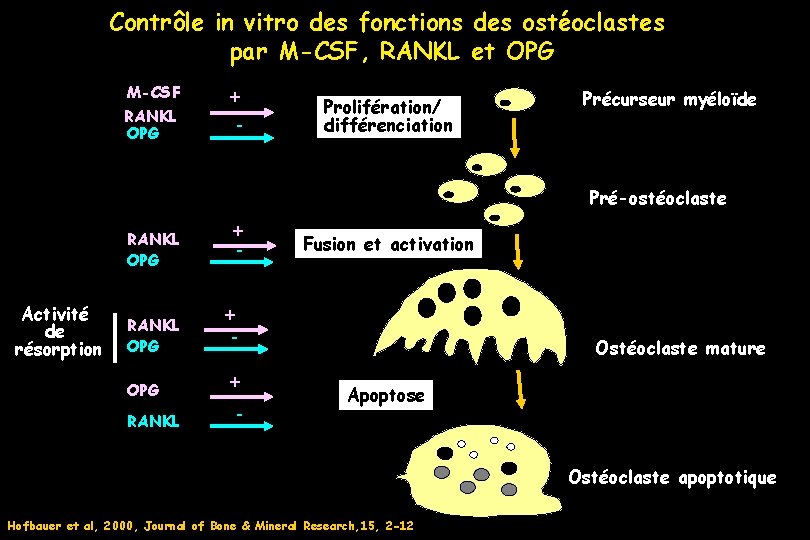
Contrôle in vitro des fonctions des ostéoclastes par M-CSF, RANKL et OPG M-CSF RANKL OPG + - Prolifération/ différenciation Précurseur myéloïde Pré-ostéoclaste RANKL OPG Activité de résorption RANKL OPG RANKL + - Fusion et activation + - Ostéoclaste mature Apoptose Ostéoclaste apoptotique Hofbauer et al, 2000, Journal of Bone & Mineral Research, 15, 2 -12

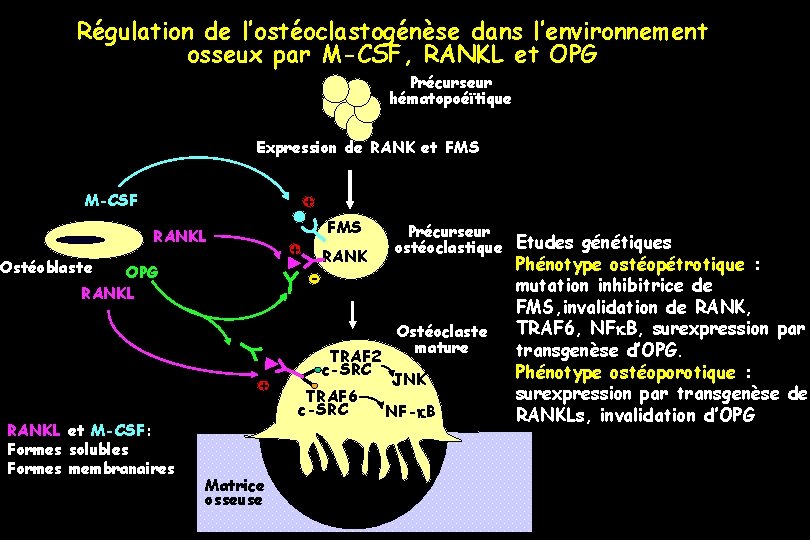
Régulation de l’ostéoclastogénèse dans l’environnement osseux par M-CSF, RANKL et OPG Précurseur hématopoéïtique Expression de RANK et FMS M-CSF + RANKL + Ostéoblaste OPG RANKL - + RANKL et M-CSF: Formes solubles Formes membranaires FMS Matrice osseuse RANK TRAF 2 c-SRC TRAF 6 c-SRC Précurseur ostéoclastique Etudes génétiques Ostéoclaste mature JNK NF-k. B Phénotype ostéopétrotique : mutation inhibitrice de FMS, invalidation de RANK, TRAF 6, NFk. B, surexpression par transgenèse d’OPG. Phénotype ostéoporotique : surexpression par transgenèse de RANKLs, invalidation d’OPG

Facteurs influençant l’ostéoclastogénèse Effet +/résorption Hormones PTH (2, 4) 1, 25(OH)2 Vit D (2, 4) Glucocorticoïdes Hormones thyroïdiennes Facteurs locaux ILI a & b IL 6 TNFa & b PTHr. P (2, 4) PGE 2 M-CSF RANKL Prolifération 1 Différenciation 2 effet négatif/résorption calcitonine (4) Estrogènes & androgènes IL 18 & IFN TGF b OPG Survie /fusion 3 Activation 4 Apoptose 5

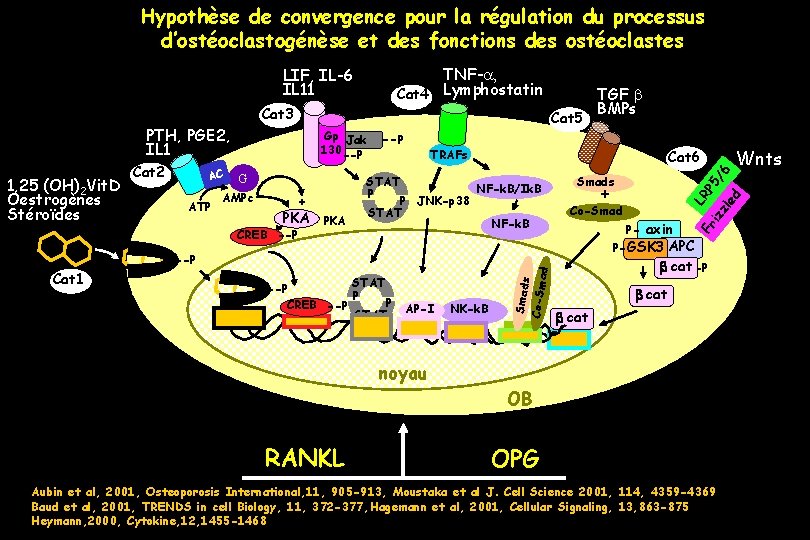
Hypothèse de convergence pour la régulation du processus d’ostéoclastogénèse et des fonctions des ostéoclastes TNF-a Cat 4 Lymphostatin Cat 3 AC ATP G AMPc CREB --P TRAFs STAT P + PKA --P PKA P JNK-p 38 STAT Cat 6 NF-k. B/Ik. B --P Cat 1 STAT --P P P CREB --P STAT AP-I NK-k. B NF-k. B Smads + Co-Smad P- axin P- GSK 3 APC Fr 1, 25 (OH)2 Vit. D Oestrogènes Stéroïdes Cat 2 Gp Jak 130 --P Smads Co-Sm ad PTH, PGE 2, IL 1 Cat 5 TGF b BMPs b cat -P b cat noyau OB RANKL Wnts LR iz P 5/ zl ed 6 LIF, IL-6 IL 11 OPG Aubin et al, 2001, Osteoporosis International, 11, 905 -913, Moustaka et al J. Cell Science 2001, 114, 4359 -4369 Baud et al, 2001, TRENDS in cell Biology, 11, 372 -377, Hagemann et al, 2001, Cellular Signaling, 13, 863 -875 Heymann, 2000, Cytokine, 12, 1455 -1468

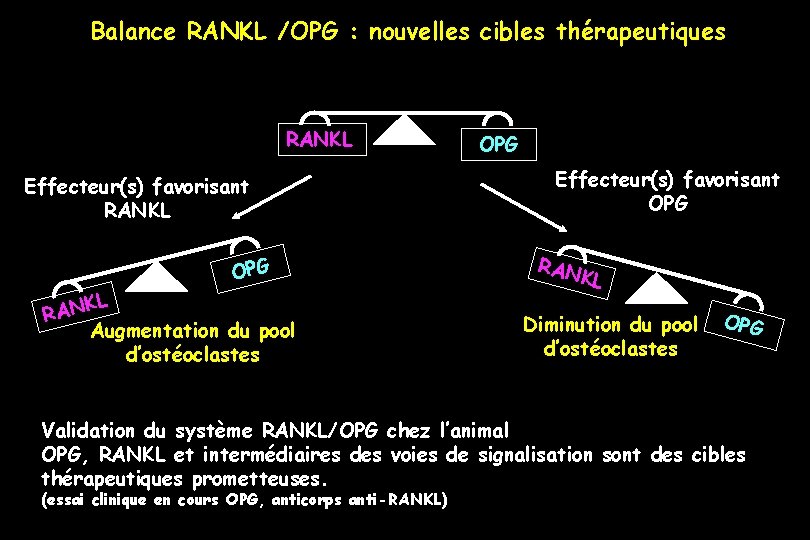
Balance RANKL /OPG : nouvelles cibles thérapeutiques RANKL Effecteur(s) favorisant RANKL OPG KL Augmentation du pool d’ostéoclastes RAN OPG Effecteur(s) favorisant OPG RAN KL Diminution du pool d’ostéoclastes OPG Validation du système RANKL/OPG chez l’animal OPG, RANKL et intermédiaires des voies de signalisation sont des cibles thérapeutiques prometteuses. (essai clinique en cours OPG, anticorps anti-RANKL)

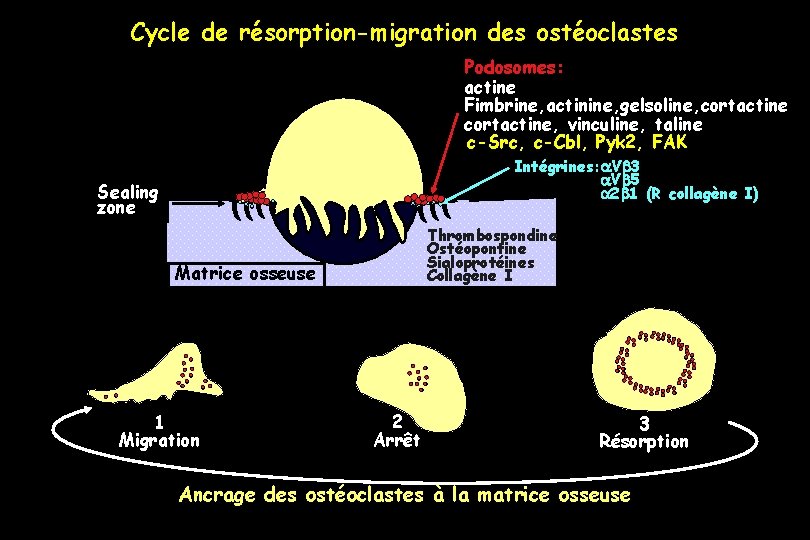
Cycle de résorption-migration des ostéoclastes Podosomes: actine Fimbrine, actinine, gelsoline, cortactine, vinculine, taline c-Src, c-Cbl, Pyk 2, FAK Intégrines: a. Vb 3 a. Vb 5 a 2 b 1 (R collagène I) Sealing zone Thrombospondine Ostéopontine Sialoprotéines Collagène I Matrice osseuse 1 Migration 2 Arrêt 3 Résorption Ancrage des ostéoclastes à la matrice osseuse

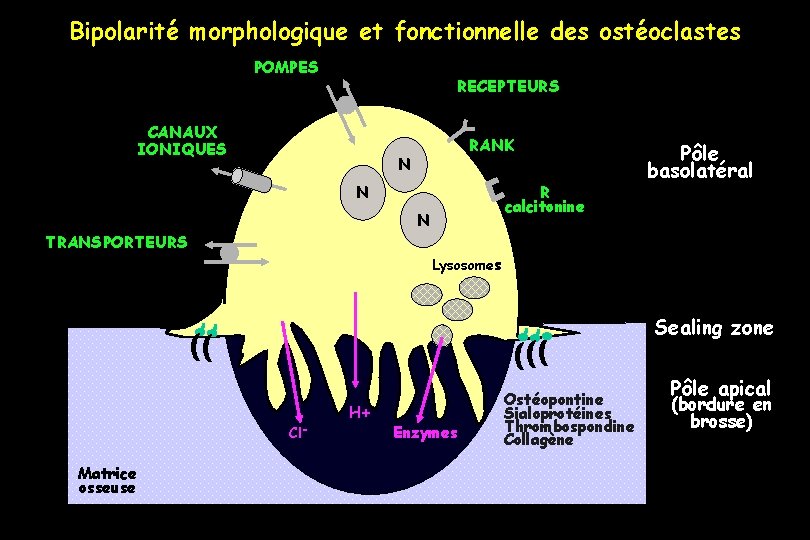
Bipolarité morphologique et fonctionnelle des ostéoclastes POMPES RECEPTEURS CANAUX IONIQUES RANK N R calcitonine N N TRANSPORTEURS Pôle basolatéral Lysosomes Sealing zone Cl- Matrice osseuse H+ Enzymes Ostéopontine Sialoprotéines Thrombospondine Collagène Pôle apical (bordure en brosse)

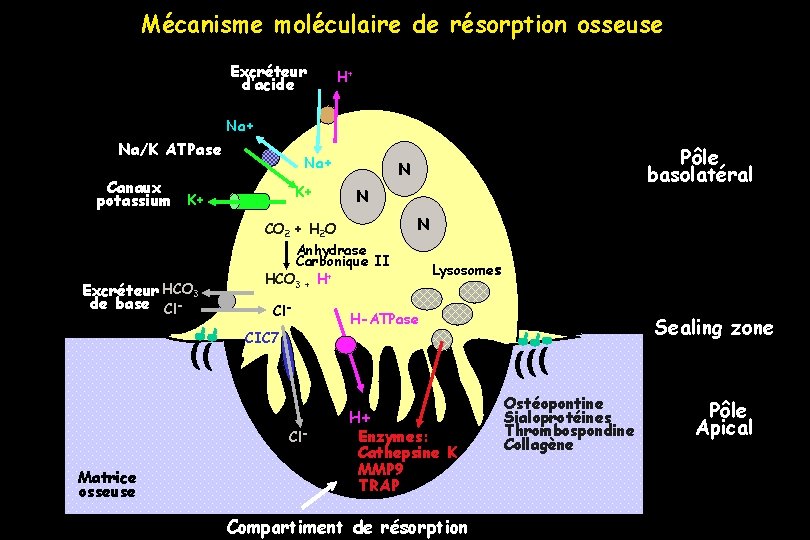
Mécanisme moléculaire de résorption osseuse Excréteur d’acide H+ Na/K ATPase Canaux potassium Na+ K+ K+ Excréteur HCO 3 de base Cl- CIC 7 Cl- Matrice osseuse N CO 2 + H 2 O Anhydrase Carbonique II HCO 3 + H+ Cl- Pôle basolatéral N N Lysosomes H-ATPase H+ Enzymes: Cathepsine K MMP 9 TRAP Compartiment de résorption Sealing zone Ostéopontine Sialoprotéines Thrombospondine Collagène Pôle Apical

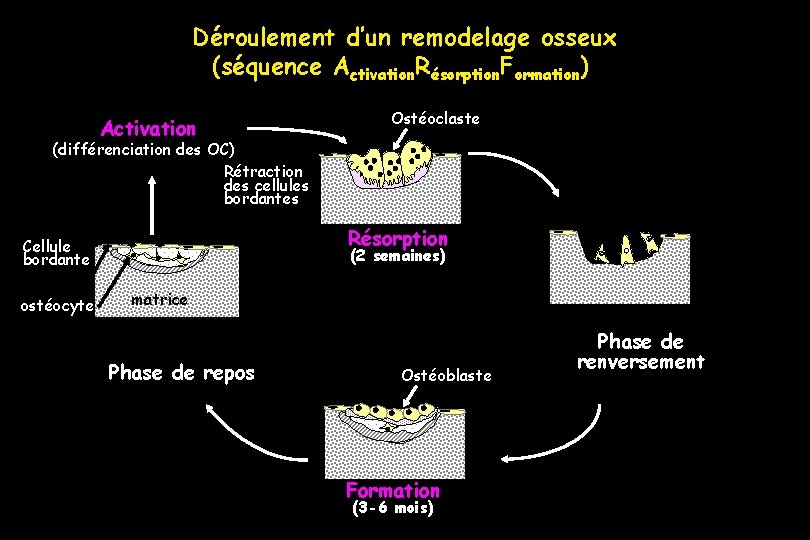
Déroulement d’un remodelage osseux (séquence Activation. Résorption. Formation) Activation Ostéoclaste (différenciation des OC) Rétraction des cellules bordantes Résorption Cellule bordante ostéocyte (2 semaines) matrice Phase de repos Ostéoblaste Formation (3 -6 mois) Phase de renversement

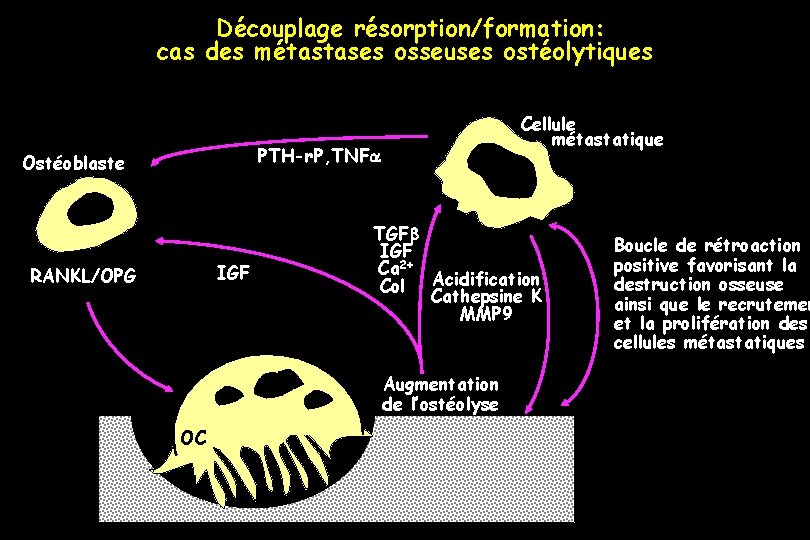
Découplage résorption/formation: cas des métastases osseuses ostéolytiques Cellule métastatique PTH-r. P, TNFa Ostéoblaste IGF RANKL/OPG TGFb IGF Ca 2+ Col Acidification Cathepsine K MMP 9 Augmentation de l’ostéolyse OC Boucle de rétroaction positive favorisant la destruction osseuse ainsi que le recrutemen et la prolifération des cellules métastatiques