SIFAT KOLIGATIF LARUTAN PEMBELAJARAN KIMIA KELAS XII SEMESTER

SIFAT KOLIGATIF LARUTAN PEMBELAJARAN KIMIA KELAS XII SEMESTER 1 SUNARTO SULKAN, S. Pd

SK / KD / Indikator Standar Kompetensi : Menjelaskan sifat- sifat koligatif larutan non-elektrolit dan elektrolit Kompetensi Dasar : Ø Menjelaskan penurunan tekanan uap, kenaikan titik didih penurunan titik beku larutan, dan tekanan osmosis termasuk sifat koligatif larutan Ø Membandingkan antara sifat koligatif larutan non elektrolit dengan sifat koligatif larutan elektrolit yang konsentrasinya sama berdasarkan data percobaan Indikator : ü Menjelaskan arti kemolalan dan fraksi mol serta penggunaannya. ü Menjelaskan pengaruh zat terlarut yang sukar menguap terhadap tekanan uap pelarut. ü Menjelaskan hubungan penurunan tekanan uap dengan fraksi mol zat terlarut. ü Menjelaskan pengertian osmosis dan tekanan osmotik serta terapannya. ü Menemukan hubungan jumlah partikel zat terlarut dengan sifat koligatif larutan elektrolit encer dan non elektrolit berdasarkan data. ü Menyimpulkan perbedaan sifat koligatif larutan elektrolit dengan sifat koligatif larutan non elektrolit.

Konsentrasi Larutan Penurunan tekanan uap jenuh Kenaikan titik didih Penurunan titik beku Tekanan osmotik Koligatif larutan elektrolit Banyaknya partikel dalam larutan ditentukan oleh konsentrasi larutan dan sifat Larutan itu sendiri. Jumlah partikel dalam larutan non elektrolit tidak sama dengan jumlah partikel dalam larutan elektrolit, walaupun konsentrasi keduanya sama. (Hal ini dikarenakan larutan elektrolit terurai menjadi ion -ionnya, sedangkan larutan non elektrolit tidak terurai menjadi ion-ion. )
KONSENTRASI LARUTAN Menyatakan banyaknya zat terlarut dalam suatu larutan Cara untuk menyatakan konsentrasi larutan diantaranya : 1. Konsentrasi Molar 2. Konsentrasi Molal 3. Fraksi Mol

Menyatakan jumlah 1 mol zat terlarut dalam 1 liter larutan (mol/liter)

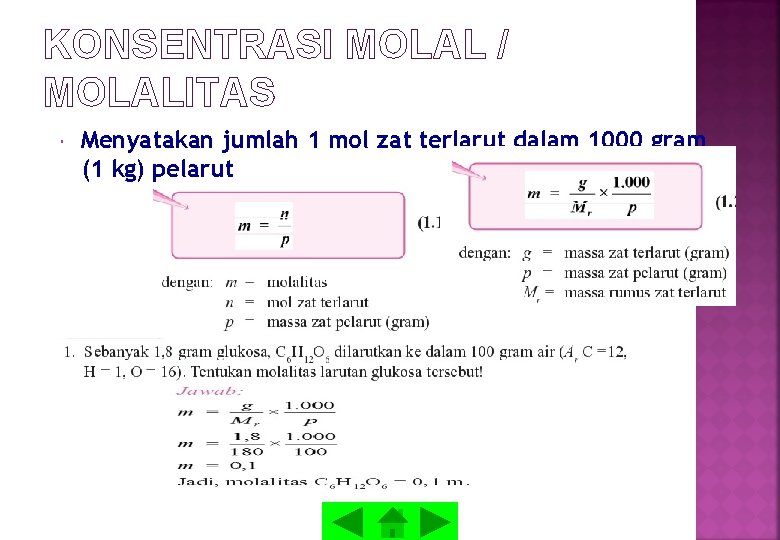
KONSENTRASI MOLAL / MOLALITAS Menyatakan jumlah 1 mol zat terlarut dalam 1000 gram (1 kg) pelarut

1. 2. 3. Jika kita melarutkan 18 gram glukosa ke dalam 500 gram air, maka tentukan kemolalan larutan glukosa (Mr = 180) tersebut. Seorang siswa yang sedang praktikum akan membuat larutan Na. OH 1 molal. Ke dalam berapa gram air harus dilarutkan 20 gram Na. OH? Ibu akan membuat larutan gula pasir (sukrosa) Mr = 342. Berapa gram sukrosa harus dilarutkan ke dalam 100 gram air agar diperoleh larutan sukrosa 0, 1 molal?

FRAKSI MOL Fraksi mol (X) zat terlarut atau zat pelarut menyatakan perbandingan mol (n) zat terlarut atau n pelarut dengan n total larutan (terlarut + pelarut) X terlarut X pelarut = = n terlarut + n pelarut X terlarut n pelarut + X pelarut n terlarut + n pelarut Contoh : sebanyak 2 mol urea terdapat dalam 8 mol air, maka : X terlarut (urea) = X pelarut (air) = 2 2 + 8 8 2 + 8 = 0, 2 = 0, 8 = 1

1. 2. Ani melarutkan 2 gram Na. OH ke dalam 90 gram air. Tentukan fraksi mol Na. OH (Mr = 40) ! Seorang petani akan membuat larutan urea untuk pupuk. Berapa gram air yang diperlukan untuk melarutkan 15 gram urea agar diperoleh fraksi mol larutan urea 0, 1?

Jika 45 gr C 6 H 12 O 6 dilarutkan dalam 500 gr air, maka molalitas larutan adalah … (Ar C = 12; H = 1; ) = 16). a. 0, 50 b. 0, 75 c. 0, 80 d. 0, 90 e. 1, 00 Fraksi mol Urea (Mr = 60), suatu larutan urea dalam air (Mrair = 18) adalah 0, 05, maka molalitas larutan urea tersebut adalah …. a. 0, 95 b. 1, 71 c. 2, 00 d. 2, 92 e. 3, 80 Fraksi mol urea dalam larutan urea 0, 30 m (larutan dalam air) adalah …. a. 0, 0050 b. 0, 0053 c. 0, 0300 d. 0, 0530 e. 0, 9947

SIFAT KOLIGATIF LARUTAN NON ELEKTROLIT adalah sifat larutan yang tidak tergantung pada macamnya zat terlarut tetapi semata-mata hanya ditentukan oleh banyaknya zat terlarut (konsentrasi zat terlarut).

PENURUNAN TEKANAN UAP JENUH Pada setiap suhu, zat cair selalu mempunyai tekanan tertentu. Tekanan ini adalah tekanan uap jenuhnya pada suhu tertentu. Penambahan suatu zat ke dalam zat cair menyebabkan penurunan tekanan uapnya. Hal ini disebabkan karena zat terlarut itu mengurangi bagian atau fraksi dari pelarut, sehingga kecepatan penguapan berkurang. CONTOH

Menurut RAOULT: p = p°. XB dimana: p = tekanan uap jenuh larutan p° = tekanan uap jenuh pelarut murni XB = fraksi mol pelarut Karena XA + XB = 1, maka persamaan di atas dapat diperluas menjadi : p = p° (1 - XA) p = p°- p°. XA p°- p = p°. XA ∆P = penurunan tekanan uap jenuh pelarut p° = tekanan uap pelarut murni XA = fraksi mol zat terlarut

Contoh : Hitunglah penurunan tekanan uap jenuh air, bila 45 gram glukosa (Mr = 180) dilarutkan dalam 90 gram air ! Diketahui tekanan uap jenuh air murni pada 20°C adalah 18 mm. Hg. mol glukosa = 45/180 = 0, 25 mol air = 90/18 = 5 mol fraksi mol glukosa = 0, 25/(0, 25 + 5) = 0, 048 Penurunan tekanan uap jenuh air: ∆p = p°. XA = 18 x 0, 048 = 0, 864 mm. Hg

1. 2. Sebanyak 24 gram urea (Mr=60) dilarutkan dalam 180 gram air pada suhu 25°C. Pada suhu tersebut tekanan uap jenuh air adalah 23, 76 mm. Hg. Tentukanlah tekanan uap larutan! Dalam sebuah percobaan, seorang siswa harus melarutkan glukosa dalam 360 gram air. Agar diperoleh larutan dengan tekanan uap jenuh 0, 1 mm. Hg lebih kecil daripada tekanan uap air pada 25°C, berapa gram glukosa yang harus Ia timbang?

KENAIKAN TITIK DIDIH Adanya penurunan tekanan uap jenuh mengakibatkan titik didih larutan lebih tinggi dari titik didih pelarut murni. Untuk larutan non elektrolit kenaikan titik didih dinyatakan dengan: ∆Tb = m. Kb dimana: ∆Tb = kenaikan titik didih (°C) m = molalitas larutan Kb = tetapan kenaikan titik didih molal CONTOH

Karena : m = (gr/Mr). (1000/p) w = massa zat terlarut Maka kenaikan titik didih larutan dapat dinyatakan sebagai: ∆Tb = (gr/Mr). (1000/p). Kb Apabila pelarutnya air dan tekanan udara 1 atm, maka titik didih larutan dinyatakan sebagai: Tb = (100 + ∆Tb) °C DIAGRAM P-T

1. 2. Sebanyak 6 gram urea (Mr= 60) dilarutkan dalam 500 gram air. Tentukan titik didih larutan. Sebanyak 15 gram zat X non elektrolit dilarutkan dalam 250 gram air. Larutan ini mendidih pada suhu 100, 156°C. Kb air = 0, 52. Tentukan Mr senyawa X!

PENURUNAN TITIK BEKU Untuk penurunan titik beku persamaannya dinyatakan sebagai : ∆Tf = m. Kf = w/Mr. 1000/p. Kf dimana: ∆Tf = penurunan titik beku m = molalitas larutan Kf = tetapan penurunan titik beku molal w = massa zat terlarut Mr = massa molekul relatif zat terlarut p = massa pelarut CONTOH DIAGRAM P-T Apabila pelarutnya air dan tekanan udara 1 atm, maka titik beku larutannya dinyatakan sebagai: Tf = (0 - ∆Tf) °C

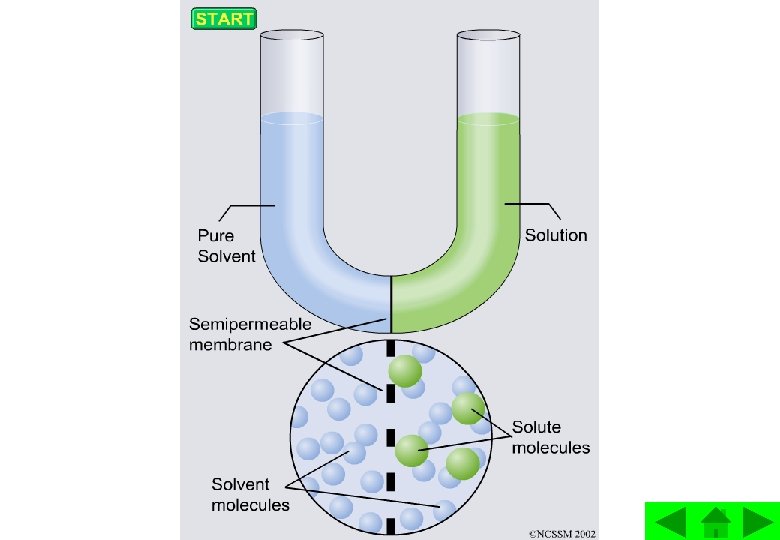
TEKANAN OSMOTIK Tekanan osmotik adalah tekanan yang diberikan pada larutan yang dapat menghentikan perpindahan molekul-molekul pelarut ke dalam larutan melalui membran semi permeabel (proses osmosis). CONTOH Menurut VAN'T HOFF tekanan osmotik mengikuti hukum gas ideal: PV = n. RT

Karena tekanan osmotik = π , maka : π = n/V R T = C R T dimana : π = tekanan osmotik (atmosfir) C = konsentrasi larutan (mol/liter= M) R = tetapan gas universal = 0. 082 liter. atm/mol °K T = suhu mutlak (°K)

Larutan yang mempunyai tekanan osmotik lebih rendah dari yang lain disebut larutan Hipotonis. Larutan yang mempunyai tekanan osmotik lebih tinggi dari yang lain disebut larutan Hipertonis. Larutan-larutan yang mempunyai tekanan osmotik sama disebut Isotonis.

SIFAT KOLIGATIF LARUTAN ELEKTROLIT Larutan elektrolit di dalam pelarutnya mempunyai kemampuan untuk mengion. Hal ini mengakibatkan larutan elektrolit mempunyai jumlah partikel yang lebih banyak daripada larutan non elektrolit pada konsentrasi yang sama

Contoh: Larutan 0. 5 molal glukosa dibandingkan dengan iarutan 0, 5 molal garam dapur. Untuk larutan glukosa dalam air jumlah partikel (konsentrasinya) tetap, yaitu 0, 5 molal. Untuk larutan garam dapur : Na. Cl(aq) Na+ (aq) + Cl(aq) karena terurai menjadi 2 ion, maka konsentrasi partikelnya menjadi 2 kali semula = 1, 0 molal.

Yang menjadi ukuran langsung dari keadaan (kemampuannya) untuk mengion adalah derajat ionisasi. Besarnya derajat ionisasi ini dinyatakan sebagai: α = jumlah mol zat yang terionisasi jumlah mol zat mula-mula Untuk larutan elektrolit kuat, harga derajat ionisasinya mendekati 1, sedangkan untuk elektrolit lemah, harganya berada di antara 0 dan 1 (0 < α < 1).

Atas dasar kemampuan ini, maka larutan elektrolit mempunyai pengembangan di dalam perumusan sifat koligatifnya : 1. Untuk Kenaikan Titik Didih ∆Tb = m. Kb [1 + α(n-1)] = w/Mr. 1000/p. Kb [1+ α(n-1)] n = jumlah ion dari larutan elektrolitnya. 2. Untuk Penurunan Titik Beku dinyatakan sebagai: ∆Tf = m. Kf [1 + α(n-1)] = w/Mr. 1000/p. Kf [1+ α(n-1)] 3. Untuk Tekanan Osmotik dinyatakan sebagai: π = C R T [1+ α(n-1)]

Contoh: Hitunglah kenaikan titik didih dan penurunan titik beku dari larutan 5, 85 gram garam dapur (Mr = 58, 5) dalam 250 gram air ! (bagi air, Kb= 0, 52 dan Kf= 1, 86) Jawab: Larutan garam dapur, Na. Cl(aq) - Na. F+ (aq) + Cl- (aq) Jumlah ion = 2 ∆Tb = 5, 85/58, 5 x 1000/250 x 0, 52 [1+1(2 -1)] = 0, 208 x 2 = 0, 416 °C ∆Tf = 5, 85/58, 5 x 1000/250 x 0, 86 [1+1(2 -1)] = 0, 744 x 2 = 1, 488 °C
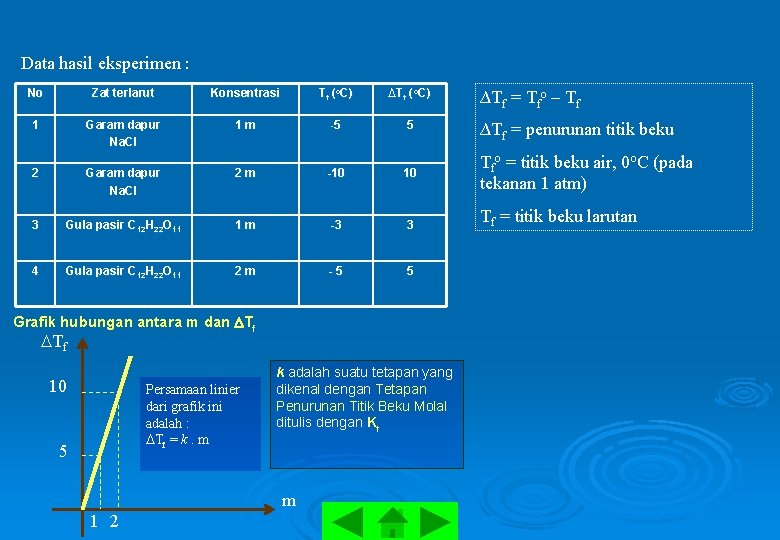
Data hasil eksperimen : No Zat terlarut Konsentrasi Tf (o. C) ∆Tf (o. C) 1 Garam dapur Na. Cl 1 m -5 5 2 Garam dapur Na. Cl 2 m -10 10 3 Gula pasir C 12 H 22 O 11 1 m -3 3 4 Gula pasir C 12 H 22 O 11 2 m -5 5 Grafik hubungan antara m dan Tf 10 Persamaan linier dari grafik ini adalah : Tf = k. m 5 k adalah suatu tetapan yang dikenal dengan Tetapan Penurunan Titik Beku Molal ditulis dengan Kf m 1 2 ∆Tf = Tfo – Tf ∆Tf = penurunan titik beku Tfo = titik beku air, 0 o. C (pada tekanan 1 atm) Tf = titik beku larutan
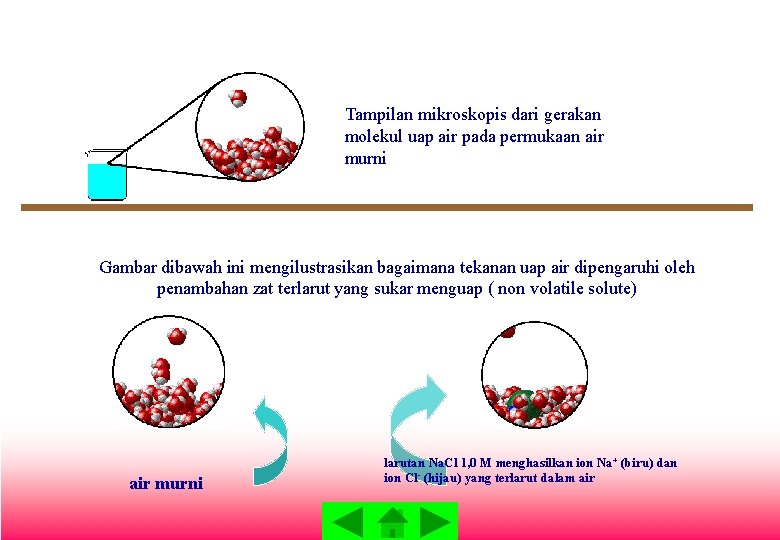
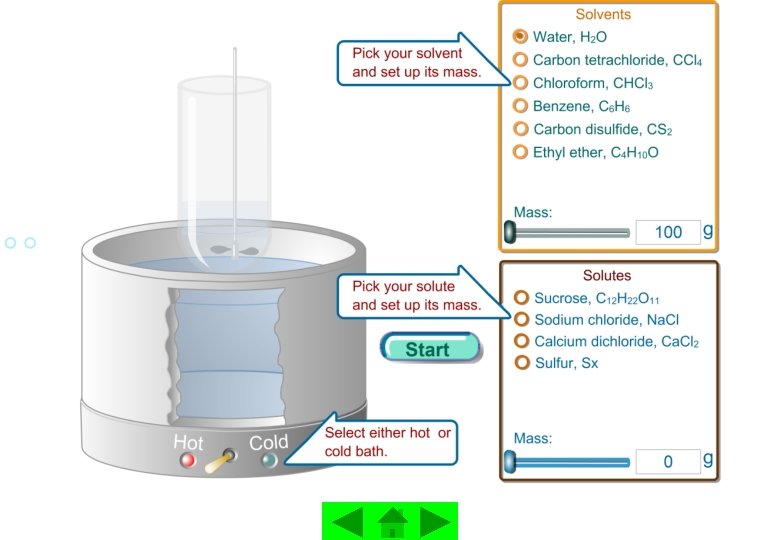
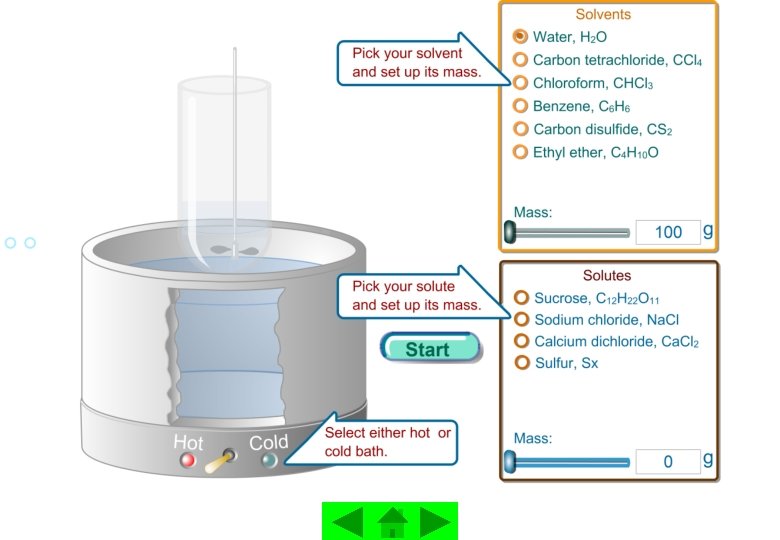
Tampilan mikroskopis dari gerakan molekul uap air pada permukaan air murni Gambar dibawah ini mengilustrasikan bagaimana tekanan uap air dipengaruhi oleh penambahan zat terlarut yang sukar menguap ( non volatile solute) air murni larutan Na. Cl 1, 0 M menghasilkan ion Na+ (biru) dan ion Cl- (hijau) yang terlarut dalam air

Di negara bermusim dingin, Na. Cl ditaburkan di jalan-jalan untuk mencairkan salju. Bagi penjual es krim, Na. Cl di- gunakan untuk mempertahan agar es krim tidak cepat mencair. Mengapa bisa begitu ya ?
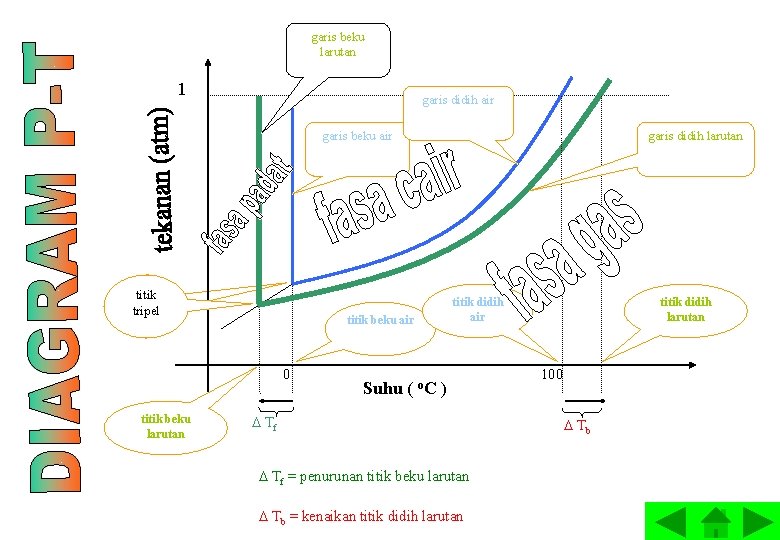
garis beku larutan 1 garis didih air garis beku air titik tripel titik didih air titik beku air 0 titik beku larutan garis didih larutan Suhu ( o. C ) Tf = penurunan titik beku larutan Tb = kenaikan titik didih larutan 100 Tb
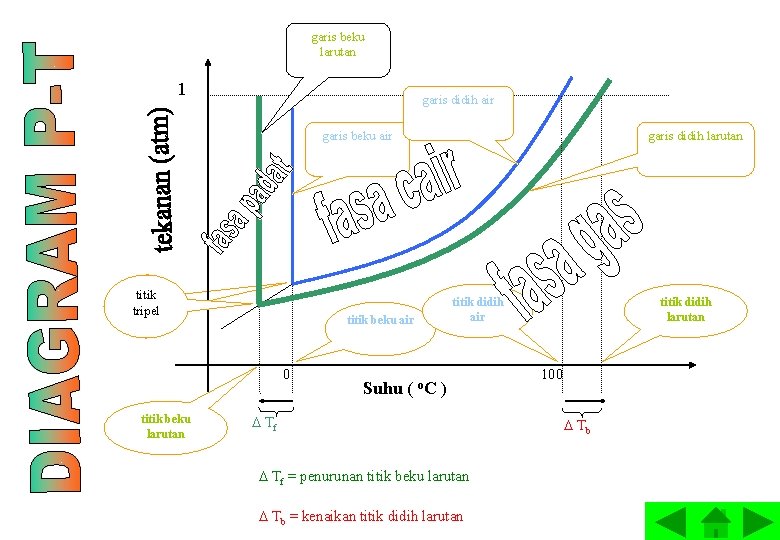
garis beku larutan 1 garis didih air garis beku air titik tripel titik didih air titik beku air 0 titik beku larutan garis didih larutan Suhu ( o. C ) Tf = penurunan titik beku larutan Tb = kenaikan titik didih larutan 100 Tb
- Slides: 36