SIFAT KOLIGATIF LARUTAN Disusun Oleh Nama NIM Jurusan














- Slides: 34

SIFAT KOLIGATIF LARUTAN Disusun Oleh : Nama NIM Jurusan : Nova deswita : 1630110014 : Tadris Kimia

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi BERANDA Penyusun SELESAI BAB 1 SIFAT KOLIGATIF LARUTAN Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi SK - KD Penyusun SELESAI STANDAR KOMPETENSI §Menjelaskan sifat- sifat koligatif larutan non-elektrolit dan elektrolit KOMPETENSI DASAR §Menjelaskan penurunan tekanan uap, kenaikan titik didih penurunan titik beku larutan, dan tekanan osmosis termasuk sifat koligatif larutan §Membandingkan antara sifat koligatif larutan non elektrolit dengan sifat koligatif larutan elektrolit yang konsentrasinya sama berdasarkan data percobaan Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi INDIKATOR Penyusun SELESAI INDIKATOR q Menjelaskan arti kemolalan dan fraksi mol serta penggunaannya. q Menjelaskan pengaruh zat terlarut yang sukar menguap terhadap tekanan uap pelarut. q Menjelaskan hubungan penurunan tekanan uap dengan fraksi mol zat terlarut. q Menjelaskan pengertian osmosis dan tekanan osmotik serta terapannya. q Menemukan hubungan jumlah partikel zat terlarut dengan sifat koligatif larutan elektrolit encer dan non elektrolit berdasarkan data. q Menyimpulkan perbedaan sifat koligatif larutan elektrolit dengan sifat koligatif larutan non elektrolit. Back Next

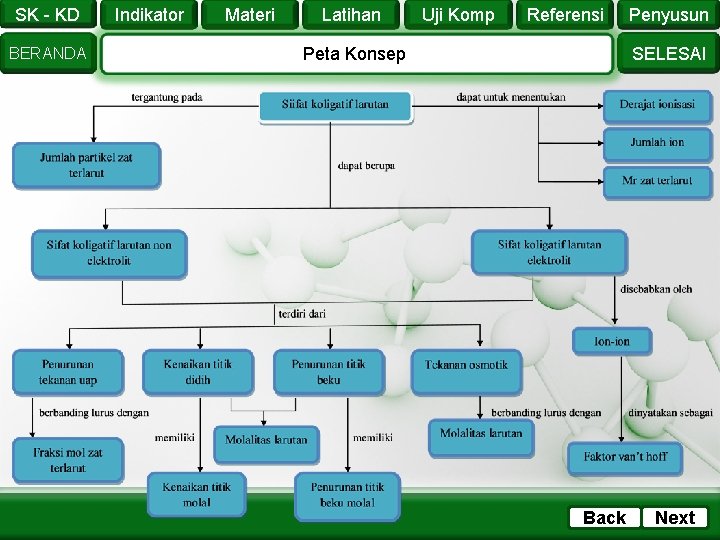
SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI Peta Konsep Back Next

SK - KD Indikator BERANDA Materi Latihan Uji Komp Referensi MATERI Penyusun SELESAI APA ITU SIFAT KOLIGATIF? SIFAT KOLIGATIF adalah sifat-sifat larutan yang tidak bergantung pada jenis zat terlarut, tetapi hanya pada konsentrasi partikel terlarutnya Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi MATERI Penyusun SELESAI q Banyaknya partikel dalam larutan ditentukan oleh konsentrasi larutan dan sifat Larutan itu sendiri. q Jumlah partikel dalam larutan non elektrolit tidak sama dengan jumlah partikel dalam larutan elektrolit, walaupun konsentrasi keduanya sama. (Hal ini dikarenakan larutan elektrolit terurai menjadi ion-ionnya, sedangkan larutan non elektrolit tidak terurai menjadi ion-ion). Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi MATERI Penyusun SELESAI KONSENTRASI LARUTAN PENURUNAN TEKANAN UAP JENUH KENAIKAN TITIK DIDIH PENURUNAN TITIK BEKU TEKANAN OSMOTIK SIFAT KOLIGATIF LARUTAN ELEKTROLIT Back Next

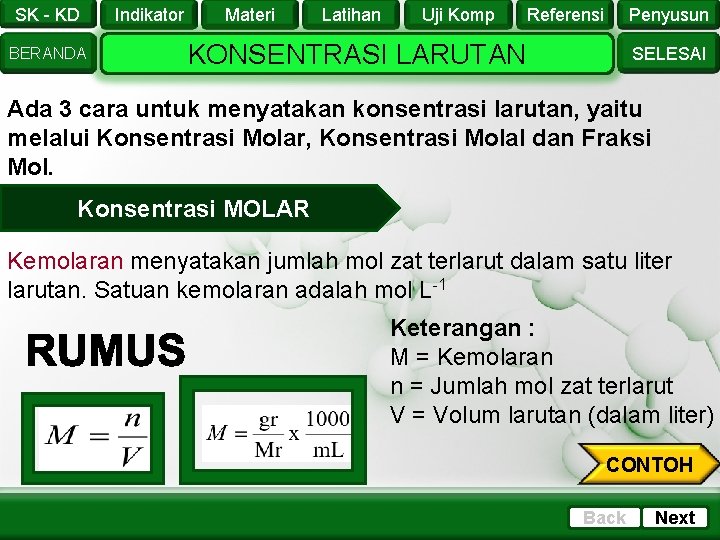
SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi Penyusun KONSENTRASI LARUTAN SELESAI Ada 3 cara untuk menyatakan konsentrasi larutan, yaitu melalui Konsentrasi Molar, Konsentrasi Molal dan Fraksi Mol. Konsentrasi MOLAR Kemolaran menyatakan jumlah mol zat terlarut dalam satu liter larutan. Satuan kemolaran adalah mol L-1 Keterangan : M = Kemolaran n = Jumlah mol zat terlarut V = Volum larutan (dalam liter) CONTOH Back Next

SK - KD Indikator BERANDA Materi Latihan Uji Komp Referensi CONTOH Penyusun SELESAI Jika dalam 500 m. L larutan terdapat 6 gram urea (Mr =60), maka molaritas larutan adalah : Jawab : INGAT Back Next

SK - KD Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI BERANDA Konsentrasi MOLAL Kemolalan atau molalitas menyatakan jumlah mol (n) zat terlarut dalam 1 kg (=1000 g) pelarut. Oleh karena itu, kemolalan dinyatakan dalam mol kg-1 Keterangan : m = Kemolalan larutan n = Jumlah mol zat terlarut p = masa pelarut (dalam kg) CONTOH Back Next

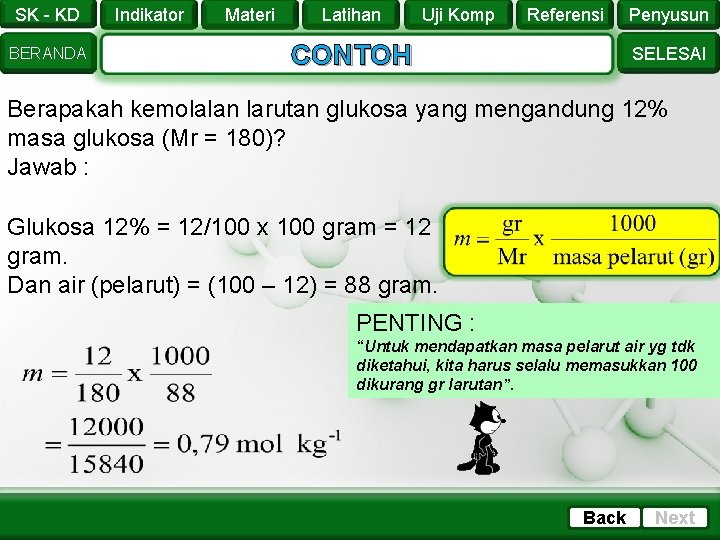
SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi CONTOH Penyusun SELESAI Berapakah kemolalan larutan glukosa yang mengandung 12% masa glukosa (Mr = 180)? Jawab : Glukosa 12% = 12/100 x 100 gram = 12 gram. Dan air (pelarut) = (100 – 12) = 88 gram. PENTING : “Untuk mendapatkan masa pelarut air yg tdk diketahui, kita harus selalu memasukkan 100 dikurang gr larutan”. Back Next

SK - KD Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI BERANDA Fraksi Mol Fraksi mol (X) zat terlarut atau zat pelarut menyatakan perbandingan mol (n) zat terlarut atau n pelarut dengan n total larutan (terlarut + pelarut) X terlarut X pelarut = = n terlarut + n pelarut X terlarut + X pelarut = 1 n terlarut + n pelarut CONTOH Kembali ke MENU Back Next

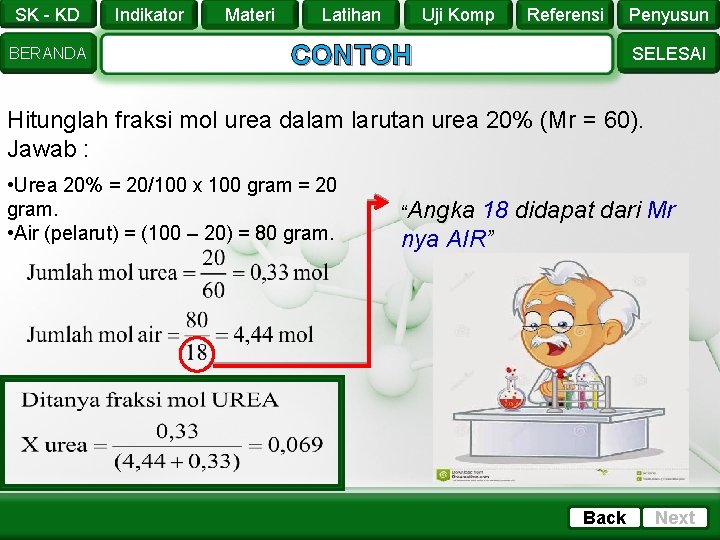
SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi CONTOH Penyusun SELESAI Hitunglah fraksi mol urea dalam larutan urea 20% (Mr = 60). Jawab : • Urea 20% = 20/100 x 100 gram = 20 gram. • Air (pelarut) = (100 – 20) = 80 gram. “Angka 18 didapat dari Mr nya AIR” Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi Penyusun PENURUNAN TEKANAN UAP JENUH SELESAI Pada setiap suhu, zat cair selalu mempunyai tekanan tertentu. Tekanan ini adalah tekanan uap jenuhnya pada suhu tertentu. Penambahan suatu zat ke dalam zat cair menyebabkan penurunan tekanan uapnya. Hal ini disebabkan karena zat terlarut itu mengurangi bagian atau fraksi dari pelarut, sehingga kecepatan penguapan berkurang. CONTOH Back Next

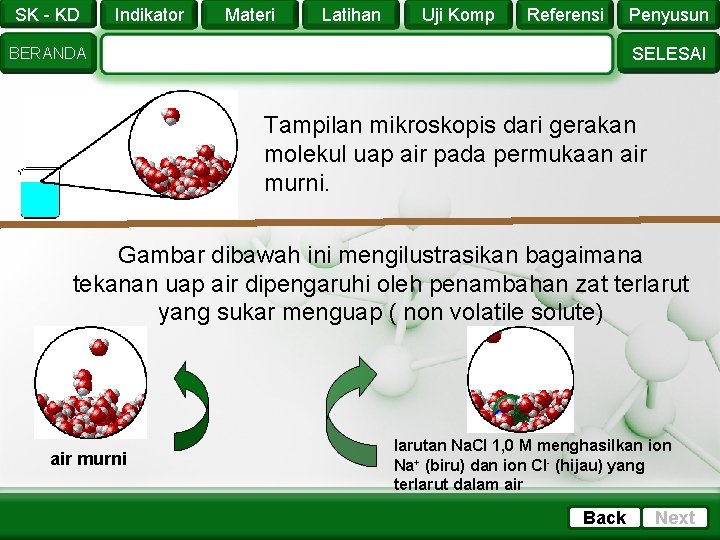
SK - KD Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI BERANDA Tampilan mikroskopis dari gerakan molekul uap air pada permukaan air murni. Gambar dibawah ini mengilustrasikan bagaimana tekanan uap air dipengaruhi oleh penambahan zat terlarut yang sukar menguap ( non volatile solute) air murni larutan Na. Cl 1, 0 M menghasilkan ion Na+ (biru) dan ion Cl- (hijau) yang terlarut dalam air Back Next

SK - KD Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI BERANDA Menurut Francois Marie Raoult mengemukakan bahwa tekanan uap suatu komponen bergantung pada fraksi mol komponen itu dalam larutan, dengan hubungan sebagai berikut. P = tekanan uap komponen A A XA = fraksi mol komponen P 0 A = tekanan uap A murni PA = X A x Po. A Untuk menentukan tekanan uap larutan dapat menggunakan rumus berikut : Plarutan = Xpelarut x Popelarut Selisih antara tekanan uap pelarut dengan tekanan uap larutan disebut penurunan tekanan uap (∆P). Dapat digunakan rumus sebagai berikut : ∆P = Xter x Po Kembali ke MENU CONTOH Back Next

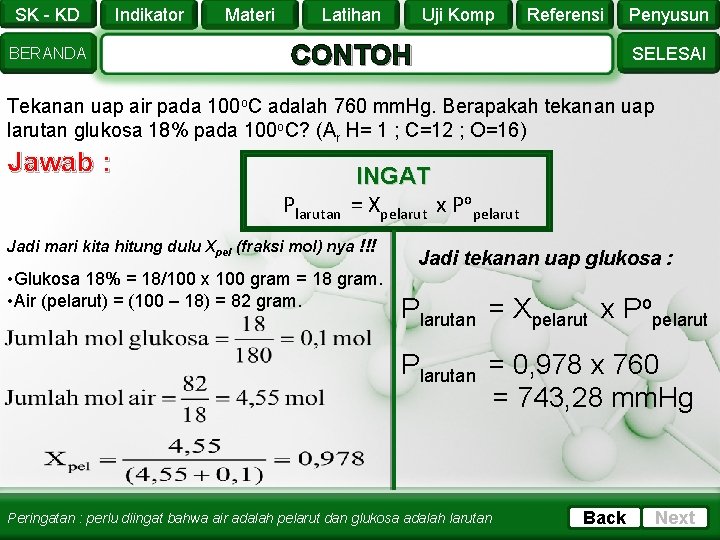
SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi CONTOH Penyusun SELESAI Tekanan uap air pada 100 o. C adalah 760 mm. Hg. Berapakah tekanan uap larutan glukosa 18% pada 100 o. C? (Ar H= 1 ; C=12 ; O=16) Jawab : Plarutan INGAT = Xpelarut x Popelarut Jadi mari kita hitung dulu Xpel (fraksi mol) nya !!! • Glukosa 18% = 18/100 x 100 gram = 18 gram. • Air (pelarut) = (100 – 18) = 82 gram. Jadi tekanan uap glukosa : Plarutan = Xpelarut x Popelarut Plarutan = 0, 978 x 760 = 743, 28 mm. Hg Peringatan : perlu diingat bahwa air adalah pelarut dan glukosa adalah larutan Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi Penyusun KENAIKAN TITIK DIDIH (∆Tb) SELESAI Titik didih adalah suhu pada saat tekanan uap cairan sama dengan tekanan di permukaan. Oleh karena itu, titik didih bergantung pada tekanan di permukaan. Perlu diingat beberapa ketentuan berikut : q q Suatu pelarut jika di + zat terlarut titik didih akan naik Besarnya kenaikan titik didih ~ konsentrasi molal ( m ) Tb = titik didih larutan – titik didih pelarut murni Kb = tetapan kenaikan titik didih Tb = m x Kb atau bisa juga pakai rumus yang m = gr/mr x 1000/p Liat DIAGRAM P-T Kembali ke MENU CONTOH Back Next

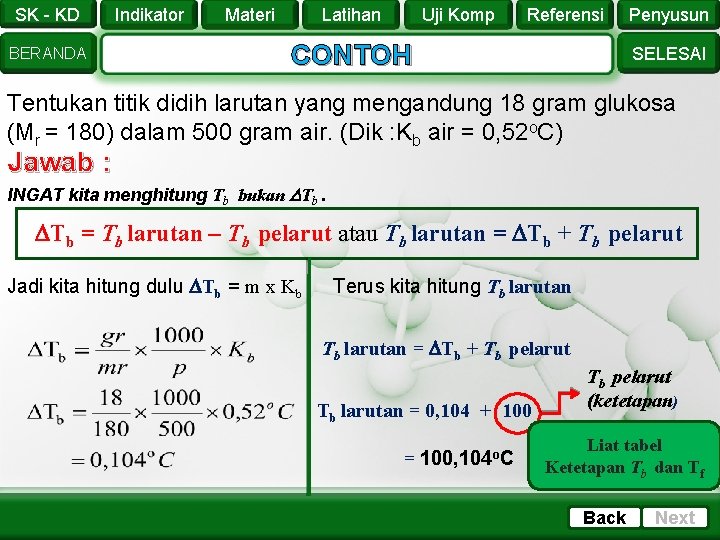
SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi CONTOH Penyusun SELESAI Tentukan titik didih larutan yang mengandung 18 gram glukosa (Mr = 180) dalam 500 gram air. (Dik : Kb air = 0, 52 o. C) Jawab : INGAT kita menghitung Tb bukan Tb. Tb = Tb larutan – Tb pelarut atau Tb larutan = Tb + Tb pelarut Jadi kita hitung dulu Tb = m x Kb Terus kita hitung Tb larutan = Tb + Tb pelarut Tb larutan = 0, 104 + 100 = 100, 104 o. C Tb pelarut (ketetapan) Liat tabel Ketetapan Tb dan Tf Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi Penyusun PENURUNAN TITIK BEKU (∆Tf) SELESAI Titik beku adalah suhu pada saat tekanan uap cairan sama dengan tekanan uap padatnya. Perlu diingat beberapa ketentuan berikut : q q Suatu pelarut jk di + zat terlarut titik bekunya akan turun Besarnya penurunan titik beku ~ konsentrasi molal ( m ) Tf = titik beku pelarut murni – titik beku larutan Kf = tetapan penurunan titik beku Atau Tf = m x Kf Liat DIAGRAM P-T CONTOH Kembali ke MENU Back Next

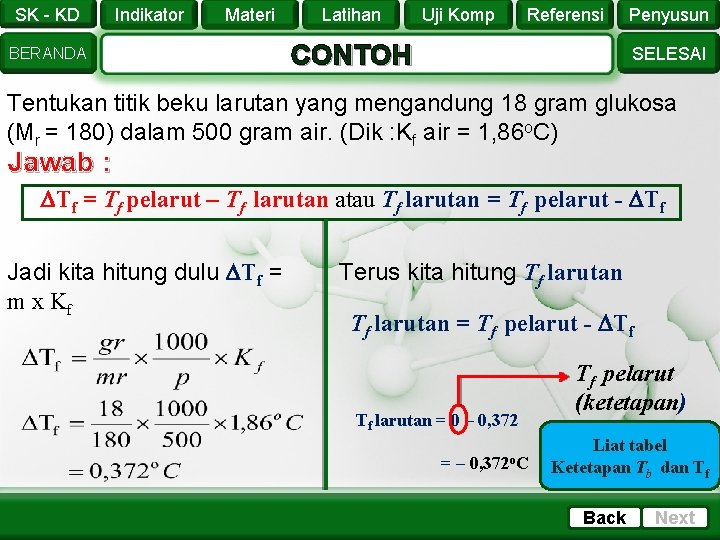
SK - KD Indikator Materi BERANDA Latihan Uji Komp Referensi CONTOH Penyusun SELESAI Tentukan titik beku larutan yang mengandung 18 gram glukosa (Mr = 180) dalam 500 gram air. (Dik : Kf air = 1, 86 o. C) Jawab : Tf = Tf pelarut – Tf larutan atau Tf larutan = Tf pelarut - Tf Jadi kita hitung dulu Tf = m x Kf Terus kita hitung Tf larutan = Tf pelarut - Tf Tf larutan = 0 – 0, 372 =– 0, 372 o. C Tf pelarut (ketetapan) Liat tabel Ketetapan Tb dan Tf Back Next

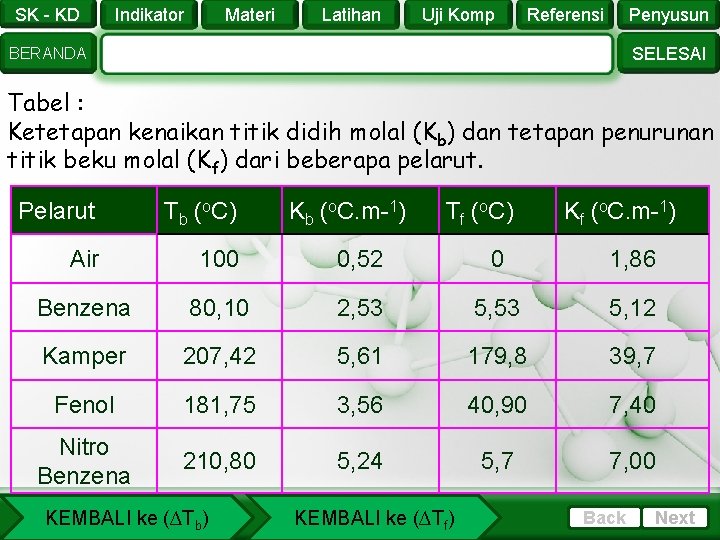
SK - KD Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI BERANDA Tabel : Ketetapan kenaikan titik didih molal (Kb) dan tetapan penurunan titik beku molal (Kf) dari beberapa pelarut. Pelarut Tb (o. C) Air 100 0, 52 0 1, 86 Benzena 80, 10 2, 53 5, 12 Kamper 207, 42 5, 61 179, 8 39, 7 Fenol 181, 75 3, 56 40, 90 7, 40 Nitro Benzena 210, 80 5, 24 5, 7 7, 00 KEMBALI ke (∆Tb) Kb (o. C. m-1) Tf (o. C) KEMBALI ke (∆Tf) Kf (o. C. m-1) Back Next

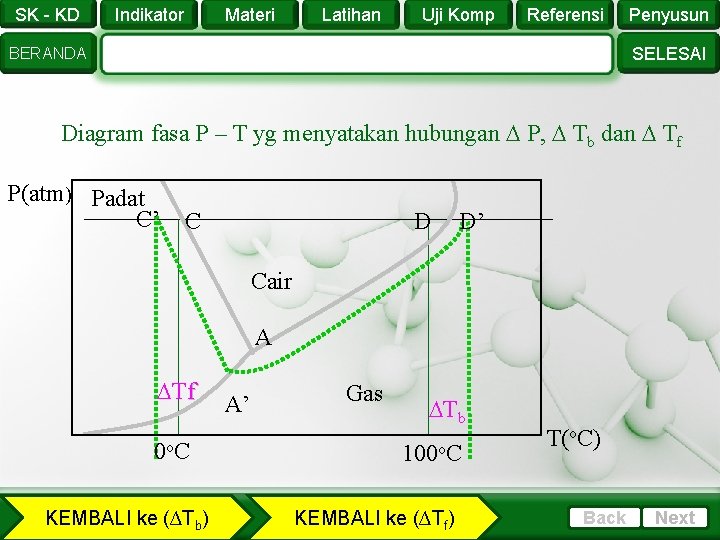
SK - KD Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI BERANDA Diagram fasa P – T yg menyatakan hubungan P, Tb dan Tf P(atm) Padat C’ C D D’ Cair A Tf 0 o. C KEMBALI ke (∆Tb) A’ Gas Tb 100 o. C KEMBALI ke (∆Tf) T(o. C) Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi TEKANAN OSMOTIK Penyusun SELESAI Osmosis adalah proses berpindahnya pelarut dari larutan yg lebih encer ke larutan pekat melalui membran semipermeabel ( hanya dapat dilalui oleh pelarut). Tekanan osmotik adalah tekanan yang diperlukan untuk menghentikan aliran dari pelarut murni ke dalam larutan Alat yang digunakan untuk mengukur besarnya tekanan osmotik adalah Osmometer Back Next

SK - KD Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI BERANDA Menurut Van’t Hoff , tekanan osmotik larutan-larutan encer dapat dihitung dengan rumus yang serupa dengan persamaan gas ideal, yaitu : πV = n. RT Atau π = MRT π = tekanan osmotik V = volum larutan (dalam liter) n = jumlah mol zat terlarut T = suhu absolut larutan (suhu kelvin) R = tetapan gas (0, 082 L atm mol-1 K-1) CONTOH Back Next

SK - KD Indikator Materi BERANDA Latihan Uji Komp Referensi CONTOH Penyusun SELESAI Hitunglah tekanan osmotik dari 500 m. L larutan yang mengandung 9 gram glukosa (Mr = 180) pada suhu 27 o. C. Jawab : Dik : R = 0, 08 T = 27 o. C = 300 o. K π = MRT Back Next

SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi SIFAT KOLIGATIF LARUTAN ELEKTROLIT Penyusun SELESAI Dari teori ion Svante August Arrhenius dikemukakan bahwa larutan asam, basa ataupun garam termasuk larutan elektrolit. Larutan elektrolit yaitu larutan yg dapat terionisasi atau terurai menjadi ion – ion. Dan akibat peruraian itu maka dapat mengakibatkan bertambahnya jumlah partikel Back Next

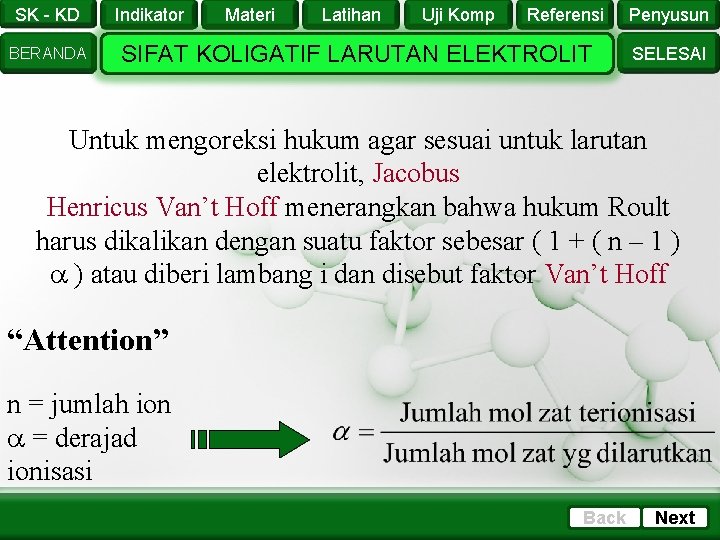
SK - KD BERANDA Indikator Materi Latihan Uji Komp Referensi SIFAT KOLIGATIF LARUTAN ELEKTROLIT Penyusun SELESAI Untuk mengoreksi hukum agar sesuai untuk larutan elektrolit, Jacobus Henricus Van’t Hoff menerangkan bahwa hukum Roult harus dikalikan dengan suatu faktor sebesar ( 1 + ( n – 1 ) ) atau diberi lambang i dan disebut faktor Van’t Hoff “Attention” n = jumlah ion = derajad ionisasi Back Next

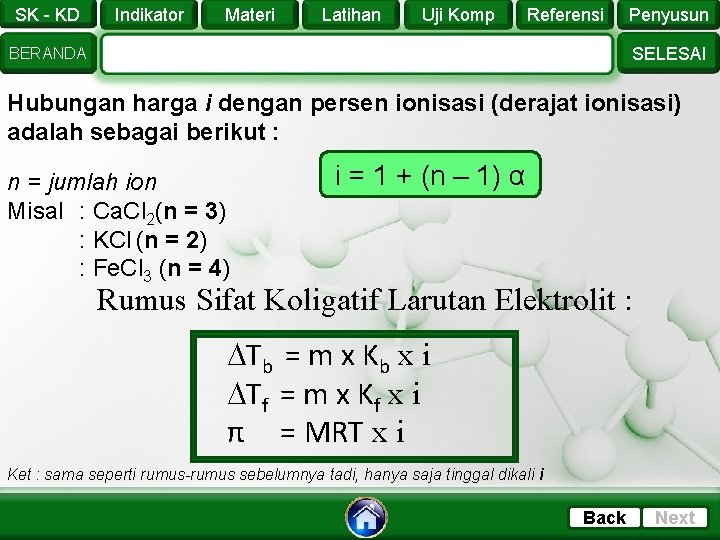
SK - KD Indikator Materi Latihan Uji Komp Referensi Penyusun SELESAI BERANDA Hubungan harga i dengan persen ionisasi (derajat ionisasi) adalah sebagai berikut : n = jumlah ion Misal : Ca. Cl 2(n = 3) : KCl (n = 2) : Fe. Cl 3 (n = 4) i = 1 + (n – 1) α Rumus Sifat Koligatif Larutan Elektrolit : Tb = m x Kb x i Tf = m x Kf x i π = MRT x i Ket : sama seperti rumus-rumus sebelumnya tadi, hanya saja tinggal dikali i Back Next

SK - KD Indikator Materi Latihan Uji Komp Referensi LATIHAN BERANDA Penyusun SELESAI 1. Kemolalan suatu larutan 20% masa C 2 H 5 OH (Mr = 46) adalah. . A 6, 4 mol D 3, 4 mol B 5, 4 mol E 0, 4 mol C 4, 4 mol PILIH SOAL : 1 2 3 Back Next

SK - KD Indikator Materi Latihan Uji Komp Referensi LATIHAN BERANDA A 75 C 120 B 90 D 150 Penyusun SELESAI E 180 PILIH SOAL : 1 2 3 Back Next

SK - KD Indikator BERANDA Materi Latihan Uji Komp Referensi LATIHAN A 1/2 C 2/3 B 1/4 D 2/5 Penyusun SELESAI E 3/4 PILIH SOAL : 1 2 3 Back Next

SK - KD Indikator BERANDA Materi Latihan Uji Komp Referensi Penutup Penyusun SELESAI Thank you Back Next