si RNA Small interfering RNA Luz Angela Betancourt
si. RNA (Small interfering RNA). Luz Angela Betancourt Cano
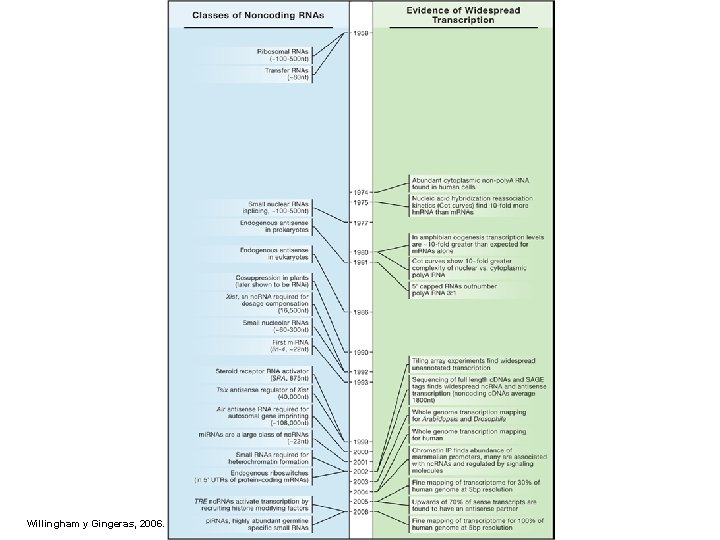
Willingham y Gingeras, 2006.

1990 Silenciamiento Genético Post Transcripcional (SGPT ó PTGS). Petunia: La petúnia posee un gen cuya misión es dar color a la flor. Si se añade una copia del mismo, se neutraliza la acción del gen existente. http: //www. cultek. com/aplicaciones. asp? p=Aplicacion_s. IRNA&opc=introduccion&idap=8

Descubrimiento del i. ARN Caenorhabditis elegans A finales de la década pasada. Andrew Fire, Craig Mello y sus colaboradores demostraron en el nematodo Caenorhabditis elegans, que el causante final de este silenciamiento postranscripcional eran moléculas de ARN de doble cadena (ARNdc ó ds. RNA). (Grishot et al, 1998; Fire et al 1998).

i. RNA (RNA DE INTERFERENCIA) Molécula pequeñas de RNA (20 -25 nucleótidos) generados por precursores más largos que suprime la acción de genes específicos. En plantas esto puede ocurrir durante la transcripción como después de la misma. En animales sólo se conoce que ocurra después de la transcripción. (Bernstein et al, 2001). Clasificación: • si. RNA (small interference RNAs). • mi. RNAs (micro. RNAs). • pi. RNAs (Piwi-interacting RNAs, ARNs asociados a Piwi). http: //www. cultek. com/aplicaciones. asp? p=Aplicacion_s. IRNA&opc=introduccion
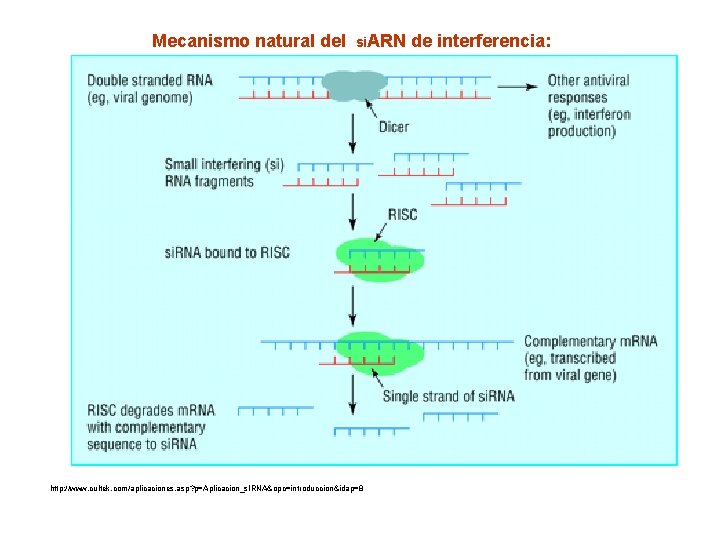
Mecanismo natural del si. ARN de interferencia: http: //www. cultek. com/aplicaciones. asp? p=Aplicacion_s. IRNA&opc=introduccion&idap=8
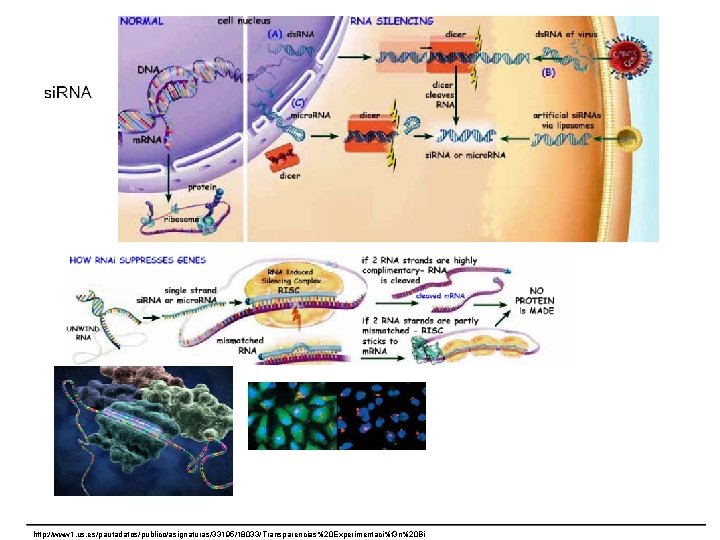
http: //www 1. us. es/pautadatos/publico/asignaturas/33195/18033/Transparencias%20 Experimentaci%f 3 n%20 Bi


DISEÑO DE si. RNA Diseño aleatorio. Con este método se seleccionan 19 -21 bases del ARNm diana sin tener en cuenta la secuencia o la información posicional que tiene en el transcrito. Es decir, sin saber si pertenece a la fase abierta de lectura o a las regiones 5’ ó 3’ no traducidas. Diseño convencional Se seleccionan dianas de 19 -21 bases mediante parámetros simples desarrollados por los pioneros de la técnica (Calipel, A. et al. , 2003) completados con un análisis BLAST de nucleótidos. http: //www. cultek. com/aplicaciones. asp? p=Aplicacion_s. IRNA&opc=introduccion

Los cuatro criterios fundamentales del diseño convencional son: 1. Identifica regiones a partir de 75 -100 bases por debajo del codón de iniciación y evita secuencias que puedan estar ocupadas por proteínas reguladoras o que puedan estar implicadas en la traducción. 2. En la zona codificante queda identifica regiones con el motivo AA(N 19)TT, donde N equivale a cualquier nucleótido. Si no se encuentra, se relajan las condiciones de búsqueda a secuencias con el motivo NA(N 21). N 19 representa los 9 nucleótidos del centro del dúplex mientras que NA, AA y TT definen las secuencias sobresalientes (overhangs). 3. Evalúa el contenido GC de las secuencias si. RNA potenciales. Idealmente el contenido GC debería ser lo mas cercano posible al 50% o entre un rango 30%-70%. 4. Compara el candidato con marcadores de secuencia expresados (GST) en bases de datos públicas (BLAST por ejemplo) para asegurarse especificidad. http: //www. cultek. com/aplicaciones. asp? p=Aplicacion_s. IRNA&opc=introduccion

Diseño racional es un procedimiento informático dirigido a identificar las dianas óptimas de si. RNA en un ARNm. Las secuencias diana se analizan en grupos de 19 nucleótidos a la vez y se identifican las que tienen mejores características. El algoritmo de la plataforma SMARTselection se distingue por: 1. Evalúa las dianas en base atributos asociados con si. RNAs funcionales. 2. Lleva a cabo comparaciones sistemáticas de secuencias. 3. Elimina de forma efectiva los si. RNAno funcionales del conjunto de candidatos. http: //www. cultek. com/aplicaciones. asp? p=Aplicacion_s. IRNA&opc=tecnicas

SMARTPool® Posteriormente se comprobó que usando una mezcla de si. RNAs diseñados por el método racional (SMARTselection) se obtiene un potente silenciamiento >95%, frente al 61, 5 con duplex individuales. Adicionalmente se observó una disminución clara en las reacciones secundarias de inhibición. Métodos de producción de si. RNAs Transcripción “in Vitro”. Transcripción enzimática del si. RNA a partir de un molde de ADNdc. Ventajas: - Bajo coste Inconvenientes - Terminación temprana de la transcripción - Baja pureza del transcrito “in Vitro” - No hay probabilidades de modificaciones químicas http: //www. cultek. com/aplicaciones. asp? p=Aplicacion_s. IRNA&opc=tecnicas

Cassettes de expresión por PCR El cassette de expresión incorpora un promotor para la polimerasa H 1 ó U 6 de la ARN polimerasa III. El cassette codifica para la cadena sentido, antisentido, o para una cadena con horquilla (sh. RNA). Una vez amplificado, se transfecta en las células, donde se expresa si. RNA ó sh. RNA dependiente de la ARN polimerasa III. Ventajas: - Bajo coste - Los cassettes se pueden introducir a un vector para hacer sh. RNA Problemas: -Proceso complejo e ineficiente. - Actividad de la ARN polimerasa III varía de una célula a otra, variando también la capacidad de silenciamiento. - si. RNA se debe formar a partir de dos promotores, separados y anillarse dentro de la célula.

Plásmidos Expresión a partir de plásmidos de transcritos de una cadena que forman horquillas (sh. RNA) Ventajas - Bajo coste - Eficiencia y silenciamiento estables en el tiempo. Inconvenientes - Dificultad de diseño - Problemas de mantenimiento del plásmido, ya que los antibióticos pueden afectar a la célula huésped.

Química La síntesis de ARN mediante la química 2’-ACE permite la síntesis de ARN de alta calidad. Ventajas - Altos niveles de pureza - Gran estabilidad en fluidos biológicos - Posibilidad de modificaciones químicas que permiten hacer seguimiento del si. RNA (Fluoróforos) o mejorar la especificidad o mejorar la estabilidad “in vivo” Inconvenientes - Precios altos

Métodos de transfección Entre los métodos mas habituales para la transfección de si. RNA se encuentran: Transfección mediada por lípidos Parámetros a tener en cuenta: 1. Proporción si. RNA: lípido 2. Concentración total de si. RNA 3. Tipo celular: adherente, no adherente, diferenciado, no diferenciado, linea primaria o transformada.

Electroporación Parámetros a tener en cuenta: -Tamaño, duración y frecuencia del campo eléctrico. - Estatus celular (fase semilogarítmica o casi confluentes). 106 - 107 células. Microinyección No muy usado. Principalmente en C. elegans. Aplicaciones “in vivo” La mayoría de los estudios se han hecho siguiendo los estudios realizados en el pasado con oligonucleótidos antisentido y con ribozimas. Actualmente se trabaja con si. RNA para poner a punto la técnica

Dharmacon es una compañía fundada en 1995 con base en Lafayette, Colorado, E. E. U. U. , es líder mundial en el suministro de oligonucleótidos RNA de alta calidad, de small interfering RNAs (si. RNAs) y de una amplia gama de productos y tecnologías relacionados con interferencia de RNA (RNAi), de importante aplicación e introducción en investigación biotecnológica y farmacéutica. Dharmacon es el líder de una alianza global de instituciones de investigación genómica, denominada RNAi global, cuyo objetivo es unir recursos para acelerar la investigación RNAi como herramienta genómica funcional. http: //www. cultek. com/index. asp? p=soporte-perfil&id_prf=69

si. Array RTF de si. RNA Libraries – Human and Mouse de Dharmacon • Potentes y específicos si. RNAs dirigidos a familias de genes y a pathways completos. • Nuevo formato de transfección en reverso (RTF) que permite analizar cientos de genes en un único experimento. • Rápido, sencillo, fiable, fácil automatización. • Proceso en 4 pasos: Mezclar Reactivo de Transfección Dharma. FECT (DF) y el Medio de Cultivo Dharma. FECT (DCCR) y añadirlo a la placa para rehidratar los si. RNA. • Incubar durante 20 - 90 minutos. • Sembrar las células. • Tras 48 horas realizar un ensayo fenotípico para identificar las dianas. http: //www. cultek. com/index. asp? p=productos-destacados-detalles&id_pdt=56
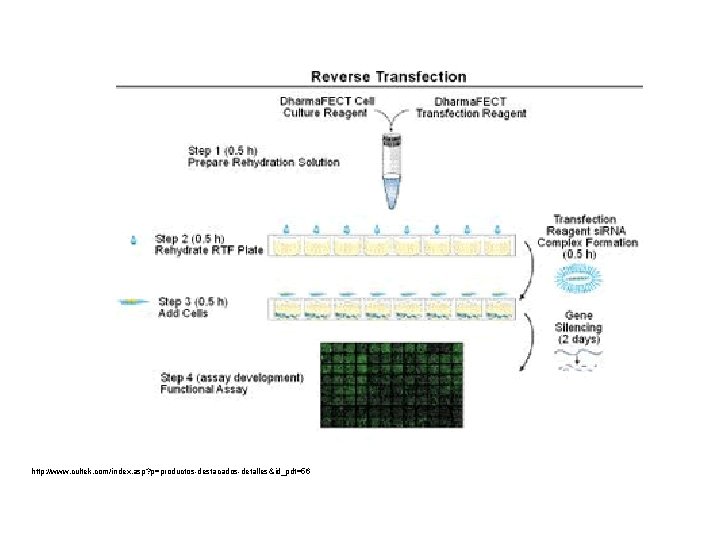
http: //www. cultek. com/index. asp? p=productos-destacados-detalles&id_pdt=56

- Slides: 21