Si O 2 SILIKTY SILOXANY Oxid kemiit Si
























- Slides: 25

Si. O 2, SILIKÁTY, SILOXANY

Oxid křemičitý (Si. O 2) po H 2 O nejstudovanější látka (tvoří 22 fází a tucet polymorfních forem) nejběžnější formou α-křemen výskyt v horninách (žula, pískovec) čistá forma (křišťál) nečistá forma (růženín, kouřový křemen, morion, ametyst, citrín) nedokonalé krystalické formy (chalcedon, chrysopras, karneol, achát, jaspis, heliotrop, pazourek) méně běžné formy (tridymit, cristobalit)

Formy křemene mineralogická exkurze křišťál růženín ametyst citrín karneol achát ☻ kouřový křemen chalcedon jaspis heliotrop morion chrysopras pazourek

Oxid křemičitý (Si. O 2) krystalické modifikace složené z nekonečných seskupení tetraedrů Si. O 4 (sdílejí společný vrchol) strukturní změny: β-křemen ↔ β-tridymit ↔ β-cristobalit ↔ Si. O 2 (l) ↨ ↨ ↨ α-křemen α-tridymit α-cristobalit coesit – zahříváním Na 2 Si. O 3 a (NH 4)2 HPO 4

Oxid křemičitý (Si. O 2) modifikace Si. O 2 (největší hustota, k. č. 6) v rutilové struktuře vláknitý křemen w-Si. O 2 (nízká ρ) Si. O 2 + Si → 2 Si. O → w-Si. O 2 + Si vlhkostí se rozpadá na amorfní Si. O 2 Obecně křemen: odolný vůči působení kyselin kromě HF rozpouští se v MOH nebo M 2 CO 3 za vzniku M 2 Si. O 3

Oxid křemičitý (Si. O 2) z halogenů napadá pouze F 2, reaguje i s H 2 a C s oxidy kovů a polokovů – význam ve sklářské technologii = křemenné sklo použití: průmysl, elektromechanické přístroje, křemenné skla, silikagel křemičitany: lepidla, pojiva, žáruvzdorné materiály ve zředěných roztocích přítomnost málo rozpustných křemičitých kyselin (H 2 Si 2 O 5, H 2 Si. O 3, H 6 Si 2 O 7, H 4 Si. O 4, H 10 Si 2 O 9)

Oxid křemičitý (Si. O 2) - silikagel amorfní forma Si. O 2 – velmi porézní strukturu, vzniká okyselením křemičitanu sodného, vzniklá gelovitá sraženina se dehydratuje pražením vlastnosti mikroporézního materiálu: póry o průměru 2200 -2600 pm, chemicky inertní použití: sušidlo, selektivné sorbent, chromatografie,

Silikátové minerály horniny + produkty rozkladu, zeminy, jíly, písky proměnlivé složení = různé strukturní typy (u všech strukturní typ tetraedru Si. O 4, různé prostorové uspořádání) možnost tvořit lineární a násobné řetězce, cykly, vrstevnaté trojrozměrné struktury

Silikátové minerály dělení do 6 skupin: 1. neso-křemičitany (izolované Si. O 4) 2. soro-křemičitany (izolované Si. O 4) 3. cyklo-křemičitany (uzavřené cyklické str. ) 4. ino-křemičitany (souvislé řetězce) 5. phyllo-křemičitany (souvislé vrstvy) 6. tekto-křemičitany (souvislé 3 D struktury)

neso-křemičitany s izolovanými jednokami {Si. O 4} orthokřemičitany M 2 IISi. O 4 (Na, K, Mg, Mn, Fe, Zn, Zr), možnost izomorfní substituce (Mg, Fe, Mn)2 IISi. O 4 olivín) granáty M 3 IIM 2 III(Si. O 4)3 (MII: Ca, Mg, Fe k. č. 8; MIII: Al, Cr, Fe k. č. 6) součástí portlandského cementu granát

soro-křemičitany s izolovanými jednokami Si 2 O 7 poměrně vzácné např: thortveitit Sc 2 Si 2 O 7, Ln 2 Si 2 O 7, Zn: hemimorfit trojnásobné tetraedrické jednotky – vzácné (aminoffit, kinoit) thortveitit hemimorfit

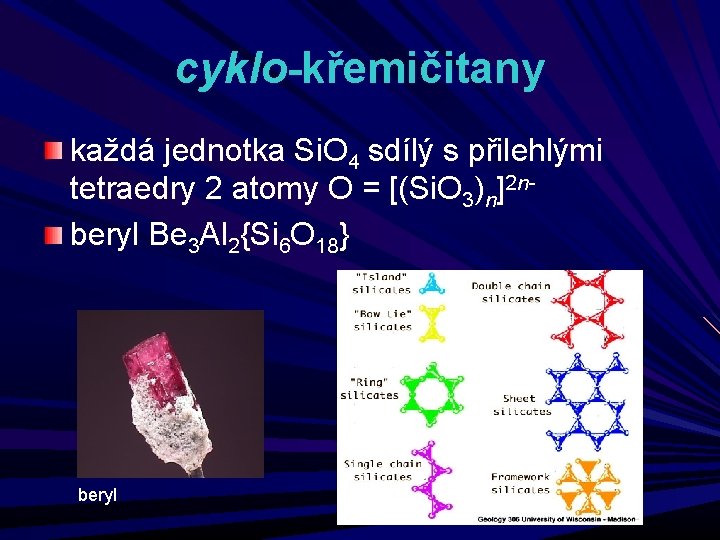
cyklo-křemičitany každá jednotka Si. O 4 sdílý s přilehlými tetraedry 2 atomy O = [(Si. O 3)n]2 nberyl Be 3 Al 2{Si 6 O 18} beryl

ino-křemičitany řetězovité–sdílení vrcholů tetraedru {Si. O 4} pestré, hojné a důležité minerály pyroxenové: enstatit (Mg 2 Si 2 O 6), diopsid (Ca. Mg. Si 2 O 6), jadeit (Na. Al. Si 2 O 6), spodumen (Li. Al. Si 2 O 6) pásové–příčné spojení {Si. O 32 -} tremolit (Ca 2 Mg 5(Si 4 O 11)2(OH)2)

ino-křemičitany mineralogická exkurze enstatit ☻ diopsid spodumen jadeit tremolit

Azbest vláknité křemičité materiály (řec. asbestos – nezhasitelný) součástí více než 3000 výrobků (filtry, izolace, ohnivzdorné oděvy) vysoká pevnost, ohebnost, odolnost vůči teplu a plameni, kyselinám a zásadám bílý azbest (chrysotil) Mg 3(Si 2 O 5)(OH)4, serpentiny, amfiboly azbestosa-dlouhodobý styk s prachem azbestových vláken ve vzduchu

phyllo-křemičitany vodorovné zesíťováné řetězce {Si 2 O 64 -} nebo kondenzované jednotky {Si 6 O 1812 -} v rovině nejznámější a nejdůležitější minerály (jíly, slídy, mastek) M 2 Si 2 O 5, M = Li, Na, Ag, H slída-biotit mastek

jíly, slídy jíly: podstatná složka půdy slída vznikají zvětráváním vyvřelých hornin např. kaolinitu 2 KAl. Si 3 O 8 + CO 2 + H 2 O → Al 2(OH)4 Si 2 O 5 + 4 Si. O 2 + K 2 CO 3 směs s vodou – tvarovatelný měkký materiál slídy: vznikají pozdní krystalizací vyvřelých hornin, vznikají když ¼ Si. IV nahrazena Al. III a záporný náboj vyrovnán K+ (K+ pevnější a tvrdší než mastek biotit (tmavá slída), margarit

tekto-křemičitany sestaveny z jednotek Si. O 4, v nichž každý atom O je sdílen vždy dvěma tetraedry, polovina atomu Si je nahrazena Al hlinitokřemičitany, živce, zeolity, ultramariny

tekto-křemičitany-zeolity: mají mnohem otevřenější kostru než živce, zachycují volně vázanou vodu nebo jiné molekuly (řec. zein – vařit, lithos – kámen) vhodně definované kanálky, systém propojených dutin výroba: krystalizace vodných gelů smíšených alkalických křemičitanů a hlinitanů použití: plnidlo detergentů

tekto-křemičitany-zeolity faujasit Na. Ca 0, 5(Al 2 Si 5 O 14)· 10 H 2 O chabazit Ca(Al 2 Si 4)O 12· 6 H 2 O faujasit chabazit

Siloxany (silikony) silikony a minerální křemičitany – mezi nimi je vztah (methylenová skupina v silikonech je nahrazena izoelek. skupinou O– v křemičitanech) silikony - polymery [R 2 Si. O]n, kde R je organický substituent. vlastnosti: dobrá tepelná a oxidační stálost, odolnost vůči změnám teplot, hydrofobní, dielektrické vlastnosti, fyziologická inertnost připraveny jako oleje, mazadla, emulze, elastomery (kaučuky) a pryskyřice

Siloxany (silikony) silikonové oleje – třepáním O(Si. Me 3)2 a cyklo(Me 2 Si. O)4 s malým množstvím konc. H 2 SO 4 ≡Si-O-Si≡ + H 2 SO 4 → ≡Si-O-Si. O 3 H + ≡Si-OH + ≡Si-O-Si. O 3 H → ≡Si-O-Si≡ + H 2 SO 4 použití: dielektrická izolační média, hydraulické oleje, náplň do kapalinových tlumičů, mazadla, kosmetické přípravky (rtěnky, krémy na opalování, atd. ), nejsou jedovaté (odpěňovadla do stolních olejů)

Siloxany (silikony) silikonové elastiomery (kaučuky) – zpevněné lineární dimethylpolysiloxany výroba: polymerace katalizovaná KOH, H 2 SO 4 : zesíťování kaučuku pomocí oxidačních činidel (benzoylperoxidem) použití: izolační pouzdra, kyslíkové masky, zdravotnické hadice, kosmické skafandry, implantáty

Siloxany (silikony) silikonové pryskyřice – připravují se hydrolýzou fenylsubstituovaných dichlor- a trichlorsilanů v toluenu, promytí H 2 O a následná polymerizace a kondenzace silanových skupin použití: izolace, lamináty, elektronika, kuchyňské nádobí, hydrofóbní (chirurgické implantáty)

DĚKUJI ZA POZORNOST POZ