Shrnut z minula BornOppenheimerova aproximace Co udl BO

Shrnutí z minula

Born-Oppenheimerova aproximace • Co udělá BO s Hamiltoniánem? • Co je jednoelektronová a víceelektronová část? • Co je separace proměnných? Který člen neumožňuje separaci proměnných?

Atom vodíku • • Jak vypadá symbolicky Hamiltonián? V jakých souřadnicích se problém řeší? Z jakých částí se skládá vlnová funkce? Kvantová čísla? radiální (n, l) úhlová (l, m) – n. . . hlavní – l. . . vedlejší, l = 0. . . n-1 (s, p, d, f) – m. . . magnetické, m = -l, . . . , 0, . . . , l (px, py, pz)

http: //winter. group. shef. ac. uk/orbitron/

Nový materiál

Centrální dogma výpočetní chemie

Spin • nemožnost vysvětlit výsledky některých experimentů pomocí pouhých tří kvantových čísel vedla k tomu, že v 1925 Wolfgang Pauli postuloval, že elektron existuje ve dvou možných stavech charakterizovaných spinovým kvantovým číslem ms = ± 1/2 • původní představa – moment kuličky rotující kolem vlastní osy (tato představa je odůvodněná – leč problematická, spin se ale opravdu chová jako úhlový moment) http: //commons. wikimedia. org/w/index. php? title=File%3 AQuantum_spin_and_the_Stern-Gerlach_experiment. ogv

• v kvantové mechanice je úhlový moment kvantován, jeho velikost nabývá hodnot S = ħ [s(s+1)]1/2, s je spinové kvantové číslo, pro elektron s = 1/2 • spin je skutečná experimentálně měřitelná veličina, tudíž jí přísluší operátor + jeho vlastní funkce – α, β • sekundární spinové kvantové číslo ms = ± s • v rovnicích se spin projevuje jakoby elektron měl další souřadnici (up, down)

Pauliho vylučovací princip • stejný orbital může být obsazen maximálně dvěma elektrony • jsou-li v orbitálu dva elektrony, pak se musí lišit spinovým kvantovým číslem • ergo, v systému nemohou existovat dva elektrony se stejnými všemi čtyřmi kvantovými čísly

Molekulové orbitaly • atomy: jednoelektronová vlnová funkce – atomový orbital AO • molekuly: jednoelektronová vlnová funkce - molekulový orbital MO • jak zkonstruovat MO? • MO je lineární kombinací AO MO LCAO



LUMO virtuální orbitály HOMO obsazené orbitály O 2 O

Spin • spin je fyzikální veličina a tudíž jí přísluší operátor • tomuto operátoru pak přísluší spinové vlastní funkce označované a • zahrneme spinovou funkci do prostorové jednoelektronové vlnové funkce spinorbital prostorová část spinová část

• Víceelektronová vlnová funkce – zkonstruuji Hamiltonián pro víceelektronový systém, strčím ho do Schrodingerovy rovnice • pro připomenutí, problémem v Hamiltoniánu je dvouelektronový repulzní člen
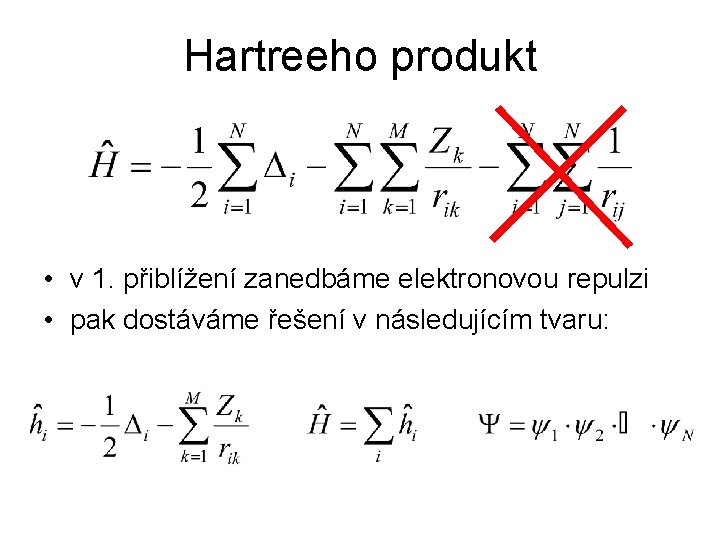
Hartreeho produkt • v 1. přiblížení zanedbáme elektronovou repulzi • pak dostáváme řešení v následujícím tvaru:

• S Hartreeho produktem je ovšem spjat koncepční problém – porušuje nerozlišitelnost elektronů. • Co to je? – elektrony nemohou být označeny - jsou nerozlišitelné

• př: He – 2 elektrony, oba dva v 1 s orbitalu – Hartreeho produkt nám dává výslednou vlnovou funkci jako produkt dvou jednoelektronových vlnových funkcí – tento tvar vlnové funkce ovšem porušuje podmínku nerozlišitelnosti, neboť musím přiřadit jeden elektron do 1 sα a druhý elektron do 1 sβ. A to je možno udělat dvěma způsoby. – Chci-li zavést nerozlišetolnst, pak musím φ(1, 2) a φ(2, 1) zkombinovat

• obě dvě vlnové funkce jsou akceptovatelné, ale experimentálně pouze fce ψ2 je vlnovou fcí He • ψ2 je antisymetrická vůči záměně dvou elektronů, tzn. mění při záměně znaménko

Slaterův determinant • víceelektronová vlnová fce musí být antisymetrická vůči záměně elektronů • máme sadu N spinorbitalů, jak zkonstruujeme antisymetrickou Nelektronovou funkci? • 1930, Slater použil determinanty spinorbitaly elektrony
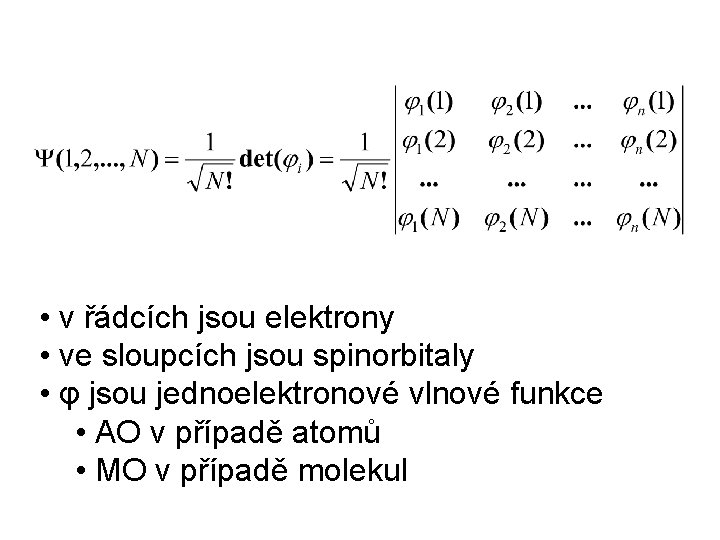
• v řádcích jsou elektrony • ve sloupcích jsou spinorbitaly • φ jsou jednoelektronové vlnové funkce • AO v případě atomů • MO v případě molekul

AO → MO → SD Kvantově chemický výpočet: 1) zvolíme vhodné atomové orbitály (tzv. bázi atomových orbitalů, basis set) 2) pak vypočítáme koeficienty v MO = Σci AO 3) zkonstruujeme výslednou vlnovou funkci z jednoelektronových MO jako Slaterův determinant
- Slides: 22