Setelah menyaksikan tayangan ini Anda dapat 1 Menentukan






























- Slides: 36


Setelah menyaksikan tayangan ini, Anda dapat: 1. Menentukan unsur-unsur golongan utama 2. Menentukan sifat fisis unsur golongan utama 3. Menentukan sifat kimia unsur golongan utama

H Hidrogen Li Litium Na Natrium K Kalium Rb Rubidium Cs Cesium Fr Fransium

Be Berilium Mg Magnesium Ca Calsium Sr Stronsium Ba Barium Ra Radium

B Al Boron Aluminium Ga Galium In Indium Tl Talium

C Carbon Si Silikon Ge Germanium Sn Stanum Pb Plumbum

N Nitrogen P Phospor As Arsen Sb Stibium Bi Bismut

O Oksigen S Sulfur Se Selenium Te Telurium Po Polonium

F Fluorin Cl Clorin Br Bromin I Iodin At Astatin

He Ne Helium Neon Ar Argon Kr Kripton Xe Xenon Rn Radon

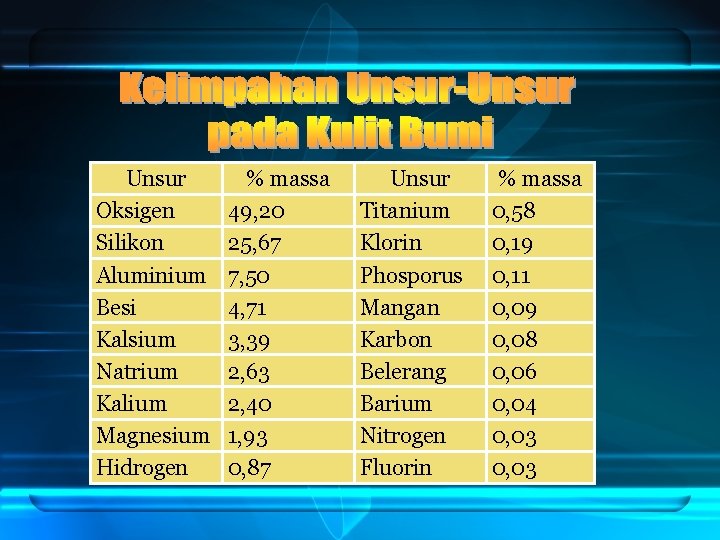
Unsur Oksigen Silikon Aluminium Besi Kalsium Natrium Kalium Magnesium Hidrogen % massa 49, 20 25, 67 7, 50 4, 71 3, 39 2, 63 2, 40 1, 93 0, 87 Unsur Titanium Klorin Phosporus Mangan Karbon Belerang Barium Nitrogen Fluorin % massa 0, 58 0, 19 0, 11 0, 09 0, 08 0, 06 0, 04 0, 03

Unsur Mineral Li spodumen lepidolit Na Air laut mirabilit Salpeter K Syilvit Sylvinite karnalit Produk Pelumas mesin Bhn pesawat terbang Na. OH, Na 2 SO 4 untuk pembuatan kertas, sabun, dan gelas. Pupuk, sabun, bahan peledak, alat pernafasan menyelam

Unsur Mineral Produk Be Beril Aliase dengan Cu Mg Dolomit Badan pesawat (aliase Mg magnesit dengan Al), mesin sepeda motor, obat maag Ca Gibs, Gips untuk pembalut fluorit (Ca. SO 4. 2 H 2 O) Sr salestit Bhn kembang api warna merah Ba barit Bhn kembang api warna hijau

Unsur Mineral Al Bauksit Si Mika Sn Kasiterit N P Produk Badan pesawat terbang Bahan semikonduktor Bahan kaleng dan minuman CO(NH 2)2 Pupuk tanaman fluoropatit Pupuk phosfat ((NH 4)3 PO 4)

Unsur F Cl Br I Mineral Ca. F 2 Produk Pendingin (Freon (CF 2 Cl 2)), Air laut Pemutih dan (Na. Cl) desinfektan (Ca. OCl 2) KBr, Pelat fotografi dan film Mg. Br 2 (Ag. Br) KI Desinfektan dan antiseptik.

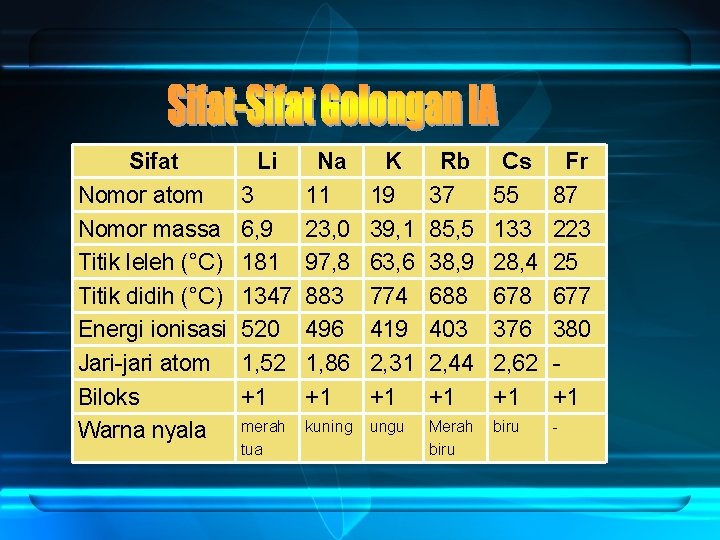
Sifat Nomor atom Nomor massa Titik leleh (°C) Titik didih (°C) Energi ionisasi Jari-jari atom Biloks Warna nyala Li Na 3 11 6, 9 23, 0 181 97, 8 1347 883 520 496 1, 52 1, 86 +1 +1 K 19 39, 1 63, 6 774 419 2, 31 +1 Rb 37 85, 5 38, 9 688 403 2, 44 +1 Cs 55 133 28, 4 678 376 2, 62 +1 Fr 87 223 25 677 380 +1 merah tua ungu Merah biru - kuning

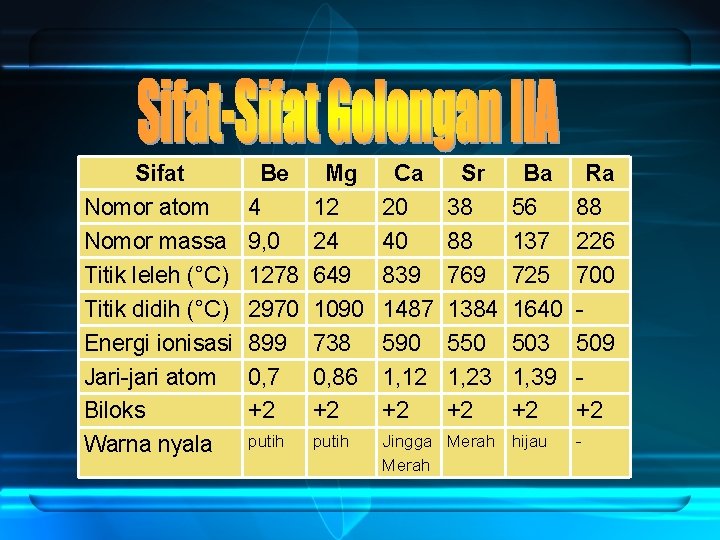
Sifat Nomor atom Nomor massa Titik leleh (°C) Titik didih (°C) Energi ionisasi Jari-jari atom Biloks Warna nyala Be 4 9, 0 1278 2970 899 0, 7 +2 Mg 12 24 649 1090 738 0, 86 +2 Ca 20 40 839 1487 590 1, 12 +2 Sr 38 88 769 1384 550 1, 23 +2 Ba 56 137 725 1640 503 1, 39 +2 putih Jingga Merah hijau Merah Ra 88 226 700 509 +2 -

KEREAKTIFAN UNSUR GOLONGAN IA DAN IIA Semakin besar jari-jari atom, kekuatan ikatan akan semakin lemah sehingga energi ionisasinya semakin kecil dan semakin mudah melepaskan elektron. Urutan kereaktifan unsur: IA : Li < Na < K < Rb < Cs < Fr IIA : Be < Mg < Ca < Sr < Ba < Ra


Air sadah: Air sadah air yang mengandung garam-garam Mg 2+ dan Ca 2+. Air sadah dibedakan atas: 1. Kesadahan sementara 2. Kesadahan tetap

1. Kesadahan Sementara Air yang mengandung garam Ca(HCO 3)2 dan Mg(HCO 3)2 dapat dihilangkan dengan cara dipanaskan. Reaksinya: Ca(HCO 3)2 (aq) → Ca. CO 3(s) + H 2 O(l) + CO 2(g)

2. Kesadahan Tetap Air yang mengandung garam Ca. Cl 2, Mg. Cl 2, Ca(NO 3)2, Mg(NO 3)2, atau garam lainnya yang tidak larut dengan pemanasan dapat dihilangkan dengan mereaksikannya dengan Na 2 CO 3. Reaksinya: Ca. Cl 2(aq) + Na 2 CO 3(aq)→ Ca. CO 3(s) + 2 Na. Cl(aq)

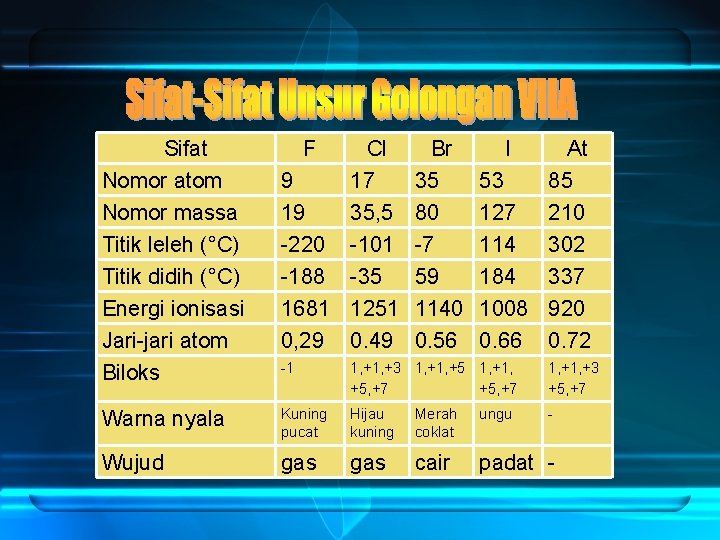
Sifat Nomor atom Nomor massa Titik leleh (°C) Titik didih (°C) Energi ionisasi Jari-jari atom Biloks F Cl 9 17 19 35, 5 -220 -101 -188 -35 1681 1251 0, 29 0. 49 Br 35 80 -7 59 1140 0. 56 I At 53 85 127 210 114 302 184 337 1008 920 0. 66 0. 72 -1 1, +3 1, +1, +5, +7 1, +3 +5, +7 Warna nyala Kuning pucat Hijau kuning Merah coklat ungu - Wujud gas cair padat -

SIFAT OKSIDATOR DAN REDUKTOR GOLONGAN VIIA • Daya pengoksidasi/oksidator unsur -unsur golongan VIIA: F 2 > Cl 2 > Br 2 > I 2 • Daya pereduksi/reduktor halida: HI > HBr > HCl > HF

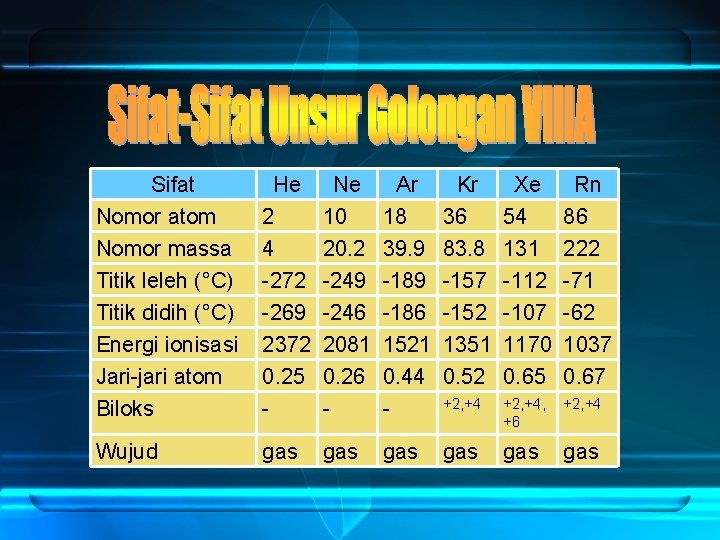
Sifat Nomor atom Nomor massa Titik leleh (°C) Titik didih (°C) Energi ionisasi Jari-jari atom Biloks He 2 4 -272 -269 2372 0. 25 - Ne 10 20. 2 -249 -246 2081 0. 26 - Ar 18 39. 9 -186 1521 0. 44 - Kr 36 83. 8 -157 -152 1351 0. 52 Xe 54 131 -112 -107 1170 0. 65 Rn 86 222 -71 -62 1037 0. 67 +2, +4, +6 +2, +4 Wujud gas gas gas

Unsur Manfaat Li Pelumas mesin (C 17 H 35 COOLi) Na Na. OH & Na 2 SO 4 untuk pembuatan kertas K Be Mg Ca Pupuk tanaman (KCl), Aliase dengan Cu Badan pesawat (aliase Mg dengan Al) Gips untuk pembalut (Ca. SO 4. 2 H 2 O) Sr Ba Al Bahan kembang api warna merah. Bahan kembang api warna hijau Badan pesawat terbang, kapal, mobil

Unsur Manfaat Si Bahan semikonduktor Sn Bahan kaleng dan minuman N Pupuk tanaman (CO(NH 2)2) P F Cl Br I Pupuk phosfat ((NH 4)3 PO 4) Pendingin (Freon (CF 2 Cl 2)), Pemutih dan desinfektan (Ca. OCl 2), Pelat fotografi dan film (Ag. Br), Desinfektan dan antiseptik.

Unsur He Ne Ar Kr Xe Manfaat Pengisi balon udara, tabung pernafasan penyelam Pengisi lampu reklame Pengelasan stainless steel, pengisi bola lampu pijar Lampu kilat (blitz) kamera, lampu menara mercusuar Lampu pembunuh bakteri

1. 2. 3. 4. 5. 6. Alkali Tanah Aluminium Asam Sulfat Halogen Gas Mulia

1. Pembuatan Unsur Alkali Diperoleh dengan cara elektrolisis lelehan garam halidanya dengan elektroda inert. Secara umum dapat dituliskan sebagai berikut: (M = logam alkali) • Anoda : 2 Cl−(l) → Cl 2(g) + 2 e • Katoda : 2 M+(l) + 2 e → 2 M(s) 2 M+(l) + 2 Cl−(l) → 2 M(s) + Cl 2(g)

2. Unsur Alkali Tanah Diperoleh dengan cara elektrolisis lelehan garam halidanya dengan elektroda inert. Secara umum dapat dituliskan sebagai berikut: (M = logam alkali tanah) • Anoda : 2 Cl−(l) → Cl 2(g) + 2 e • Katoda : M 2+(l) + 2 e → M(s) M 2+(l) + 2 Cl−(l) → M(s) + Cl 2(g)

3. Alumunium Diperoleh dengan proses Hall-Heroult. Al 2 O 3 yang berasal dari bauksit dilelehkan dengan kriolit (Na 3 Al. F 6) kemudian dielektrolisis dengan elektroda grafit. Reaksi yang terjadi: Al 2 O 3 ↔ 2 Al 3+ + 3 O 2− • Katoda : Al 3+ + 3 e → Al × 4 • Anoda : 2 O 2− → O 2 + 4 e × 3 4 Al 3+ + 6 O 2− → 4 Al + 3 O 2

4. Asam Sulfat (H 2 SO 4) Pembuatan asam sulfat dengan proses kontak: 2 SO 2 + O 2 ↔ 2 SO 3 (+ katalis V 2 O 5) SO 3 + H 2 O → H 2 SO 4

5. Unsur Halogen Dapat diperoleh dengan cara elektrolisis lelehan garam halidanya dengan elektroda inert. Secara umum dapat dituliskan sebagai berikut: (X = unsur halogen) • Anoda : 2 X−(l) → X 2(g) + 2 e • Katoda : 2 Na+(l) + 2 e → 2 Na(s) 2 Na+(l) + 2 Xl−(l) → 2 Na(s) + X 2(g)

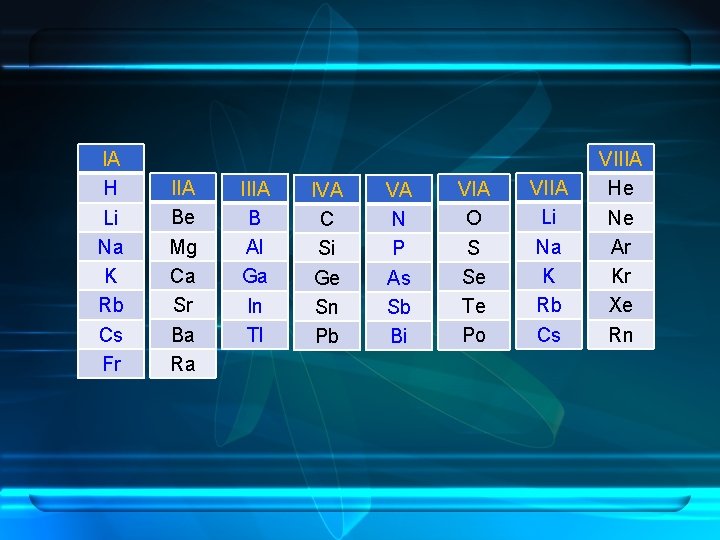
SOAL 1. Tuliskan unsur-unsur golongan utama! H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Ga Ge As Se Br Kr Rb Sr In Sn Sb Te I Xe Cs Ba Tl Pb Bi Po At Rn Fr Ra

IA H Li Na K Rb Cs Fr IIA Be Mg Ca Sr Ba Ra IIIA B Al Ga In Tl IVA C Si Ge Sn Pb VA N P As Sb Bi VIA O S Se Te Po VIIA Li Na K Rb Cs VIIIA He Ne Ar Kr Xe Rn