Senyawasenyawa Alkena PERTEMUAN 6 Harizal S Pd M












































































- Slides: 112

Senyawa-senyawa Alkena PERTEMUAN 6 Harizal, S. Pd. , M. Sc Program Studi Farmasi Universitas Esa Unggul 1

KEMAMPUAN AKHIR YANG DIHARAPKAN 2

Pendahuluan • Alkena merupakan hidrokarbon yang memiliki ikatan rangkap dua. • Alkena juga disebut olefin yang berarti “gas pembentuk minyak” • Gugus fungsi alkena merupakan ikatan karbon rangkap dua yang relatif lebih reaktif. 3

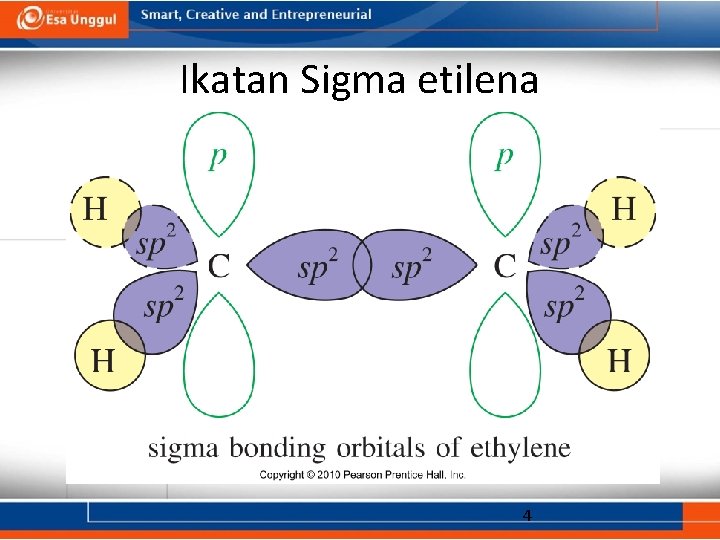
Ikatan Sigma etilena 4

Deskripsi orbital • Ikatan sigma pada ikatan rangkap dua berasal dari orbital atom karbon yang terhibridisasi sp 2. • Sudut ikatan lebih kurang sebesar 120º dan geometri molekulnya segitiga planar. • Orbital p yang tidak terhibridisasi yang memiliki satu elektron akan bertumpang tindih membentuk ikatan rangkap dua (ikatan pia). 5

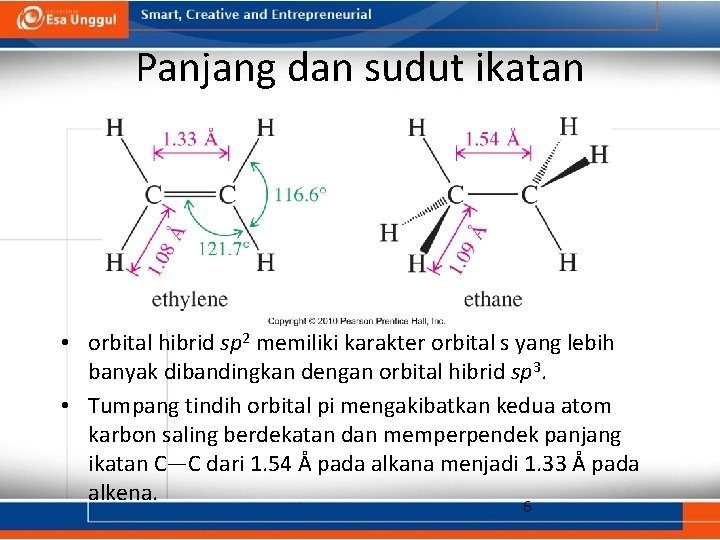
Panjang dan sudut ikatan • orbital hibrid sp 2 memiliki karakter orbital s yang lebih banyak dibandingkan dengan orbital hibrid sp 3. • Tumpang tindih orbital pi mengakibatkan kedua atom karbon saling berdekatan dan memperpendek panjang ikatan C—C dari 1. 54 Å pada alkana menjadi 1. 33 Å pada alkena. 6

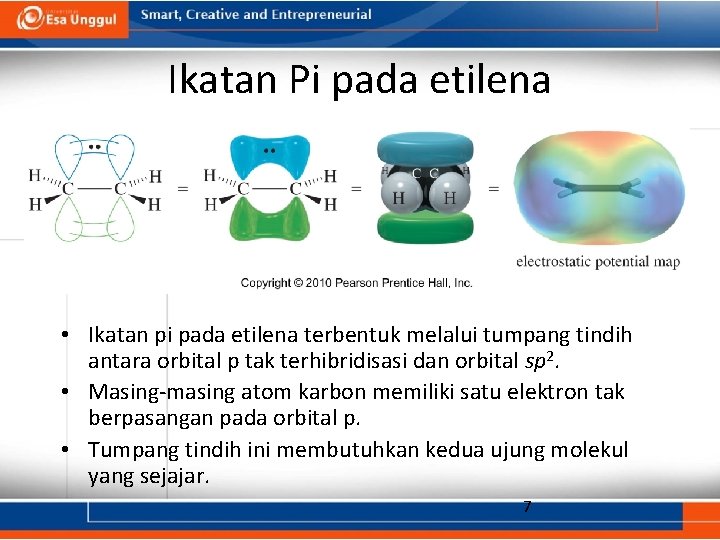
Ikatan Pi pada etilena • Ikatan pi pada etilena terbentuk melalui tumpang tindih antara orbital p tak terhibridisasi dan orbital sp 2. • Masing-masing atom karbon memiliki satu elektron tak berpasangan pada orbital p. • Tumpang tindih ini membutuhkan kedua ujung molekul yang sejajar. 7

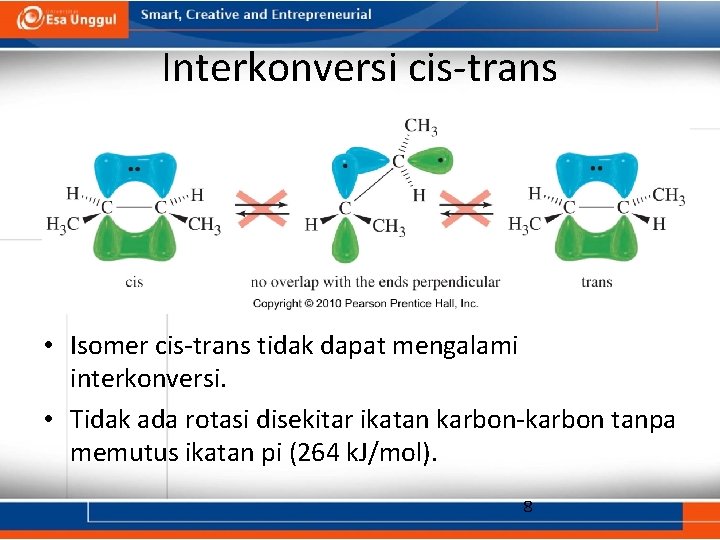
Interkonversi cis-trans • Isomer cis-trans tidak dapat mengalami interkonversi. • Tidak ada rotasi disekitar ikatan karbon-karbon tanpa memutus ikatan pi (264 k. J/mol). 8

Tatanama IUPAC • Tentukan rantai atom karbon terpanajang yang memiliki ikatan karbon rangkap dua. • Akhiran -ana diubah menjadi -ena. • Nomori rantai sedemikian sehingga karbon ikatan rangkap memiliki nomor terendah. • Pada senyawa cincin, ikatan rangkap diasumsikan berada diantara karbon 1 dan karbon 2. 9

Tatanama IUPAC dan IUPAC yang baru 10

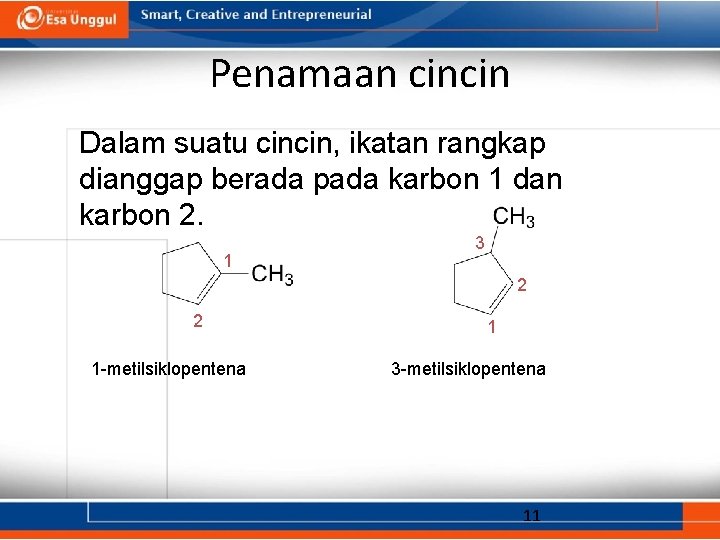
Penamaan cincin Dalam suatu cincin, ikatan rangkap dianggap berada pada karbon 1 dan karbon 2. 1 3 2 2 1 -metilsiklopentena 1 3 -metilsiklopentena 11

Ikatan rangkap ganda • Berikan ikatan rangkap dengan nomor terkecil. • Gunakan awalan di-, tri-, tetra- sebelum akhiran “ena” untuk menunjukkan berapa banyak ikatan rangkap yang ada pada senyawa. 12

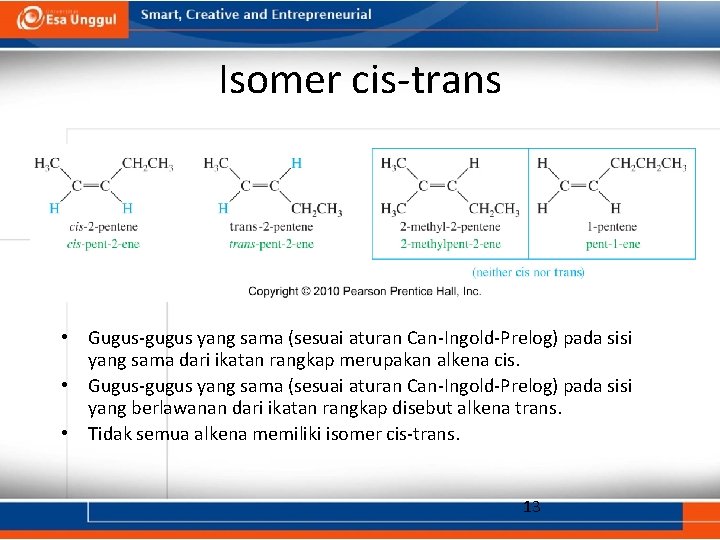
Isomer cis-trans • Gugus-gugus yang sama (sesuai aturan Can-Ingold-Prelog) pada sisi yang sama dari ikatan rangkap merupakan alkena cis. • Gugus-gugus yang sama (sesuai aturan Can-Ingold-Prelog) pada sisi yang berlawanan dari ikatan rangkap disebut alkena trans. • Tidak semua alkena memiliki isomer cis-trans. 13

Senyawa siklik • Trans sikloalkena merupakan senyawa yang kurang stabil sehingga relatif jarang dijumpai, kecuali untuk senyawa siklik dengan jumlah karbon lebih dari 8 atom. • Sikloalkena selalu dianggap memiliki bentuk cis, kecuali sudah ditunjukkan sebelumnya sebagai trans pada nama senyawa. 14

Contoh Soal 1 Manakah yang merupakan alkena yang paling stabil? Penyelesaian Senyawa (a) relatif stabil. Meskipun ikatan rangkapnya berada pada salah satu atom karbon jembatan, namun, ikatan ini tidak berada diantara dua cincin. Ikatan rangkap trans berada pada sistem cincin beranggotakan 10 atom. . Senyawa (b) melanggar aturan Bredt sehingga kurang stabili. Ikatan rangkap trans berada pada cincin beranggotakan 6 atom. senyawa (c) (norbornene) merupakan senyawa stabil. Ikatan rangkap cis tidak berada pada karbon jembatan. Senyawa (d) juga merupakan senyawa stabil. Meskipun ikatan rangkap berada pada karbon jembatan dari sistem bisiklik, terdapat sistem cincin beranggotakan 8 atom yang mengakomodasi ikatan rangkap trans 15

Tatanama E-Z • Gunakan aturan Cahn–Ingold–Prelog untuk menandai prioritas gugus yang berikatan langsung dengan tiap atom karbon pada ikatan rangkap. • Jika dua gugus dengan prioritas tertinggi berada pada sisi yang sama, maka senyawa tersebut dinamai Z (untuk zusammen). • Jika dua gugus dengan prioritas tertinggi berada pada sisi yang berseberangan, maka senyawa tersebut dinamai E (untuk entgegen). 16

Contoh 1 2 E-1 -bromo-1 -kloropropena • Tandai prioritas dari substituen berdasarkan nomor atom masing-masing (gugus 1 memeiliki prioritas tertinggi) • Jika gugus dengan priorits tertinggi berada pada sisi yang berseberangan, maka isomer itu memiliki nama E. • Jika gugus dengan prioritas tertinggi berada pada sisi yang sama, maka isomer tersebut memiliki nama Z. 17

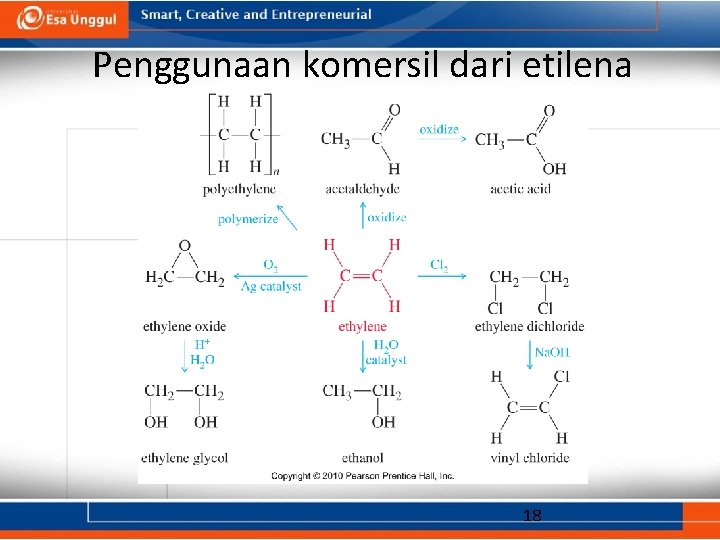
Penggunaan komersil dari etilena 18

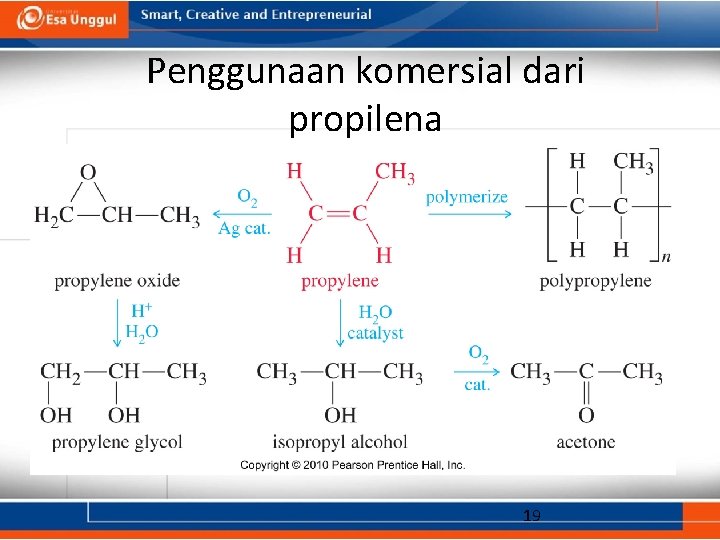
Penggunaan komersial dari propilena => 19

Polimer adisi 20

Energi hidrogenasi • Pembakaran suatu alkena dan hidrogenasi alkena dapat memberikan data yang berharga untuk mengetahui stabilitas ikatan rangkap. • Semakin banyak substituen yang terikat pada ikatan rangkap, semakin rendah energi hidrogenasinya. 21

Stabilitas Relatif 22

Efek substituen • Diantara sesama isomer konstitusional, semakin banyak substituen pada ikatan rangkap, semakin stabil isomer tersebut. • Semakin lebar jarak antar gugus yang terikat, semakin kecil efek sterik yang dihasilkan sehingga semakin meningkatkan stabilitas senyawa. 23

Isomer dengan dua substituen • Stabilitas: cis < geminal < trans isomer • Isomer yang kurang stabil memiliki energi hidrogenasi eksotermik yang semakin tinggi. cis-2 -butena iso-butena trans-2 -butena -120 k. J (CH 3)2 C=CH 2 -117 k. J -116 k. J 24

Stabilitas Sikloalkena • • Isomer Cis memiliki stabilitas yang lebih tinggi dibandingkan dengan isomer trans pada molekul sikloalkana kecil. Cincin kecil memiliki tambahan tegangan cincin tambahan. Setidaknya dibutuhkan sistem cincin dengan 8 anggota atom untuk membentuk isomer dengan ikatan rangkap trans yang stabil. Untuk senyawa siklodekena (atau cincin yang lebih besar), ikatan rangkap trans memiliki stabilitas yang sama dengan ikatan rangkap cis. 25

Aturan Bredt • Senyawa bisiklik berjembatan tidak dapat memiliki iktan rangkap pada posisi karbon jembatan kecuali memiliki satidaknya satu sistem cincin dengan 8 anggota atom. 26

Sifat Fisik Alkena • Titik didih rendah, semakin meningkat dengan kenaikan massa molekul. • Alkena bercabang memiliki titik didih yang lebih rendah. • Memiliki kerapatan yang lebih kecil dibandingkan air. • Sedikit polar: – Ikatan Pi mudah terpolarisasi, sehingga interaksi dipol-dipol sesaat dapat terjadi. – Gugus alkil merupakan gugus pendonor elektron terhadap ikatan pi, sehingga dapat terbentuk momen dipol kecil. 27

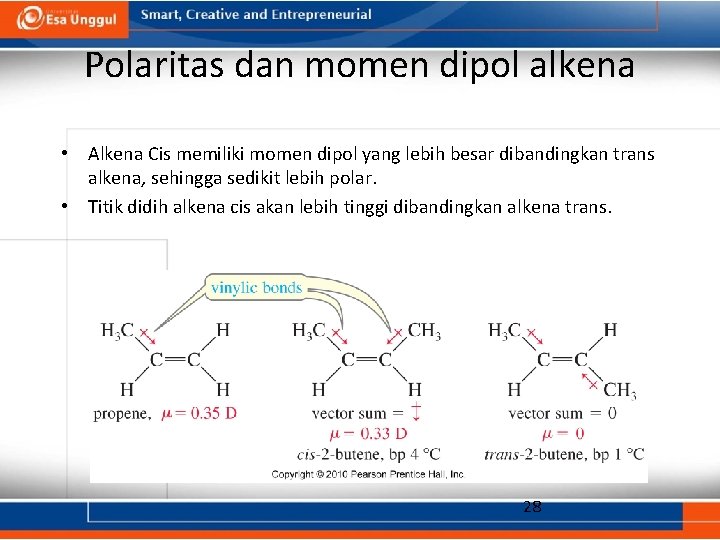
Polaritas dan momen dipol alkena • Alkena Cis memiliki momen dipol yang lebih besar dibandingkan trans alkena, sehingga sedikit lebih polar. • Titik didih alkena cis akan lebih tinggi dibandingkan alkena trans. 28

Rangkuman Sintesis alkena • • Dehidrohalogenasi E 2 (-HX) Dehidrohalogenasi E 1 (-HX) Dehalogenasi dari dibromida vicinal (-X 2) Dehidrasi alkohol (-H 2 O) 29

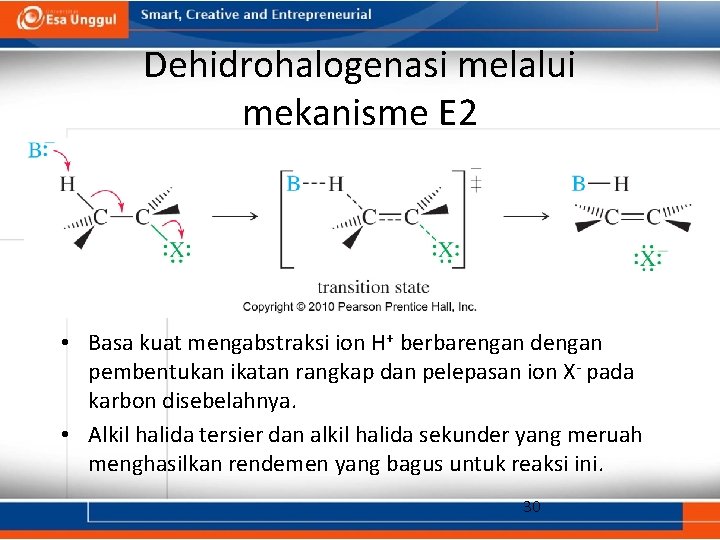
Dehidrohalogenasi melalui mekanisme E 2 • Basa kuat mengabstraksi ion H+ berbarengan dengan pembentukan ikatan rangkap dan pelepasan ion X- pada karbon disebelahnya. • Alkil halida tersier dan alkil halida sekunder yang meruah menghasilkan rendemen yang bagus untuk reaksi ini. 30

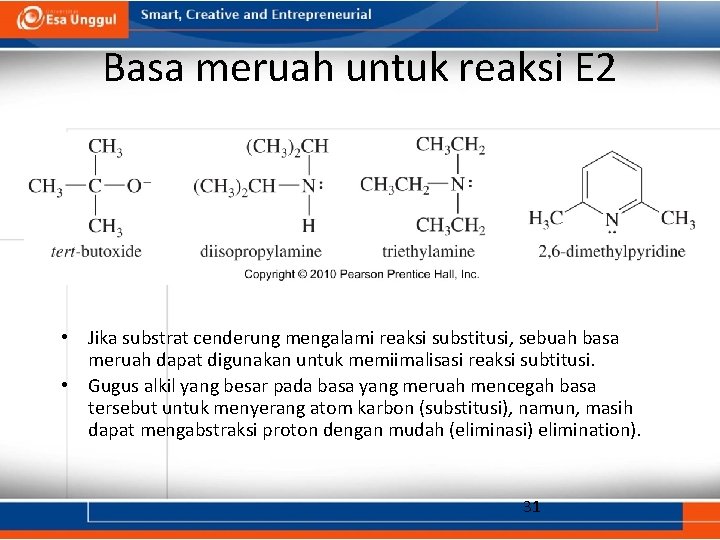
Basa meruah untuk reaksi E 2 • Jika substrat cenderung mengalami reaksi substitusi, sebuah basa meruah dapat digunakan untuk memiimalisasi reaksi subtitusi. • Gugus alkil yang besar pada basa yang meruah mencegah basa tersebut untuk menyerang atom karbon (substitusi), namun, masih dapat mengabstraksi proton dengan mudah (eliminasi) elimination). 31

Produk Hofmann Basa yang gemuk, seperti kalium tert-butoksida, mengabstraksi H+ yang paling terbuka, sehingga menghasilkan alkena yang memiliki subtituen yang lebih sedikit sebagai produk mayor (Produk Hofmann). 32

Stereokimia pada eliminasi E 2 • Tergantung pada stereokimia dari alkil halida, reaksi eliminasi E 2 dapat menghasilkan hanya isomer cis atau isomer trans. • Geometri produk akan bergantung pada hubungan koplanar antara proton dan gugus pergi. 33

Contoh Soal 2 Tunjukkan bahwa reaksi dehalogenasi 2, 3 -dibromobutanea oleh ion iodida merupakan reaksi yang stereospesifik dengan menunjukkan bahwa dua diastereomer pada bahan dasar menghasilkan produk distereomer yang berbeda. Penyelesaian Rotasikan lah senyawa meso-2, 3 -dibromobutana menjadi suatu konformer dimana atom bromin berada posisi anti dan koplanar satu sama lain, makan diperoleh produk berupa trans-2 -butena. Konformasi yang sama dari enansiomer dari (±) diastereomer menunjukkan bahwa produk yang dihasilkan akan berupa cis-2 -butena. 34

Reaksi E 2 pada Sikloheksana • Suatu konformasi anti-koplanar (180°) hanya dapat dicapai ketika baik hidrogen maupun atom halogen berada posisi aksial. • Konformasi kursi akan mengalami interkonversi konformasi untuk mengakomodasi posisi atom Halida dan hidrogen agar reaksi eliminasi bisa terjadi. 35

Contoh Soal 3 Jelaskan mengapa senyawa terdeuterasi berikut 1 -bromo-2 -metilsikloheksana mengalami dehidrohalogenasi melalui mekanisme E 2 menghasilkan satu produk berikut dan buka dua produk lainnya. Penyelesaian Dalam reaksi eliminasi E 2, atom hidrogen dan gugus pergi harus berada posisi trans-aksial satu sama lain. Pada senyawa ini, hanya satu atom hidrogen, deuterium, yang memiliki posisi trans terhadap atom bromin. Ketika atom bromin berada posisi aksila, atom deuterium yang berada di sebelahnya juga berada dalam posisi aksial sehingga dihasilkan posisi trans-diaksial satu sama lain. 36

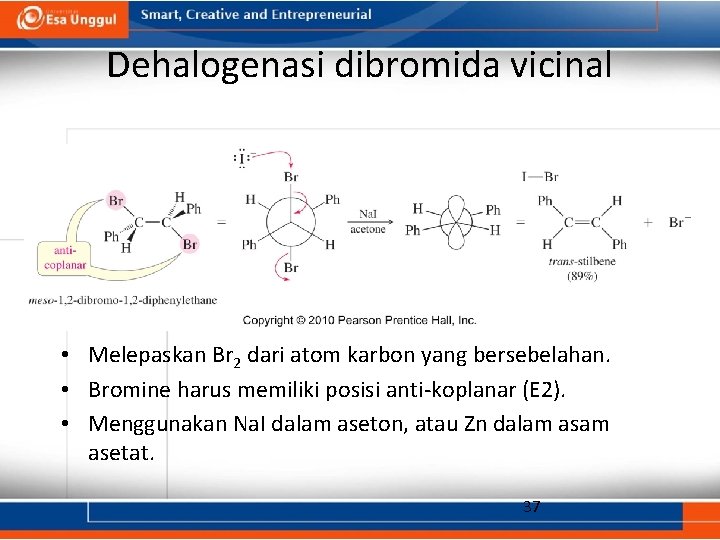
Dehalogenasi dibromida vicinal • Melepaskan Br 2 dari atom karbon yang bersebelahan. • Bromine harus memiliki posisi anti-koplanar (E 2). • Menggunakan Na. I dalam aseton, atau Zn dalam asetat. 37

Mekanisme eliminasi E 1 • Kecenderungan reaksi pada alkil halida tersier dan sekunder sbb: 3º > 2º • Intermediet reaksi berupa karbokation. • Memungkinkan terjadinya penataulangan. • Menggunakan nukleofil lemah seperti air dan alkohol. • Biasanya menghasilkan campuran produk dari reaksi substitusi dan eliminasi. 38

Dehidrasi alkohol • Gunakan asam sulfat atau asam fosfat pekat sebagai katalis, uapkan alkena yang memiliki titik didih yang lebih rendah untuk menggeser kesetimbangan, dan menaikkan rendemen reaksi. • Intermediet karbokation: alkohol 3º bereaksi lebih cepat dibandingkan alkohol 2º. Alkohol primer paling tidak reaktif pada reaksi ini. • Memungkinkan terjadinya penataulangan • Reaksi ini mengikuti aturan Zaitsev. 39

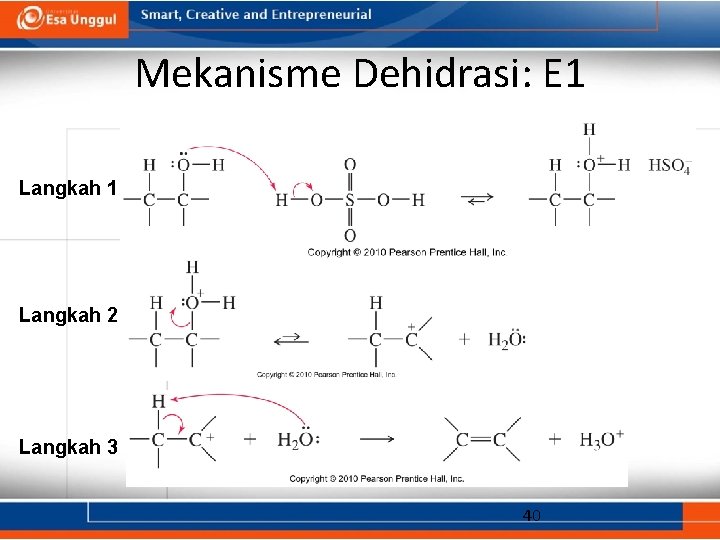
Mekanisme Dehidrasi: E 1 Langkah 2 Langkah 3 40

Contoh Soal 4 Tuliskan mekanisme reaksi untuk reaksi dehidrasi t-butil alkohol terkatalisis asam sulfat. Penyelesaian Tahap pertama merupakan protonasi gugus hidroksil yang mengubah gugus ini menjadi gugus pergi yang bagus. Tahap kedua adalah ionisasi gugus hidroksil terprotonasimenghasilkan karbokation. Abstraksi proton menghasilkan alkena. 41

Perengkahan alkana terkatalisis • Alkana rantai panjang dipanaskan untuk menghasilkan satu alkena dan alkana dengan rantai yang lebih pendek. • Biasanya dihasilkan campuran yang rumit. 42

Reaksi-reaksi Alkena 43

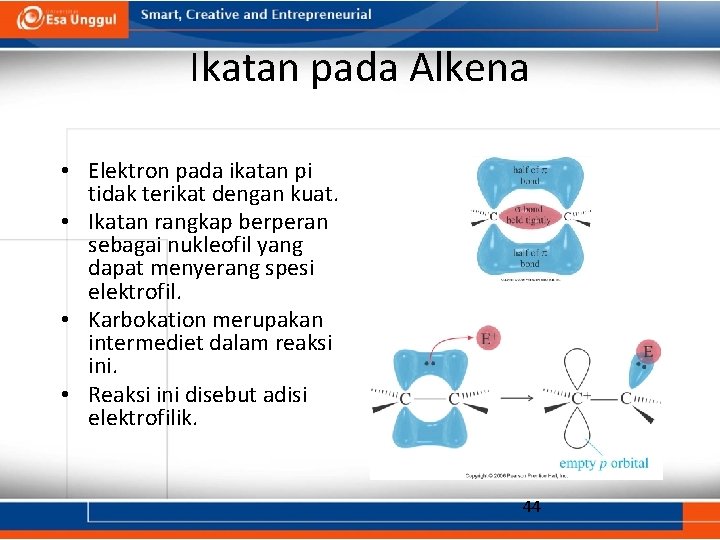
Ikatan pada Alkena • Elektron pada ikatan pi tidak terikat dengan kuat. • Ikatan rangkap berperan sebagai nukleofil yang dapat menyerang spesi elektrofil. • Karbokation merupakan intermediet dalam reaksi ini. • Reaksi ini disebut adisi elektrofilik. 44

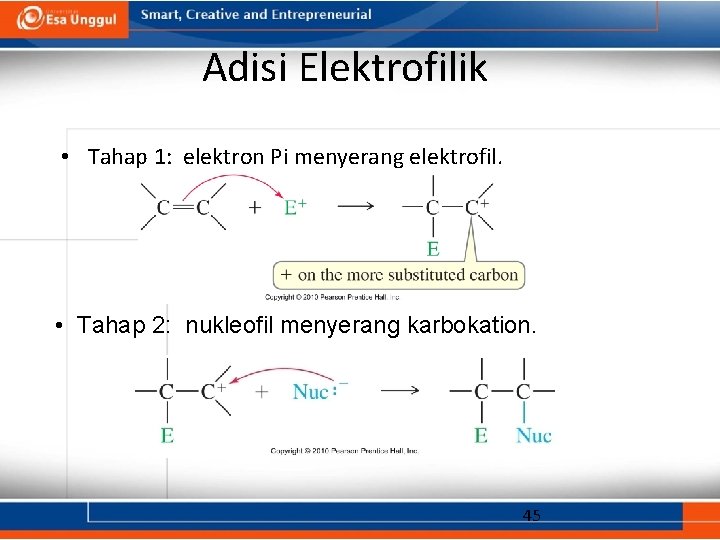
Adisi Elektrofilik • Tahap 1: elektron Pi menyerang elektrofil. • Tahap 2: nukleofil menyerang karbokation. 45

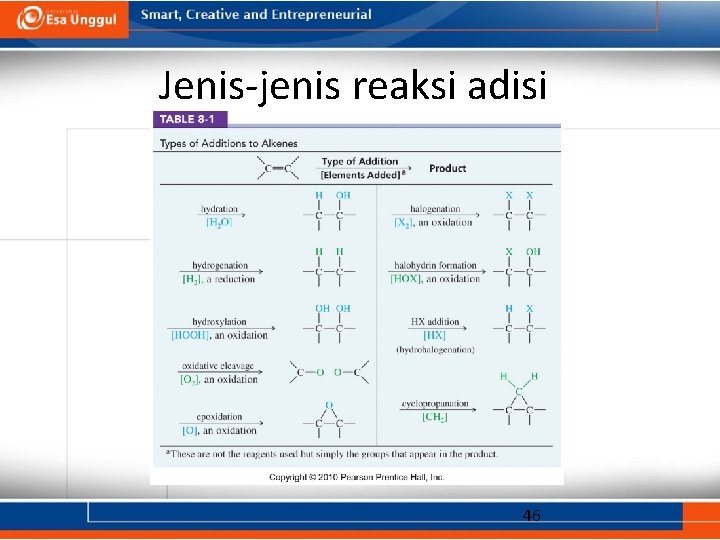
Jenis-jenis reaksi adisi 46

Adisi HX pada alkena • Tahap 1 merupakan protonasi ikatan rangkap. • Tahap protonasi membentuk karbokation yang paling stabil. • Pada tahap 2, nukleofil menyerang karbokation membentuk suatu alkil halida. • HBr, HCl, dan HI dapat digunakan pada reaksi ini. 47

Mekanisme adisi HX Tahap 1: Protonasi ikatan rangkap. Tahap 2: serangan nukleofilik dari halida pada karbokation. 48

Regioselektivitas • Aturan Markovnikov: adisi suatu proton ke suatu ikatan rangkap senyawa alkena menghasilkan suatu produk dengan proton asam berikatan dengan karbon yang memiliki hidrogen terbanyak. • Aturan Markovnikov (tambahan): dalam suatu reaksi adisi elektrofil pada alkena, elektrofil mengadisi sedemikian sehingga dihasilkan intermediet karbokation yang paling stabil. 49

Aturan Markovnikov Proton asam akan berikatan pada karbon tersier untuk menghasilkan intermediet yang paling stabil. 50

Adisi radikal bebas HBr • Dalam keberadaan peroksida, HBr mengadisi alkena membentuk produk “anti-Markovnikov”. • Peroksida menghasilkan radikal bebas. • Hanya HBr yang memiliki energi ikatan yang sesuai. • Ikatan pada HCl terlalu kuat, sehingga biasanya menghasilkan produk sesuai dengan aturan Markovnikov, bahkan dengan keberadaan peroksida. • Ikatan HI cenderung putus secara heterolitik membentuk ion, dan ion-ion ini akan mengadisi alkena sesuai dengan aturan Markovnikov. 51

Inisiasi radikal bebas • Ikatan peroksida pecah secara homolitik membentuk radikalmbebas: • Hidrogen diabstraksi dari HBr. 52

Tahap propagasi • Bromin ditambahkan pada ikatan rangkap membentuk intermediet radikal yang paling stabili: • Hidrogen diabstraksi dari HBr yang kedua: 53

Stereokimia Anti-Markovnikov • Intermediet radikal tersier terbentuk lebih cepat karenan lebih stabil. 54

Hidrasi alkena • Adisi Markovnikov air pada ikatan rangkap akan membentuk alkohol. • Reaksi ini merupakan kebalikan dari dehidrasi alkohol. • Penggunaan larutan H 2 SO 4 atau H 3 PO 4 encer menggeser kesetimbangan ke arah reaksi hidrasi 55

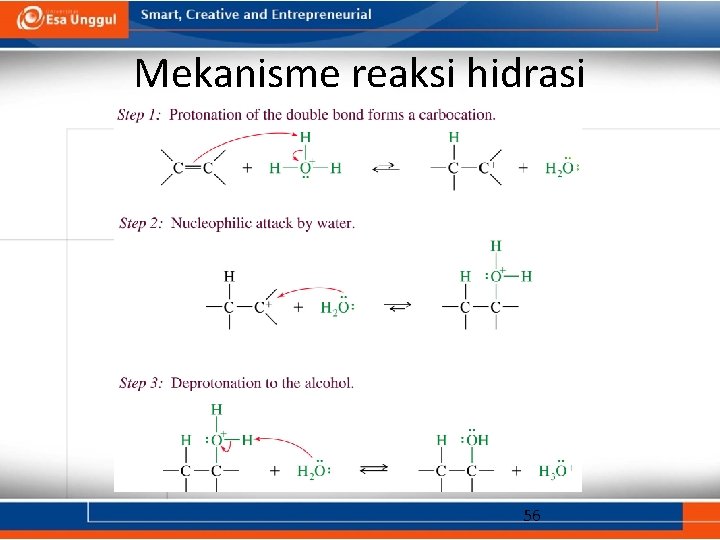
Mekanisme reaksi hidrasi 56

Orientasi reaksi hidrasi Protonasi mengikuti aturan Markovnikov: hidrogen ditambahkan pada karbon yang memiliki substituen yang lebih sedikit untuk membentuk intermediet yang lebih stabil. , 57

Penataanulang: • Penataanulang dapat terjadi setelah pembentukan intermediet karbokation. • Pergeseran metil setelah protonasi akan menghasilkan karbokation tersier yang lebih stabil. 58

Contoh Soal 1 Tunjukkan bagaimana cara melakukan reaksi berikut. (a) Mengubah 1 -metilsikloheksene menjadi 1 -bromo-1 -metilsikloheksana. Penyelesaian Reaksi ini membutuhkan adisi HBr pada alkena sesuai dengan orientasi Markovnikov. Adisi ionik HBr menghasilkan produk yang tepat. 59

Contoh Soal 2 Ubahlah 1 -metilsikloheksanol menjadi 1 -bromo-2 -metilsikloheksana. Penyelesaian Sintesis ini membutuhkan konversi suatu alkohol menjadi alkil, bromida pada karbon yang bersebelahan. Produk anti-Markovnikov dapat terbentuk melalui adisi radikal bebas HBr pada 1 metilsikloheksena. 1 -Metilsikloheksena dapat dengan mudah disintesis melalui dehidrasi 1 -metilsikloheksanol. Alkena yang paling banyak memiliki substituen merupakan produk yang paling cenderung terbentuk, . 60

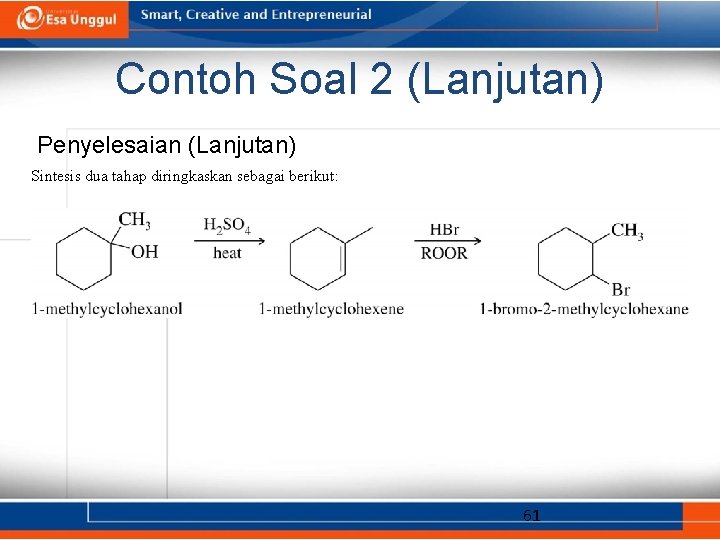
Contoh Soal 2 (Lanjutan) Penyelesaian (Lanjutan) Sintesis dua tahap diringkaskan sebagai berikut: 61

Reaksi Oksimerkurasi–Demerkurasi • Adisi Markovnikov air pada ikatan rangkap. • Tidak terjadi penataanulang. • Reaksi terjadi dalam dua tahap. 62

Reaksi Oksimerkurasi • Reagen yang digunakan adalah mercuri(II) asetat, yang sedikit terdisosiasi menjadi +Hg(OAc). • +Hg(OAc) merupakan elektrofil yang mengadisi ikatan pi. • Intermediet yang terbentuk merupakan spesis cincin tiga atom yang disebut ion merkurinium. • Secara keseluruhan, adisi air mengikuti aturan Markovnikov. 63

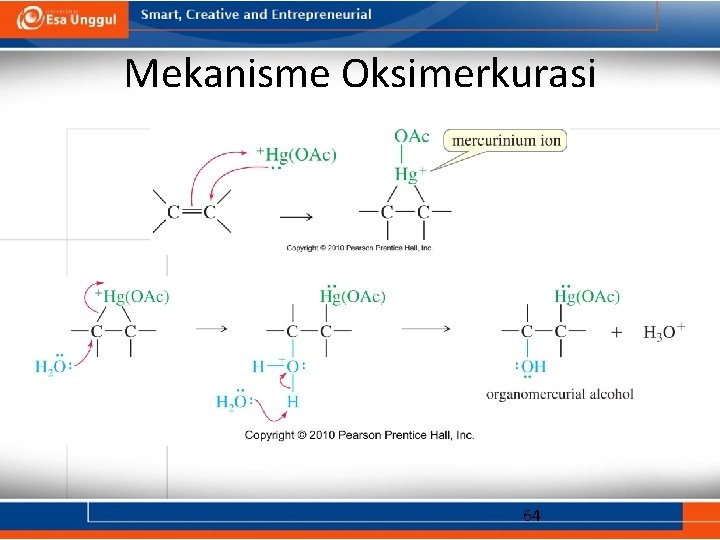
Mekanisme Oksimerkurasi 64

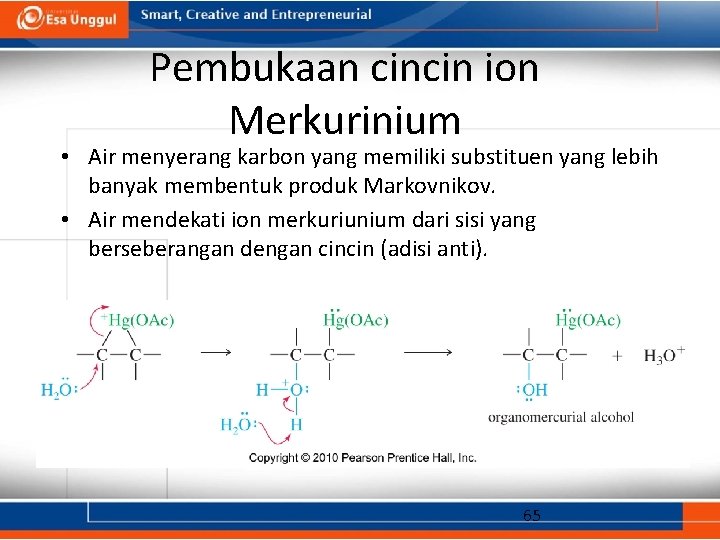
Pembukaan cincin ion Merkurinium • Air menyerang karbon yang memiliki substituen yang lebih banyak membentuk produk Markovnikov. • Air mendekati ion merkuriunium dari sisi yang berseberangan dengan cincin (adisi anti). 65

Reaksi Demerkurasi • Pada reaksi demerkurasi, suatu In the demercuration reaction, hidrida diperoleh dari natrium borohidrida (Na. BH 4) menggantikan merkuri asetat. • Reaksi oksimerkurasi-demerkurasi menghasilkan produk Markovnikov dengan gugus hidroksil berada pada karbon yang memiliki subtituen terbanyak. 66

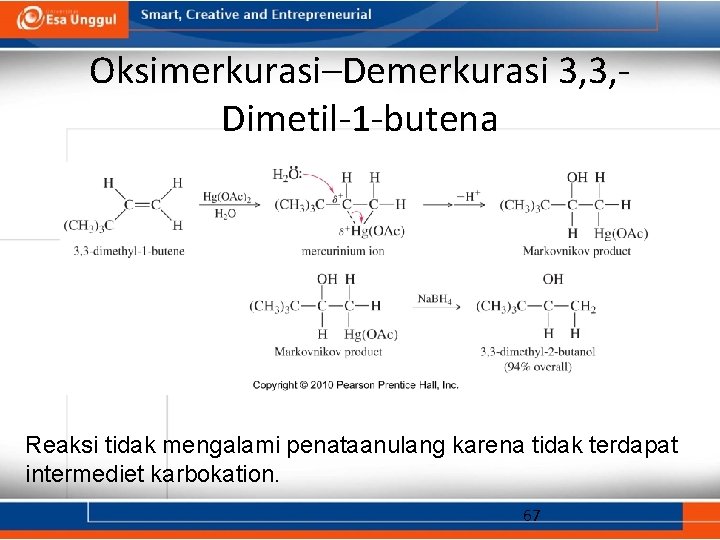
Oksimerkurasi–Demerkurasi 3, 3, Dimetil-1 -butena Reaksi tidak mengalami penataanulang karena tidak terdapat intermediet karbokation. 67

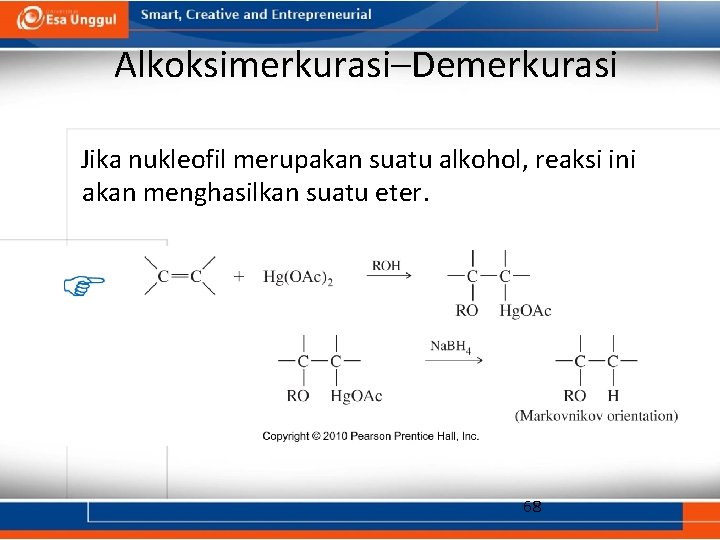
Alkoksimerkurasi–Demerkurasi Jika nukleofil merupakan suatu alkohol, reaksi ini akan menghasilkan suatu eter. 68

Contoh Soal 3 Tunjukkan intermediet dan produk yang dihasilkan dari reaksi alkoksimerkurasi–demerkurasi 1 -metilsiklopentena, menggunakan metanol sebagai pelarut. Penyelesaian Merkuri asetat mengadisi 1 -metilsiklopentena menghasilkan ion merkurinium siklik. Ion ini memiliki muatan positif yang cukup pada atom karbon yang memiliki substituen yang lebih banyak (karbon tersier). Metanol menyerang karbon ini. Reduksi intermediet menghasilkan produk Markovnikov, 1 -metoksi-1 -metilsiklopentana. 69

Hidroborasi alkena • Reaksi adisi air pada ikatan rangkap dengan produk berorientasi anti-Markovnikov. • BH 3 (boran) merupakan suatu asam Lewis. • Diboran (B 2 H 6) merupakan suatu dimer dari senyawa boran yang mengalami reaksi kesetimbangan menghasilkan boran dalam jumlah kecil (BH 3) • BH 3 • THF merupakan bentuk boran yang paling sering digunakan. 70

Mekanisme hidroborasi • Boran mengadisi ikatan rangkap dalam satu tahap reaksi, dima boran mengadisi atom karbon yang memiliki substituen paling sedikit dan hidrogen mengadisi karbon dengan substituen terbanyak. • Orientasi ini menempatkan muatan positif parsial pada lkeadaaan transisi di bagian atom karbon yang memiliki substituen terbanyak. 71

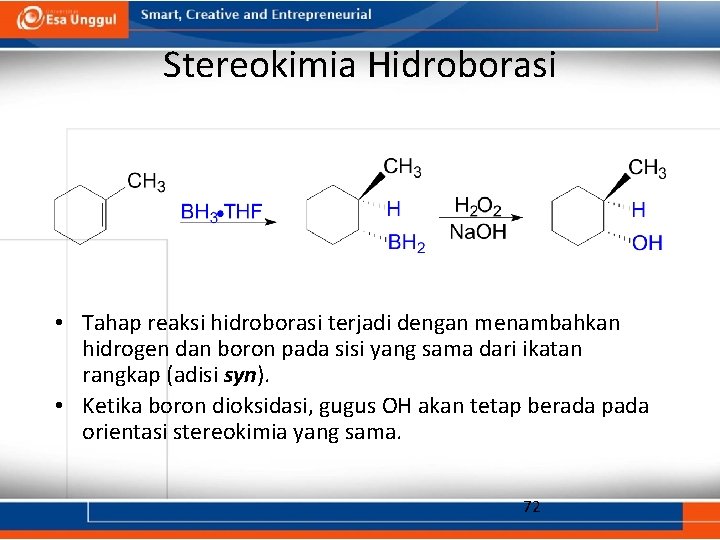
Stereokimia Hidroborasi • Tahap reaksi hidroborasi terjadi dengan menambahkan hidrogen dan boron pada sisi yang sama dari ikatan rangkap (adisi syn). • Ketika boron dioksidasi, gugus OH akan tetap berada pada orientasi stereokimia yang sama. 72

Contoh soal 4 Tunjukkan bagaimana cara mengubah 1 -metilsiklopentanol menjadi 2 -metilsiklopentanol. Penyelesaian Gunakan reaksi hidroborasi–oksidasi untuk membentuk 2 -metil siklopentanol dari 1 -metilsiklopentena. Gunakan lambang (1) dan (2) diatas dan dibawah tanda panah untuk menunjukkan tiap tahap dari reaksi yang dilakukan. 2 -metilsiklopentanol yang dihasilkan dari sintesis ini murni merupakan isomer trans. 1 Metilsiklopentena merupakan alkena dengan substituen terbanyak yang dihasilkan dari dehidrasi 1 metilsiklopentanol. Dehidrasi alkohol akan menghasilkan alkena yang tepat. 73

Contoh Soal 5 Molekul norbornena yang dilabeli dengan deuterium dijadikan bahandasar dalam reaksi hidroborasioksidasi. Tentukan struktur intermediet dan produk dari reaksi ini. Solution Adisi syn dari BH 3 pada ikatan rangkap dua norbornena terjadi pada sisi yang paling mudah diakses (ekso). Oksidasi menghasilkan produk dimana atom hidrogen dan atom hidroksilberada posisi ekso. (sisi ikatan rangkap yang lebih sulit dijangkau oleh BH 3 disebut sisi endo) 74

Oksidasi alkil boran menjadi alkohol • Oksidasi alkil boran dengan hidrogen peroksida basa menghasilkan alkohol. • Produk yang dihasilkan memiliki orientasi anti. Markovnikov. 75

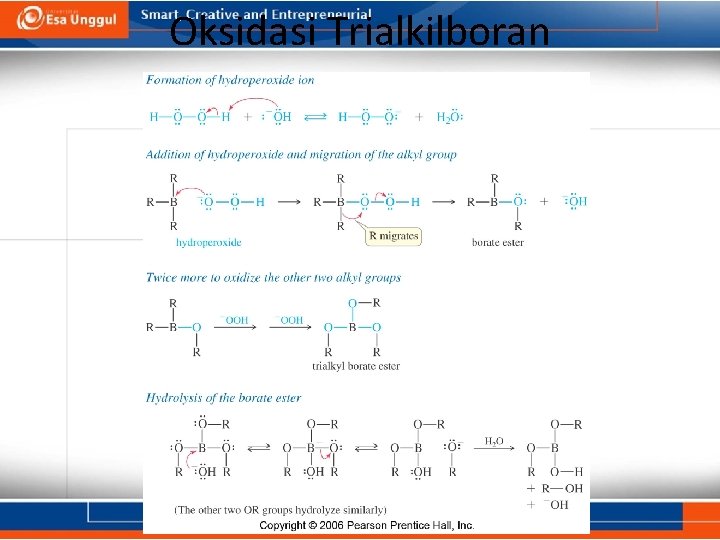
Oksidasi Trialkilboran 76

Adisi Halogen • Cl 2, Br 2, dan kadang I 2 dapat mengadisi ikatan rangkap membentuk suatu visinal dihalida. • Reaksi ini merupakan adisi halida pada posisi anti. 77

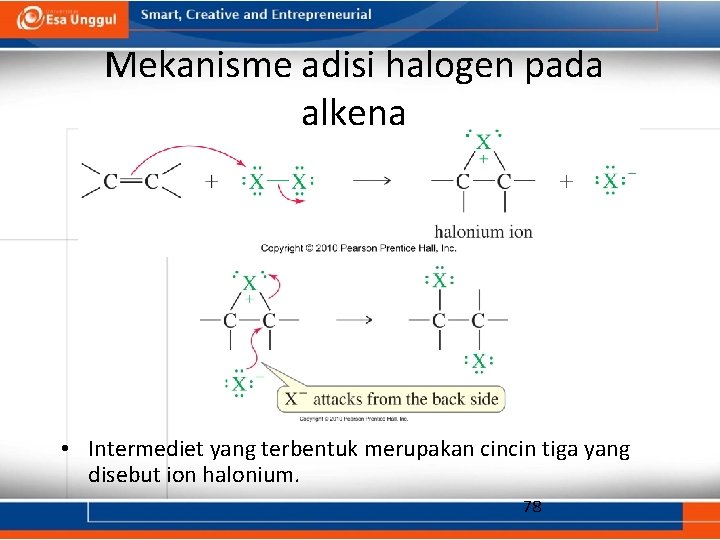
Mekanisme adisi halogen pada alkena • Intermediet yang terbentuk merupakan cincin tiga yang disebut ion halonium. 78

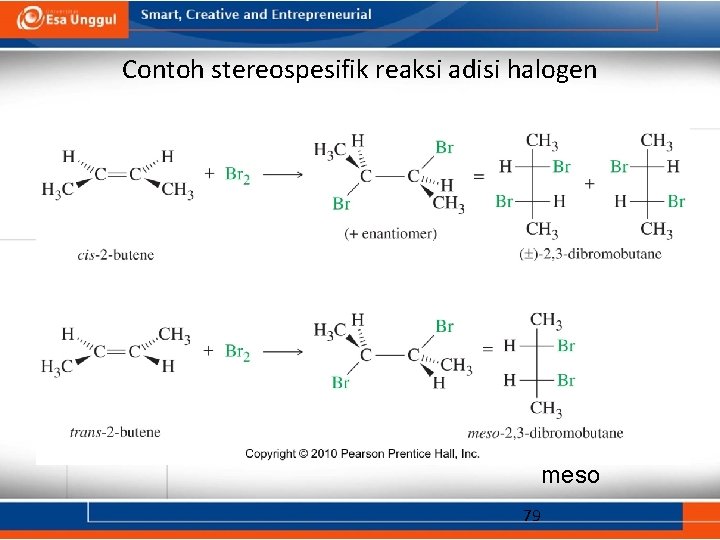
Contoh stereospesifik reaksi adisi halogen meso 79

Uji ketidakjenuhan • Tambahkan Br 2 ke dalam CCl 4 (warna merah coklat gelap) ke dalam suatu senyawa alkena. • Warna akan hilang dengan cepat karena molekul bromin mengadisi ikatan rangkap (tabung reaksi sebelah kiri). • Jika tidak terdapat ikatan rangkap pada sampel, maka bromin akan membuat sampel menjadi warna kecoklatan. • Reaksi ini merupakan uji keberadaan gugus alkena. 80

Pembentukan halohidrin • Jika suatu halogen ditambahkan dengan keberadaan air pada suatu alkena maka akan terbentuk suatu halohidrin. • Air berperan sebagai nukleofil. • Reaksi ini merupakan suatu adisi Markovnikov: bromin (elektrofil) akan mengadisi karbon dengan subtituen yang lebih sedikit. 81

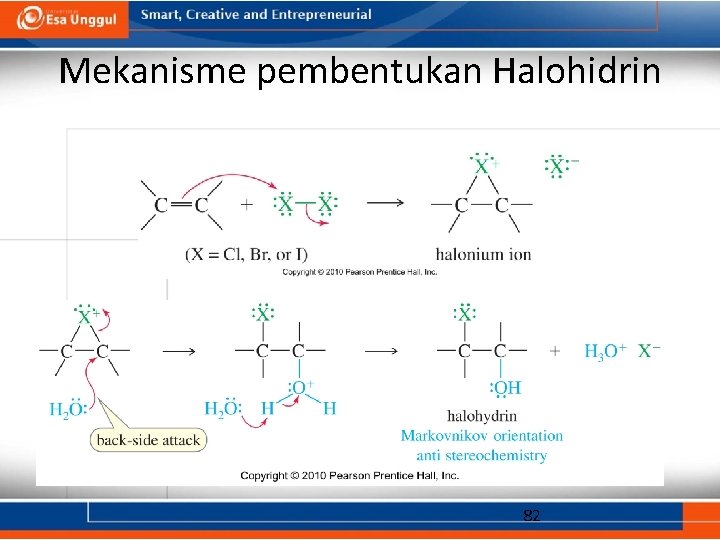
Mekanisme pembentukan Halohidrin 82

Contoh Soal 6 Buatlah mekanisme reaksi untuk reaksi antara 1 -metilsiklopentena dengan air bromin. Penyelesaian 1 -Metilsiklopentena bereaksi dengan bromin menghasilkan suatu ion bromonium. Serangan oleh air dapat terjadi baik pada karbon sekunder maupun karbon tersier dari ion bromonium. Serangan oleh air pada akhirnya terjadi pada karbon yang memiliki subtituen yang lebih banyak (dengan muatan positif yang lebih banyak). 83

Contoh Soal 7 Ketika sikloheksena direaksikan dengan bromin dalam larutan natrium klorida jenuh, dihasilkan campuran trans-2 -bromosikloheksanol dan trans-1 -bromo-2 -klorosikloheksana. Tuliskan mekanisme reaksi pembentukan kedua produk ini. Penyelesaian Sikloheksena bereaksi dengan bromin menghasilkan ion bromonium yang bereaksi dengan nukleofil yang ada pada campuran reaksi. Nukleofil terbanyak yang ada pada campuran reaksi adalah air dan ion klorida. Serangan oleh air menghasilkan bromohidrin dan serangan oleh klorida menghasilkan dihalida. Kedua serangan nukleofil tersebut menghasilkan produk anti. 84

Hidrogenasi Alkena • Hidrogen (H 2) dapat mengadisi ikatan rangkap dalam melalui proses yang dikenal sebagai hidrogenasi terkatalitik. • Reaksi hanya terjadi jika terdapat katalis pada campuran reaksi. Katalis yang biasa digunakan adalah paladium (Pd), platina (Pt), dan nikel (Ni), namun logam lain juga dapat digunakan. • Hidrogenasi ini menghasilkan produk adisi syn. 85

Mekanisme hidrogenasi terkatalitik • Hidrogen dan alkena diserap pada permukaan logam. • Setelah diserap, hidrogen ditambahkan pada sisi yang sama, dan kemudian dilepaskan dari logam. • Reaksi memiliki stereokimia syn karena hidrogen ditambahkan pada sisi yang sama. 86

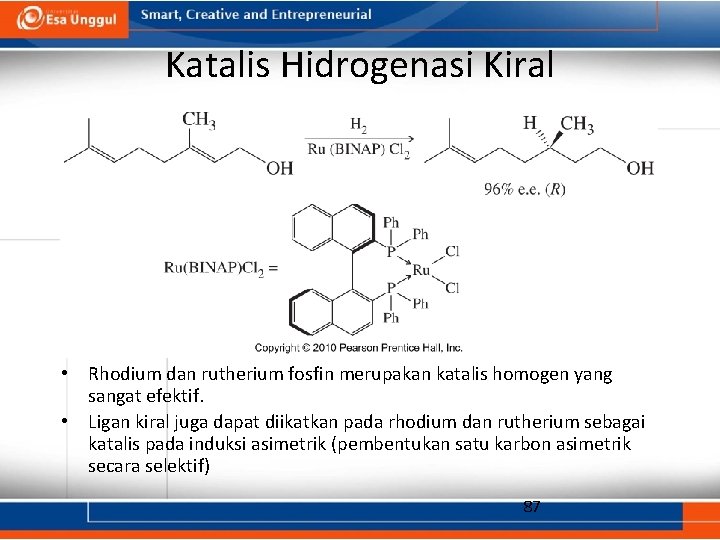
Katalis Hidrogenasi Kiral • Rhodium dan rutherium fosfin merupakan katalis homogen yang sangat efektif. • Ligan kiral juga dapat diikatkan pada rhodium dan rutherium sebagai katalis pada induksi asimetrik (pembentukan satu karbon asimetrik secara selektif) 87

Adisi Karbena • Insersi gugus —CH 2 pada suatu ikatan rangkap menghasilkan cincin siklopropana. • Tiga metode dalam adisi karbena: – Diazometana (CH 3 N 2, cahaya UV atau panas). – Reaksi Simmons–Smith (CH 2 I 2 dan Zn(Cu)). – Eliminasi alfa pada suatu haloform (CHX 3, Na. OH, H 2 O). 88

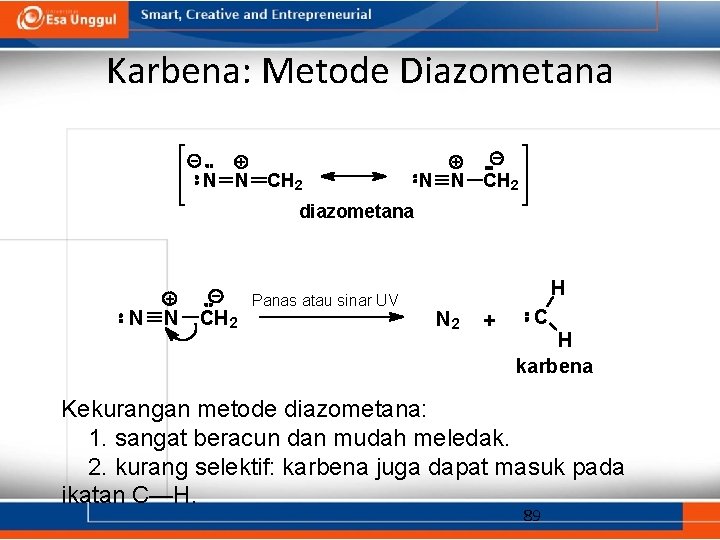
Karbena: Metode Diazometana N N CH 2 diazometana N N CH 2 Panas atau sinar UV H N 2 + C H karbena Kekurangan metode diazometana: 1. sangat beracun dan mudah meledak. 2. kurang selektif: karbena juga dapat masuk pada ikatan C—H. 89

Reaksi Simmons–Smith Metode terbaik dalam pembuatan siklopropana. CH 2 I 2 + Zn(Cu) ICH 2 Zn. I Reagen Simmons– Smith 90

Reaksi Eliminasi alfa • Dalam keberadaan basa, kloroform dan bromoform dapat dihidrogenasi membentuk suatu karbena. 91

Stereospesifisitas • Siklopropana akan mempertahankan bentuk cis/trans dari alkena. 92

Contoh karbena Reaksi Simmons–Smith Reaksi Elimination alfa 93

Epoksidasi • alkena bereaksi dengan suatu asam peroksi membentuk suatu epoksida (juga disebut oksiran). • Reagen yang biasa digunakan adalah asam peroksibenzoat. 94

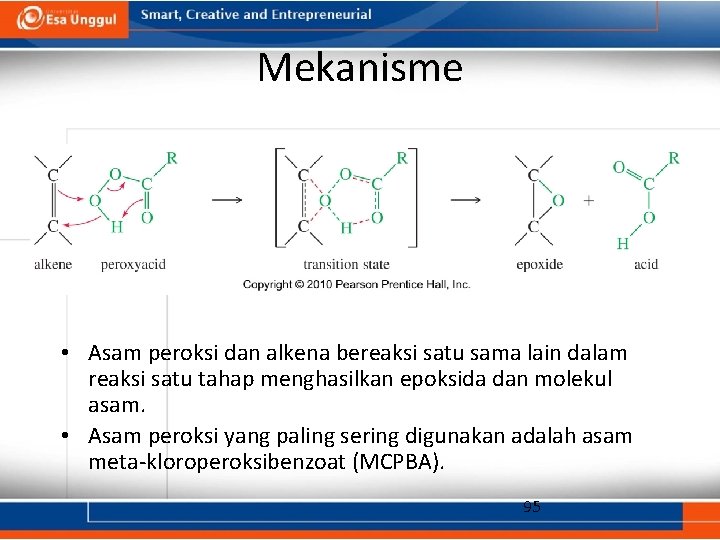
Mekanisme • Asam peroksi dan alkena bereaksi satu sama lain dalam reaksi satu tahap menghasilkan epoksida dan molekul asam. • Asam peroksi yang paling sering digunakan adalah asam meta-kloroperoksibenzoat (MCPBA). 95

Stereokimia Epoksida 96

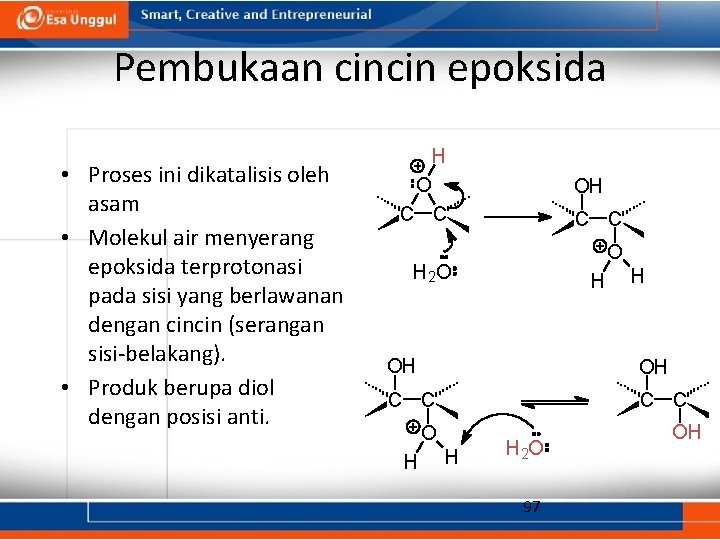
Pembukaan cincin epoksida • Proses ini dikatalisis oleh asam • Molekul air menyerang epoksida terprotonasi pada sisi yang berlawanan dengan cincin (serangan sisi-belakang). • Produk berupa diol dengan posisi anti. H O OH C C O H 2 O H H OH OH C C O H H H 2 O 97 OH

Hidroksilasi Syn alkena • Alkena diubah menjadi suatu syn-1, 2 -diol • Reaksi ini umumnya menggunakan dua reagen berikut: – Osmium tetroksida, Os. O 4, diikuti dengan hidrogen peroksida – Larutan KMn. O 4 encer dam dingin dalam suasana basa. 98

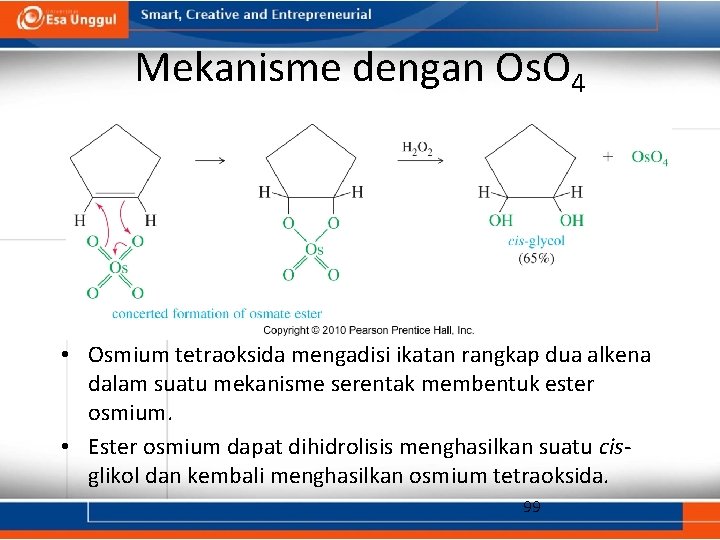
Mekanisme dengan Os. O 4 • Osmium tetraoksida mengadisi ikatan rangkap dua alkena dalam suatu mekanisme serentak membentuk ester osmium. • Ester osmium dapat dihidrolisis menghasilkan suatu cisglikol dan kembali menghasilkan osmium tetraoksida. 99

Ozonolisis • Ozon dapat memecah ikatan rangkap dua secara oksidatif menghasilkan aldehida dan keton. • Ozonolisis merupakan proses yang lebih lunak dibandingkan oksidasi menggunakan KMn. O 4 dan tidak akan lebih lanjut mengoksidasi aldehida. • Tahap kedua ozonolisis merupakan reduksi intermediet oleh Zink atau dimetil sulfida. 100

Mekanisme Ozonolisis • Ozon mengadisi ikatan rangkap dua membentuk intermediet cincin dengan lima anggota yang disebut molozonida yang lebih lanjut mengalami penataulangan membentuk ozonida. 101

Reduksi ozonida • Ozonida tidak perlu diisolasi , namun segera direduksi menggunakan reduktor lunak seperti Zink atau dimetil sulfida menghasilkan aldehida dan keton sebagai produk utama. • Ketika dimetil sulfida digunakan dalam proses ini, atom sulfur teroksidasi menghasilkan dimetil sulfoksida (DMSO) 102

Contoh soal 8 Reaksi ozonolisis-reduksi suatu alkena yang blm diketahui menghasilkan campuran sikloheksanakarbaldehida dan 2 -butanon dalam jumlah yang sama. Terntukan struktur awal dari alkena tersebut. Penyelesaian Struktur molekul alkena ini dapat direkonstruksi dengan menghilangkan dua atom oksigen karbonil (C=O) dan menghubungkan atom karbonil satu sama lain membentuk ikatan rangkap dua. Satu hal yang masih belum diketahi adalah geometri dari alkena yang digunakan. Dapat berupa isomer cis atau trans. . 103

Pembelahan oleh KMn. O 4 • Permanganat merupakan suatu oksidator kuat. • Sebelum produk pembelahan alkena dihasilkan, senyawa glikol akan dihasilkan dan teroksidasi lebih lanjut. • Karbon dengan dua substituen akan menghasilkan keton, sedangkan karbon dengan satu substituen akan menghasilkan asam karboksilat. • Ikatan rangkap dua terminal ═CH 2 akan menghasilkan CO 2. 104

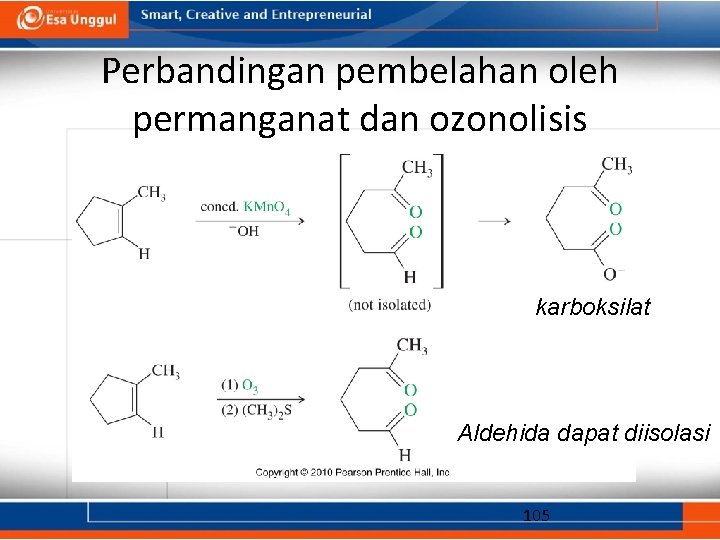
Perbandingan pembelahan oleh permanganat dan ozonolisis karboksilat Aldehida dapat diisolasi 105

Polimerisasi • Suatu alkena (monomer) dapat mengadisi molekul alkena lain membentuk rantai polimer • Terdapat tiga metode pembentukan polimer: – Kationik, reaksi terjadi melalui intermediet karbokation – Radikal bebas – Anionik, reaksi terjadi melalui intermediet karbokation (jarang ditemukan) 106

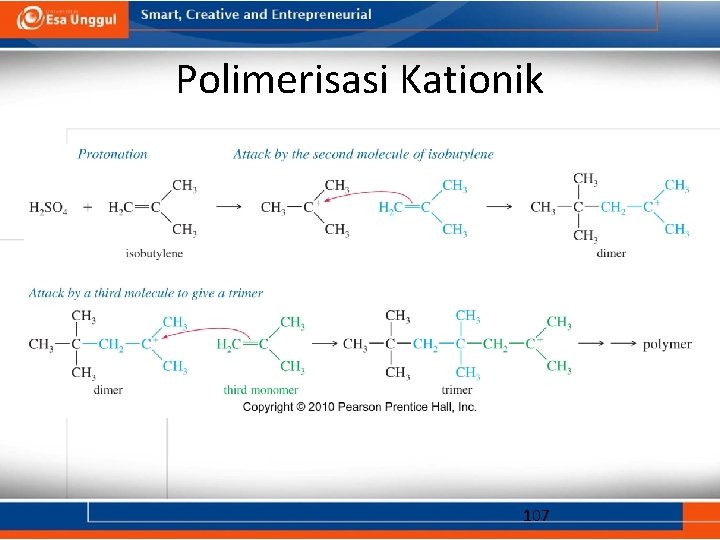
Polimerisasi Kationik 107

Tahap terminasi polimerisasi kationik • Pertumbuhan rantai terhenti ketika suatu proton diabstraksi oleh basa lemah dari asam yang digunakan untuk menginisiasi reaksi. • Lepasnya satu atom hidrogen lebih lanjut akan membentuk ikatan rangkap dua dan sehingga tidak lagi terdapat intermediet karbokation (tahap terminasi) 108

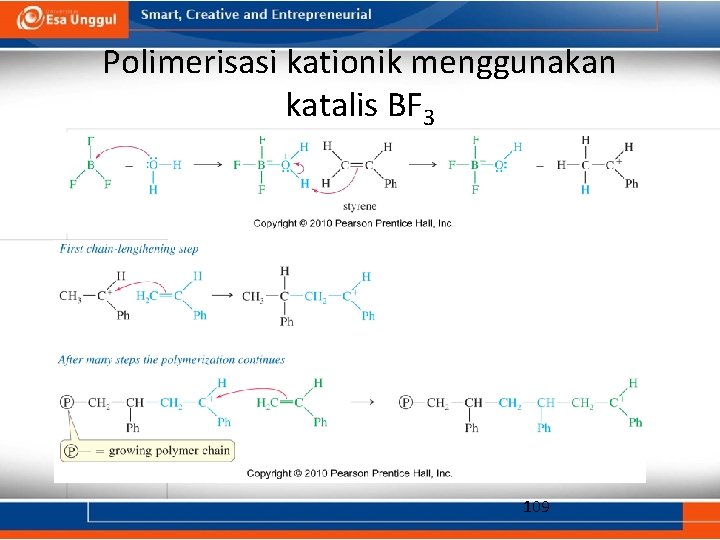
Polimerisasi kationik menggunakan katalis BF 3 109

Polimerisasi radikal • Pada keberadaan inisiator seperti peroksida, akena dapat bereaksi membentuk polimer melalui mekanisme radikal bebas. 110

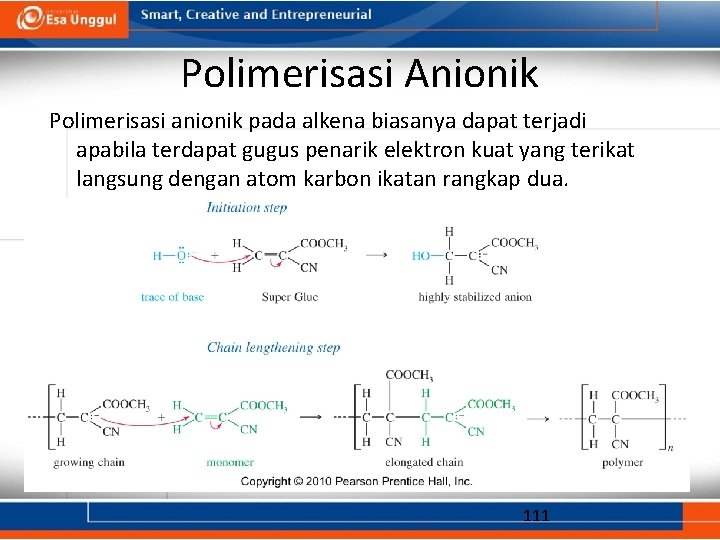
Polimerisasi Anionik Polimerisasi anionik pada alkena biasanya dapat terjadi apabila terdapat gugus penarik elektron kuat yang terikat langsung dengan atom karbon ikatan rangkap dua. electron-withdrawing groups such as nitro, cyano, or carbonyl must be attached to the carbons in the double bond. 111

Sekian 112