SENYAWA AMINA NITRO SENYAWA AMINA Turunan amonia dg





















- Slides: 50

SENYAWA AMINA, NITRO

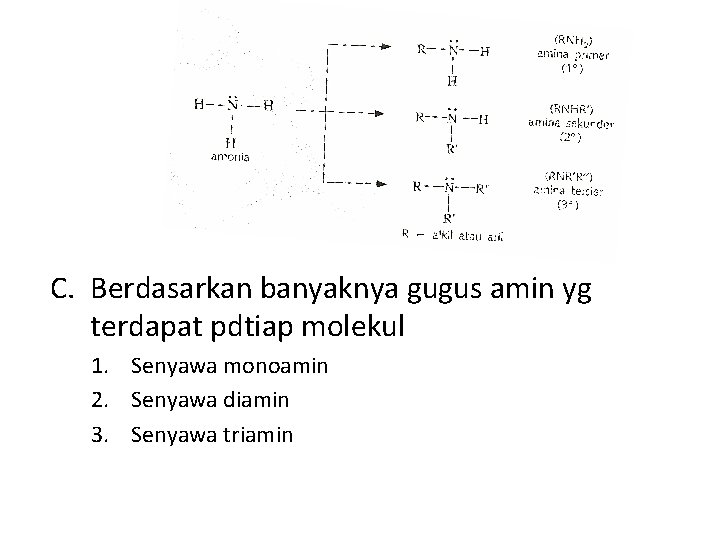
SENYAWA AMINA Turunan amonia dg mengganti 1, 2, at 3 H dari amonia dg gugus alkil at aril Penggolongan Amina : A. Berdasarkan intinya B. Berdasarkan banyaknya atom H dr NH 3 yg digantikan dg gugus aril at alkil 1. 2. 3. Amina 1˚ : 1 atom H pd NH 3 digantikan Amina 2˚ : 2 atom H pd NH 3 digantikan Amina 3˚ : 3 atom H pd NH 3 digantikan

C. Berdasarkan banyaknya gugus amin yg terdapat pdtiap molekul 1. Senyawa monoamin 2. Senyawa diamin 3. Senyawa triamin

Tatanama (IUPAC) • Amin sederhana akhiran –amin CH 3 – CH 2 – NH 2 Propilamin • > 1 gugus fungsi -NH 2 substituen amino pd molekul induk 3 -Amino-2 -propanon

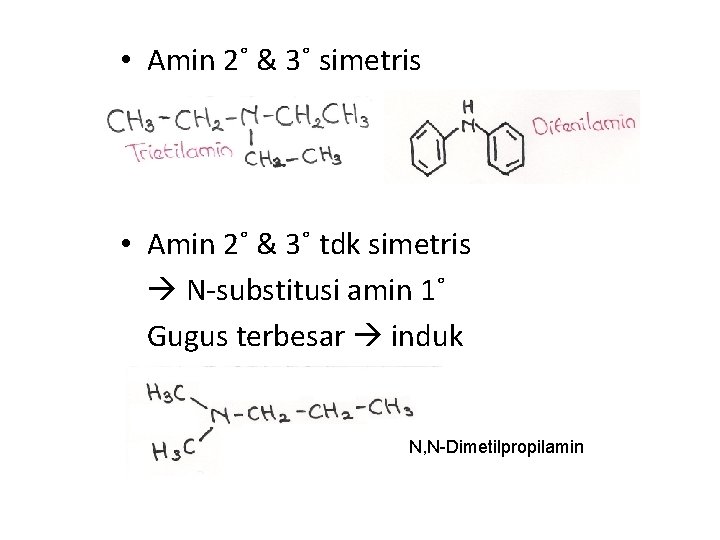
• Amin 2˚ & 3˚ simetris • Amin 2˚ & 3˚ tdk simetris N-substitusi amin 1˚ Gugus terbesar induk N, N-Dimetilpropilamin

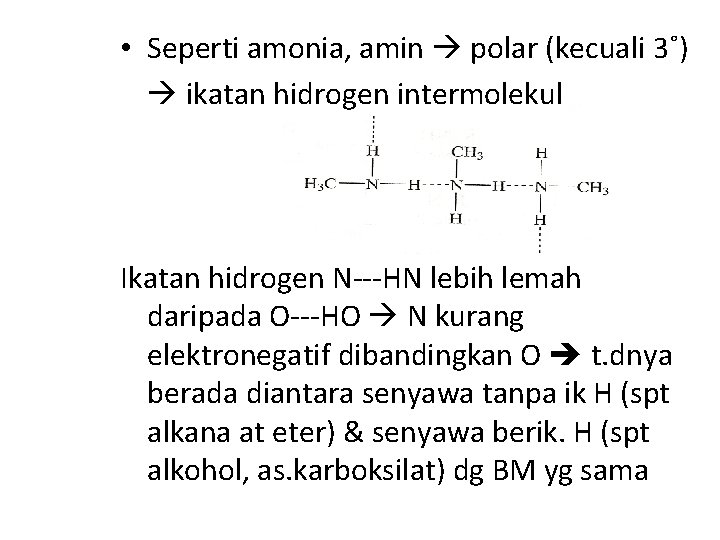
• Seperti amonia, amin polar (kecuali 3˚) ikatan hidrogen intermolekul Ikatan hidrogen N---HN lebih lemah daripada O---HO N kurang elektronegatif dibandingkan O t. dnya berada diantara senyawa tanpa ik H (spt alkana at eter) & senyawa berik. H (spt alkohol, as. karboksilat) dg BM yg sama

CH 3 CH 2 OCH 2 CH 3 dietileter t. d 34, 5 ˚C (CH 3 CH 2)2 NH dietilamin t. d 56 ˚C CH 3 CH 2 CH 2 OH butanol t. d 117 ˚C • Amin 3˚ tdk mpyi ik. H t. d < 1˚ & 2˚ (BM sama) • Adanya elektron sunyi 1˚, 2˚, 3˚ dpt membentuk ik H dg air amin BM rendah (± 6 C) larut dalam air • Amin dapat larut dlm pelarut kurang polar eter, alkohol, benzen dll

• Metilamina dan etilamina mpyi bau spt amonia, sdgkan alkilamina yg lebih tinggi amis spt ikan • Arilamina tdk sebau busuk alkilamina ttp lebih toksik c/ anilin terserap mll kulit kanker • Garam amin & garam ammonium kuarterner = garam anorganik larut dalam air dan tdk berbau

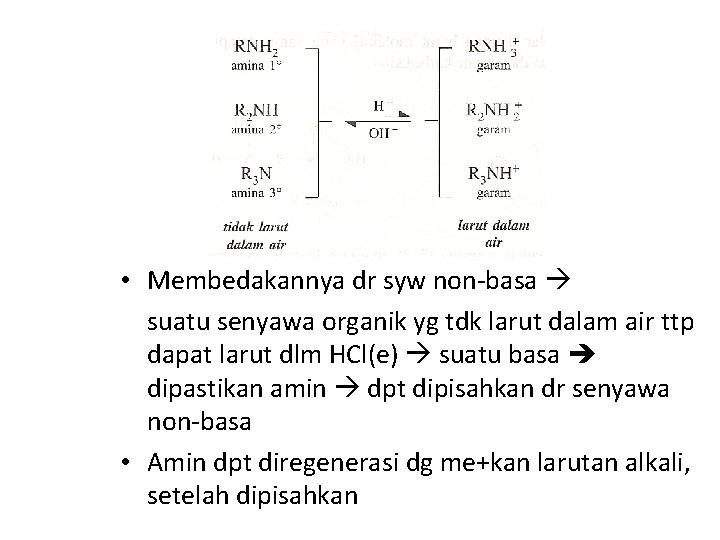
Garam dari amina • Amin alifatis = amonia basa • Amin aromatis kurang basa (lebih lemah dr ion OH at etoksida, ttp lebih kuat dibandingkan alkohol, eter, ester dan air) Pe+ asam-asam mineral at asam-asam karboksilat garam, dg adanya ion OH amin bebas

• Membedakannya dr syw non-basa suatu senyawa organik yg tdk larut dalam air ttp dapat larut dlm HCl(e) suatu basa dipastikan amin dpt dipisahkan dr senyawa non-basa • Amin dpt diregenerasi dg me+kan larutan alkali, setelah dipisahkan

Amina dalam industri • Anilin dapat dibuat : a. Reduksi nitrobenzen dg Fe, HCl (e) at hidrogenasi katalitis b. Mereaksikan klorobenzen pd t↑ & tek↑ dg adanya katalis

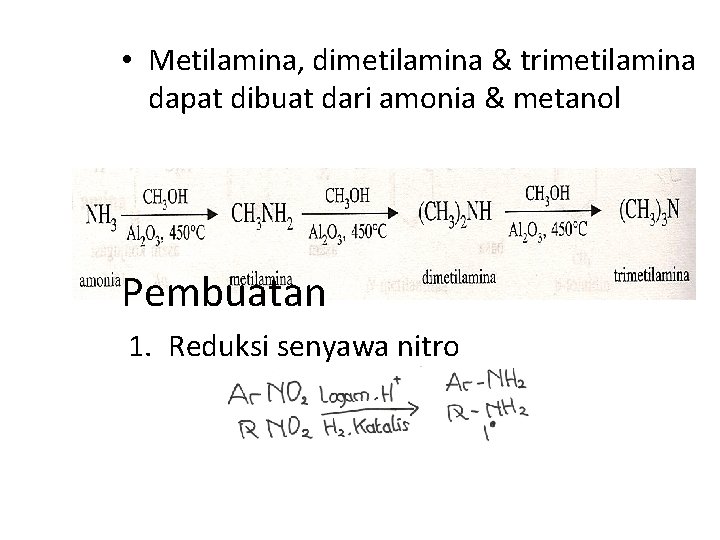
• Metilamina, dimetilamina & trimetilamina dapat dibuat dari amonia & metanol Pembuatan 1. Reduksi senyawa nitro

• Metode ini tdk dpt dgnkan jk molekul mengandung gugus lain yg mudah dihidrogenasi spt alkena, –C=C • Logam yg dpt dgnkan Fe, Al, Zn 2. Reaksi halida dg amonia at amin = reaksi alkilasi substitusi nukleofilik

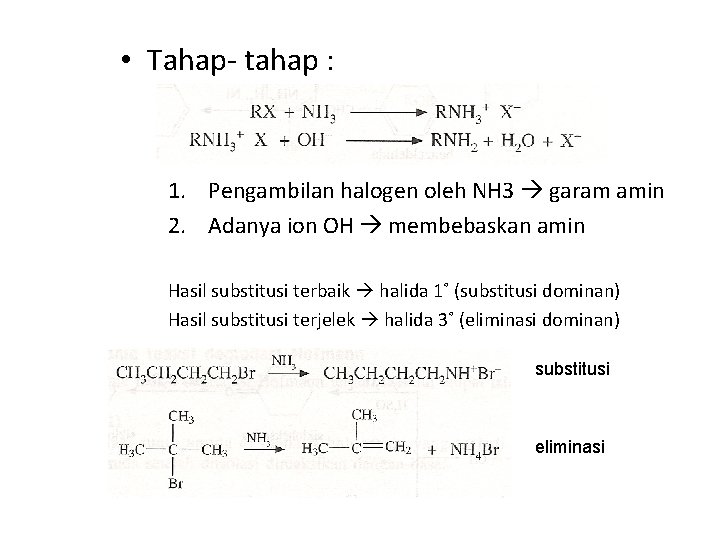
• Tahap- tahap : 1. Pengambilan halogen oleh NH 3 garam amin 2. Adanya ion OH membebaskan amin Hasil substitusi terbaik halida 1˚ (substitusi dominan) Hasil substitusi terjelek halida 3˚ (eliminasi dominan) substitusi eliminasi

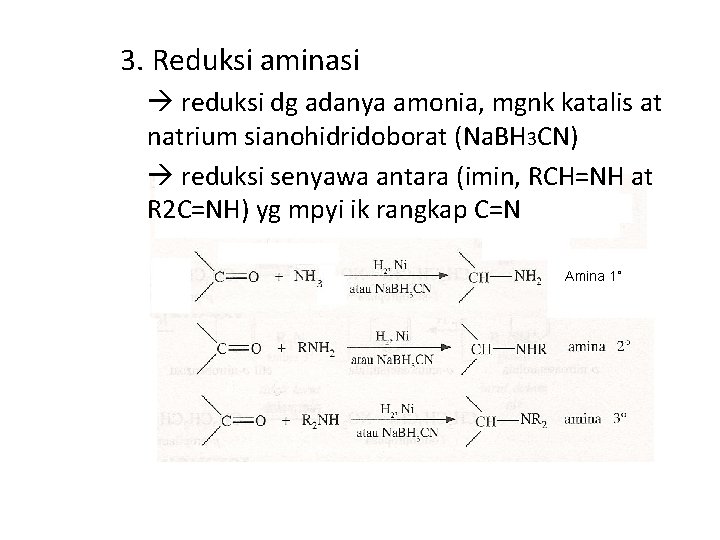
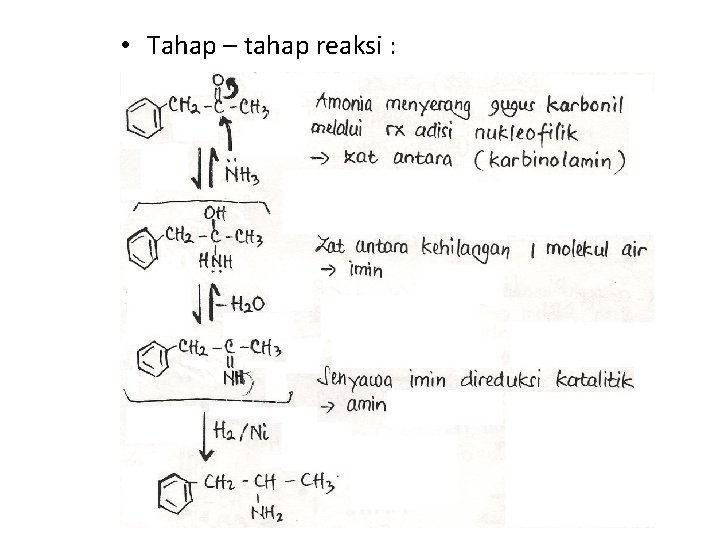
3. Reduksi aminasi reduksi dg adanya amonia, mgnk katalis at natrium sianohidridoborat (Na. BH 3 CN) reduksi senyawa antara (imin, RCH=NH at R 2 C=NH) yg mpyi ik rangkap C=N Amina 1˚

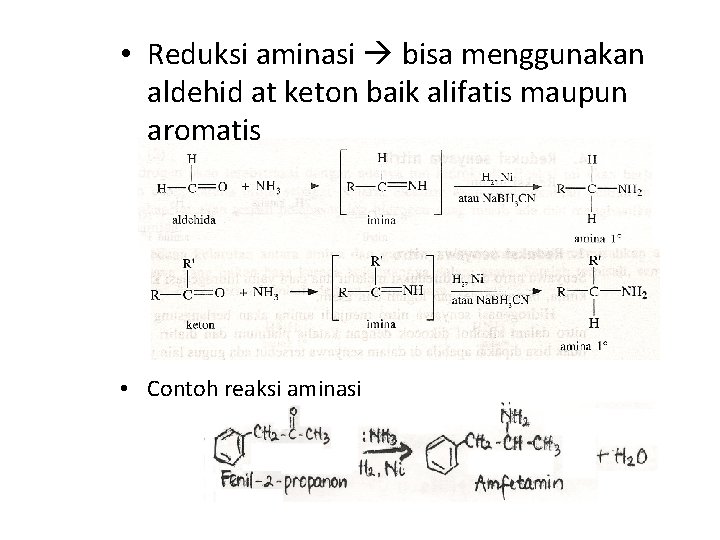
• Reduksi aminasi bisa menggunakan aldehid at keton baik alifatis maupun aromatis • Contoh reaksi aminasi

• Tahap – tahap reaksi :

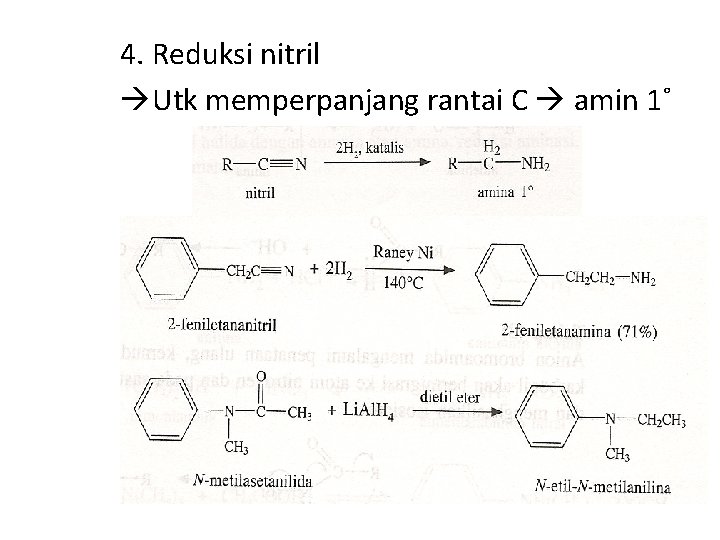
4. Reduksi nitril Utk memperpanjang rantai C amin 1˚

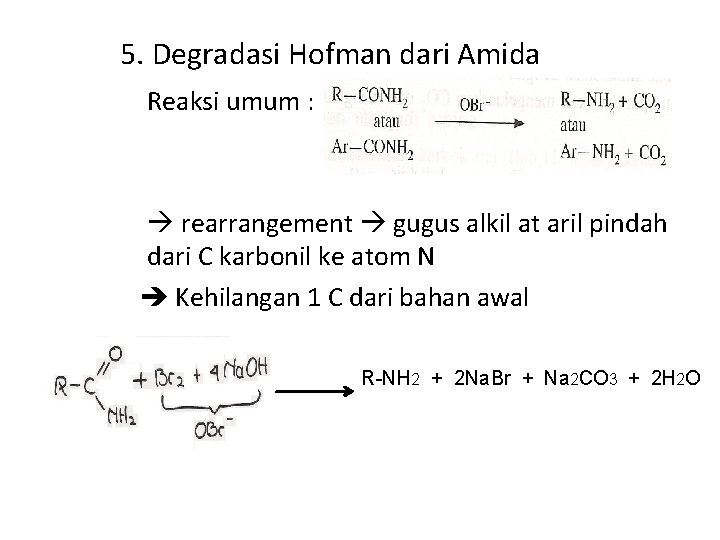
5. Degradasi Hofman dari Amida Reaksi umum : rearrangement gugus alkil at aril pindah dari C karbonil ke atom N Kehilangan 1 C dari bahan awal R-NH 2 + 2 Na. Br + Na 2 CO 3 + 2 H 2 O

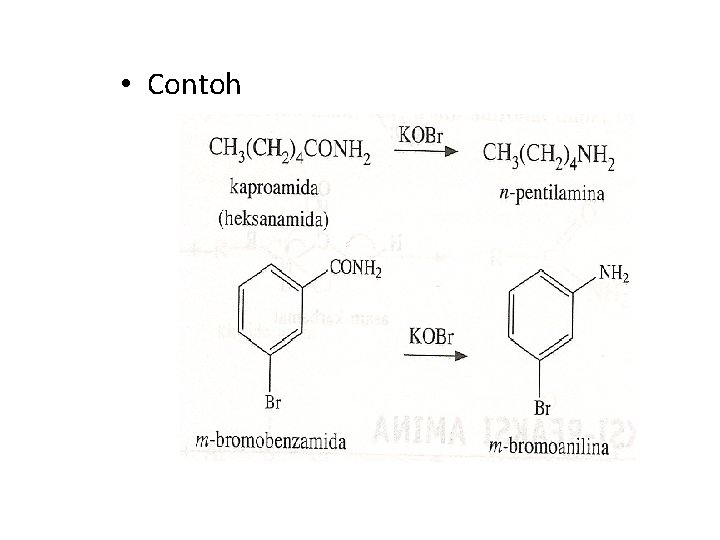
• Contoh

Mekanisme reaksi degradasi Hofman Tahap (1) Halogenasi suatu amida dimana N-haloamida yg terjadi dpt diisolasi, kemudian N-haloamida setelah diisolasi direaksikan dg basa. Basa akan menarik proton dari NH 2 anion Anion bereaksi dg bromin pd rx α-substitusi Nbromoamida

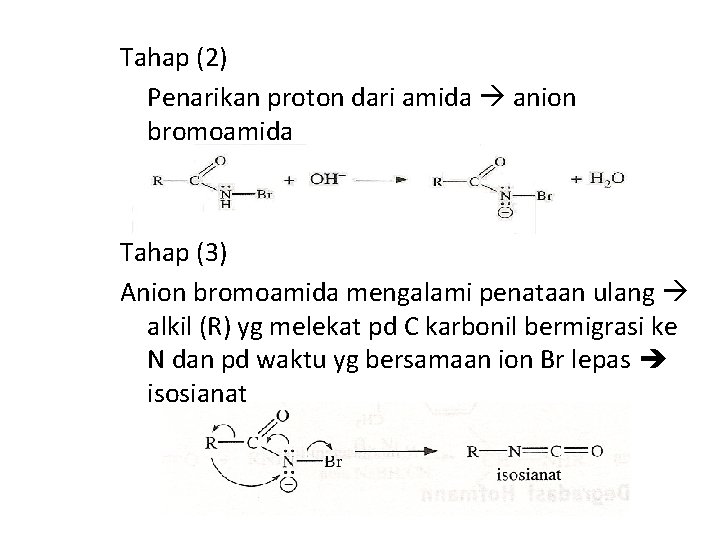
Tahap (2) Penarikan proton dari amida anion bromoamida Tahap (3) Anion bromoamida mengalami penataan ulang alkil (R) yg melekat pd C karbonil bermigrasi ke N dan pd waktu yg bersamaan ion Br lepas isosianat

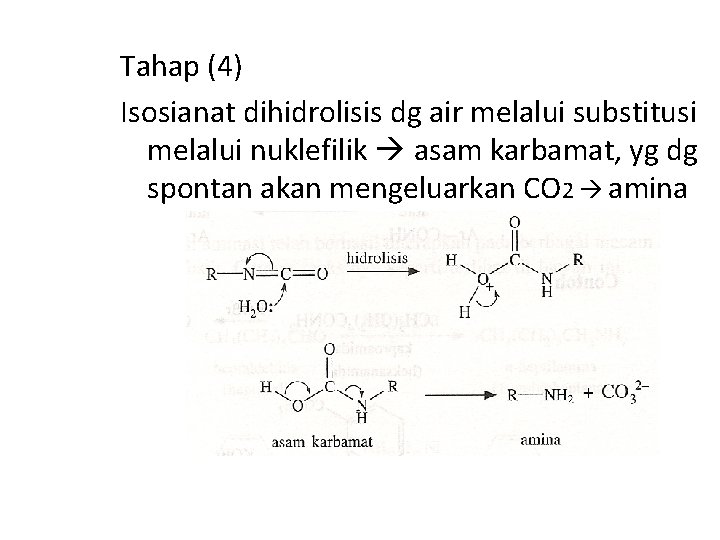
Tahap (4) Isosianat dihidrolisis dg air melalui substitusi melalui nuklefilik asam karbamat, yg dg spontan akan mengeluarkan CO 2 amina

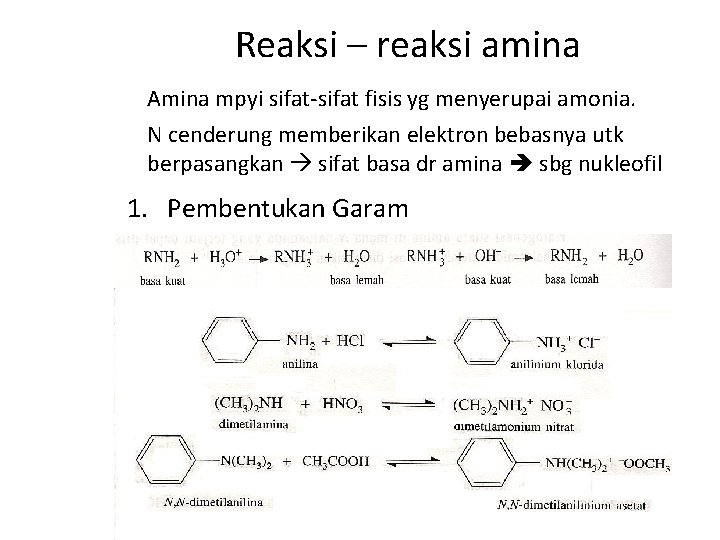
Reaksi – reaksi amina Amina mpyi sifat-sifat fisis yg menyerupai amonia. N cenderung memberikan elektron bebasnya utk berpasangkan sifat basa dr amina sbg nukleofil 1. Pembentukan Garam

2. Reaksi dg asil halida amida Tujuan : utk mensintesa amin lain dg merubahnya amida reduksi amin Senyawa amin nukleofilik menyerang C karbonil mengusir/menggantikan Cl dg kehilangan sebuah proton -Cl diganti oleh gugus –NHR at NR 2

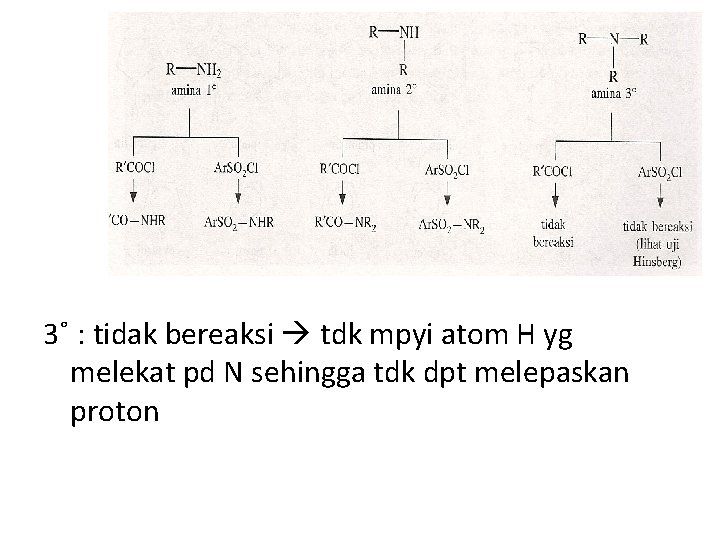
3˚ : tidak bereaksi tdk mpyi atom H yg melekat pd N sehingga tdk dpt melepaskan proton

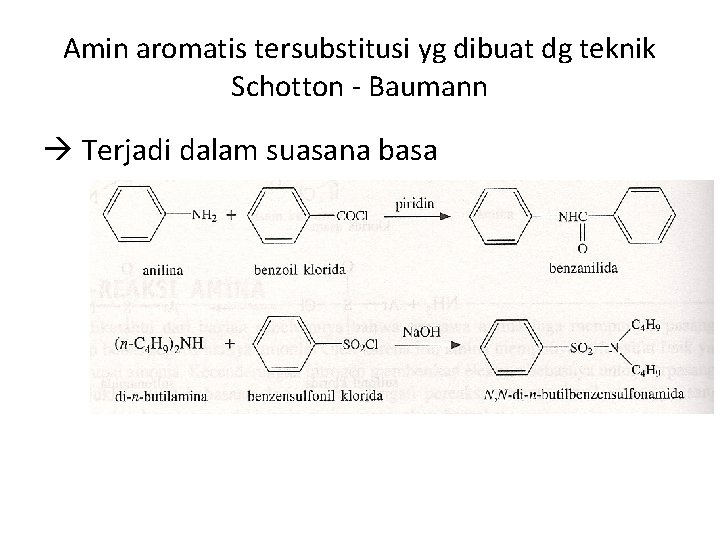
Amin aromatis tersubstitusi yg dibuat dg teknik Schotton - Baumann Terjadi dalam suasana basa

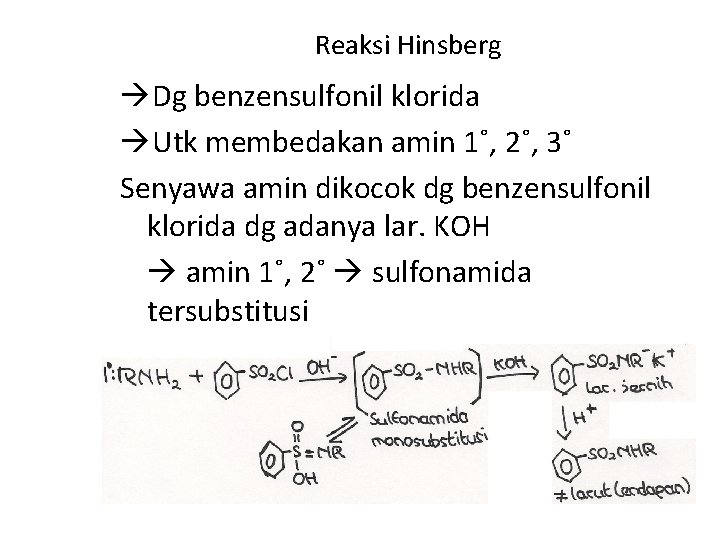
Reaksi Hinsberg Dg benzensulfonil klorida Utk membedakan amin 1˚, 2˚, 3˚ Senyawa amin dikocok dg benzensulfonil klorida dg adanya lar. KOH amin 1˚, 2˚ sulfonamida tersubstitusi 3˚ tdk bereaksi

• Sulfonamida monosubstitusi dari amin 1˚ I H pd N dg KOH garam yg larut ( C<8) ≠ larut (endapan) • Sulfonamida disubstitusi dr amin 2˚ tdk mpyi H yg bersifat asam tdk larut dalam basa kuat

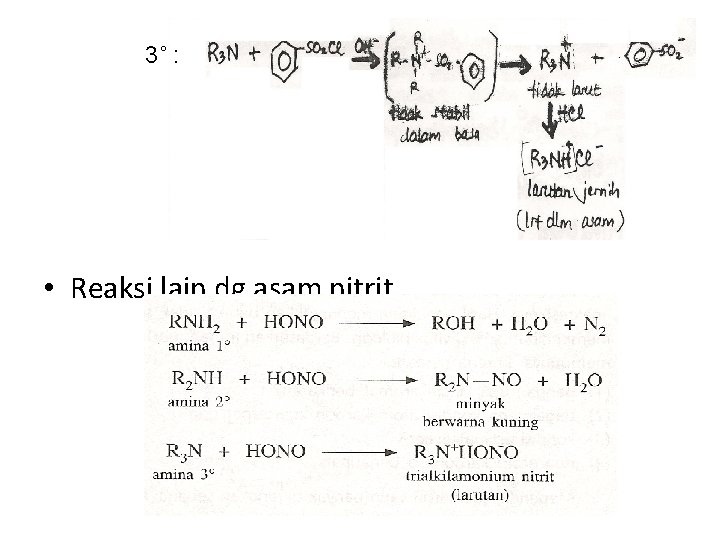
3˚ : • Reaksi lain dg asam nitrit

Sulfanilamid (Sulfonamida) = p-aminobenzen sulfonamida Obat – obat sulfa Amida dari asam sulfanilat Bersifat amfoter dapat bereaksi dg asam at basa

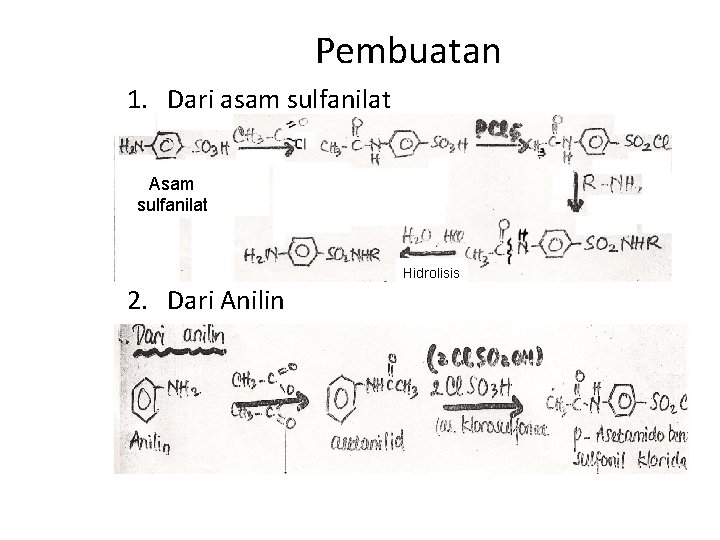
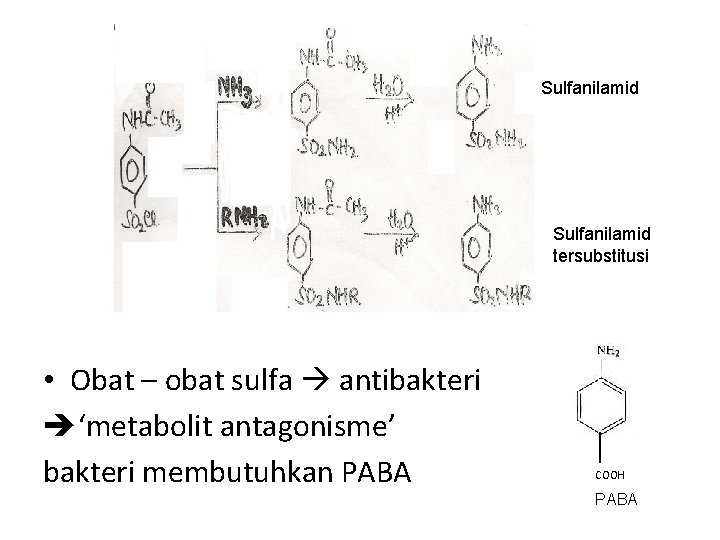
Pembuatan 1. Dari asam sulfanilat Asam sulfanilat Hidrolisis 2. Dari Anilin

Sulfanilamid tersubstitusi • Obat – obat sulfa antibakteri ‘metabolit antagonisme’ bakteri membutuhkan PABA COOH PABA

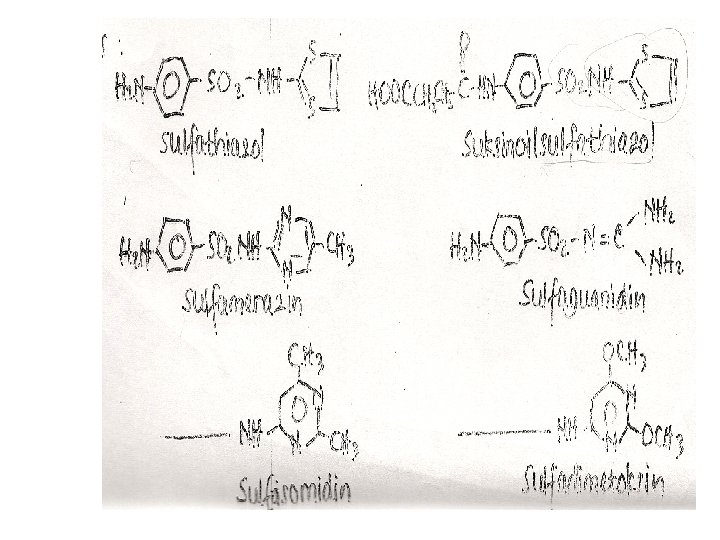
• Rumus sulfa mirip dg PABA terjadi kompetisi sulfa & PABA bakteri mengambil sulfa COOH PABA • Bakteri antivitamin metanolisme gagal pertumbuhan terhambat • Untuk mendapatkan sulfa berkhasiat baik tergantung pd R yg melekat pd N amida yg paling efektif jika R heterosiklik


Reaksi substitusi pd amin aromatis - NH 2 Penunjuk o, p pd substitusi NHR elektrofilik aromatis NR 2 NHCOR aktivator yg iebih lemah dibandingkan NH 2 ( penarikan elektron oleh O dr C karbonil N amida sumber elektron lebih miskin dar N amin) 1. Halogenasi substitusi terjadi pd setiap posisi orto & para

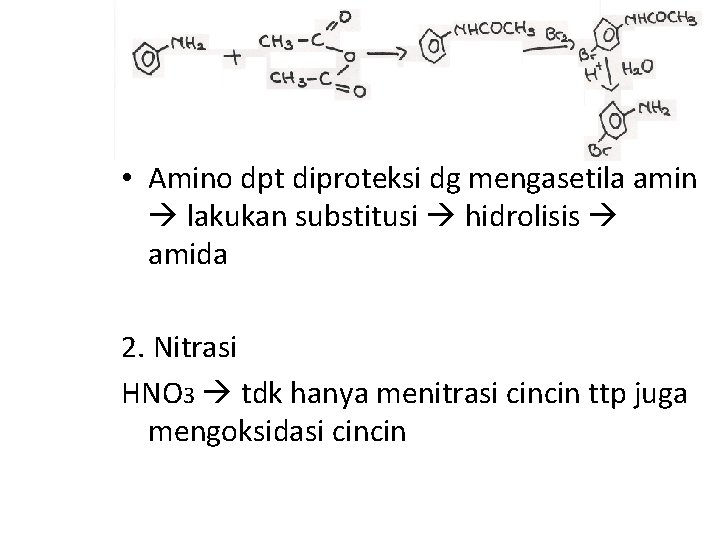
• Amino dpt diproteksi dg mengasetila amin lakukan substitusi hidrolisis amida 2. Nitrasi HNO 3 tdk hanya menitrasi cincin ttp juga mengoksidasi cincin

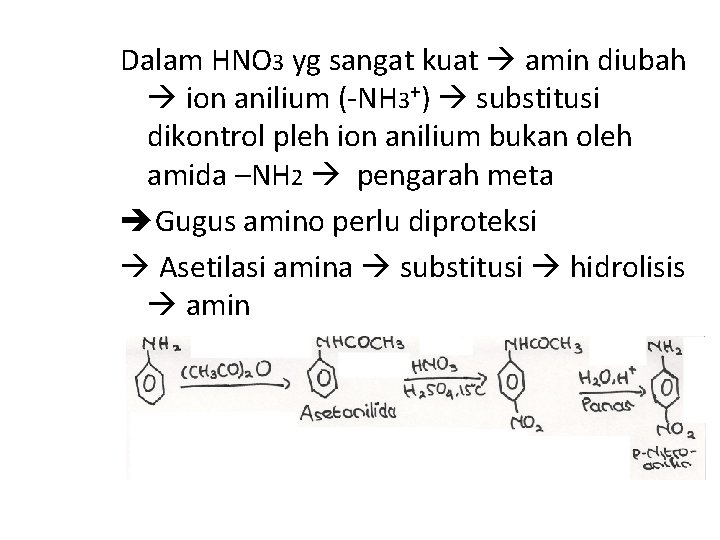
Dalam HNO 3 yg sangat kuat amin diubah ion anilium (-NH 3+) substitusi dikontrol pleh ion anilium bukan oleh amida –NH 2 pengarah meta Gugus amino perlu diproteksi Asetilasi amina substitusi hidrolisis amin

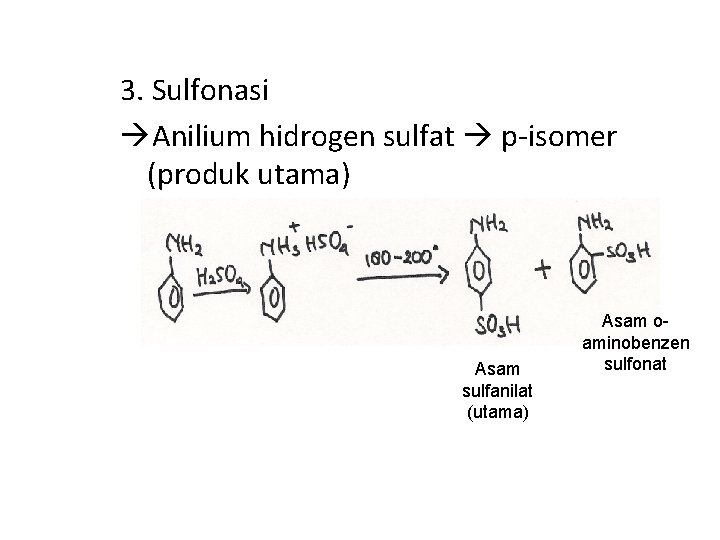
3. Sulfonasi Anilium hidrogen sulfat p-isomer (produk utama) Asam sulfanilat (utama) Asam oaminobenzen sulfonat

SENYAWA R – NO 2 NITROAr – NO 2 • Senyawa dg inti alifatis at aromatis yg mpyi gugus nitro sebagai satu-satunya substituen. • Derivat alkana dg menggantikan 1 ato Hnya dg -NO 2 • Nitroalkana adalah isomer dari ester alkil dg asam nitri alkil nitrit gugus nitro NO 2 terikat pd atom C melalui atom O H 3 C – NO 2 H 3 C – O – NO Nitrometana Metil nitrit

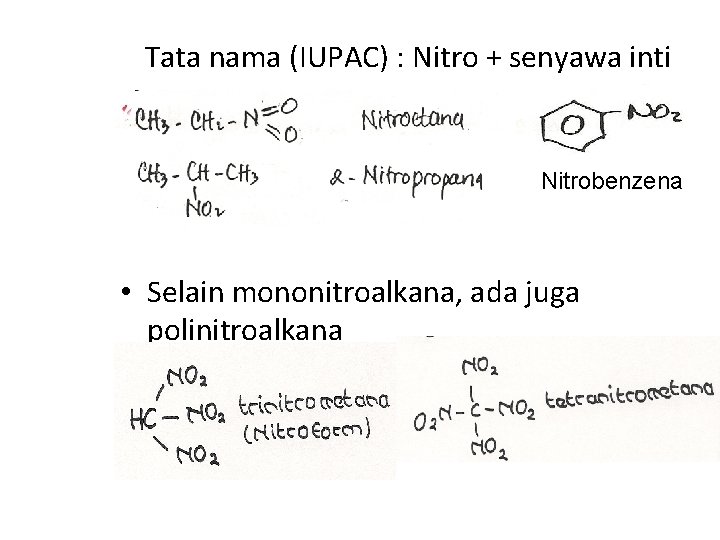
Tata nama (IUPAC) : Nitro + senyawa inti Nitrobenzena • Selain mononitroalkana, ada juga polinitroalkana

Senyawa nitro alifatis Nitroalkana (nitroparafin) Pembuatan 1. Nitrasi alkana dg HNO 3 Reaktivitas : alkana dg atom C 2˚ & 3˚ > mudah bereaksi dg HNO 3

• Jika alkana yg lebih tinggi dinitrasi akan dihasilkan campuran isomer senyawa nitro Propana Isomer nitro propana 2. Dalam laboratorium nitroalkana dibuat dg memanaskan alkil bromida/iodida dg lar. Na. NO 2 dalam DMF yg mengandung sedikit urea (kornblum)

2 -n-oktil nitrit 30% (1 -metilheptil nitrit) • Na. NO 2 dapat diganti dg Ag. NO 2 jumlah nitroalkana 1˚ lebih diperbaiki (prx. Meyer) Oktanaiodida Nitroaoktana

3. Nitroalkana 3˚ dibuat dg hasil terbaik oksidasi t-alkilamin dg KMn. O 4 4. Nitrometana dapat juga dibuat dg memanaskan asam kloroasetat dg lar. Na. NO 2 (kolbe) dekarboksilasi 5. Tetranitroalkana dapat dibuat dg mereaksikan HNO 3(p) berasap dg asetat anhidrat pd suhu rendah (dingin)

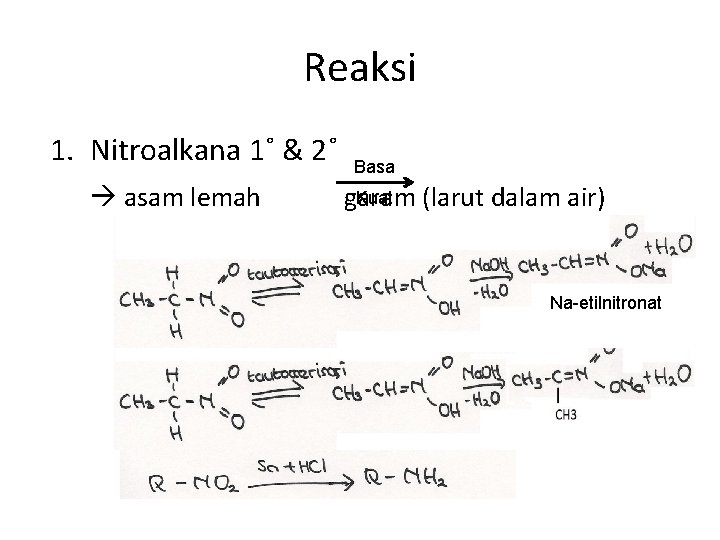
Reaksi 1. Nitroalkana 1˚ & 2˚ asam lemah Basa Kuat garam (larut dalam air) Na-etilnitronat

Sifat fisik • Cairan tidak berwarna • Bau haru, enak • Sedikit larut dalam air, mudah larut dalam pelarut organik Nitro Aromatis • Nitrobenzena • Nitrotoluena

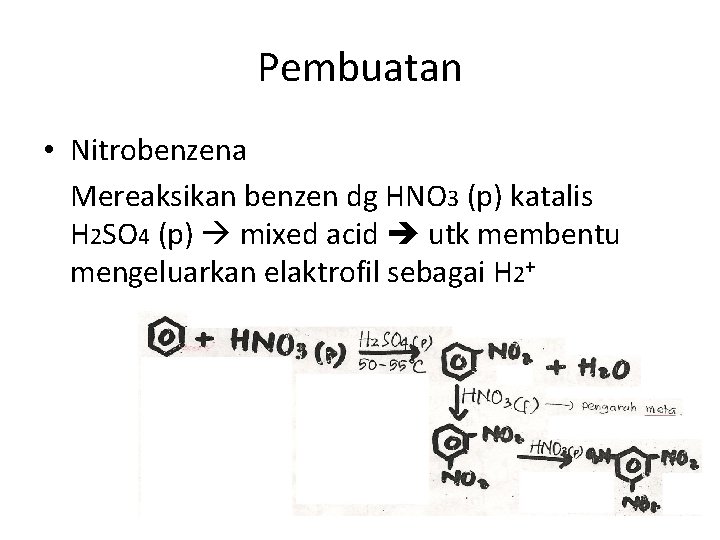
Pembuatan • Nitrobenzena Mereaksikan benzen dg HNO 3 (p) katalis H 2 SO 4 (p) mixed acid utk membentu mengeluarkan elaktrofil sebagai H 2+

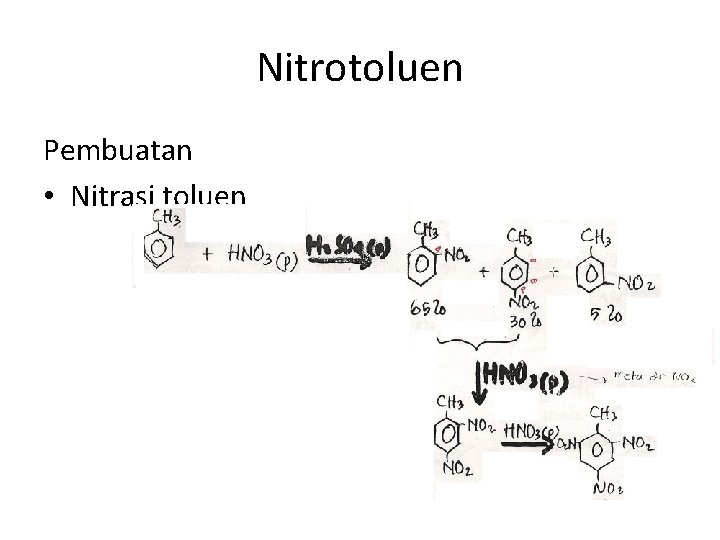
Nitrotoluen Pembuatan • Nitrasi toluen

• Nitrobenzen Sifat fisik – Cairan kuning pucat – Bau tajam (uap beracun, bereaksi dg Hb) – Tdk larut/sedikit larut dalam air, larut dalam pelarut organik • DNB – Kristal kuning pucat – Tdk larut dalam air, larut dalam pelarut organik • TNT – Kristal kuning pucat – Sedikit larut dalam air, alkohol & eter – Bersifat eksplosif, hanya bisa diledakkan dg bantuan detonator (Mercury fulminate)