SEMANA No 6 ESTEQUIOMETRA Licda E Sofa Tobas

SEMANA No. 6 ESTEQUIOMETRÍA Licda. E. Sofìa Tobìas de Rodrìguez

ESTEQUIOMETRÍA Parte de la química que se encarga del estudio de las relaciones cuantitativas entre elementos o compuestos que participan en reacciones químicas. La palabra se deriva de los vocablos griegos: STOICHEION: elemento o sustancia. METRON: medir.

Las relaciones cuantitativas, se expresan generalmente en unidades de masa: mol, g, lb etc. (gases: indicadores de volumen y presión). En las soluciones se puede utilizar la concentración para hacer los cálculos estequiométricos.

PESO ATÓMICO: Masas relativas de los elementos, que son el promedio de los pesos de los isótopos del elemento. Se obtiene en la tabla periódica en uma, pero puede ser expresado en cualquier unidad de masa.

PESO MOLECULAR: (MASA MOLAR) Es la suma de las masas atómicas de todos los átomos de una molécula de un compuesto específico. Ej. H 2 SO 4 Átomo Cantidad de átomos Peso atómico Peso total H 2 1. 00 uma 2 x 1. 00 = S 1 32. 00 uma 1 x 32. 00 = 32. 00 O 4 16. 00 uma 4 x 16. 00 = 64. 00 PESO MOLECULAR 2. 00 98. 00 1 MOL

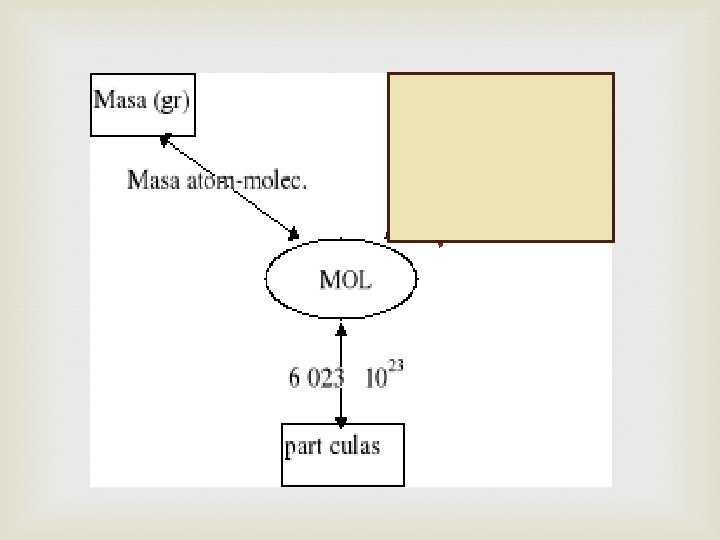
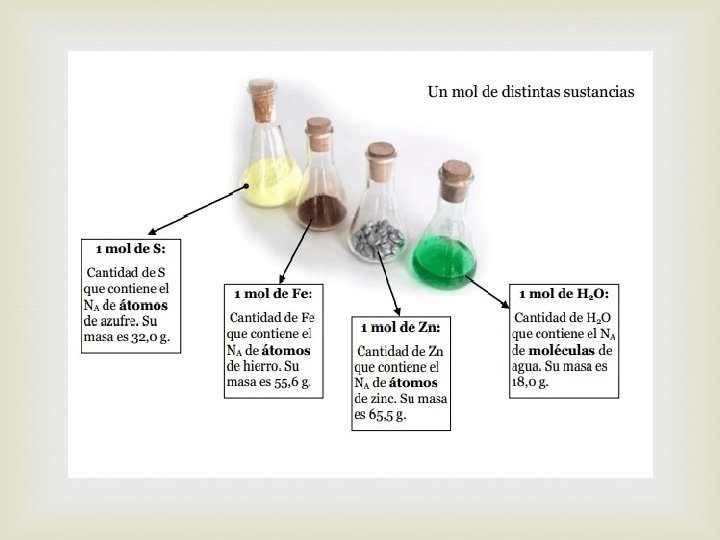
MOL: Cantidad de una sustancia cuya masa en gramos es igual al peso molecular de la sustancia. Un peso molecular = 1 mol = 1, 000 mmoles Un mol= 6. 022 x 1023 átomos, moléculas, fórmulas unitarias o iones (Número de Avogadro).

Ej. N 2(g) + 3 H 2(g) 2 NH 3(g) Los coeficientes numéricos que permiten balancear la ecuación indican que 1 mol de N 2 gaseoso, reacciona con 3 moles de H 2 gaseoso para producir 2 moles de amoníaco.

Leyes Ponderales de la Materia Con la aplicación de éstas leyes, se pueden realizar los cálculos estequiométricos. • Ley de la Conservación de la Masa: Enunciada por el químico francés Antonio Lavoissier originalmente como “La masa no se crea, no se destruye, solamente se transforma”.
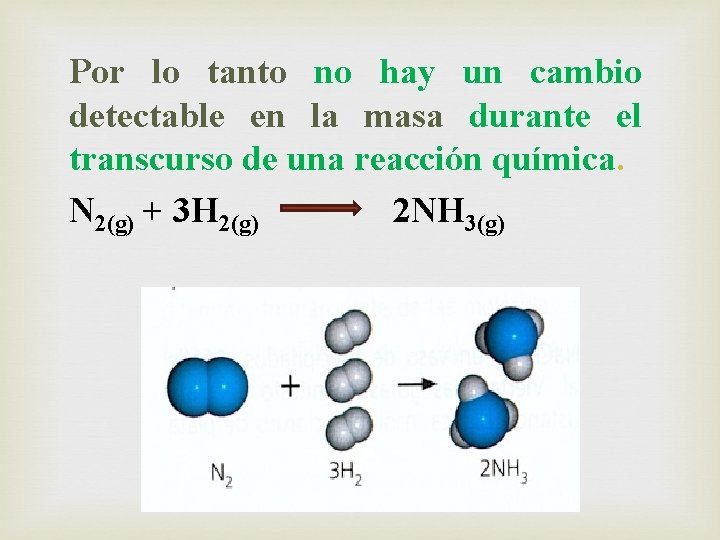
Por lo tanto no hay un cambio detectable en la masa durante el transcurso de una reacción química. N 2(g) + 3 H 2(g) 2 NH 3(g)

• Ley de las Proporciones definidas: Propuesta por Joseph Proust, dice que “un compuesto puro consiste siempre en los mismos elementos combinados en la misma proporción de peso” Ej. H 2 SO 4 2 H: 1 S: 4 O


Ejercicios 1. Cuál es el peso atómico gramo de: a. Mn b. K 2. Cuál es el peso molecular gramo de: C 6 H 12 O 6 3. Cuál es el peso fórmula de: Ba. SO 4 4. A cuántos moles corresponden : a. 320 g de Fe b. 72 g de H 3 PO 4

5. Cuantos g hay en: a. 8. 20 moles de Fe b. 43 moles de Ca(OH)2 6. Cuantos g hay en: a. 32 mmoles de H 2 O 7. A cuántos milimoles corresponden: a. 54. 40 moles de Ca. Cl 2 b. 12 g de Na. Cl

A. Cálculo de Moles a Moles (trabajar con coeficientes) 1. Para la siguiente ecuación calcule: “Para efectuar cálculos estequiométricos la ecuación debe estar balanceada” N 2(g) + 3 H 2(g) → 2 NH 3(g) ¿Cuántos moles de NH 3 se producen a partir de 5 moles de H 2? • Utilizando los coeficientes se pueden escribir factores mol-mol entre reactivos y productos.

N e H 1 mol N 3 mol H 3 mol H 1 mol N N y NH 3 1 mol N 2 mol NH 3 1 mol N H y NH 3 3 mol H 2 mol NH 3 3 mol H • Elabore las relaciones molares que corresponden al problema. • Proceda a hacer el cálculo. 5 mol N 2(g) + 3 H 2(g) → ¿mol? 2 NH 3(g) 5 mol H 2 x 2 mol NH 3 = 3. 33 mol NH 3 3 mol H 2

B. Cálculo de Gramos a. Ecuación balanceada. b. Relacionar gramos de las substancias entre reactivos y productos; o sea factores de masa molar. c. Efectuar cálculos. 1. Cuántos gramos de oxígeno se necesitan para quemar 12 gramos de alcohol etílico, C 2 H 5 OH? 12 g ¿g? C 2 H 5 OH + 3 O 2(g) → 12 g C 2 H 5 OH x Alcohol etílico 96 g O 2 = 25. 04 g O 2 46 g C 2 H 5 OH 2 CO 2 + 3 H 2 O

Cálculo de Moles a Gramos a. Ecuación balanceada b. Obtenga el peso o masa molar de la substancia mencionada en gramos y el número de moles de la substancia mencionada en la misma dimensional en los coeficientes de la reacción. c. Relacione reactivos o reactivos y productos haciendo relación en mol por un lado y en masa por el otro. 1. Calcule cuántos gramos de sulfuro de plomo(II) se pueden oxidar con 7. 5 moles de oxígeno. ¿g? 7. 5 mol 2 Pb. S(s) +3 O 2(g) → 7. 5 mol O 2 x 2 Pb. O(s) + 2 SO 2(g) 478. 4 g Pb. S 3 mol O = 1, 195 g Pb. S

Porcentaje de Composición % = Peso del elemento en el compuesto * 100 Peso del compuesto 1. Calcule el porcentaje de composición de cada uno de los elementos que forman el H 2 SO 4.

FIN
- Slides: 21