SEMANA 5 REACCIONES DE OXIDOREDUCCIN Redox Balanceo por

SEMANA 5 REACCIONES DE OXIDOREDUCCIÓN (Redox). Balanceo por el método Redox QUÍMICA 2020 1

SEMANA 5 REACCIONES REDOX Y BALANCEO POR REDOX REACCIONES DE OXIDACIÓN-REDUCCIÓN Definición de: Oxidación, Reducción, Sustancia oxidada, Sustancia reducida, Agente oxidante, Agente reductor BALANCEO DE ECUACIONES POR EL MÉTODO REDOX. Aplicación de los conceptos en la salud y el ambiente Lecturas en libro de texto. -La Química en el Ambiente “Celdas de combustible, energía limpia para el Futuro” “El esmog y la salud” LABORATORIO: REACCIONES DE OXIDO REDUCCIÓN O REDOX. 2

Reacciones de Oxidación-Reducción o REDOX • Son reacciones químicas donde hay transferencia de electrones entre los reactivos y los productos. Si una sustancia o compuesto pierde electrones , otro los gana. • Se dá en las reacciones de Síntesis, Análisis, Simple sustitución, Combustión y otras. No se dá en Doble sustitución ni en Neutralización. • ¿Cómo se determina si hay Redox? Cuando hay átomos que presenta # de oxidación diferente en los reactivos y en los productos. 3

ES CUANDO HAY UN AUMENTO DE LOS ESTADOS DE OXIDACIÓN o # DE OXIDACIÓN DE LOS ÁTOMOS ES CUANDO HAY UNA DISMINUCIÓN DE LOS ESTADOS DE OXIDACIÓN o # DE OXIDACIÓN DE LOS ÁTOMOS
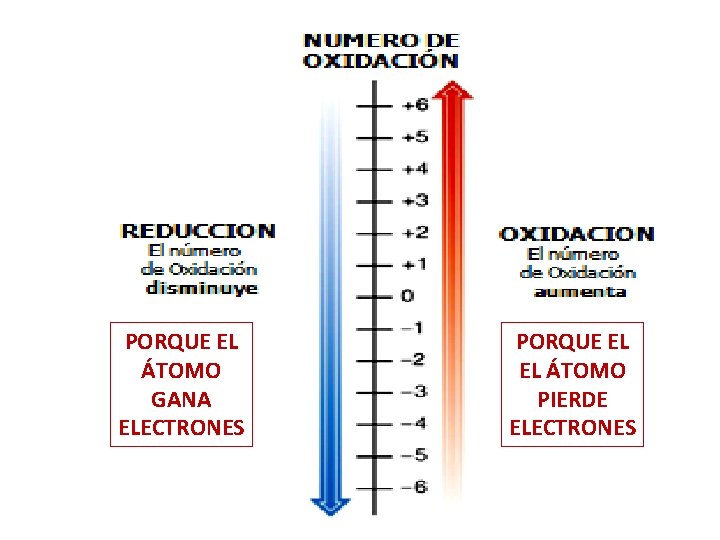
PORQUE EL ÁTOMO GANA ELECTRONES PORQUE EL EL ÁTOMO PIERDE ELECTRONES 5

6
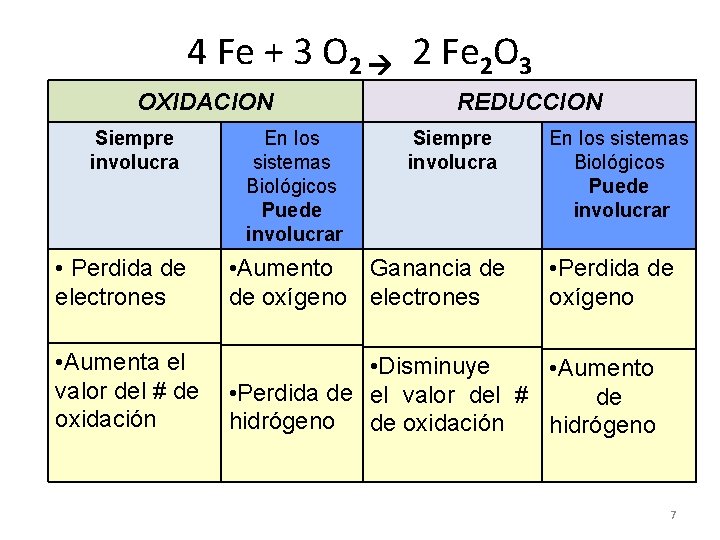
4 Fe + 3 O 2 2 Fe 2 O 3 OXIDACION Siempre involucra En los sistemas Biológicos Puede involucrar REDUCCION Siempre involucra En los sistemas Biológicos Puede involucrar • Perdida de electrones • Aumento Ganancia de de oxígeno electrones • Perdida de oxígeno • Aumenta el valor del # de oxidación • Disminuye • Aumento • Perdida de el valor del # de hidrógeno de oxidación hidrógeno 7

TODA REACCIÓN REDOX PRESENTA LOS AGENTES OXIDANTE Y REDUCTOR AGENTE OXIDANTE Provoca la reducción de Provoca la oxidación de otra sustancia. Es el reactivo que contiene al elemento que se oxida. SOLO se que se reduce. SOLO se encuentra en los reactivos. Al H 2 SO 4 8

Procedimiento para balancear por el método REDOX 1. Asignar el # de oxidación a cada reactivo y producto. 2. Observar que átomos cambiaron. 3. Determinar quién se oxidó y quién se redujo y de cuantas unidades de electrones fue el cambió de c/u. 4. Colocar estos cambios como coeficientes a c/u pero cruzados. El cambio del oxidado será coeficiente del que se redujo. El cambio del reducido será coeficiente del oxidado. 5. SI SE PUEDE, SIMPLIFICARLOS ANTES DE SEGUIR. 9

7. Balancear el resto de la ecuación por tanteo siguiendo el orden: Metales, no-metales, H y O. 8. Comprobación de la igualdad R = P El AGENTE REDUCTOR Y OXIDANTE se buscan del lado de los REACTIVOS. 9. # TOTAL DE ELECTRONES TRANSFERIDOS (se calcula en la ecuación ya balanceada). Es el total de electrones que se ganaron o que se perdieron durante la reacción. Siempre se deben multiplicar por su subíndice o por su coeficiente. Total # e de reducción= Total # e de oxidación 10
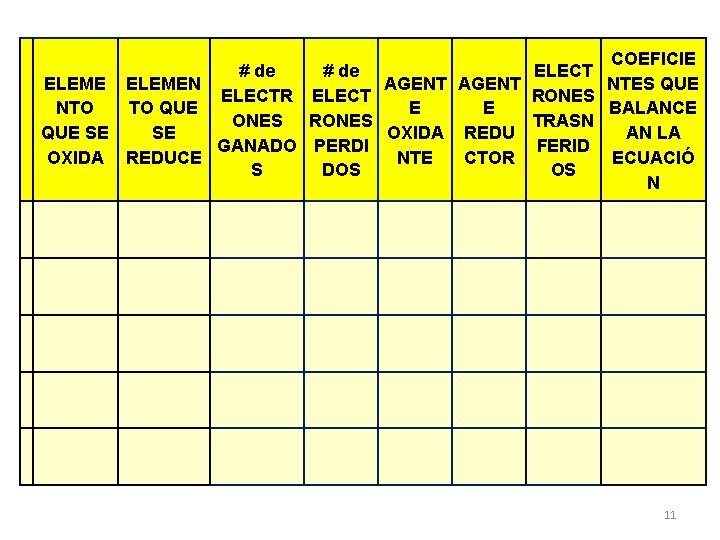
COEFICIE # de ELECT ELEMEN AGENT NTES QUE ELECTR ELECT RONES NTO TO QUE E E BALANCE ONES RONES TRASN QUE SE SE OXIDA REDU AN LA GANADO PERDI FERID OXIDA REDUCE NTE CTOR ECUACIÓ S DOS OS N 11
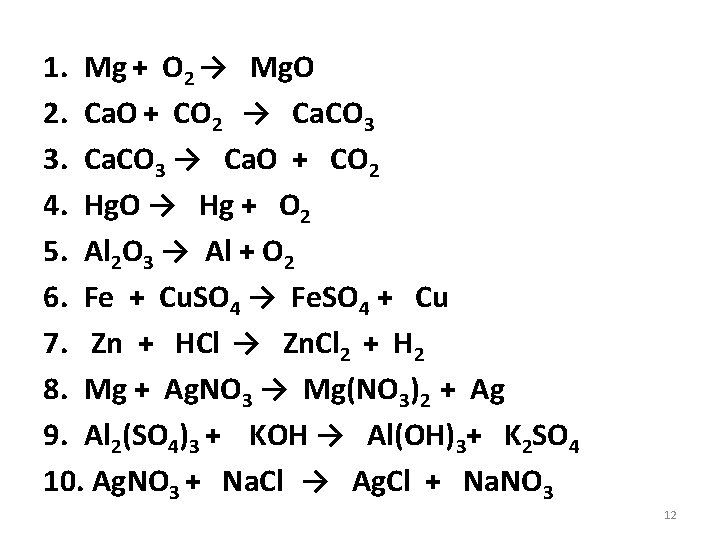
1. Mg + O 2 → Mg. O 2. Ca. O + CO 2 → Ca. CO 3 3. Ca. CO 3 → Ca. O + CO 2 4. Hg. O → Hg + O 2 5. Al 2 O 3 → Al + O 2 6. Fe + Cu. SO 4 → Fe. SO 4 + Cu 7. Zn + HCl → Zn. Cl 2 + H 2 8. Mg + Ag. NO 3 → Mg(NO 3)2 + Ag 9. Al 2(SO 4)3 + KOH → Al(OH)3+ K 2 SO 4 10. Ag. NO 3 + Na. Cl → Ag. Cl + Na. NO 3 12
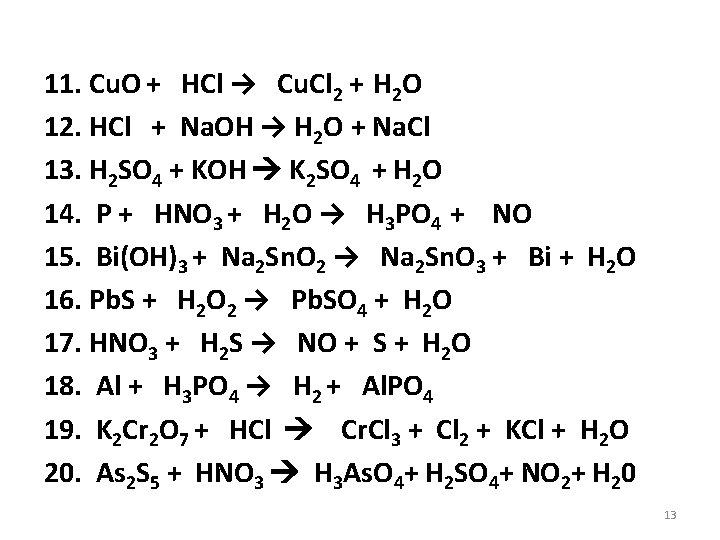
11. Cu. O + HCl → Cu. Cl 2 + H 2 O 12. HCl + Na. OH → H 2 O + Na. Cl 13. H 2 SO 4 + KOH K 2 SO 4 + H 2 O 14. P + HNO 3 + H 2 O → H 3 PO 4 + NO 15. Bi(OH)3 + Na 2 Sn. O 2 → Na 2 Sn. O 3 + Bi + H 2 O 16. Pb. S + H 2 O 2 → Pb. SO 4 + H 2 O 17. HNO 3 + H 2 S → NO + S + H 2 O 18. Al + H 3 PO 4 → H 2 + Al. PO 4 19. K 2 Cr 2 O 7 + HCl Cr. Cl 3 + Cl 2 + KCl + H 2 O 20. As 2 S 5 + HNO 3 H 3 As. O 4+ H 2 SO 4+ NO 2+ H 20 13
- Slides: 13