SEMANA 29 AMINOCIDOS Y PEPTIDOS Licenciada Sofa Tobas
SEMANA 29 AMINOÁCIDOS Y PEPTIDOS Licenciada Sofía Tobías de Rodríguez

AMINOÁCIDOS Los aminoácidos son los bloques constructores de las proteínas. Existen 20 aminoácidos que se encuentran comúnmente en las proteínas humanas. Alfa Aminoácidos: Son moléculas con un grupo amino en carbono adyacente al grupo carboxilo, (carbono α) a excepción de prolina e hidroxiprolina.
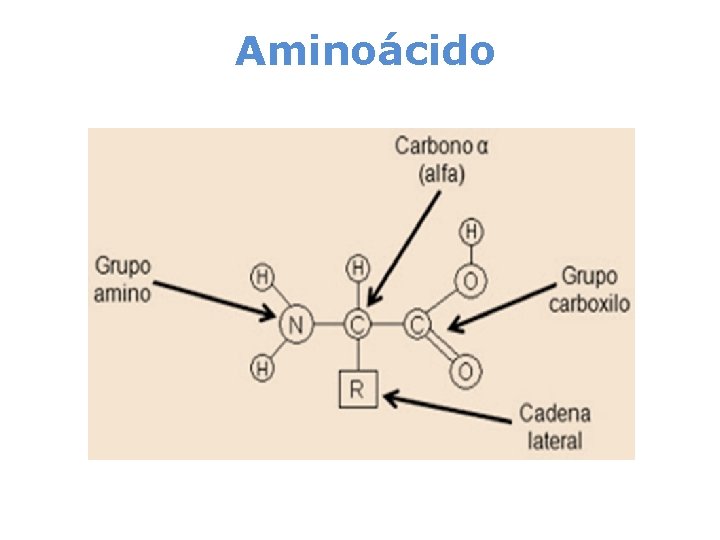
Aminoácido

Los aminoácidos se conocen exclusivamente por sus nombres comunes, con frecuencia el nombre indica algo acerca del aminoácido. Sus nombres UIQPA resultan difíciles. Aminoácido Origen del nombre Asparagina Aislado del jugo de espárrago. Glicina Aislado de la gelatina. Se le dio ése nombre por su sabor dulce. Glykos= dulce. Cada aminoácido tiene una abreviatura de 3 letras (en la mayor parte las tres primeras del nombre), puede usarse también una sola letra.
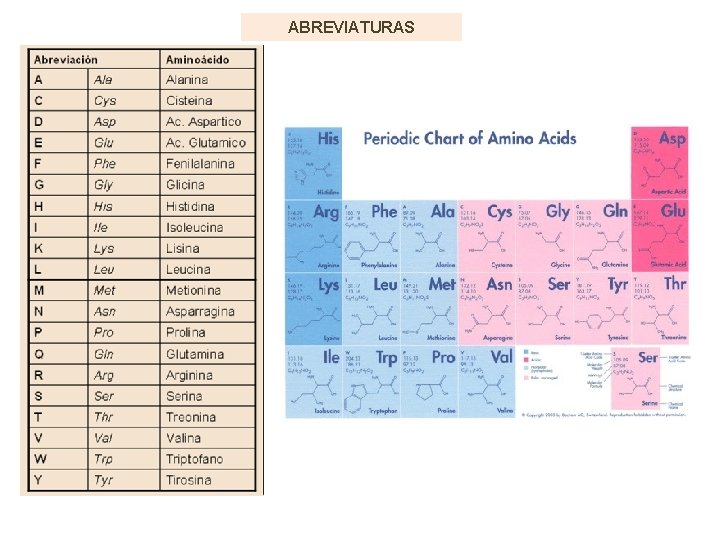
ABREVIATURAS
FUENTES
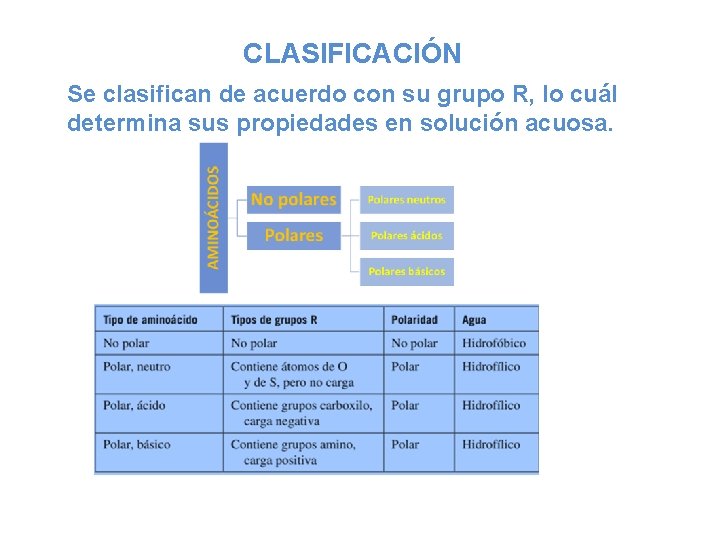
CLASIFICACIÓN Se clasifican de acuerdo con su grupo R, lo cuál determina sus propiedades en solución acuosa.
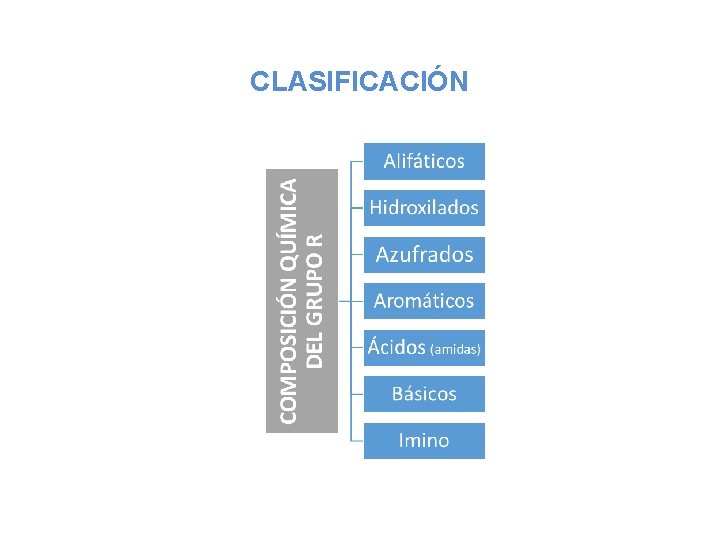
CLASIFICACIÓN
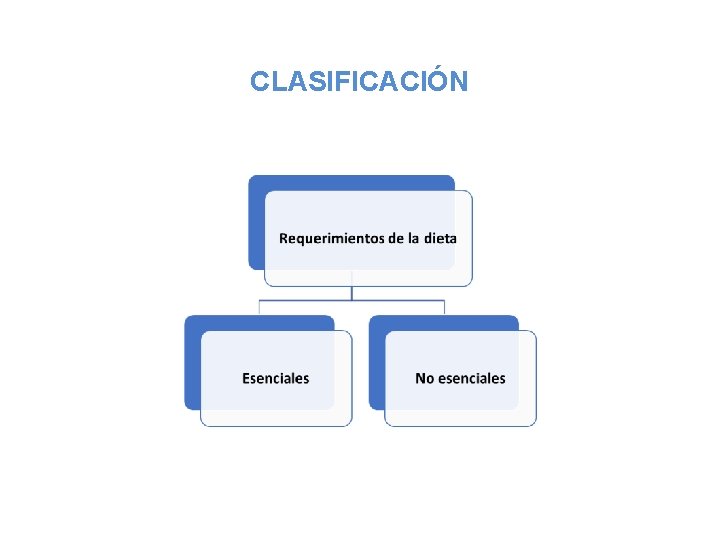
CLASIFICACIÓN

Polares y no Polares


Composición Química del Grupo R ALIFATICOS, APOLARES
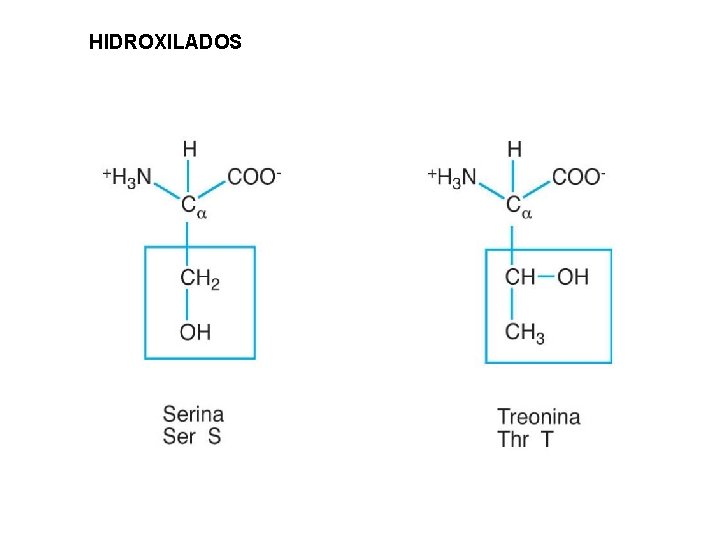
HIDROXILADOS
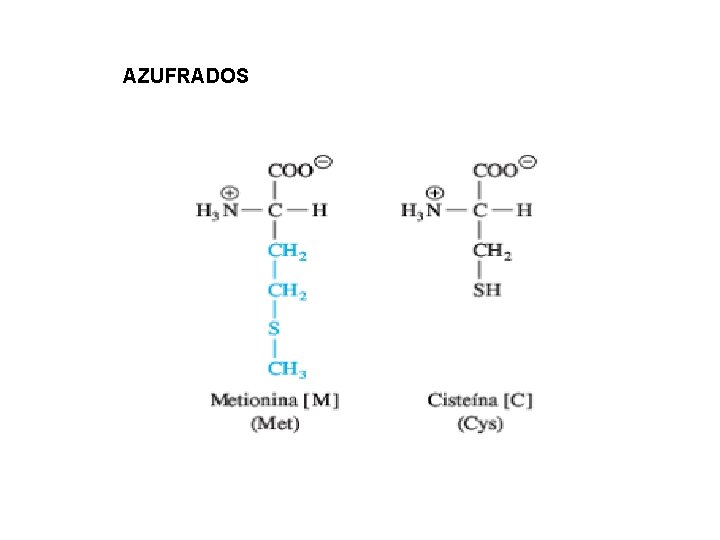
AZUFRADOS
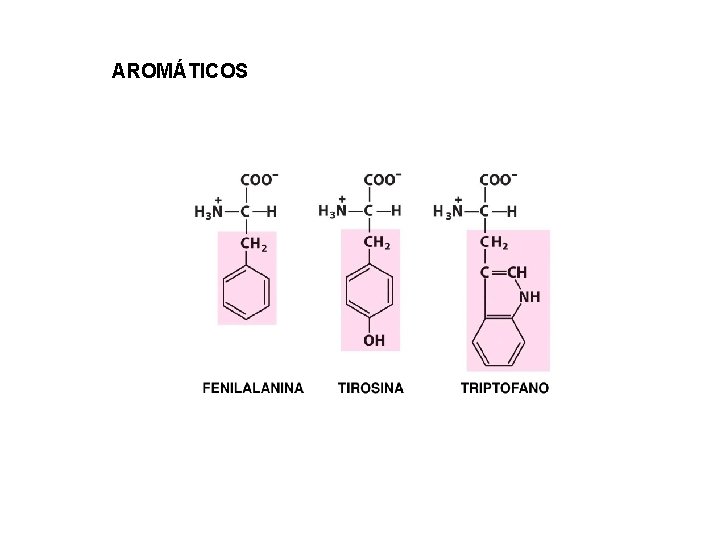
AROMÁTICOS
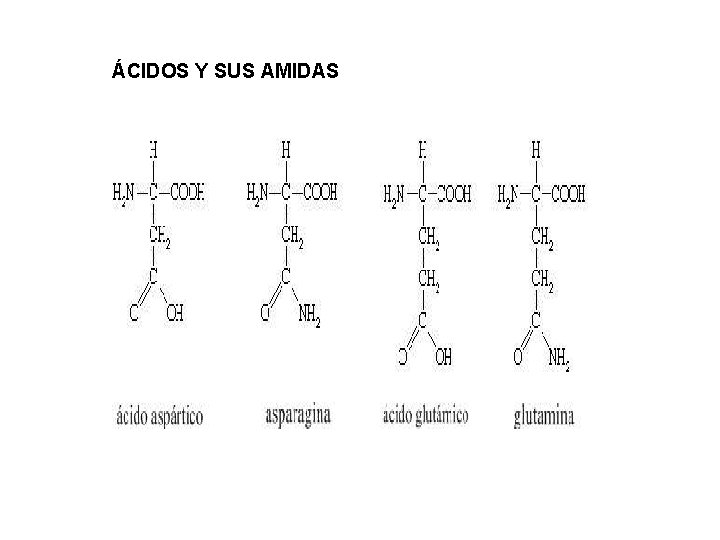
ÁCIDOS Y SUS AMIDAS



Aminoácidos Esenciales

ISOMERÍA ÓPTICA El carbono alfa de los aminoácidos tiene cuatro grupos diferentes , por lo tanto, es un átomo de carbono quiral, es ópticamente activo, por lo que los aminoácidos presentan imágenes especulares no superponibles o enantiómeros produciendo los D y L aminoácidos.

Configuración D y L

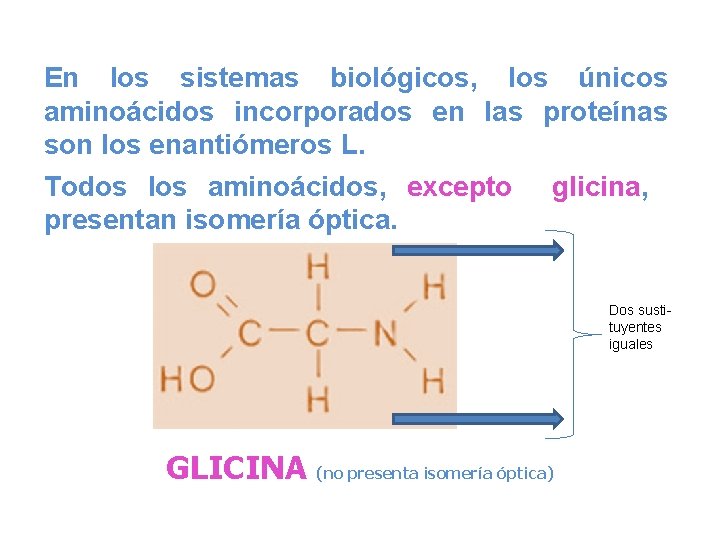
En los sistemas biológicos, los únicos aminoácidos incorporados en las proteínas son los enantiómeros L. Todos los aminoácidos, excepto glicina, presentan isomería óptica. Dos sustituyentes iguales GLICINA (no presenta isomería óptica)

Propiedades Físicas: Los aminoácidos son sólidos cristalinos, incoloros, no volátiles. Solubles en agua e insolubles en solventes orgánicos. Sus propiedades son similares a las de las sales inorgánicas. Por lo tanto en estado cristalino o disueltos en agua se les asigna una estructura iónica dipolar, la cuál se denomina sal interna o switterion Amino protonado y Carboxilo desprotonado

Los aminoácidos pueden aceptar o ceder protones al medio, dependiendo del p. H de la disolución en la que se encuentren. Si la disolución es ácida, los aminoácidos aceptan protones y se comportan como una base. Si la disolución es básica, ceden protones y se comportan como un ácido. Por tener este comportamiento, se dice que los aminoácidos son anfóteros.
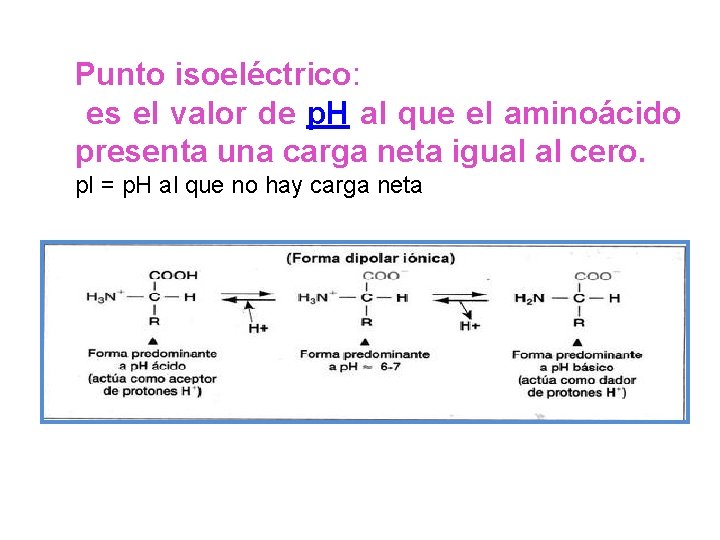
Punto isoeléctrico: es el valor de p. H al que el aminoácido presenta una carga neta igual al cero. p. I = p. H al que no hay carga neta


Ejercicio:

Un aminoácido que existe como un ion dipolar es neutro porque las cargas positiva y negativa se cancelan. Para valores de p. H altos, los aminoácidos se cargan negativamente, obtienen la forma aniónica. Para valores de p. H bajos, los aminoácidos se cargan positivamente, obtienen la forma catiónica. En solución se establece un equilibrio entre las tres formas.

Peptidos Los péptidos se forman por la unión de aminoácidos mediante un enlace peptídico, enlace covalente que se establece entre el grupo carboxilo de un aminoácido y el grupo amino del siguiente, dando lugar al desprendimiento de una molécula de agua.

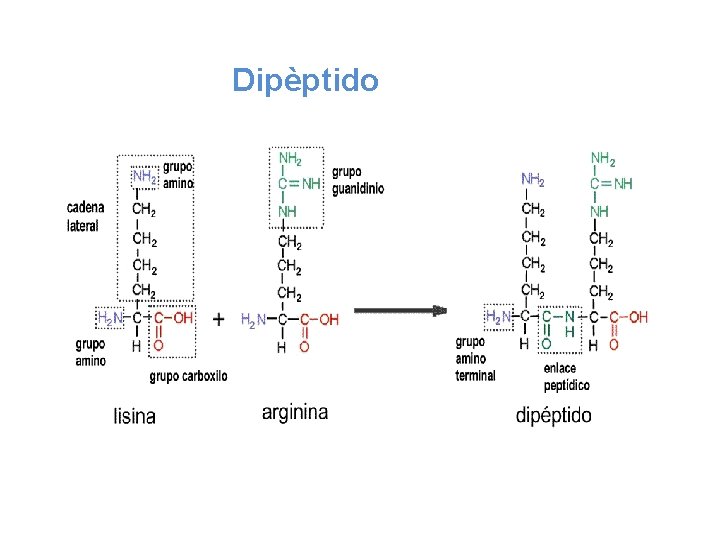
Dipèptido

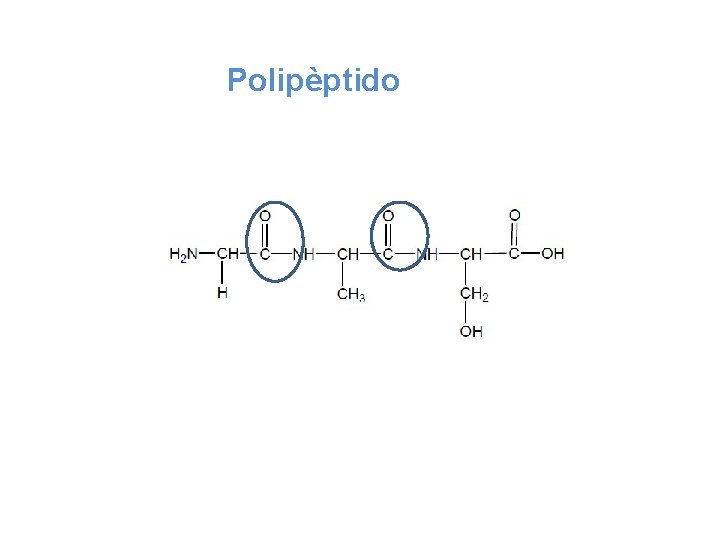
Polipèptido




La secuencia de aminoácidos se puede indicar también, dando el nombre del amino ácido (abreviatura) seguido por un guión. Se inicia a la izquierda (N-terminal) y se finaliza a la derecha (C- terminal). N-Ala-Lis-Fen-Gli-Asp-Trp-Ser-Arg-COO-
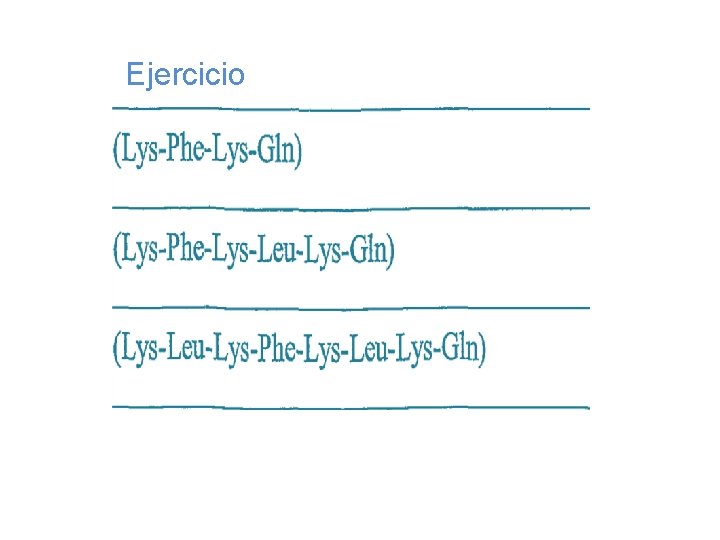
Ejercicio

N-Ala-Lis-Fen-Gli-Asp-Trp-Ser-Arg-COO-¿Cuál es el a. a. N-terminal? -¿Cuál es el a. a C- terminal? Dependiendo del número de a. a que se unen, se le colocará el prefijo al peptido: N-Ala-Val-Leu-COO- (Tripéptido) N-Leu-His-COO(Dipéptido)

Péptidos de Importancia Biológica: Entre las funciones biológicas más importantes que realizan los péptidos podemos destacar las siguientes: Agentes Vasoactivos: angiotensina II El agente hipertensor más potente, un octapéptido.
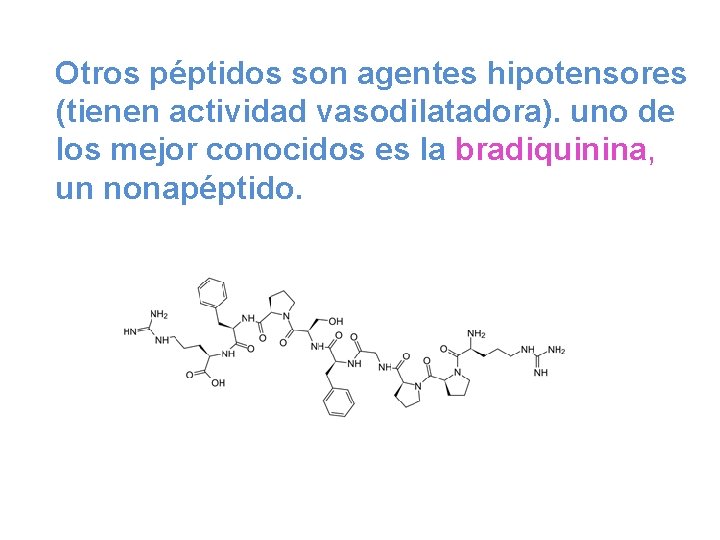
Otros péptidos son agentes hipotensores (tienen actividad vasodilatadora). uno de los mejor conocidos es la bradiquinina, un nonapéptido.
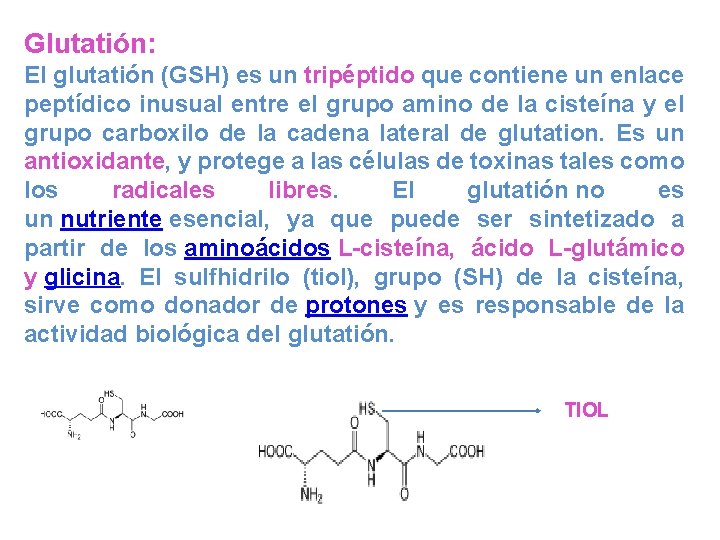
Glutatión: El glutatión (GSH) es un tripéptido que contiene un enlace peptídico inusual entre el grupo amino de la cisteína y el grupo carboxilo de la cadena lateral de glutation. Es un antioxidante, y protege a las células de toxinas tales como los radicales libres. El glutatión no es un nutriente esencial, ya que puede ser sintetizado a partir de los aminoácidos L-cisteína, ácido L-glutámico y glicina. El sulfhidrilo (tiol), grupo (SH) de la cisteína, sirve como donador de protones y es responsable de la actividad biológica del glutatión. TIOL


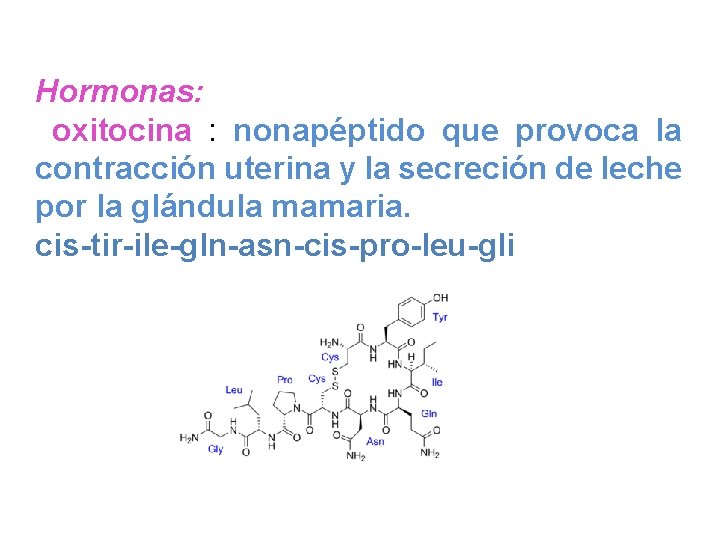
Hormonas: oxitocina : nonapéptido que provoca la contracción uterina y la secreción de leche por la glándula mamaria. cis-tir-ile-gln-asn-cis-pro-leu-gli
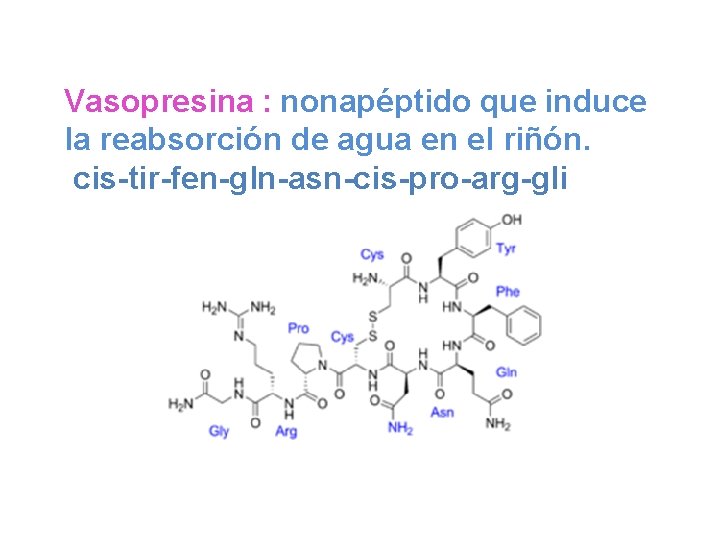
Vasopresina : nonapéptido que induce la reabsorción de agua en el riñón. cis-tir-fen-gln-asn-cis-pro-arg-gli
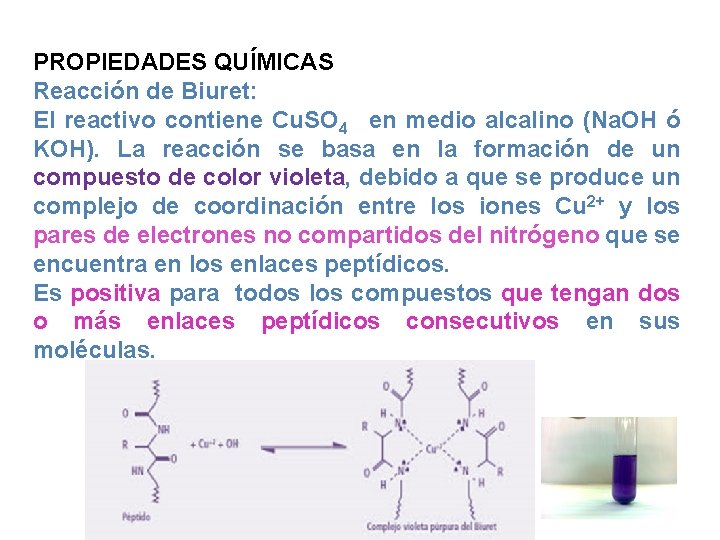
PROPIEDADES QUÍMICAS Reacción de Biuret: El reactivo contiene Cu. SO 4 en medio alcalino (Na. OH ó KOH). La reacción se basa en la formación de un compuesto de color violeta, debido a que se produce un complejo de coordinación entre los iones Cu 2+ y los pares de electrones no compartidos del nitrógeno que se encuentra en los enlaces peptídicos. Es positiva para todos los compuestos que tengan dos o más enlaces peptídicos consecutivos en sus moléculas.
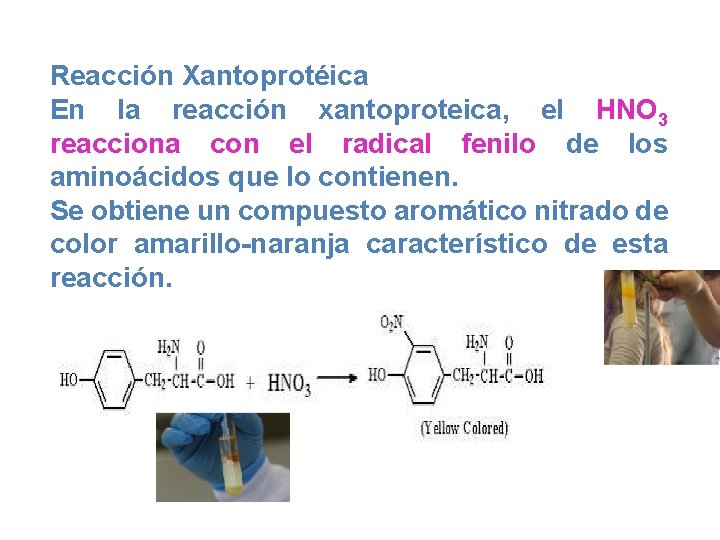
Reacción Xantoprotéica En la reacción xantoproteica, el HNO 3 reacciona con el radical fenilo de los aminoácidos que lo contienen. Se obtiene un compuesto aromático nitrado de color amarillo-naranja característico de esta reacción.

Prueba de Ninhidrina: Esta prueba es positiva tanto para proteínas como para aminoácidos. La ninhidrina reacciona con todos los α-aminoácidos dando lugar a la formación de un complejo color purpura cuyo p. H se encuentra entre 4 y 8. Solamente prolina e hidroxi-prolina dan lugar a complejos de color amarillo. En aquellos casos donde la prueba de Biuret es negativa y la de Ninhidrina es positiva, indica que no hay proteínas, pero si hay aminoácidos libres. Aplicación: Ésta prueba es comúnmente utilizada en química forense para detectar huellas dactilares, debido a que en dichas huellas quedan restos de aminoácidos de proteínas que pueden reaccionar dando el color característico.
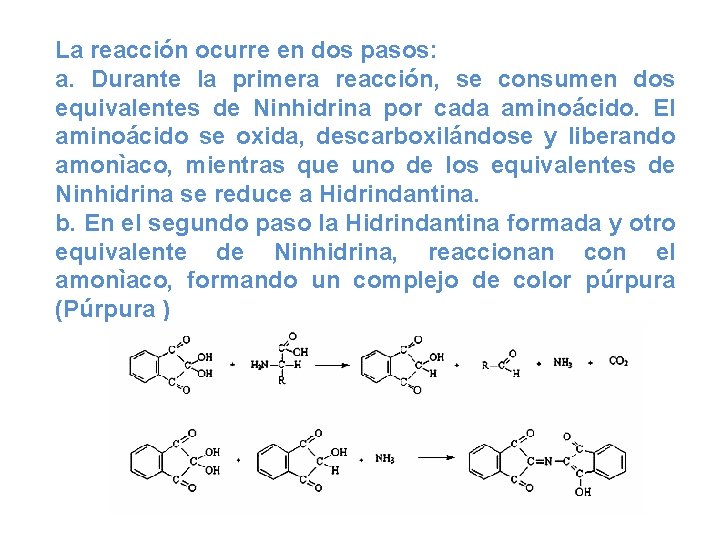
La reacción ocurre en dos pasos: a. Durante la primera reacción, se consumen dos equivalentes de Ninhidrina por cada aminoácido. El aminoácido se oxida, descarboxilándose y liberando amonìaco, mientras que uno de los equivalentes de Ninhidrina se reduce a Hidrindantina. b. En el segundo paso la Hidrindantina formada y otro equivalente de Ninhidrina, reaccionan con el amonìaco, formando un complejo de color púrpura (Púrpura )

Prueba de Sulfuro: Es una prueba positiva para aminoácidos y proteínas que contienen azufre. Al calentar el aminoácido en medio fuertemente alcalino, el azufre presente reacciona para formar sulfuros. Este sulfuro puede detectarse por la formación de un precipitado (coloración) negro/café de sulfuro de plomo por la adición de acetato de plomo. R-SH + 2 Na. OH → ROH + Na 2 S + H 2 O Na 2 S + Pb (CH 3 COO-)2 → 2 CH 3 COONa + Pb. S precipitado negro/café

FIN
- Slides: 53