Semana 23 AMINAS QUMICA 2020 1 SEMANA 23









- Slides: 24

Semana 23 AMINAS QUÍMICA 2020 1

SEMANA 23 AMINAS Definición, representación general. Clasificación. Nomenclatura: Común y UIQPA Propiedades físicas Propiedades químicas: - Carácter básico: Reacción de formación de sales. Sales de amonio cuaternarias: Estructura y nombre. Propiedades (ver libro de texto) Aminas heterocíclicas: - Estructura de: - Imidazol, pirrolidina, piperidina, pirimidina y purina. Identificación del grupo Amino en alcaloides: - Nicotina, Morfina, Atropina, Codeína y cafeína. Neurotransmisores amino: - Estructura y función de: Acetilcolina, Norepinefrina e Histamina. Aplicación de los conceptos en la salud. Lecturas en libro de texto. - La Química en la Salud: - “Porfirina, bilirrubina e ictericia” - “Síntesis de medicamentos” 2

AMINAS • Son compuestos orgánicos que contienen N son compuestos básicos (débiles, se neutralizan con ácidos). • Son derivados del NH 3 (amoníaco) en donde 1, 2 o los 3 H se sustituyen por radicales alquilo (R) ó arilo (-Ar). 3

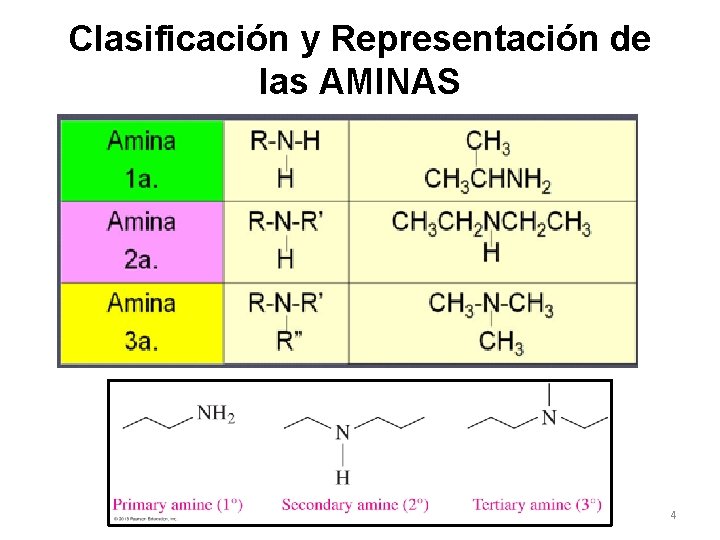
Clasificación y Representación de las AMINAS Se dividen en 3 clases según el número de grupos alquilo ó arilo unidos al nitrógeno. 4

Nomenclatura de Aminas Primarias NH 2 R Solo uno de sus H se sustituyó por un R o Ar. • Común: se nombra el radical unido al Nitrógeno terminando con la palabra amina. Ej: NH 2 CH 2 CH 3 propilamina • UIQPA: la cadena más larga será la que contenga al NH 2. Se nombra como alcano cambiando la o por la terminación amina, indicando la posición del grupo amino NH 2 CH 2 CH 3 1 -propanamina 5

Nomenclatura de AMINAS Secundarias (R-NHR’) = con 2 H sustituídos y Terciarias (R-NR’R’’) = con los 3 H sustituídos. COMÚN: Se nombran los radicales unidos al N en orden alfabético, terminando con la palabra amina. UIQPA: la cadena más larga será la que contenga al -NHR o al -NRR. Se nombra como alcano cambiando la o por la terminación amina, indicando la posición del grupo amino -N- , ese será el nombre básico. Para nombrar los radicales unidos al Nitrógeno, se antepone una o dos N- y se nombran cada radical en orden alfabético y al final el nombre básico. 6

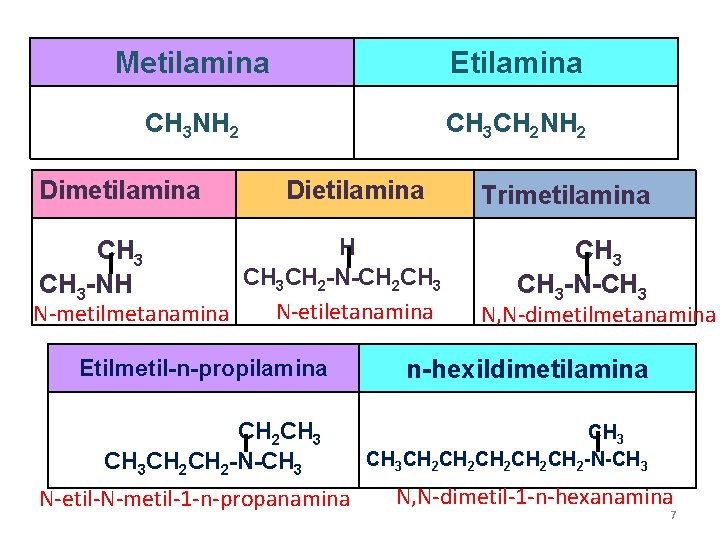
Metilamina Etilamina CH 3 NH 2 CH 3 CH 2 NH 2 Dimetilamina Dietilamina H CH 3 CH 2 -N-CH 2 CH 3 N-etiletanamina N-metilmetanamina CH 3 -NH Trimetilamina CH 3 -N-CH 3 N, N-dimetilmetanamina Etilmetil-n-propilamina n-hexildimetilamina CH 2 CH 3 CH 2 -N-CH 3 CH 2 CH 2 CH 2 -N-CH 3 N-etil-N-metil-1 -n-propanamina N, N-dimetil-1 -n-hexanamina 7

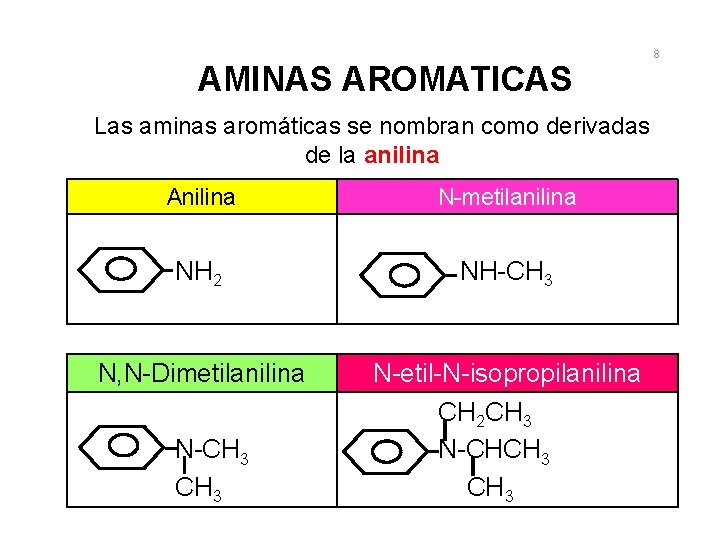
AMINAS AROMATICAS Las aminas aromáticas se nombran como derivadas de la anilina Anilina N-metilanilina NH 2 NH-CH 3 N, N-Dimetilanilina N-etil-N-isopropilanilina CH 2 CH 3 N-CHCH 3 N-CH 3 8

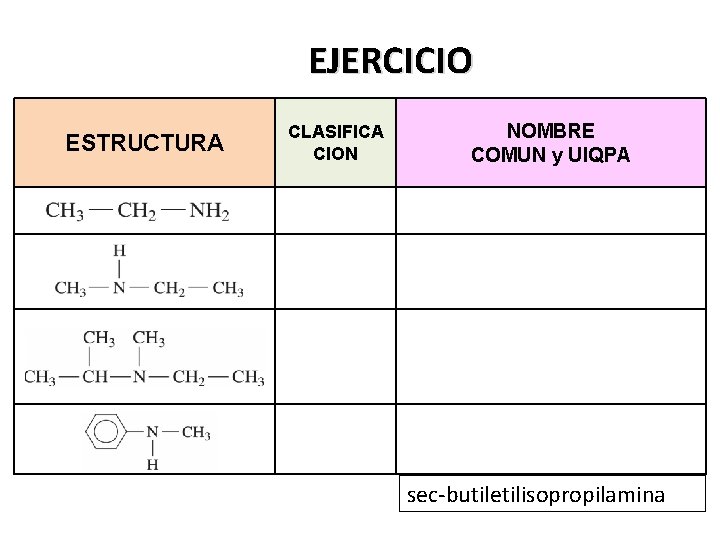
EJERCICIO ESTRUCTURA CLASIFICA CION NOMBRE COMUN y UIQPA sec-butiletilisopropilamina

Propiedades Físicas de las Aminas • Se caracterizan por sus olores penetrantes parecido al del amoníaco. • La dimetilamina y la trimetilamina son gaseosas y tienen olor a pescado. • Otras dan el olor a la carne putrefacta (animal muerto ó cadáver humano) H 2 NCH 2 CH 2 NH 2 (Putrescina) H 2 NCH 2 CH 2 CH 2 NH 2 (Cadaverina) 10

Las aminas 1 as. y 2 as. Tienen H, por lo que forman puentes de H entre sus moléculas y con el agua. Las aminas 3 as. No tienen H, no forman puentes de H por lo que son menos solubles que 1 as. y 2 as. Los puntos de ebullición de las 1 as. es mayor que las 2 as. y éstas mayor que las 3 as. Las aminas de 1 a 6 C son solubles en agua. Las aminas 1 as de 3 a 11 C son líquidas. Tienen puntos de ebullición mayores que alcanos pero menores que alcoholes y que ácidos. 11

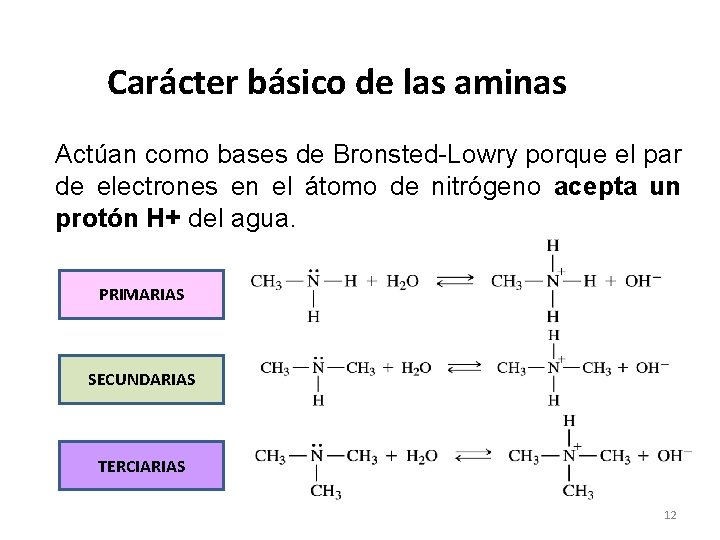
Carácter básico de las aminas Actúan como bases de Bronsted-Lowry porque el par de electrones en el átomo de nitrógeno acepta un protón H+ del agua. PRIMARIAS SECUNDARIAS TERCIARIAS 12

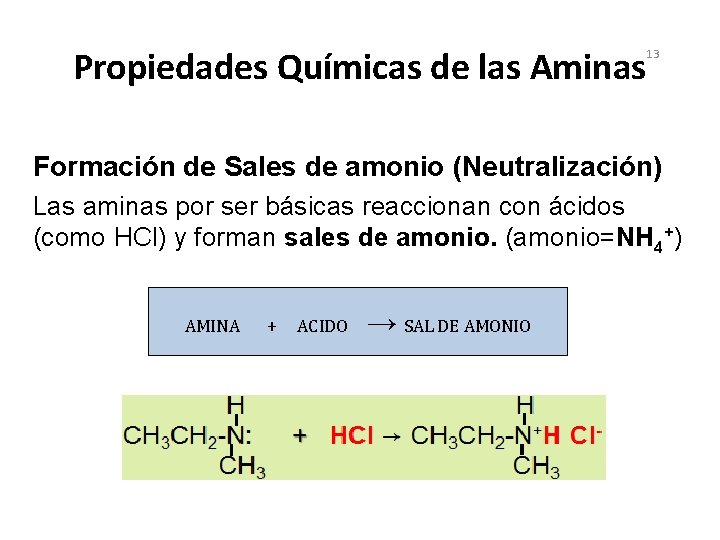
Propiedades Químicas de las Aminas 13 Formación de Sales de amonio (Neutralización) Las aminas por ser básicas reaccionan con ácidos (como HCl) y forman sales de amonio. (amonio=NH 4+) AMINA + ACIDO → SAL DE AMONIO

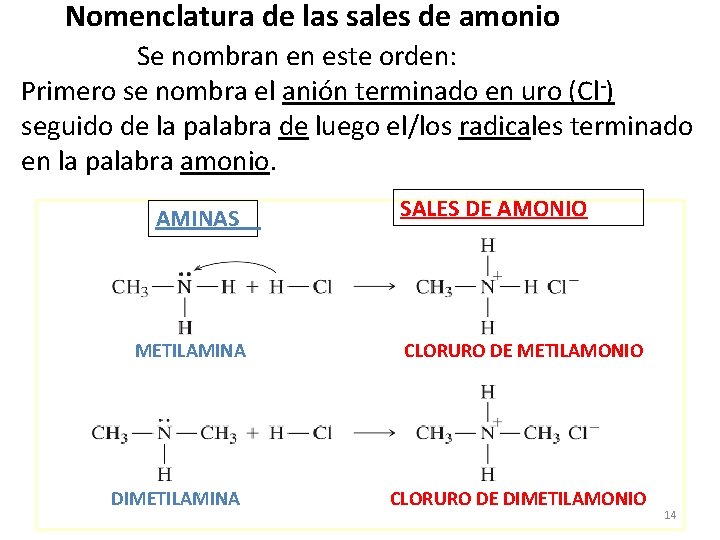
Nomenclatura de las sales de amonio Se nombran en este orden: Primero se nombra el anión terminado en uro (Cl-) seguido de la palabra de luego el/los radicales terminado en la palabra amonio. AMINAS SALES DE AMONIO METILAMINA CLORURO DE METILAMONIO DIMETILAMINA CLORURO DE DIMETILAMONIO 14

Sales de amonio cuaternarias Las sales de amonio cuaternarias se forman cuando el Nitrógeno se enlaza a 4 radicales (no tienen H). Cloruro de tetrametilamonio Colina 15

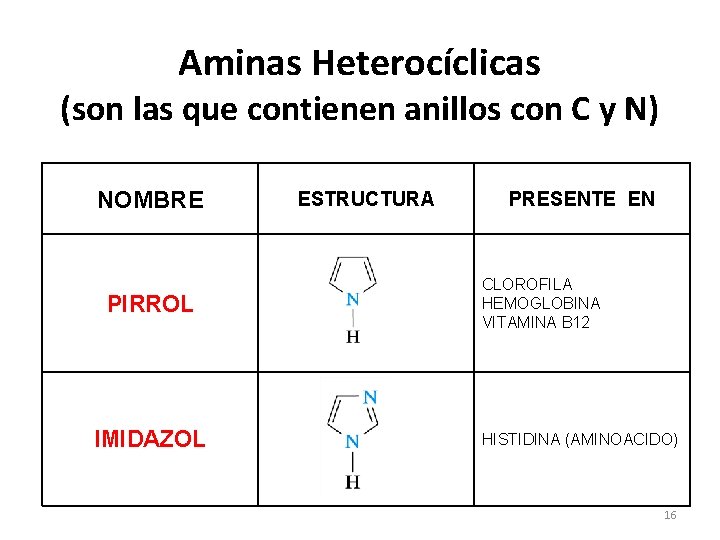
Aminas Heterocíclicas (son las que contienen anillos con C y N) NOMBRE PIRROL IMIDAZOL ESTRUCTURA PRESENTE EN CLOROFILA HEMOGLOBINA VITAMINA B 12 HISTIDINA (AMINOACIDO) 16

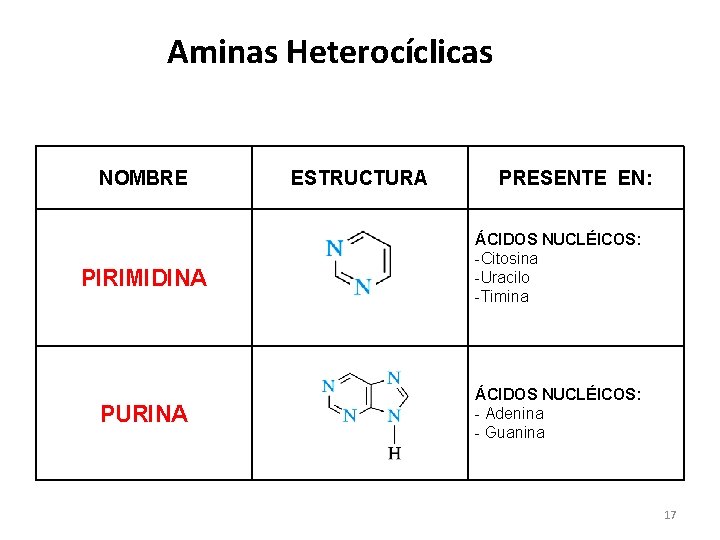
Aminas Heterocíclicas NOMBRE PIRIMIDINA PURINA ESTRUCTURA PRESENTE EN: ÁCIDOS NUCLÉICOS: -Citosina -Uracilo -Timina ÁCIDOS NUCLÉICOS: - Adenina - Guanina 17

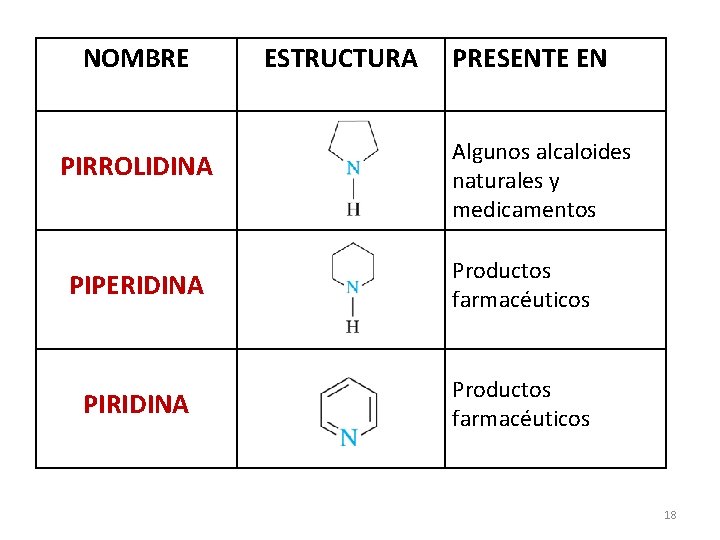
NOMBRE PIRROLIDINA ESTRUCTURA PRESENTE EN Algunos alcaloides naturales y medicamentos PIPERIDINA Productos farmacéuticos PIRIDINA Productos farmacéuticos 18

Importancia de las aminas 19 Gran cantidad de aminas se obtienen de la corteza, raíces, hojas, flores o frutos de varias plantas. Estas aminas con actividad fisiológica que se presentan en forma natural se denominan alcaloides Algunos ejemplos son: Nicotina, Morfina, Atropina, Codeína, Cafeína.

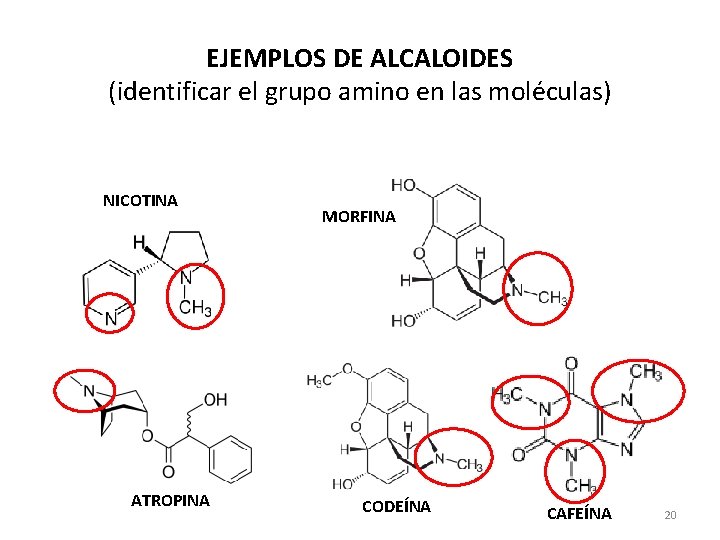
EJEMPLOS DE ALCALOIDES (identificar el grupo amino en las moléculas) NICOTINA ATROPINA MORFINA CODEÍNA CAFEÍNA 20

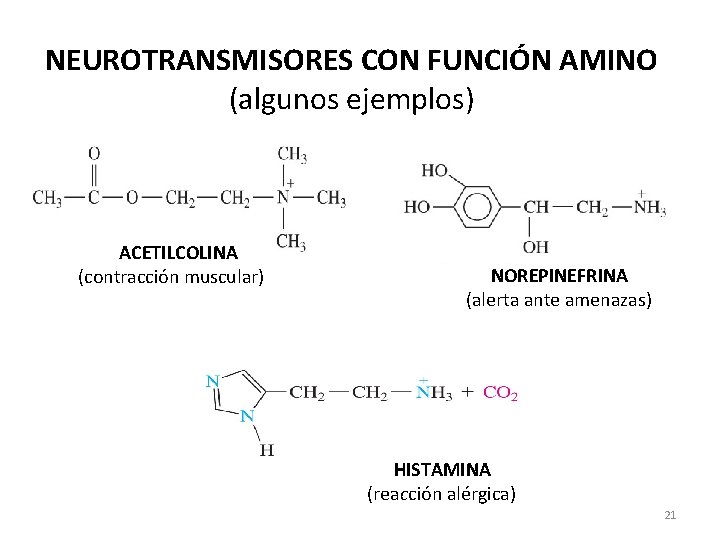
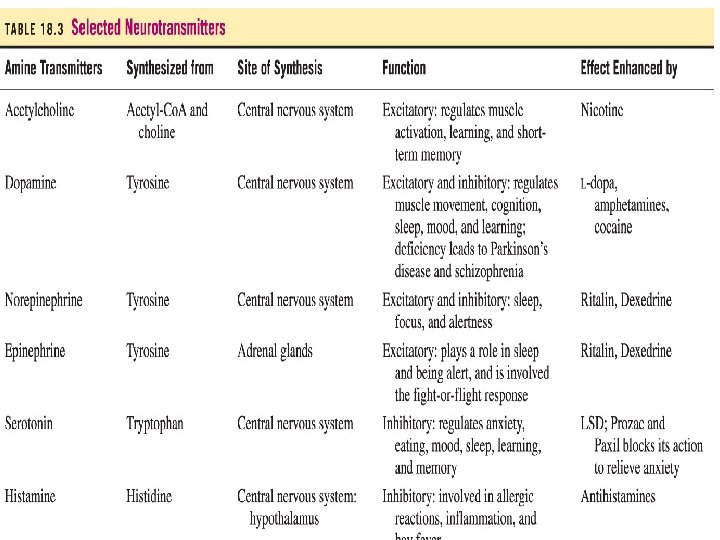
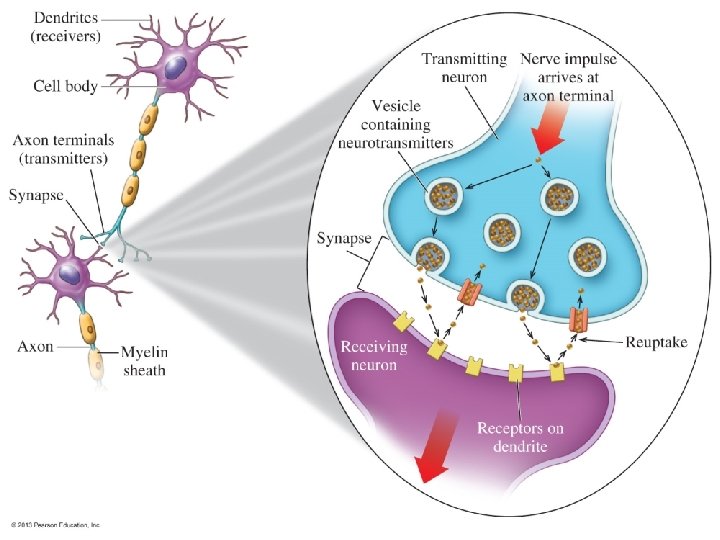
NEUROTRANSMISORES CON FUNCIÓN AMINO (algunos ejemplos) ACETILCOLINA (contracción muscular) NOREPINEFRINA (alerta ante amenazas) HISTAMINA (reacción alérgica) 21



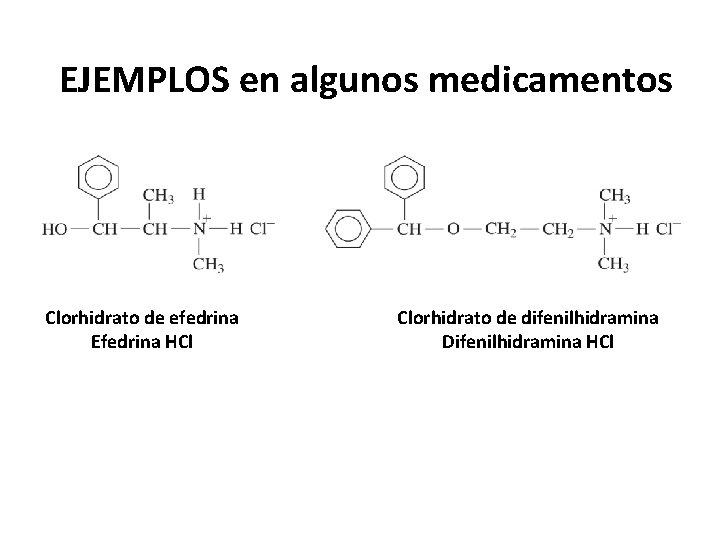
EJEMPLOS en algunos medicamentos Clorhidrato de efedrina Efedrina HCl Clorhidrato de difenilhidramina Difenilhidramina HCl