Semana 22 CIDOS CARBOXLICOS STERES Y AMIDAS QUMICA

Semana 22 ÁCIDOS CARBOXÍLICOS, ÉSTERES Y AMIDAS QUÍMICA 2016 1

ÁCIDOS CARBOXÍLICOS y sus DERIVADOS: ÉSTERES Y AMIDAS Ácidos Carboxílicos Definición, representación general y clasificación Nomenclatura UIQPA y Común (de 1 a 10 Carbonos) Estructura de ácidos dicarboxílicos: oxálico, malónico, succínico, adípico y pimélico. Estructura de ácido tricarboxílico: cítrico Propiedades físicas. Formación de dímeros. Carácter ácido Reacciones químicas: Formación de sales y Esterificación Aplicación de los conceptos en la salud y el ambiente Ésteres Definición y representación general. Nomenclatura UIQPA y Común. Propiedades físicas. Aplicación de los conceptos en la salud y el ambiente. (Salicilato de metilo uso e importancia) Amidas Definición, representación general. Clasificación. Nomenclatura UIQPA y Común. Aplicación de los conceptos en la salud y el ambiente Laboratorio: Ácidos carboxílicos y Esteres 2

ÁCIDOS CARBOXÍLICOS • Grupo funcional: carboxilo. Su nombre viene de las palabras CARBONILO e HIDROXILO. • Nombre: ÁCIDOS, porque liberan protones H+ (tienen propiedades de ácidos débiles). • Pueden ser alifáticos (-R) ó aromáticos (-Ar), mono, di, tricarboxílicos. O -C-OH -CO 2 H -COOH 3
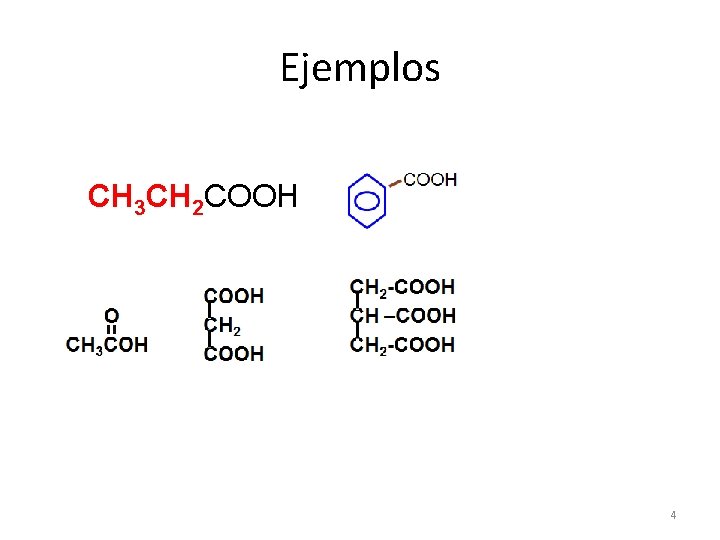
Ejemplos CH 3 CH 2 COOH 4
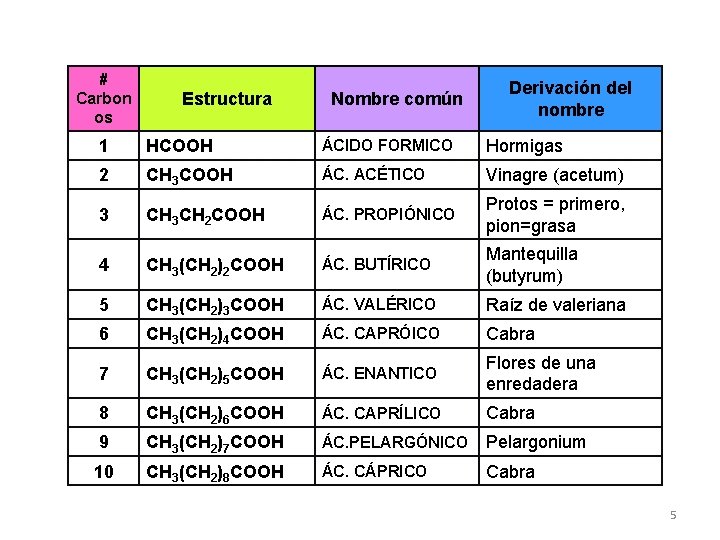
# Carbon os Estructura Nombre común Derivación del nombre 1 HCOOH ÁCIDO FORMICO Hormigas 2 CH 3 COOH ÁC. ACÉTICO Vinagre (acetum) 3 CH 3 CH 2 COOH ÁC. PROPIÓNICO Protos = primero, pion=grasa 4 CH 3(CH 2)2 COOH ÁC. BUTÍRICO Mantequilla (butyrum) 5 CH 3(CH 2)3 COOH ÁC. VALÉRICO Raíz de valeriana 6 CH 3(CH 2)4 COOH ÁC. CAPRÓICO Cabra 7 CH 3(CH 2)5 COOH ÁC. ENANTICO Flores de una enredadera 8 CH 3(CH 2)6 COOH ÁC. CAPRÍLICO Cabra 9 CH 3(CH 2)7 COOH ÁC. PELARGÓNICO Pelargonium 10 CH 3(CH 2)8 COOH ÁC. CÁPRICO Cabra 5
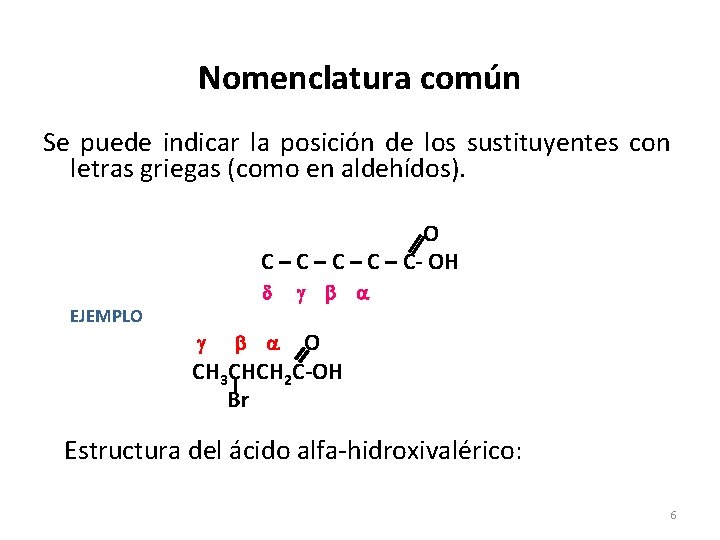
Nomenclatura común Se puede indicar la posición de los sustituyentes con letras griegas (como en aldehídos). O C – C – C- OH EJEMPLO O CH 3 CHCH 2 C-OH Br Estructura del ácido alfa-hidroxivalérico: 6

Nomenclatura UIQPA 1. La cadena mas larga que contenga el grupo carboxilo. 2. Se nombra como alcano agregando la terminación ico y anteponiendo la palabra ácido. 3. Si hay sustituyentes se aplican las reglas para alcanos. O C-C-C-OH 5 4 3 2 1 7
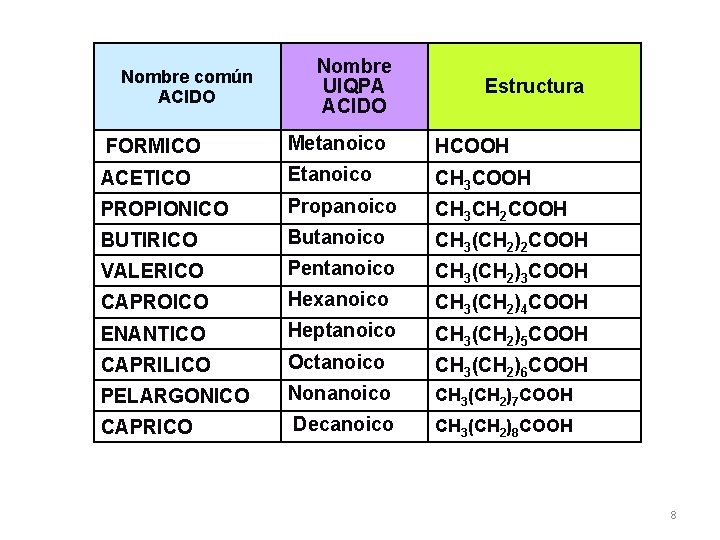
Nombre común ACIDO Nombre UIQPA ACIDO Estructura FORMICO Metanoico HCOOH ACETICO Etanoico CH 3 COOH PROPIONICO Propanoico CH 3 CH 2 COOH BUTIRICO Butanoico CH 3(CH 2)2 COOH VALERICO Pentanoico CH 3(CH 2)3 COOH CAPROICO Hexanoico CH 3(CH 2)4 COOH ENANTICO Heptanoico CH 3(CH 2)5 COOH CAPRILICO Octanoico CH 3(CH 2)6 COOH PELARGONICO Nonanoico CH 3(CH 2)7 COOH CAPRICO Decanoico CH 3(CH 2)8 COOH 8
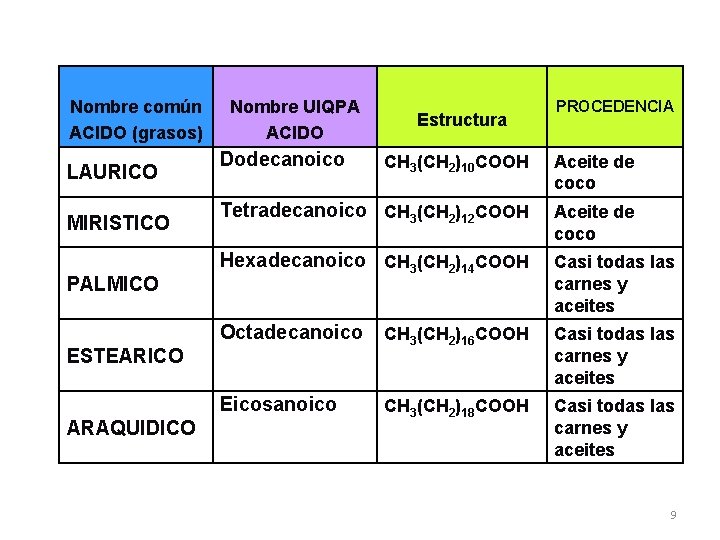
Nombre común ACIDO (grasos) LAURICO MIRISTICO PALMICO Nombre UIQPA ACIDO Dodecanoico PROCEDENCIA CH 3(CH 2)10 COOH Aceite de coco Tetradecanoico CH 3(CH 2)12 COOH Aceite de coco Hexadecanoico CH 3(CH 2)14 COOH Casi todas las carnes y aceites Octadecanoico CH 3(CH 2)16 COOH Casi todas las carnes y aceites Eicosanoico CH 3(CH 2)18 COOH Casi todas las carnes y aceites ESTEARICO ARAQUIDICO Estructura 9
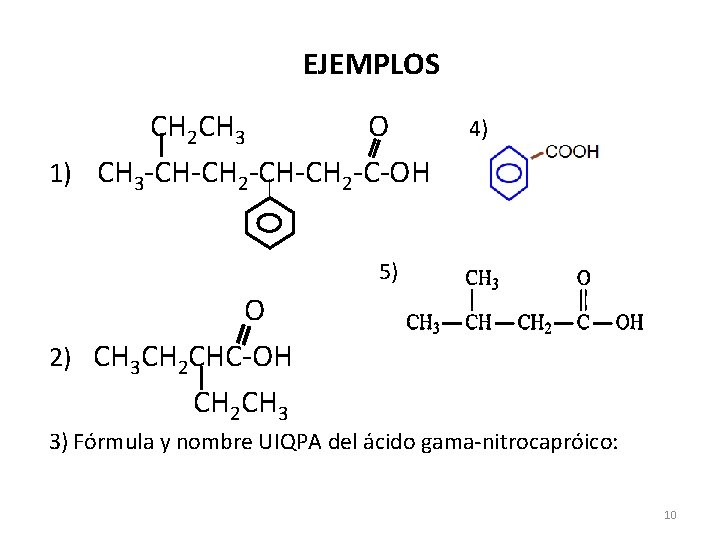
EJEMPLOS CH 2 CH 3 O 1) CH 3 -CH-CH 2 -C-OH 4) 5) O 2) CH 3 CH 2 CHC-OH CH 2 CH 3 3) Fórmula y nombre UIQPA del ácido gama-nitrocapróico: 10
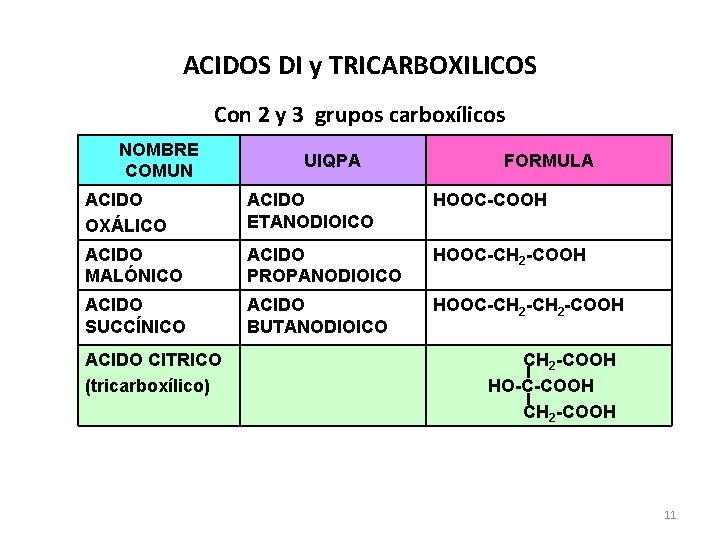
ACIDOS DI y TRICARBOXILICOS Con 2 y 3 grupos carboxílicos NOMBRE COMUN UIQPA FORMULA ACIDO OXÁLICO ACIDO ETANODIOICO HOOC-COOH ACIDO MALÓNICO ACIDO PROPANODIOICO HOOC-CH 2 -COOH ACIDO SUCCÍNICO ACIDO BUTANODIOICO HOOC-CH 2 -COOH ACIDO CITRICO (tricarboxílico) CH 2 -COOH HO-C-COOH CH 2 -COOH 11

PROPIEDADES FÍSICAS de ÁCIDOS CARBOXÍLICOS § Son los compuestos orgánicos más polares § Los homólogos de 1 a 4 C son solubles en agua. § Todos los ácidos son solubles en alcohol, benceno, CCl 4 y éter. § Los ácidos de 1 a 9 carbonos son líquidos, incoloros y olor desagradable. § Los ácidos de C 6, C 8 y C 10 tienen olores a cabra. § Los ácidos con mas de 10 átomos de carbono son sólidos cerosos y por su baja volatilidad son inodoros. Se les llama ácidos grasos porque forman parte de las grasas y aceites. 12

Los ácidos carboxílicos tienen puntos de ebullición mas elevados que los alcoholes, aldehídos y cetonas de igual peso molecular porque forman dímeros. DÍMEROS: son moléculas dobles que se mantienen unidas por medio de puentes de H intermoleculares que se forman entre los grupos C=O y los grupos OH de las dos moléculas. 13
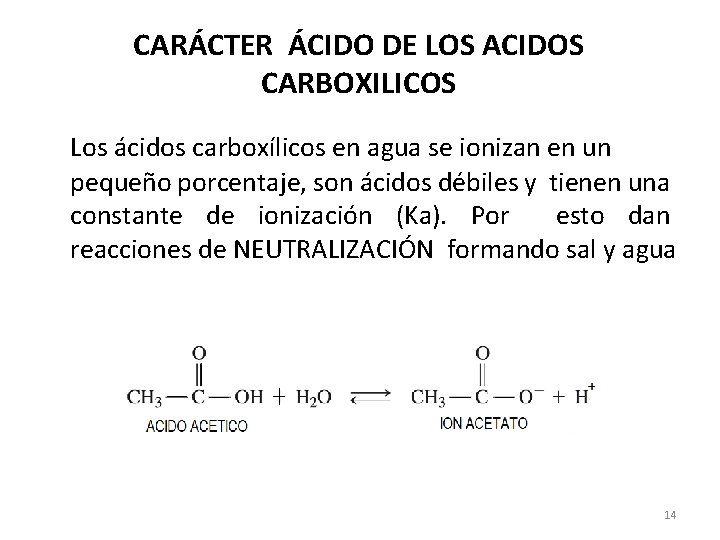
CARÁCTER ÁCIDO DE LOS ACIDOS CARBOXILICOS Los ácidos carboxílicos en agua se ionizan en un pequeño porcentaje, son ácidos débiles y tienen una constante de ionización (Ka). Por esto dan reacciones de NEUTRALIZACIÓN formando sal y agua 14
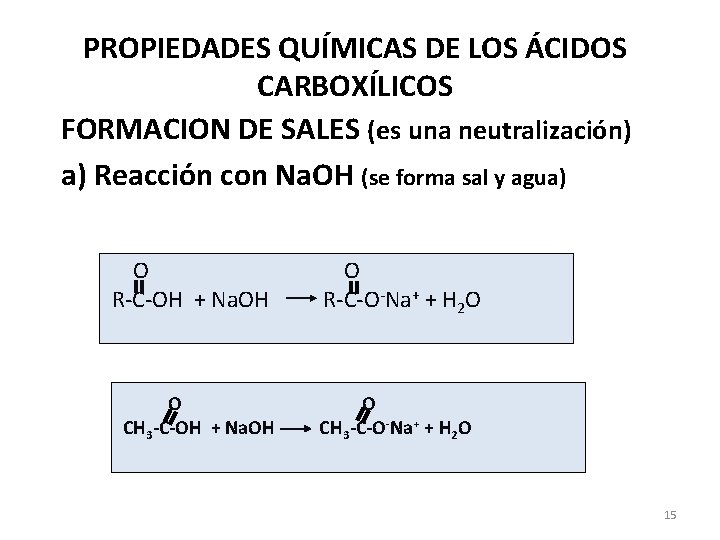
PROPIEDADES QUÍMICAS DE LOS ÁCIDOS CARBOXÍLICOS FORMACION DE SALES (es una neutralización) a) Reacción con Na. OH (se forma sal y agua) O R-C-OH + Na. OH O CH 3 -C-OH + Na. OH O R-C-O-Na+ + H 2 O O CH 3 -C-O-Na+ + H 2 O 15
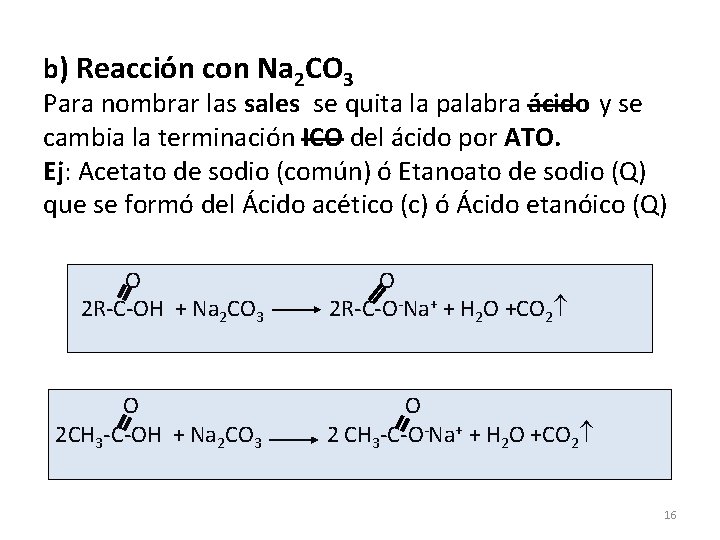
b) Reacción con Na 2 CO 3 Para nombrar las sales se quita la palabra ácido y se cambia la terminación ICO del ácido por ATO. Ej: Acetato de sodio (común) ó Etanoato de sodio (Q) que se formó del Ácido acético (c) ó Ácido etanóico (Q) O 2 R-C-OH + Na 2 CO 3 O 2 CH 3 -C-OH + Na 2 CO 3 O 2 R-C-O-Na+ + H 2 O +CO 2 CH 3 -C-O-Na+ + H 2 O +CO 2 16
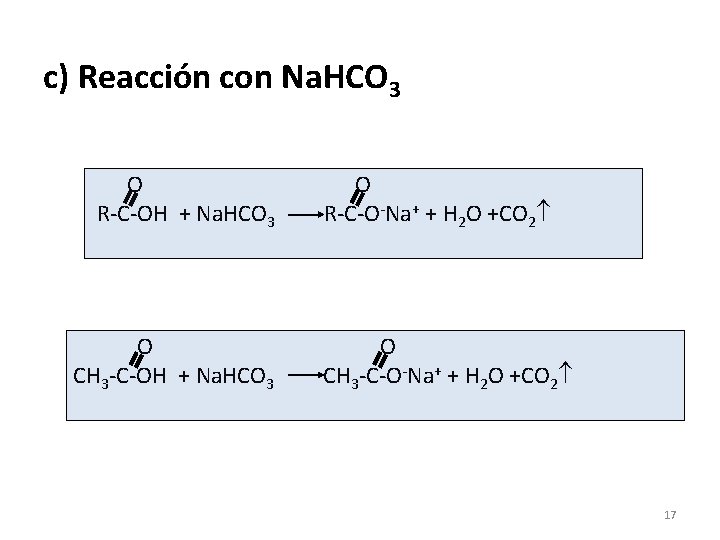
c) Reacción con Na. HCO 3 O R-C-OH + Na. HCO 3 O CH 3 -C-OH + Na. HCO 3 O R-C-O-Na+ + H 2 O +CO 2 O CH 3 -C-O-Na+ + H 2 O +CO 2 17
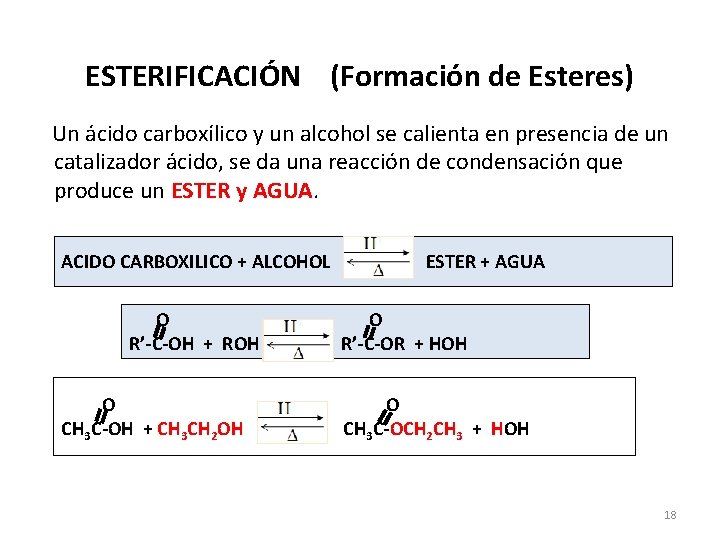
ESTERIFICACIÓN (Formación de Esteres) Un ácido carboxílico y un alcohol se calienta en presencia de un catalizador ácido, se da una reacción de condensación que produce un ESTER y AGUA. ACIDO CARBOXILICO + ALCOHOL O R’-C-OH + ROH O CH 3 C-OH + CH 3 CH 2 OH ESTER + AGUA O R’-C-OR + HOH O CH 3 C-OCH 2 CH 3 + HOH 18
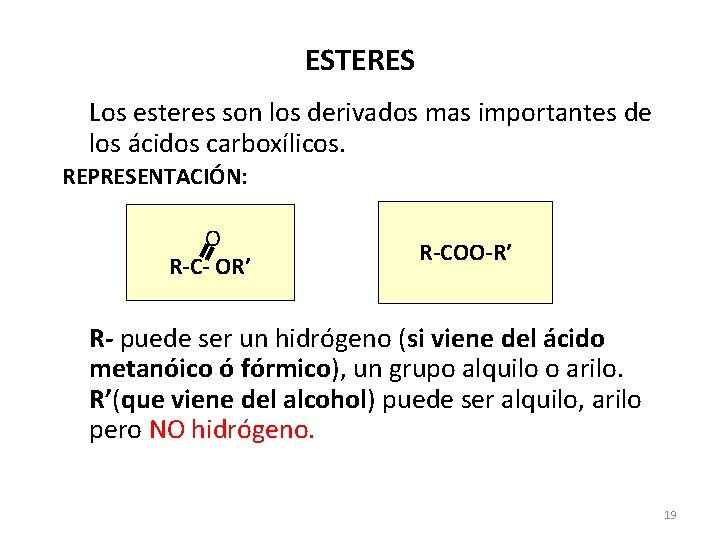
ESTERES Los esteres son los derivados mas importantes de los ácidos carboxílicos. REPRESENTACIÓN: O R-C- OR’ R-COO-R’ R- puede ser un hidrógeno (si viene del ácido metanóico ó fórmico), un grupo alquilo o arilo. R’(que viene del alcohol) puede ser alquilo, arilo pero NO hidrógeno. 19
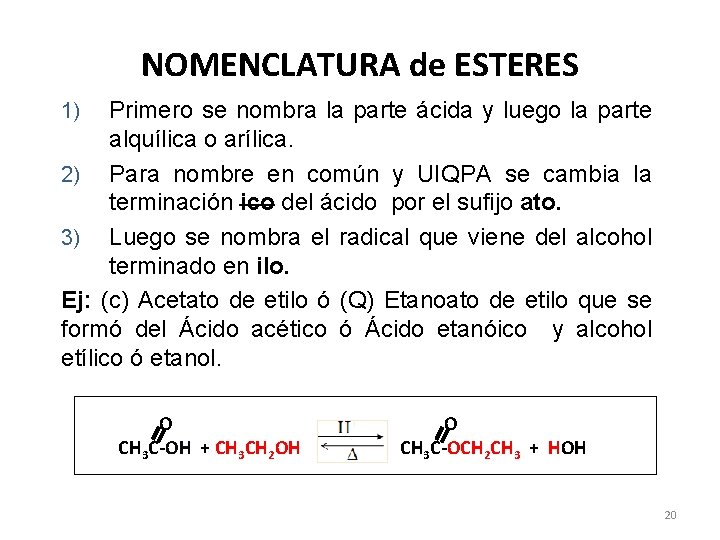
NOMENCLATURA de ESTERES Primero se nombra la parte ácida y luego la parte alquílica o arílica. 2) Para nombre en común y UIQPA se cambia la terminación ico del ácido por el sufijo ato. 3) Luego se nombra el radical que viene del alcohol terminado en ilo. Ej: (c) Acetato de etilo ó (Q) Etanoato de etilo que se formó del Ácido acético ó Ácido etanóico y alcohol etílico ó etanol. 1) O CH 3 C-OH + CH 3 CH 2 OH O CH 3 C-OCH 2 CH 3 + HOH 20
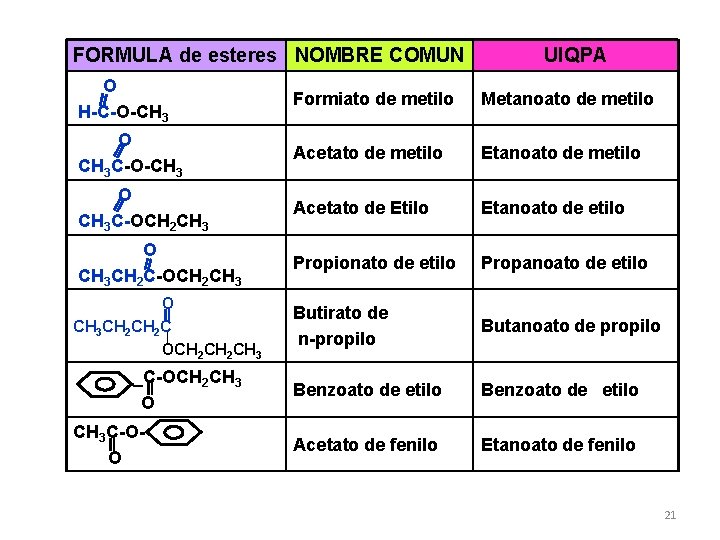
FORMULA de esteres NOMBRE COMUN UIQPA O H-C-O-CH 3 Formiato de metilo Metanoato de metilo O CH 3 C-O-CH 3 Acetato de metilo Etanoato de metilo O CH 3 C-OCH 2 CH 3 Acetato de Etilo Etanoato de etilo O CH 3 CH 2 C-OCH 2 CH 3 Propionato de etilo Propanoato de etilo Butirato de n-propilo Butanoato de propilo Benzoato de etilo Acetato de fenilo Etanoato de fenilo O CH 3 CH 2 C OCH 2 CH 3 _C-OCH 2 CH 3 O CH 3 C-OO 21

PROPIEDADES FÍSICAS de ESTERES • A diferencia de los ácidos carboxílicos de los cuales se derivan los esteres tienen olores agradables. • El aroma de muchas flores y frutos se debe a la presencia de esteres. Se utilizan como saborizantes en la fabricación de dulces, bebidas no alcohólicas y en la fabricación de perfumes. • La mayor parte de esteres son líquidos, incoloros, solubles en agua de 1 a 5 C, menos densos que el agua. • No forman puentes de H, por lo que sus puntos de ebullición son más bajos que alcoholes y ácidos carboxílicos pero más altos que alcanos y éteres. 22
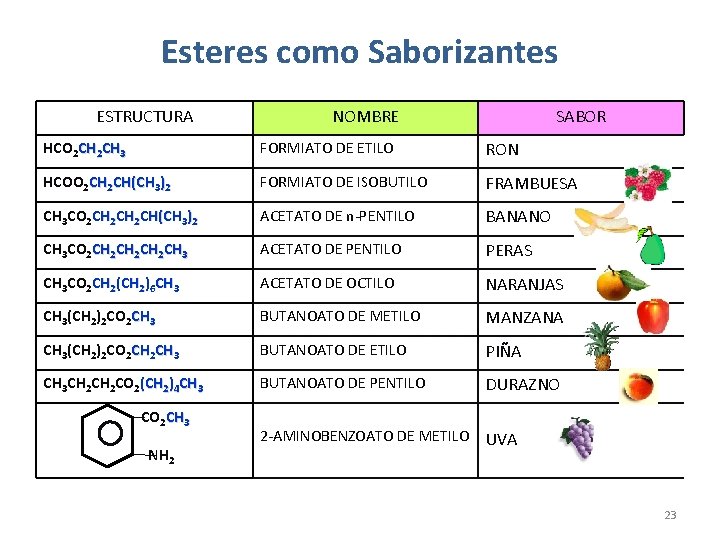
Esteres como Saborizantes ESTRUCTURA NOMBRE SABOR HCO 2 CH 3 FORMIATO DE ETILO RON HCOO 2 CH(CH 3)2 FORMIATO DE ISOBUTILO FRAMBUESA CH 3 CO 2 CH 2 CH(CH 3)2 ACETATO DE n-PENTILO BANANO CH 3 CO 2 CH 2 CH 3 ACETATO DE PENTILO PERAS CH 3 CO 2 CH 2(CH 2)6 CH 3 ACETATO DE OCTILO NARANJAS CH 3(CH 2)2 CO 2 CH 3 BUTANOATO DE METILO MANZANA CH 3(CH 2)2 CO 2 CH 3 BUTANOATO DE ETILO PIÑA CH 3 CH 2 CO 2(CH 2)4 CH 3 BUTANOATO DE PENTILO DURAZNO 2 -AMINOBENZOATO DE METILO UVA CO 2 CH 3 NH 2 23
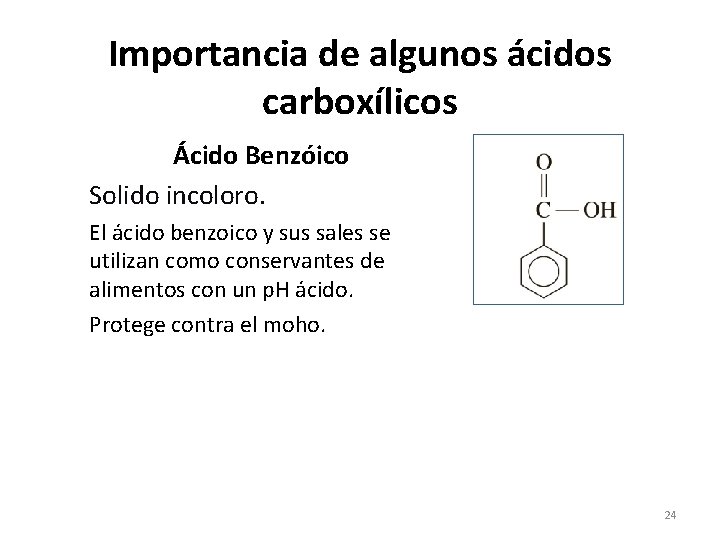
Importancia de algunos ácidos carboxílicos Ácido Benzóico Solido incoloro. El ácido benzoico y sus sales se utilizan como conservantes de alimentos con un p. H ácido. Protege contra el moho. 24
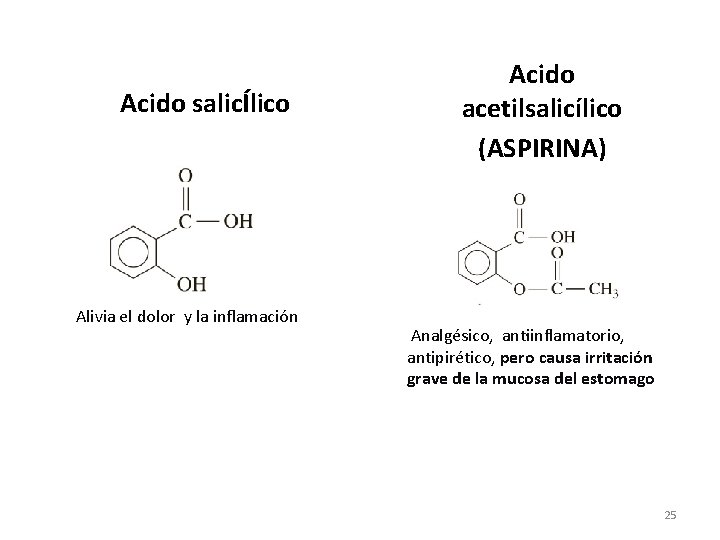
Acido salicÍlico Alivia el dolor y la inflamación Acido acetilsalicílico (ASPIRINA) . Analgésico, antiinflamatorio, antipirético, pero causa irritación grave de la mucosa del estomago 25
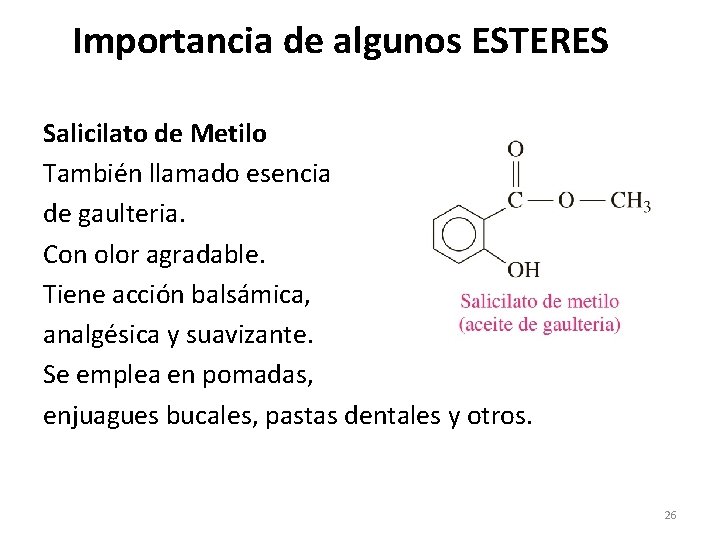
Importancia de algunos ESTERES Salicilato de Metilo También llamado esencia de gaulteria. Con olor agradable. Tiene acción balsámica, analgésica y suavizante. Se emplea en pomadas, enjuagues bucales, pastas dentales y otros. 26
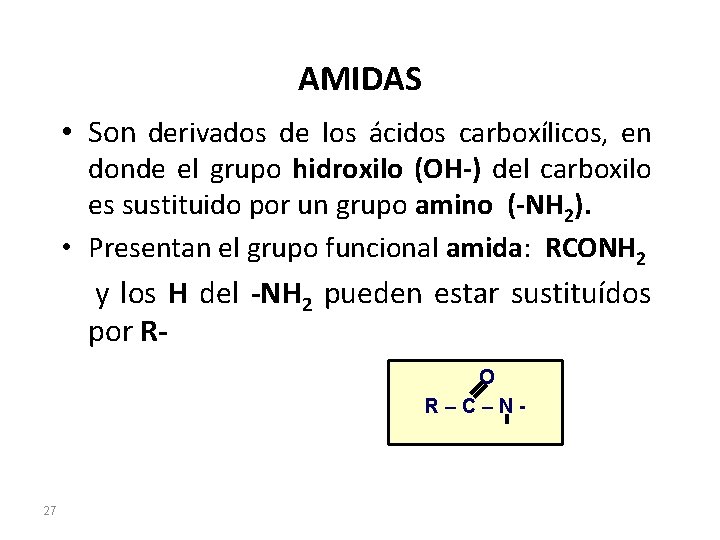
AMIDAS • Son derivados de los ácidos carboxílicos, en donde el grupo hidroxilo (OH-) del carboxilo es sustituido por un grupo amino (-NH 2). • Presentan el grupo funcional amida: RCONH 2 y los H del -NH 2 pueden estar sustituídos por RO R–C–N- 27
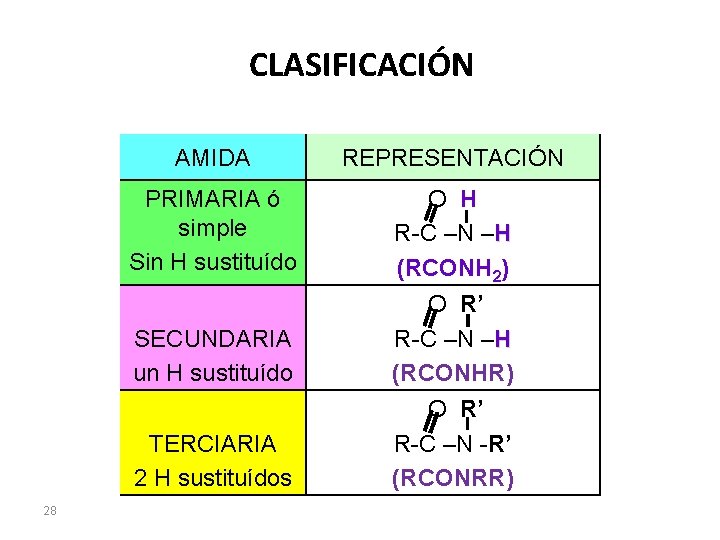
CLASIFICACIÓN AMIDA REPRESENTACIÓN PRIMARIA ó simple Sin H sustituído O H R-C –N –H (RCONH 2) SECUNDARIA un H sustituído TERCIARIA 2 H sustituídos 28 O R’ R-C –N –H (RCONHR) O R’ R-C –N -R’ (RCONRR)

NOMENCLATURA de AMIDAS Las amidas se nombran como derivados de los ácidos carboxílicos. • AMIDA 1ª: Las terminaciones del ácido carboxílico (del nombre común) u oico (del nombre UIQPA) se cambian por la terminación amida. • AMIDA 2ª y 3ª: Primero se nombran en orden alfabético los sustituyentes Alquilos ó arilos unidos al nitrógeno, anteponiéndoles la letra N(para indicar que son sustituyentes del N y no del Carbono) y se termina con el nombre de la amida simple. 29
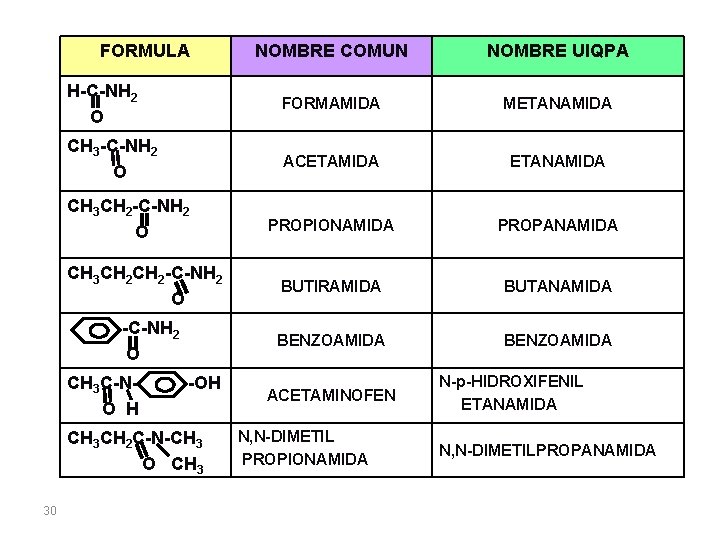
FORMULA NOMBRE COMUN NOMBRE UIQPA H-C-NH 2 O FORMAMIDA METANAMIDA CH 3 -C-NH 2 O ACETAMIDA ETANAMIDA PROPIONAMIDA PROPANAMIDA BUTIRAMIDA BUTANAMIDA BENZOAMIDA CH 3 CH 2 -C-NH 2 O CH 3 C-NO H -OH CH 3 CH 2 C-N-CH 3 O CH 3 30 ACETAMINOFEN N, N-DIMETIL PROPIONAMIDA N-p-HIDROXIFENIL ETANAMIDA N, N-DIMETILPROPANAMIDA
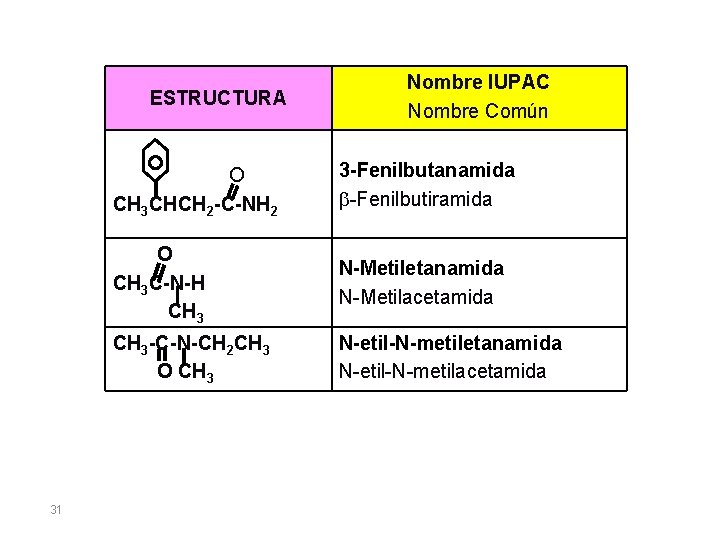
ESTRUCTURA 31 Nombre IUPAC Nombre Común O CH 3 CHCH 2 -C-NH 2 3 -Fenilbutanamida b-Fenilbutiramida O CH 3 C-N-H CH 3 N-Metiletanamida N-Metilacetamida CH 3 -C-N-CH 2 CH 3 O CH 3 N-etil-N-metiletanamida N-etil-N-metilacetamida
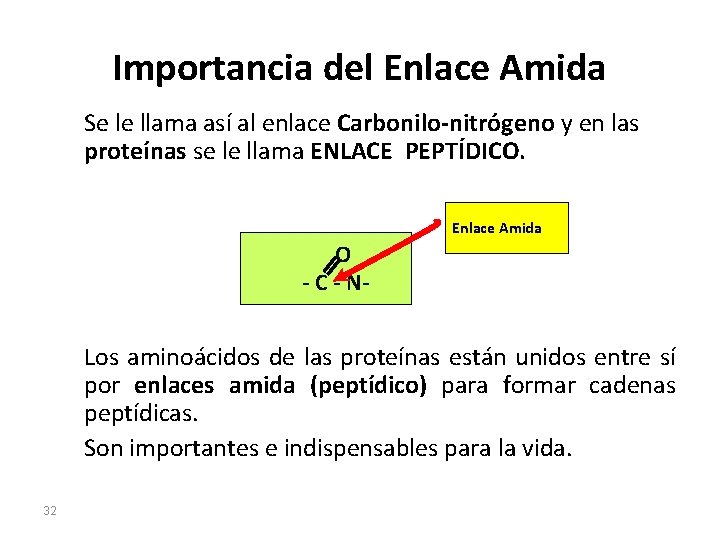
Importancia del Enlace Amida Se le llama así al enlace Carbonilo-nitrógeno y en las proteínas se le llama ENLACE PEPTÍDICO. Enlace Amida O - C - N- Los aminoácidos de las proteínas están unidos entre sí por enlaces amida (peptídico) para formar cadenas peptídicas. Son importantes e indispensables para la vida. 32

Ejercicios: • Nombre UIQPA y clasificación de la N, N-dietilbutiramida: • El ácido carboxílico y el alcohol que origina al éster Butanoato de sec-butilo: 33
- Slides: 33