SEMANA 19 ALCOHOLES y FENOLES SEMANA 20 TIOLES















- Slides: 33

SEMANA 19 ALCOHOLES y FENOLES SEMANA 20 TIOLES Y ÉTERES QUÍMICA 2020 1

Semana 19 ALCOHOLES Y FENOLES Alcoholes Definición y representación general. Clasificación. Nomenclatura UIQPA y Común. Polihidroxilados (etilenglicol, propilenglicol, trimetilenglicol, glicerol) Isomería: -Posición -Función Propiedades físicas Reacciones químicas: -Oxidación con KMn. O 4 (frío) -Prueba de Lucas -Deshidratación a 180°C, con H 2 SO 4 (conc. ) aplicando Regla de Zaitsev Fenoles Definición y representación general. Nomenclatura. Propiedades Físicas. Reacción con Fe. Cl 3 Aplicación de los conceptos en la salud y el ambiente. Lecturas en libro de texto - La Química en la Salud: “Algunos alcoholes y fenoles importantes” “Desinfectante de manos y etanol” “Intoxicación con metanol” “Oxidación de etanol en el cuerpo” - Otras que se informe. Laboratorio: Propiedades físicas y químicas de alcoholes y fenoles. 2

Semana 20 TIOLES Y ÉTERES Tioles Definición y representación general. Nomenclatura UIQPA y común Importancia y usos Éteres Definición y representación general Nomenclatura UIQPA y Común Propiedades físicas Aplicación de los conceptos en la salud y el ambiente. Lecturas en libro de texto - La Química en el Ambiente -“Éteres tóxicos” -La Química en la Salud: -“Éteres como anestésicos 3

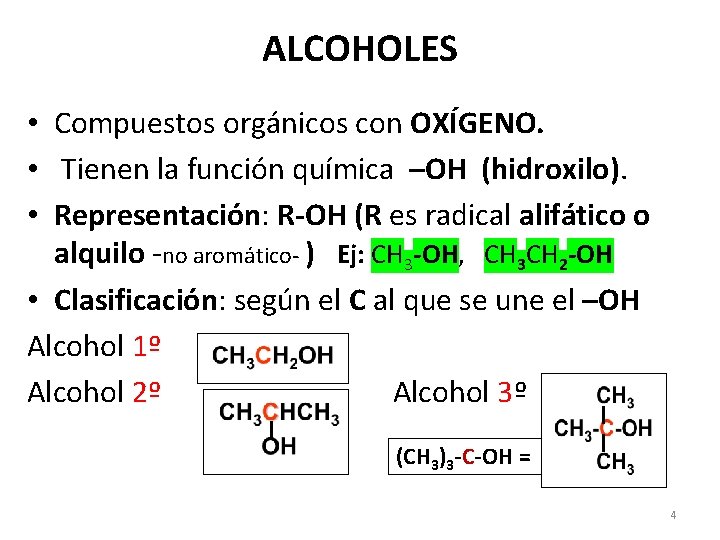
ALCOHOLES • Compuestos orgánicos con OXÍGENO. • Tienen la función química –OH (hidroxilo). • Representación: R-OH (R es radical alifático o alquilo -no aromático- ) Ej: CH 3 -OH, CH 3 CH 2 -OH • Clasificación: según el C al que se une el –OH Alcohol 1º Alcohol 2º Alcohol 3º (CH 3)3 -C-OH = 4

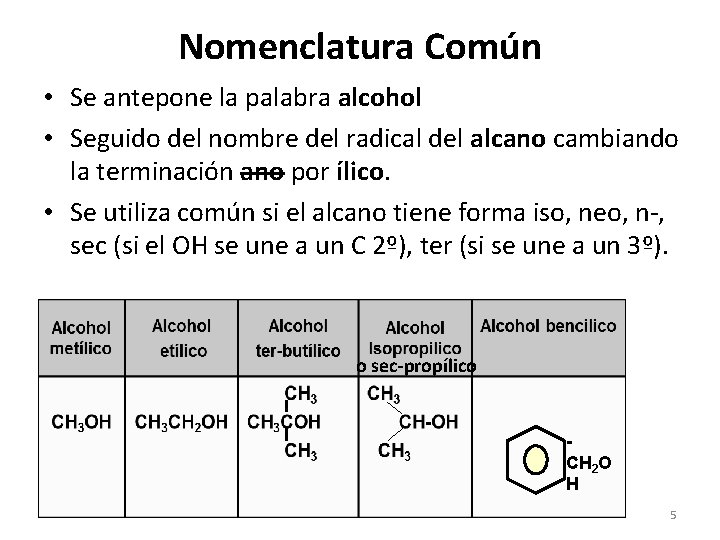
Nomenclatura Común • Se antepone la palabra alcohol • Seguido del nombre del radical del alcano cambiando la terminación ano por ílico. • Se utiliza común si el alcano tiene forma iso, neo, n-, sec (si el OH se une a un C 2º), ter (si se une a un 3º). o sec-propílico CH 2 O H 5

Nomenclatura UIQPA • Utilizar las mismas reglas básicas para alcanos. • La prioridad al numerar la cadena carbonada la tiene la función química hidroxilo (-OH), el # menor de C. • El nombre básico será el del alcano cambiando la terminación ano por ol. Se indica la posición del OH. • Si hay más de un –OH se usan prefijos diol, triol, etc. Nombrar y Clasificar: 6

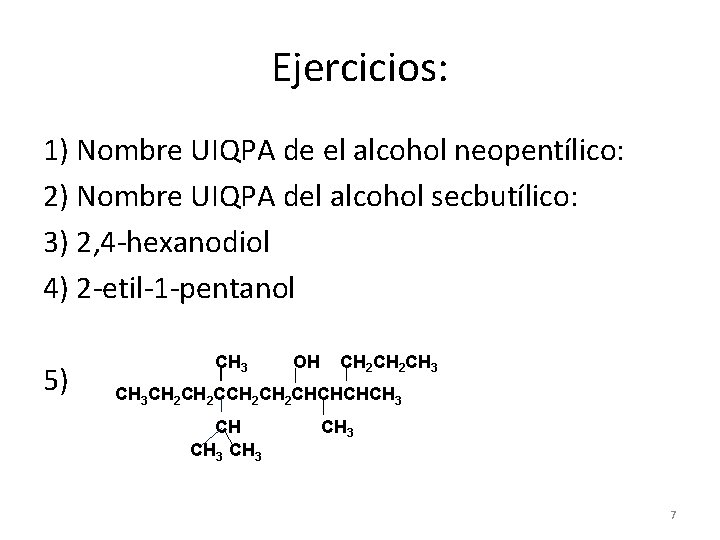
Ejercicios: 1) Nombre UIQPA de el alcohol neopentílico: 2) Nombre UIQPA del alcohol secbutílico: 3) 2, 4 -hexanodiol 4) 2 -etil-1 -pentanol 5) CH 3 OH CH 2 CH 3 CH 2 CH 2 CHCHCHCH 3 CH 3 7

Alcoholes polihidroxilados (algunos ejemplos) Los Glicoles: tiene 2 grupos hidroxilos (OH-). Ejemplos: • Etilenglicol o 1, 2 -etanodiol (uso: anticongelante, es tóxico) HO-CH 2 OH • Propilenglicol o 1, 2 -propanodiol (uso: humectante, solvente) • Trimetilenglicol o 1, 3 - propanodiol HO-CH 2 CH 2 OH (uso: síntesis de polímeros) Con 3 grupos OH • Glicerol, glicerina o 1, 2, 3 -propanotriol (humectante, forma parte de los lípidos) 8

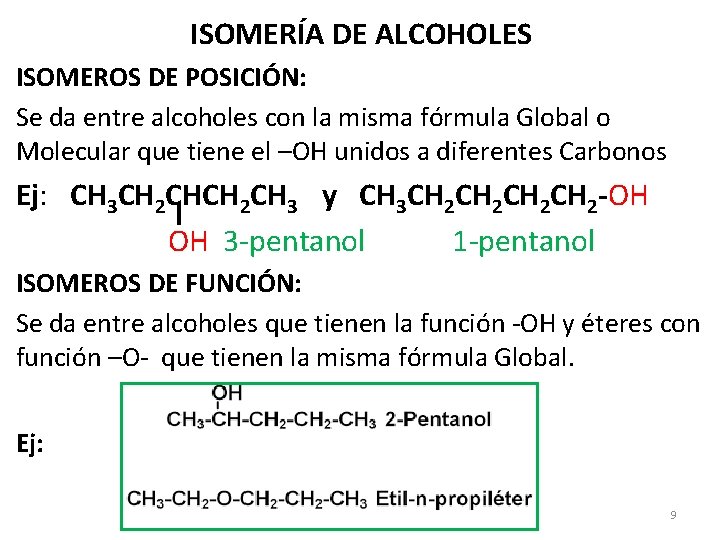
ISOMERÍA DE ALCOHOLES ISOMEROS DE POSICIÓN: Se da entre alcoholes con la misma fórmula Global o Molecular que tiene el –OH unidos a diferentes Carbonos Ej: CH 3 CH 2 CH 3 y CH 3 CH 2 CH 2 -OH OH 3 -pentanol 1 -pentanol ISOMEROS DE FUNCIÓN: Se da entre alcoholes que tienen la función -OH y éteres con función –O- que tienen la misma fórmula Global. Ej: 9

Propiedades físicas • Los alcoholes de 1 a 4 carbonos son solubles en H 2 O porque el –OH le da polaridad a la molécula. • De 5 a más C son más apolares por lo que son solubles en solventes orgánicos (apolares). • Los isómeros ramificaciones son más solubles que los lineales. • Los alcoholes tienen puntos de ebullición mas altos que los alcanos porque sus moléculas forman puentes de H entre sus grupos –OH. • Alcoholes de 1 a 10 C son líquidos, incoloros, olor característico. De 11 a más son sólidos cristalinos, blancos. 10

Usos y riesgos • Alcohol metílico ó metanol: se absorbe por la piel y es tóxico, por lo que no se debe usar para fricciones, causa ceguera, y muerte al ingerir 30 ml. • Alcohol etílico ó etanol: usado en bebidas alcohólicas. Se utiliza como desinfectante y para fricciones. (El etanol comercial no es ingerible). • Alcohol isopropílico: es tóxico al ingerirlo. No se absorbe por la piel por lo que se usa en fricciones • Etilenglicol (1, 2 -etanodiol): anticongelante, tóxico. • Glicerol o glicerina (1, 2, 3 -propanotriol): humectante. 11

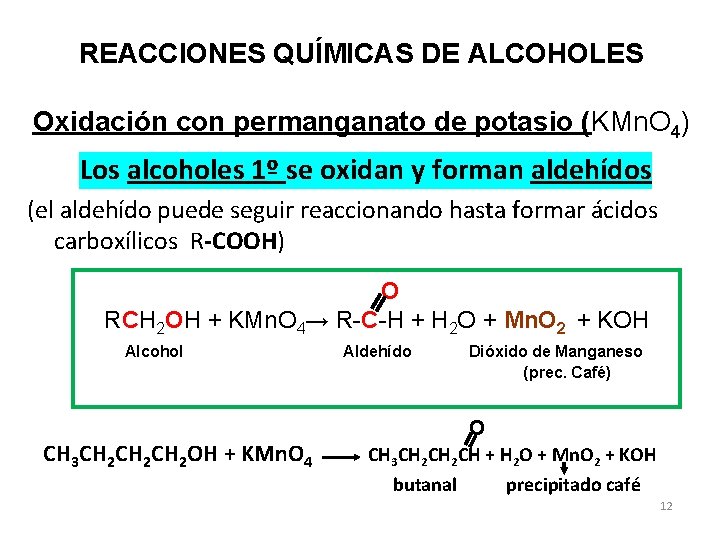
REACCIONES QUÍMICAS DE ALCOHOLES Oxidación con permanganato de potasio (KMn. O 4) Los alcoholes 1º se oxidan y forman aldehídos (el aldehído puede seguir reaccionando hasta formar ácidos carboxílicos R-COOH) O RCH 2 OH + KMn. O 4→ R-C-H + H 2 O + Mn. O 2 + KOH Alcohol CH 3 CH 2 CH 2 OH + KMn. O 4 Aldehído Dióxido de Manganeso (prec. Café) O CH 3 CH 2 CH + H 2 O + Mn. O 2 + KOH butanal precipitado café 12

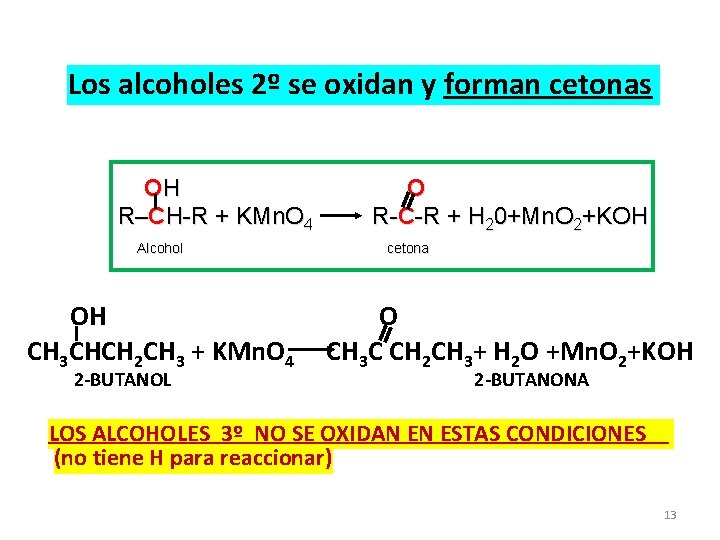
Los alcoholes 2º se oxidan y forman cetonas OH R–CH-R + KMn. O 4 Alcohol OH CH 3 CHCH 2 CH 3 + KMn. O 4 2 -BUTANOL O R-C-R + H 20+Mn. O 2+KOH cetona O CH 3 C CH 2 CH 3+ H 2 O +Mn. O 2+KOH 2 -BUTANONA LOS ALCOHOLES 3º NO SE OXIDAN EN ESTAS CONDICIONES (no tiene H para reaccionar) 13

REACCIÓN ó PRUEBA DE LUCAS esta servirá para la muestra desconocida #2 (El Reactivo de Lucas consiste en: HCl conc. + Zn. Cl 2 ) El Cloro Sustituye al –OH y forma un derivado halogenado ALCO HOL 1 o. 2 o. 3 o. MANIFESTACION REACCION CH 3 -CH 2 -OH + HCl Zn. Cl 2 NO HAY REACCION Zn. Cl 2 (CH 3)2 -CH-OH + HCl (CH 3)2 -CH-Cl + H 2 O (necesita calentamiento en baño de maria) (CH 3)3 -C-OH + HCl Zn. Cl 2 (CH 3)3 -C-Cl + H 2 O NO HAY TURBIDEZ después de calentar TURBIDEZ INMEDIATA sin calentar 14

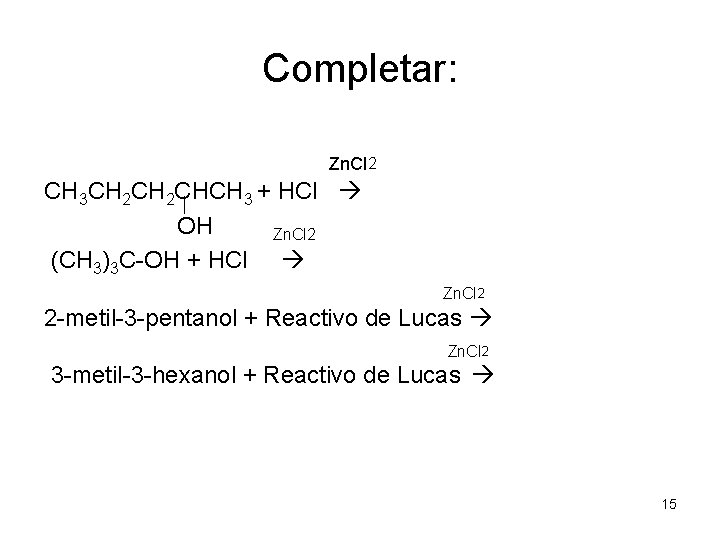
Completar: Zn. Cl 2 CH 3 CH 2 CHCH 3 + HCl OH Zn. Cl 2 (CH 3)3 C-OH + HCl Zn. Cl 2 2 -metil-3 -pentanol + Reactivo de Lucas Zn. Cl 2 3 -metil-3 -hexanol + Reactivo de Lucas 15

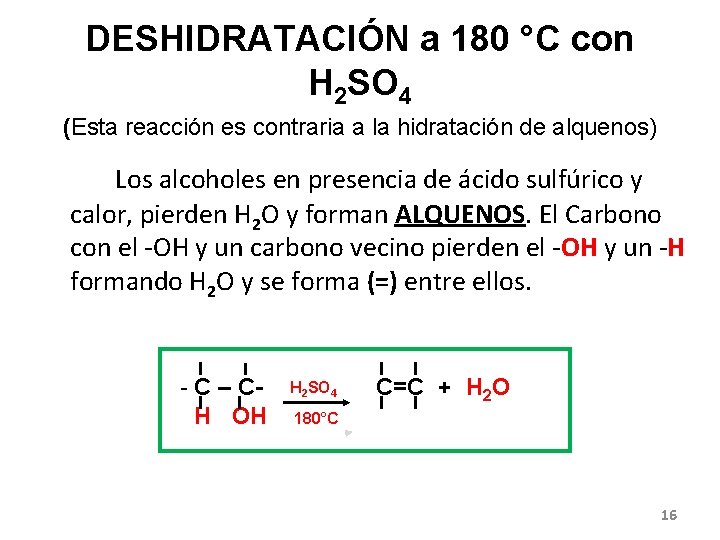
DESHIDRATACIÓN a 180 °C con H 2 SO 4 (Esta reacción es contraria a la hidratación de alquenos) • Los alcoholes en presencia de ácido sulfúrico y calor, pierden H 2 O y forman ALQUENOS. El Carbono con el -OH y un carbono vecino pierden el -OH y un -H formando H 2 O y se forma (=) entre ellos. - C – CH OH H 2 SO 4 C=C + H 2 O 180°C 16

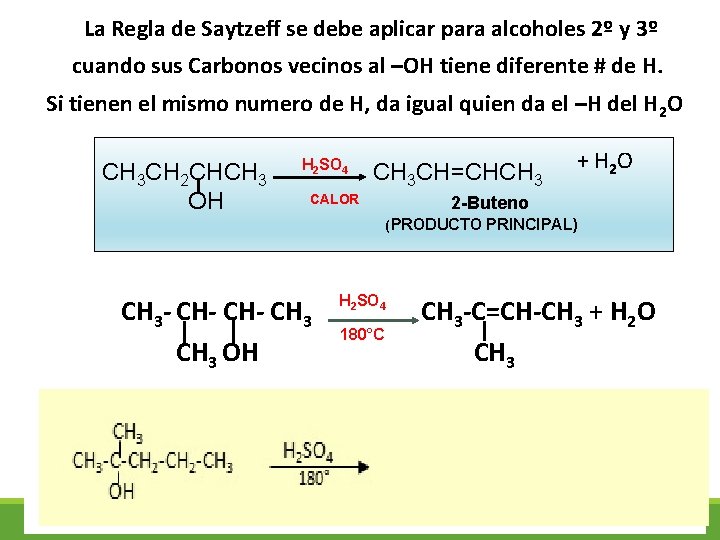
• Cuando se deshidrata un alcohol 2º o 3º se pueden formar dos alquenos dependiendo de cuál de los Hidrógenos de los C vecinos se eliminen con el –OH. • Esto lo determina la Regla de Saytzeff: El doble enlace se formará principalmente (o sea en mayor %) entre el carbono que contienen al grupo -OH y el C vecino que tenga menos hidrógenos del alcohol. (es contraria a la Regla de Markovnikof) Producto principal: es el alqueno que se forma en mayor% Producto secundario: es el que se forma en menor % 17

La Regla de Saytzeff se debe aplicar para alcoholes 2º y 3º cuando sus Carbonos vecinos al –OH tiene diferente # de H. Si tienen el mismo numero de H, da igual quien da el –H del H 2 O CH 3 CH 2 CHCH 3 OH H 2 SO 4 CH 3 CH=CHCH 3 CALOR + H 2 O 2 -Buteno ( PRODUCTO PRINCIPAL) CH 3 - CH- CH 3 OH H 2 SO 4 180°C CH 3 -C=CH-CH 3 + H 2 O CH 3 18

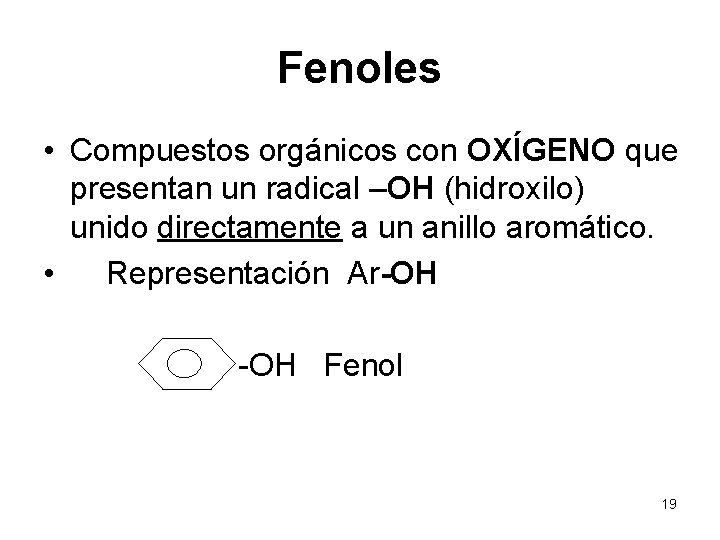
Fenoles • Compuestos orgánicos con OXÍGENO que presentan un radical –OH (hidroxilo) unido directamente a un anillo aromático. • Representación Ar-OH Fenol 19

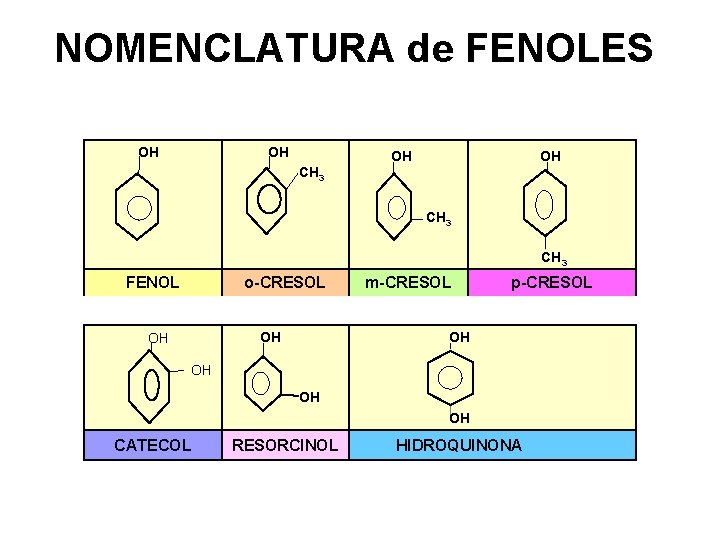
NOMENCLATURA de FENOLES OH OH CH 3 FENOL o-CRESOL OH OH m-CRESOL p-CRESOL OH OH CATECOL RESORCINOL HIDROQUINONA 20

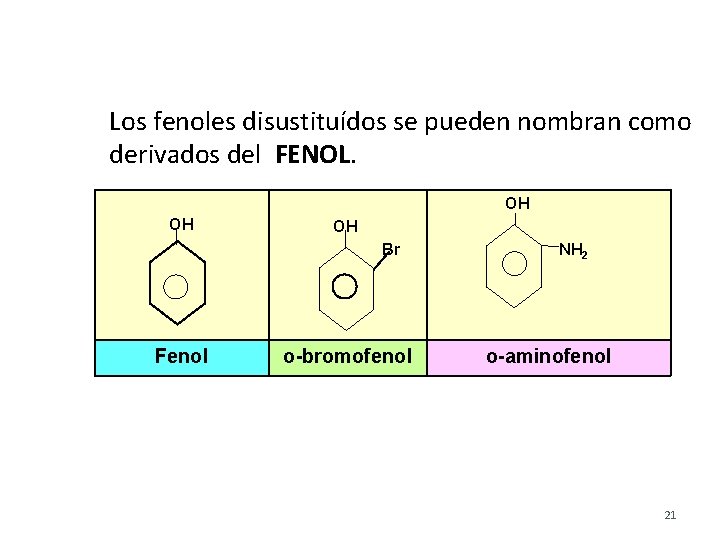
Los fenoles disustituídos se pueden nombran como derivados del FENOL. OH OH OH Br Fenol o-bromofenol NH 2 o-aminofenol 21

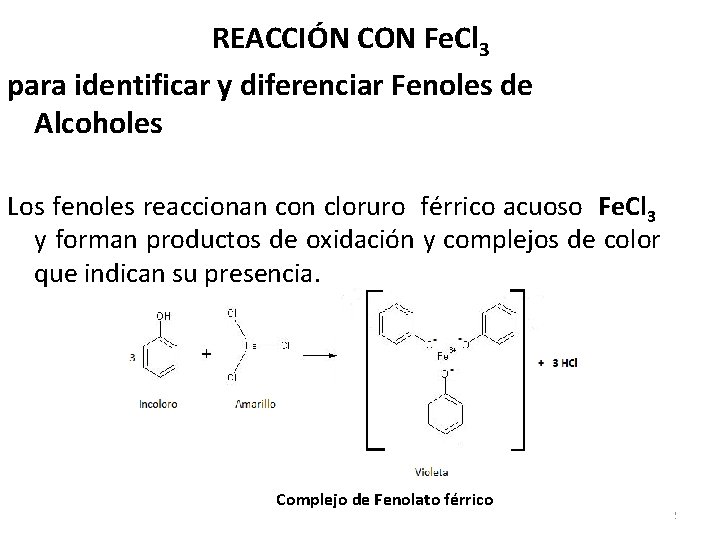
REACCIÓN CON Fe. Cl 3 para identificar y diferenciar Fenoles de Alcoholes Los fenoles reaccionan con cloruro férrico acuoso Fe. Cl 3 y forman productos de oxidación y complejos de color que indican su presencia. REACCIONES DE FENOL Complejo de Fenolato férrico 22

IMPORTANCIA , USOS Y RIESGOS del FENOL • El fenol es muy utilizado como desinfectante fungicida, bactericida, antiséptico. • Si se ingiere en altas concentraciones puede causar envenenamiento • Se absorbe por la piel • Es inflamable, corrosivo y sus gases son explosivos a la llama 23

Semana 20 TIOLES Y ÉTERES Tioles Definición y representación general. Nomenclatura UIQPA y común Importancia y usos Éteres Definición y representación general Nomenclatura UIQPA y Común Propiedades físicas Aplicación de los conceptos en la salud y el ambiente. Lecturas en libro de texto - La Química en el Ambiente -“Éteres tóxicos” -La Química en la Salud: -“Éteres como anestésicos 24

TIOLES ó MERCAPTANOS Compuestos orgánicos con AZUFRE que presentan la función química -SH Representación: R-SH R= radical puede ser alifático o aromático El grupo -SH se conoce como: MERCAPTANO ó SULFHIDRILO. TIENEN OLORES MUY DESAGRADABLES. Se le agrega al gas propano para detectar fugas. 25

Nomenclatura de tioles ó mercaptanos COMUN: Se menciona primero el nombre del radical (il) del alcano (n, iso, neo, sec, ter) terminado con la palabra mercaptano. UIQPA: Se nombra como alcano con la terminación tiol siguiendo las reglas para los alcanos. 26

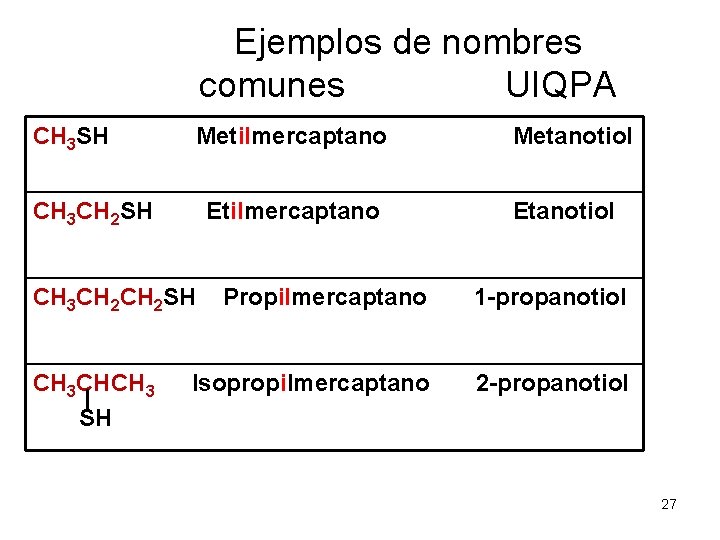
Ejemplos de nombres comunes UIQPA CH 3 SH Metilmercaptano CH 3 CH 2 SH Etilmercaptano CH 3 CH 2 SH CH 3 CHCH 3 SH Metanotiol Etanotiol Propilmercaptano 1 -propanotiol Isopropilmercaptano 2 -propanotiol 27

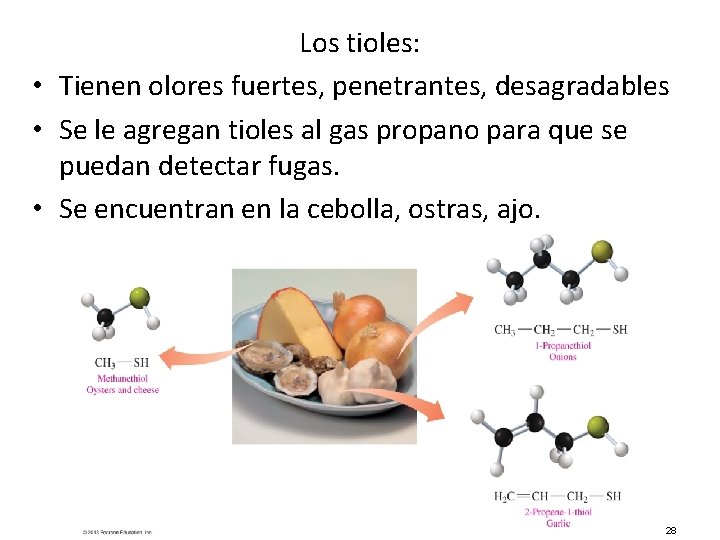
Los tioles: • Tienen olores fuertes, penetrantes, desagradables • Se le agregan tioles al gas propano para que se puedan detectar fugas. • Se encuentran en la cebolla, ostras, ajo. 28

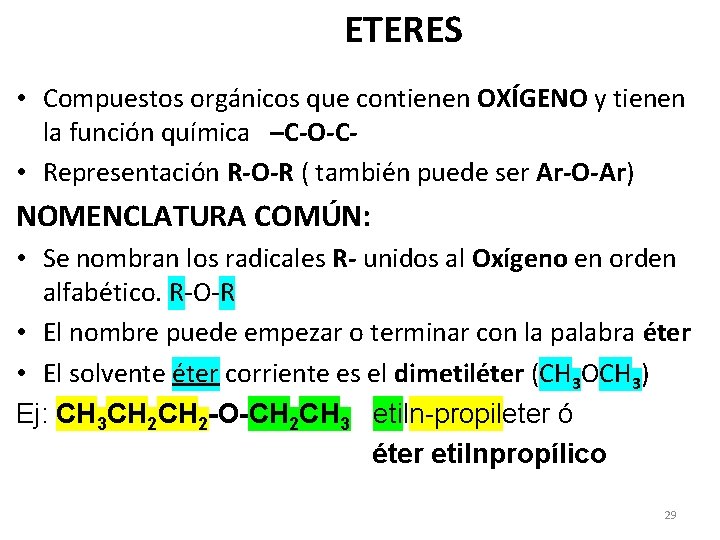
ETERES • Compuestos orgánicos que contienen OXÍGENO y tienen la función química –C-O-C • Representación R-O-R ( también puede ser Ar-O-Ar) NOMENCLATURA COMÚN: • Se nombran los radicales R- unidos al Oxígeno en orden alfabético. R-O-R • El nombre puede empezar o terminar con la palabra éter • El solvente éter corriente es el dimetiléter (CH 3 OCH 3) Ej: CH 3 CH 2 -O-CH 2 CH 3 etiln-propileter ó éter etilnpropílico 29

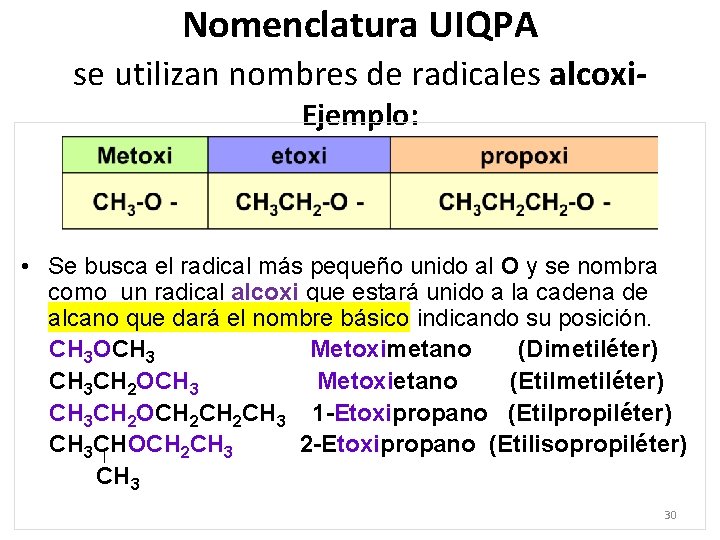
Nomenclatura UIQPA se utilizan nombres de radicales alcoxi. Ejemplo: • Se busca el radical más pequeño unido al O y se nombra como un radical alcoxi que estará unido a la cadena de alcano que dará el nombre básico indicando su posición. CH 3 OCH 3 Metoximetano (Dimetiléter) CH 3 CH 2 OCH 3 Metoxietano (Etilmetiléter) CH 3 CH 2 OCH 2 CH 3 1 -Etoxipropano (Etilpropiléter) CH 3 CHOCH 2 CH 3 2 -Etoxipropano (Etilisopropiléter) CH 3 30

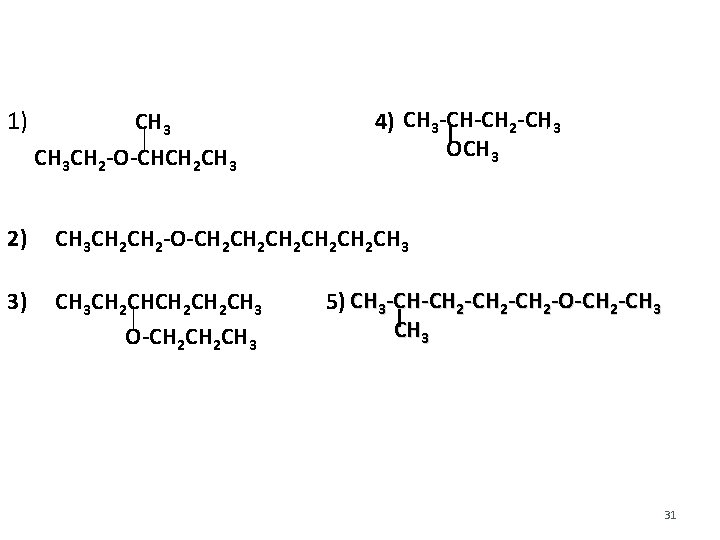
1) CH 3 CH 2 -O-CHCH 2 CH 3 4) CH 3 -CH-CH 2 -CH 3 OCH 3 2) CH 3 CH 2 -O-CH 2 CH 2 CH 2 CH 3 3) CH 3 CH 2 CH 2 CH 3 O-CH 2 CH 3 5) CH 3 -CH-CH 2 -CH 2 -O-CH 2 -CH 3 31

PROPIEDADES FISICAS de los ETERES • Incoloros • Muy volátiles • Menos densos que el agua • Inflamables • Sus moléculas no forman puentes de H entre sí • Olores característicos • Los éteres de 1 a 4 carbonos son solubles en agua porque forman puentes de hidrógeno entre su oxígeno y el agua. 32

Usos y riesgos de algunos éteres • El dietiléter: antiguamente se utilizaba como anestésico general, pero era muy volátil e inflamable y causaba efectos secundarios. Actualmente se usa como solvente de sustancias apolares. • Metilterbutiléter : se inyecta directamente en la vesícula biliar a través de un catéter, éste disuelve los cálculos que principalmente son de colesterol, no presenta efectos secundarios desagradables. 33