SEMANA 15 2020 LICDA CORINA MARROQUIN QUIMICA ORGANICA



















- Slides: 34

SEMANA 15 2020 LICDA. CORINA MARROQUIN

QUIMICA ORGANICA Es el estudio de los compuestos del carbono. Los compuestos orgánicos usualmente contienen: C, H, O, S, N, P o algún halógeno (F, Cl, I y Br). Se conocen cerca de 6 millones de compuestos orgánicos. Muchos compuestos orgánicos son moléculas no polares donde predominan enlaces covalentes. Los organismos vivos están construidos de compuestos orgánicos y utilizan ciertos compuestos orgánicos como fuente de energía.

ALGUNOS COMPUESTOS ORGANICOS. ALIMENTOS

ALGUNOS COMPUESTOS ORGANICOS. Pinturas Plásticos Medicinas Fibras naturales y sintéticas. Combustibles

En los seres vivos: Carbohidratos Lípidos (grasas y compuestos relacionados). Aminoácidos Proteínas Vitaminas Hormonas Enzimas

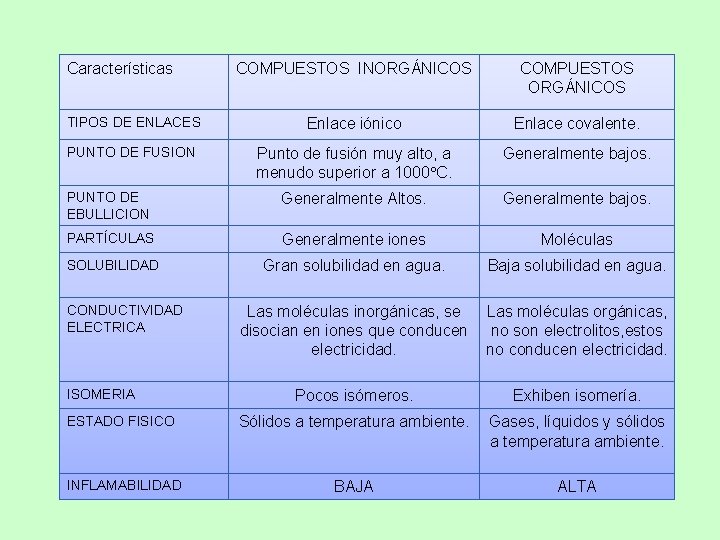
COMPARACIÓN DE UN COMPUESTO ORGÁNICO E INORGÁNICO.

Características COMPUESTOS INORGÁNICOS COMPUESTOS ORGÁNICOS Enlace iónico Enlace covalente. Punto de fusión muy alto, a menudo superior a 1000 C. Generalmente bajos. PUNTO DE EBULLICION Generalmente Altos. Generalmente bajos. PARTÍCULAS Generalmente iones Moléculas SOLUBILIDAD Gran solubilidad en agua. Baja solubilidad en agua. TIPOS DE ENLACES PUNTO DE FUSION CONDUCTIVIDAD ELECTRICA ISOMERIA Las moléculas inorgánicas, se Las moléculas orgánicas, disocian en iones que conducen no son electrolitos, estos electricidad. no conducen electricidad. Pocos isómeros. Exhiben isomería. ESTADO FISICO Sólidos a temperatura ambiente. Gases, líquidos y sólidos a temperatura ambiente. INFLAMABILIDAD BAJA ALTA

Características Generales de Carbono Numero atómico de 6 : dos electrones en la primera capa y cuatro electrones en la segunda capa. Masa atómica de 12. Dos niveles de energía. Cuatro electrones de valencia. Tetravalente, forma cuatro enlaces covalentes, en casi todos los casos. Forma enlaces covalentes fuertes con otros átomos de carbono y con hidrógeno, oxígeno, azufre y nitrógeno. La orientación espacial de los átomos de una molécula se encuentran en un arreglo tetraédrico que permite que los pares de electrones se encuentren a la mayor distancia posible.

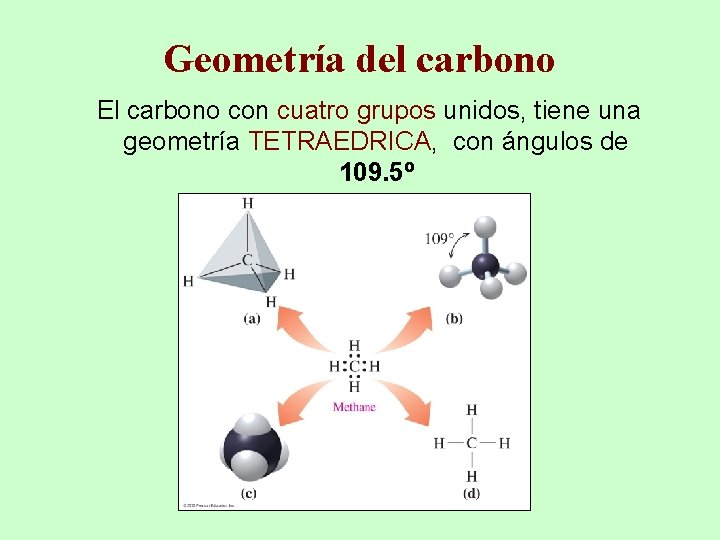
Geometría del carbono El carbono con cuatro grupos unidos, tiene una geometría TETRAEDRICA, con ángulos de 109. 5º

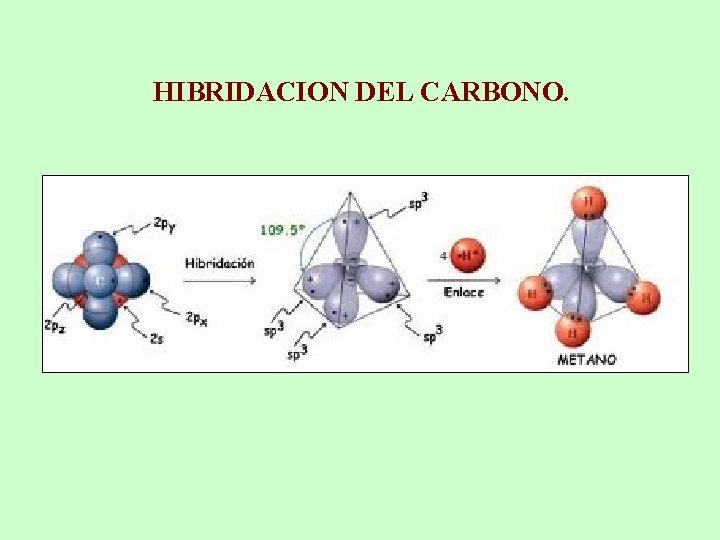
HIBRIDACION DEL CARBONO.


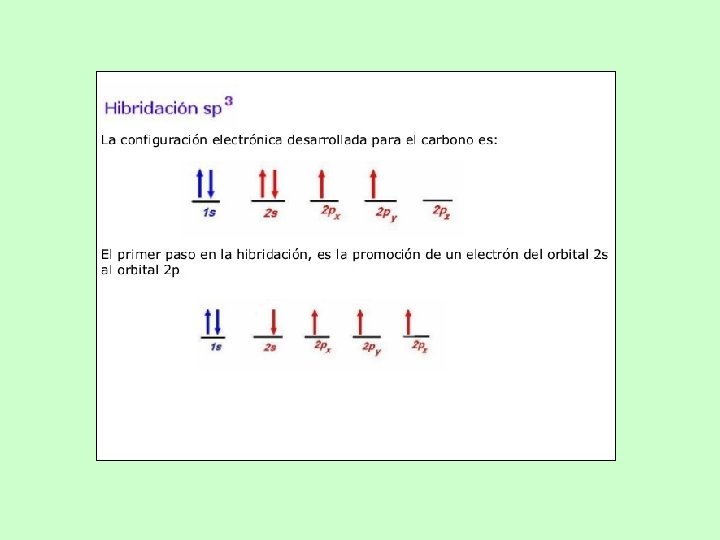
HIBRIDACIÓN SP 3 Compuestos con enlaces simples, como hidrocarburos saturados o alcanos forman 4 orbitales sp 3. HIBRIDACIÓN SP 2 Los átomos que forman hibridaciones sp 2 pueden formar compuestos con enlaces dobles y moléculas planas. Alquenos. HIBRIDACIÓN SP. Se encuentran en compuestos con triples enlaces. Alquinos. Pág. 8 -9 de su guia.

FORMAS ALOTROPICAS DEL CARBONO. Diamante, Grafito, Fullerenos.

La forma mas bonita del carbono.

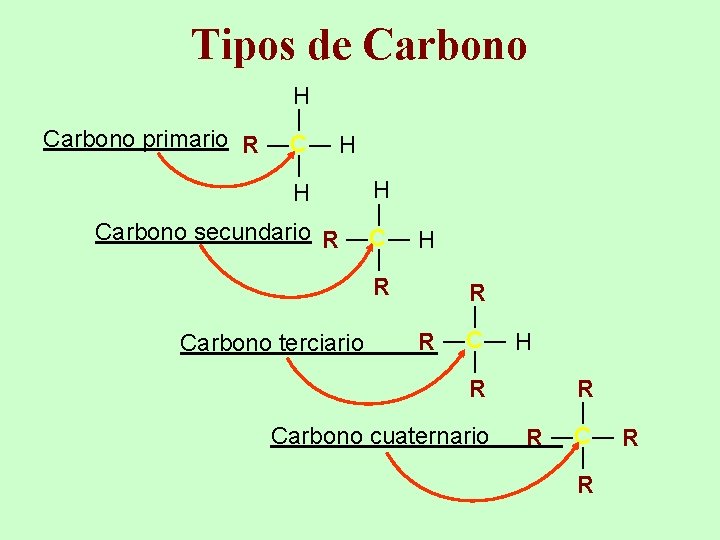
Tipos de Carbono ― ― H Carbono primario R ―C― H H ― ― H Carbono secundario R ―C― H R ― ― R R ―C― H Carbono terciario R ― ― R Carbono cuaternario R ―C― R R

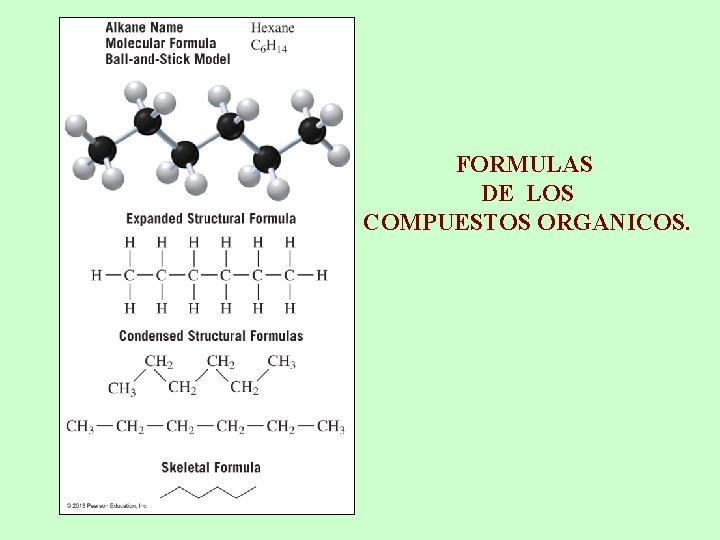
FORMULAS DE LOS COMPUESTOS ORGANICOS.

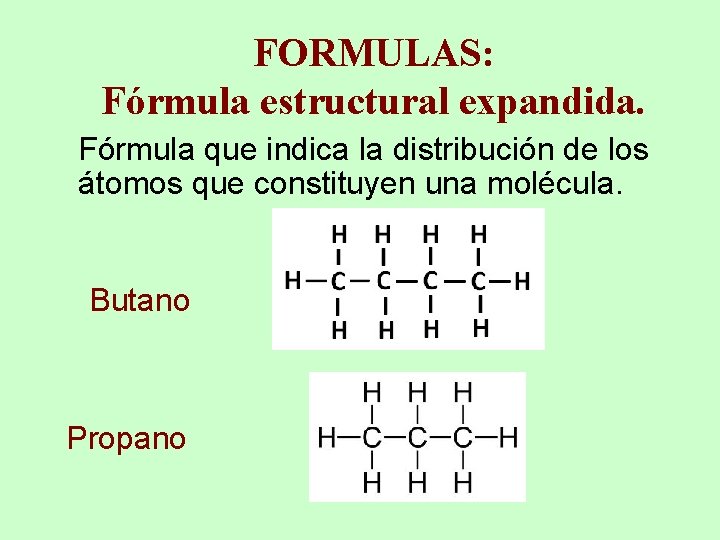
FORMULAS: Fórmula estructural expandida. Fórmula que indica la distribución de los átomos que constituyen una molécula. Butano Propano

FORMULAS: Fórmula estructural condensada Los átomos que están unidos a un átomo de carbono particular se escriben inmediatamente después de éste. Butano: CH 3 -CH 2 -CH 3 Propano: CH 3 -CH 2 -CH 3

FORMULAS: Fórmula global o molecular Fórmula que expresa el número real de átomos de una molécula. Butano: CH 3 -CH 2 -CH 3 C 4 H 10 Propano: CH 3 -CH 2 -CH 3 C 3 H 8

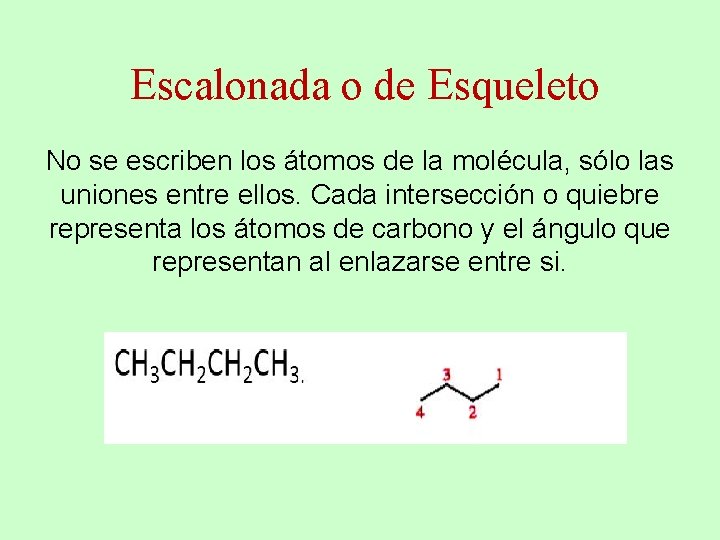
Escalonada o de Esqueleto No se escriben los átomos de la molécula, sólo las uniones entre ellos. Cada intersección o quiebre representa los átomos de carbono y el ángulo que representan al enlazarse entre si.

FORMULAS

Los compuestos orgánicos presentan: Isomería Compuestos distintos que tienen la misma fórmula molecular.

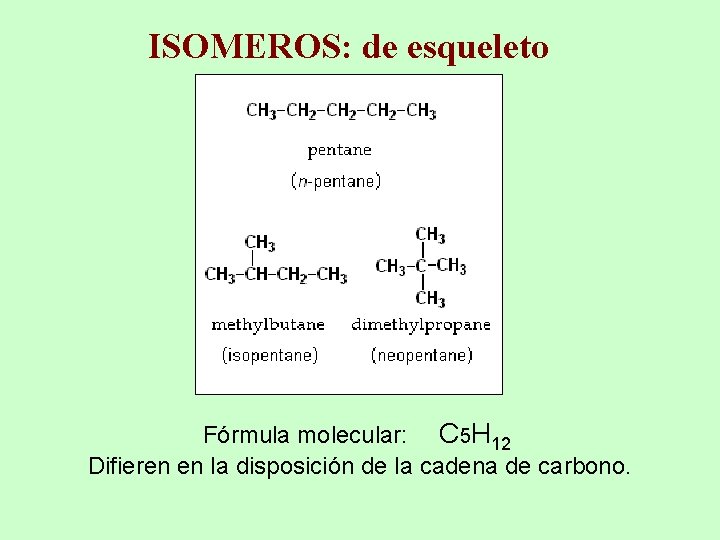
ISOMEROS: de esqueleto Fórmula molecular: C 5 H 12 Difieren en la disposición de la cadena de carbono.

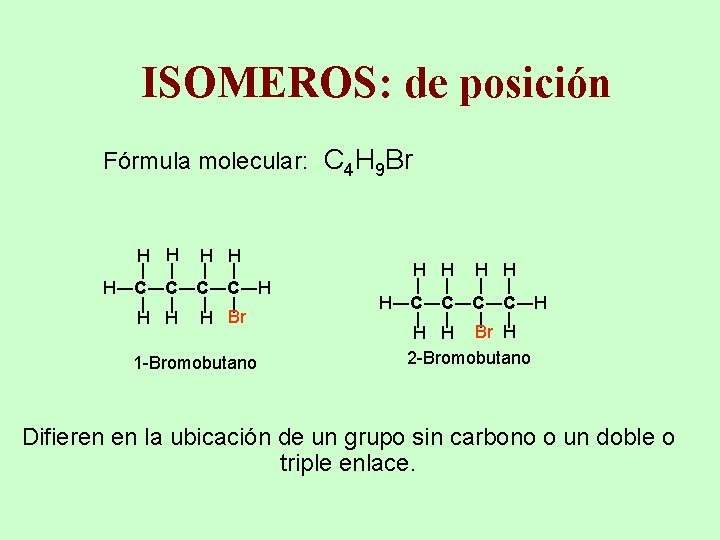
ISOMEROS: de posición Fórmula molecular: C 4 H 9 Br ― ― 1 -Bromobutano H H ― ― H H H Br ― ― H―C―C―H H H ― ― ― H H H―C―C―H H H Br H 2 -Bromobutano Difieren en la ubicación de un grupo sin carbono o un doble o triple enlace.

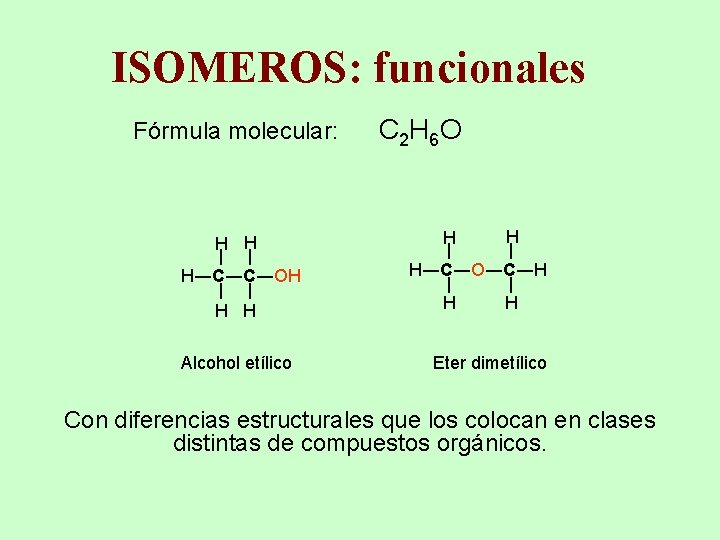
ISOMEROS: funcionales Fórmula molecular: C 2 H 6 O H H Alcohol etílico H ― ― H―C―C―OH H ― ― ― H H H―C―O―C―H H H Eter dimetílico Con diferencias estructurales que los colocan en clases distintas de compuestos orgánicos.

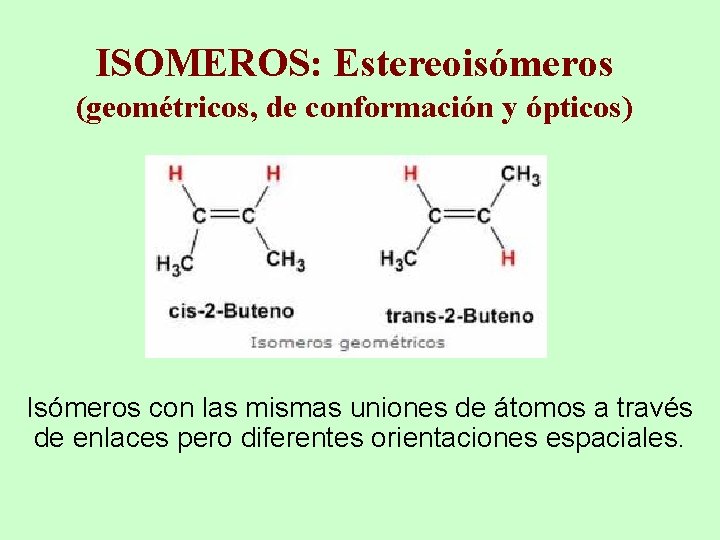
ISOMEROS: Estereoisómeros (geométricos, de conformación y ópticos) Isómeros con las mismas uniones de átomos a través de enlaces pero diferentes orientaciones espaciales.

ESTEREOISOMEROS

Serie Homóloga Una familia de compuestos semejantes. • • • Es un conjunto de compuestos que comparten el mismo grupo funcional y por ello, poseen propiedades y reacciones similares. Tienen los mismos elementos, con la misma fórmula general simple. Fórmula molecular difiere de la anterior y posterior en un CH 2. Variación gradual de las propiedades físicas. Propiedades químicas semejantes

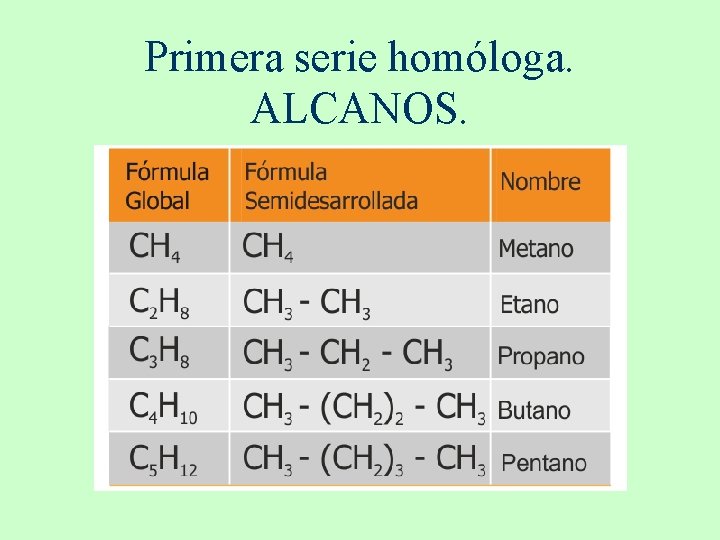
Primera serie homóloga. ALCANOS.

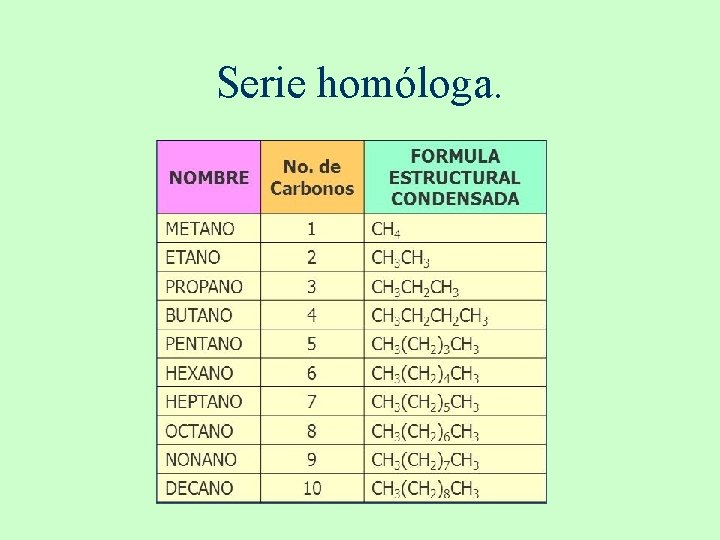
Serie homóloga.

SERIE HOMOLOGA ALCANOS

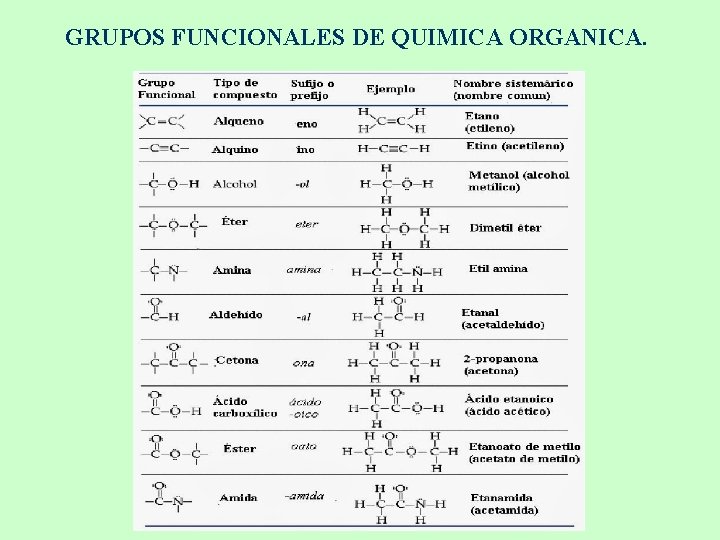
Grupos funcionales Es un átomo, o un conjunto de átomos, unido a un cadena carbonada representada por la fórmula general por R para los compuestos alifáticos y como Ar para los compuestos aromáticos y que son responsables de la reactividad y propiedades química de los compuestos orgánicos.

GRUPOS FUNCIONALES DE QUIMICA ORGANICA.
