SEMANA 13 SOLUCIONES BUFFER BUFFER Tambin llamado Solucin

SEMANA 13 SOLUCIONES BUFFER

BUFFER También llamado Solución Reguladora, Tampón o Amortiguadora. Es un sistema que tiende a mantener el p. H casi constante cuando se agregan pequeñas cantidades de ácidos (H+) ó bases (OH-).
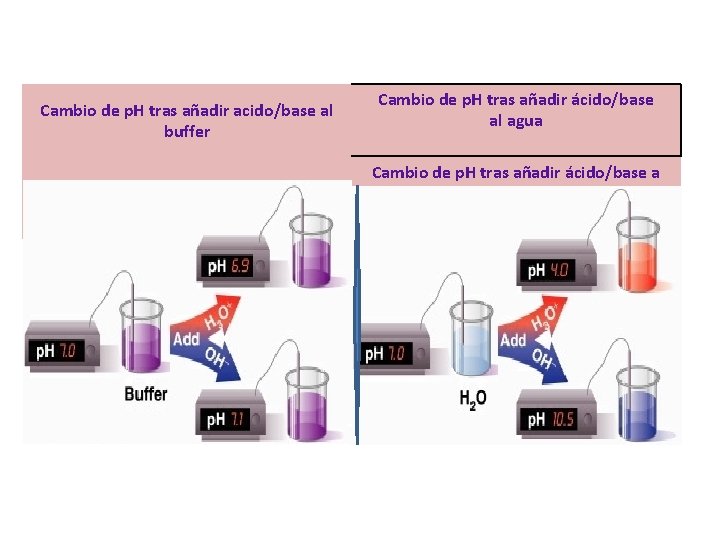
Cambio de p. H tras añadir acido/base al buffer Cambio de p. H tras añadir ácido/base al agua Cambio de p. H tras añadir ácido/base a una disolución amortiguadora

Una solución amortiguadora reduce el impacto de los cambios drásticos de H+ y OH -. Está formada por un ÁCIDO DÉBIL y una SAL del mismo ÁCIDO o por una BASE DÉBIL y una SAL de la misma BASE. La solución amortiguadora contiene especies que van a reaccionar con los iones H+ y OHagregados.

Componentes: Buffer ácido: Formado por un ácido débil y su sal. Ejemplo: CH 3 COOH/CH 3 COONa Buffer básico: Formado por una base débil y su sal. Ejemplo: NH 3/NH 4 Cl

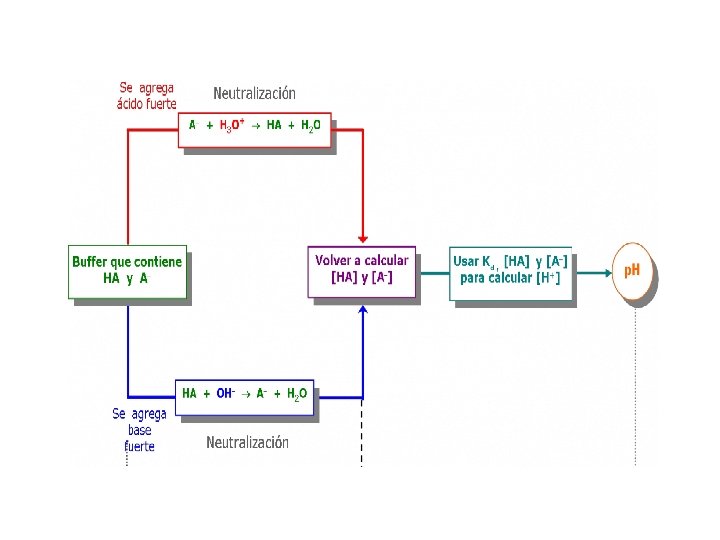
Capacidad amortiguadora de un Buffer Ácido Al agregar un ACIDO FUERTE: Los iones H+ adicionados reaccionan con la SAL del ÁCIDO DÉBIL en solución y producen el ÁCIDO DÉBIL. Buffer Ácido HCOOH/HCOO- Na+ HCOO- + H+ ↔ HCOOH

Al agregar una BASE FUERTE: los iones H+ presentes en solución neutralizan a los iones OH- produciendo H 2 O. Buffer Ácido: HCOOH/HCOO- Na+ HCOOH + OH- ↔ HCOO- + H 2 O
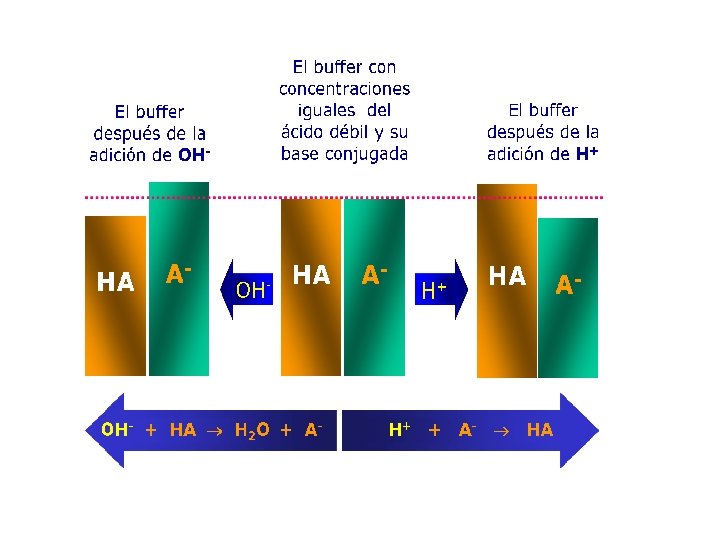
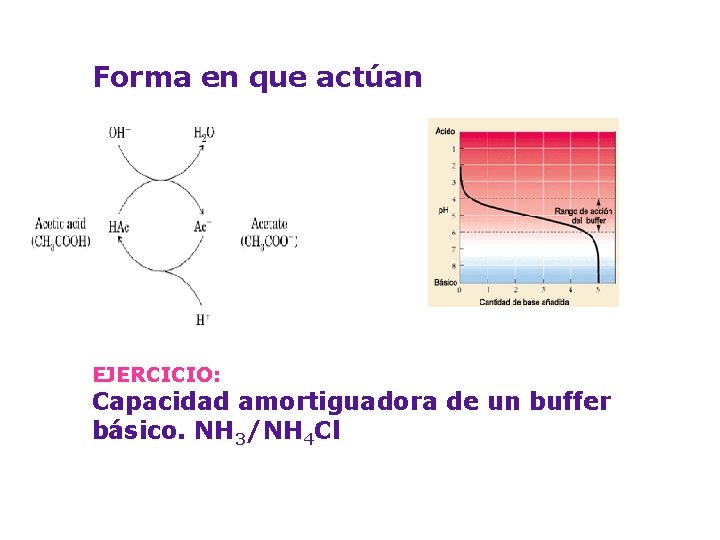
Forma en que actúan EJERCICIO: Capacidad amortiguadora de un buffer básico. NH 3/NH 4 Cl

Capacidad amortiguadora de un buffer básico Al agregar un ACIDO FUERTE: Los iones H+ adicionados reaccionan con la Base en solución y producen Sal y agua. NH 3/NH 4 Cl (NH 4 OH / NH 4 Cl ) NH 4 OH + H+ ↔ NH 4+ + H 2 O Al agregar una BASE FUERTE: Los iones OH- adicionados reaccionan con la sal para formar nuevamente la base débil. NH 4+ + OH- ↔ NH 4 OH

Función e Importancia Biológica: En los organismos vivos, las células deben mantener un p. H casi constante para la acción enzimática y metabólica. Los fluidos intracelulares y extracelulares contienen pares conjugados ácido-base que actúan como buffer.
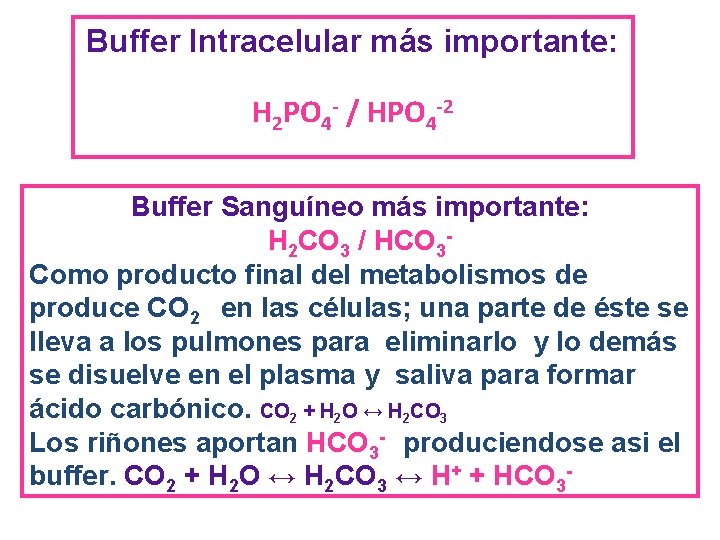
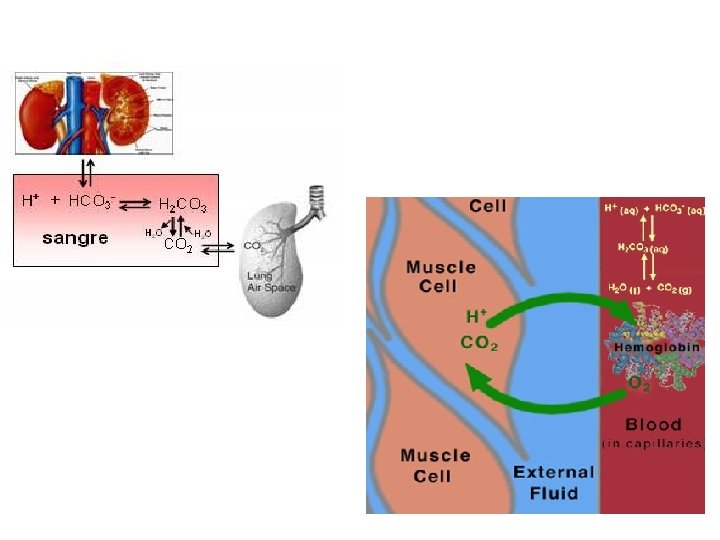
Buffer Intracelular más importante: H 2 PO 4 - / HPO 4 -2 Buffer Sanguíneo más importante: H 2 CO 3 / HCO 3 Como producto final del metabolismos de produce CO 2 en las células; una parte de éste se lleva a los pulmones para eliminarlo y lo demás se disuelve en el plasma y saliva para formar ácido carbónico. CO 2 + H 2 O ↔ H 2 CO 3 Los riñones aportan HCO 3 - produciendose asi el buffer. CO 2 + H 2 O ↔ H 2 CO 3 ↔ H+ + HCO 3 -

Otros sistemas que ayudan a mantener el p. H sanguíneo son: • Proteínas • Ácidos Nucleicos • Coenzimas • Metabolitos intermediarios Algunos poseen grupos funcionales que son ácidos o bases débiles, por consiguiente, ejercen influencia en el p. H intracelular y éste afecta la estructura y el comportamiento de las moléculas.

p. H sanguíneo 7. 35 -7. 45 Los cambios de p. H por debajo de 6. 8 y por encima de 8 no permiten el funcionamiento adecuado de las células y a éstos niveles sobreviene la muerte.

Valores Normales en Sangre Arterial Componentes Valor normal PCO 2 H 2 CO 3 HCO 3 - 40 mm. Hg 2. 4 mmoles/ L de plasma 2. 4 mmoles / L de plasma p. H 7. 35 – 7. 45
p. H sanguíneo Acidosis p. H debajo de 7. 35 -7. 45 Alcalosis p. H arriba de 7. 45

Tipos de Acidosis: Respiratoria y Metabólica Acidosis respiratoria: Al aumentar la concentración de CO 2 se produce mas H 2 CO 3; produciéndose mas H+ y por lo tanto el p. H disminuye por lo que hay acidosis, puede darse por respiración dificultosa, enfisema o neumonía. Al aumentar CO 2 el O 2 disminuye.

Resumiendo el proceso se daría así: La dificultad de respirar o un ambiente pobre en oxígeno, permite que se eleve la concentración de [CO 2] favoreciendo la formación de ácido carbónico, el cual se disocia en H+ y HCO 3 - de acuerdo a la siguiente reacción: CO 2 + H 2 O ↔ H 2 CO 3 ↔ H+ + HCO 3 -

Tipos de Alcalosis: Respiratoria y Metabólica Alcalosis respiratoria: Al aumentar la concentración O 2 disminuye la concentración de CO 2 y el p. H aumenta por lo que hay alcalosis, puede ser por hiperventilación o respiración rápida.
![La hiperventilación, genera: Alcalosis porque el incremento de la [O 2] hace bajar la La hiperventilación, genera: Alcalosis porque el incremento de la [O 2] hace bajar la](http://slidetodoc.com/presentation_image_h/0da2ea35b6fe2730afcc94492607ebbe/image-21.jpg)
La hiperventilación, genera: Alcalosis porque el incremento de la [O 2] hace bajar la [CO 2] produciéndose menos H 2 CO 3 y por consiguiente el p. H sube.
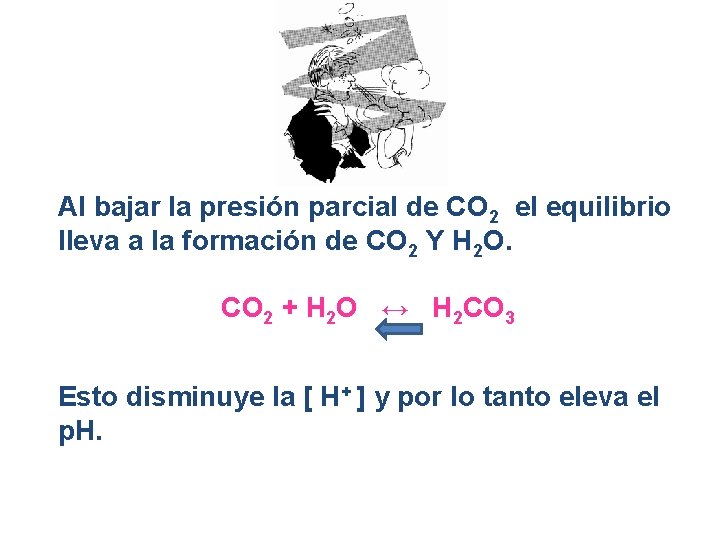
Al bajar la presión parcial de CO 2 el equilibrio lleva a la formación de CO 2 Y H 2 O. CO 2 + H 2 O ↔ H 2 CO 3 Esto disminuye la [ H+ ] y por lo tanto eleva el p. H.

p. Ka y p. Kb De la misma forma que para el p. H, hay expresiones similares para p. Ka y p. Kb, basadas en las constantes de ionización. p. Ka = - log Ka p. Kb = - log Kb Por lo tanto: cuanto mas grande es pka más débil es el ácido cuanto mas grande es p. Kb mas débil es la base Ejercicio: Encuentre el p. Ka del ácido acético, si posee un valor de Ka = 1. 8 x 10 -5.

Para un par conjugado ácido base el producto de Ka y Kb es igual a Kw. (Ka) (Kb) = Kw Por lo tanto cuando se conoce una de ellas se puede obtener el valor de la otra. Para un par conjugado ácido base : p. Ka + p. Kb = 14 (a 25 grados centígrados)
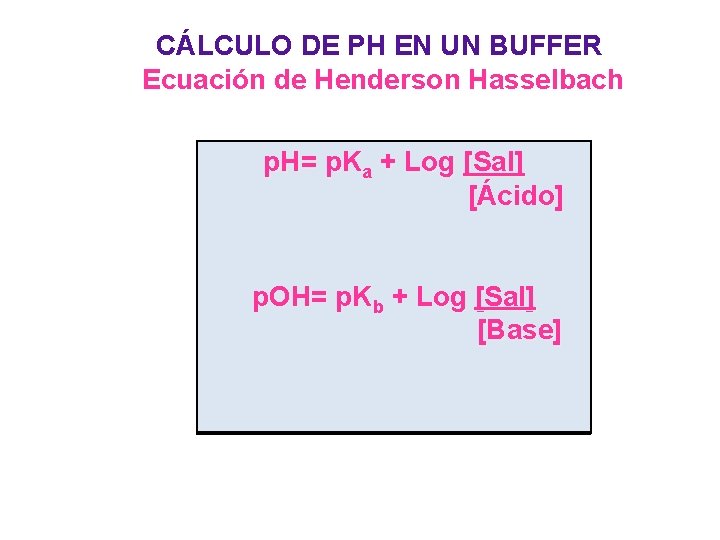
CÁLCULO DE PH EN UN BUFFER Ecuación de Henderson Hasselbach p. H= p. Ka + Log [Sal] [Ácido] p. OH= p. Kb + Log [Sal] [Base]
![Otro procedimiento para calcular p. H en soluciones Buffer: [H+] = Ka [ácido] [sal] Otro procedimiento para calcular p. H en soluciones Buffer: [H+] = Ka [ácido] [sal]](http://slidetodoc.com/presentation_image_h/0da2ea35b6fe2730afcc94492607ebbe/image-27.jpg)
Otro procedimiento para calcular p. H en soluciones Buffer: [H+] = Ka [ácido] [sal] p. H = -log [H+] [OH-] = Kb [base] [sal] [H+] = 1 X 10 -14 [OH]

1. Calcule el p. H de una solución Buffer formada por 0. 5 moles de CH 3 COOH (ácido acético) y 0. 8 moles de CH 3 COONa (acetato de sodio) disueltos en 1000 ml de solución. Ka = 1. 8 x 10 -5 [H+]= Ka [ácido] [sal] [H+]= 1. 8 x 10 -5 [0. 5 M] = 1. 125 x 10 -5 [0. 8 M] p. H = -log 1. 125 X 10 -5 = 4. 94

Resolución con la ecuación de Henderson. Hasselbach p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p. Ka = -log ( 1. 8 x 10 -5) = p. Ka =4. 74 p. H= 4. 74 + log (0. 8 M) (0. 5 M) p. H= 4. 74+0. 20= 4. 94
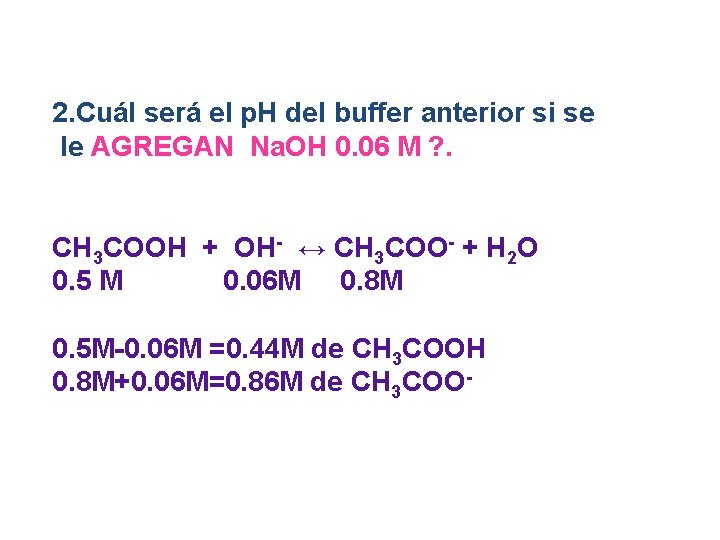
2. Cuál será el p. H del buffer anterior si se le AGREGAN Na. OH 0. 06 M ? . CH 3 COOH + OH- ↔ CH 3 COO- + H 2 O 0. 5 M 0. 06 M 0. 8 M 0. 5 M-0. 06 M =0. 44 M de CH 3 COOH 0. 8 M+0. 06 M=0. 86 M de CH 3 COO-
![NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p. NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p.](http://slidetodoc.com/presentation_image_h/0da2ea35b6fe2730afcc94492607ebbe/image-31.jpg)
NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p. Ka = -log ( 1. 8 x 10 -5) = p. Ka =4. 74 p. H= 4. 74 + log (0. 86 M) (0. 44 M) p. H= 4. 74 + 0. 29= 5. 03

3. ¿Cuál será el p. H del buffer inicial si añadimos HCl 0. 04 M ? CH 3 COONa + H+ ↔ CH 3 COOH + Na+ 0. 8 M 0. 04 M 0. 5 M 0. 8 M-0. 04 M =0. 76 M de CH 3 COO 0. 5 M+0. 04 M=0. 54 M de CH 3 COOH
![NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p. NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p.](http://slidetodoc.com/presentation_image_h/0da2ea35b6fe2730afcc94492607ebbe/image-33.jpg)
NUEVO p. H = p. Ka + log [sal] [ácido] p. Ka=-log Ka p. Ka = -log ( 1. 8 x 10 -5) = p. Ka =4. 74 p. H= 4. 74 + log (0. 76 M) (0. 54 M) p. H= 4. 74 + 0. 14= 4. 88

¿Cuál será el p. H de un buffer preparado asi: 4. 0. 2 moles de CH 3 NH 2 0. 3 moles de CH 3 NH 2 Cl en 1 Lt de solución? Kb= 4. 4 x 10 -4 [OH-]= Kb [base] [sal] [OH-]= 4. 4 x 10 -4 [0. 2 M] = 2. 93 x 10 -4 [0. 3 M] p. OH = -log 2. 93 X 10 -4 = 3. 53 p. H+ p. OH= 14 p. H= 14 - 3. 53= 10. 47

Resolución: (con la ecuación de Henderson. Hasselbach): p. OH = p. Kb + log [sal] [base] p. Kb=-log Kb p. Kb = -log ( 4. 4 x 10 -4) = p. Kb =3. 36 p. OH= 3. 36 + log (0. 3 M) (0. 2 M) p. OH= 3. 36 + 0. 176= 3. 53 p. H = 14 – 3. 53 = 10. 47

- Slides: 36