Semana 13 SISTEMAS Y SOLUCIONES REGULADORES BUFFER TAMPON

Semana 13 SISTEMAS Y SOLUCIONES REGULADORES BUFFER ó TAMPON 2013

Definición Los sistemas Buffer, amortiguadores, reguladores ó tampón son mezclas (soluciones, dispersiones coloidales), que tienden a mantener el p. H constante (con pocas variaciones) cuando se le añaden pequeñas cantidades de ácidos y bases.

Componentes de los Buffers A- Buffer ácidos: formados de un ácido débil y su sal. Ejemplos: CH 3 COOH / CH 3 COO-Na+. H 2 CO 3/ HCO 3 – ( Buffer carbonatos). H 2 PO 4 - / HPO 4 -2 ( Buffer de fosfatos). Note que el ácido débil posee un Hidrogeno más que la sal respectiva. Recuerde que todo ácido débil, tiene una Ka.

Cont. Comp. de los buffer B- Buffer Básicos: Formados por una base débil y su sal. Ejemplos: NH 3 / NH 4+Cl. C 6 H 5 NH 2 / C 6 H 5 NH 3+Cl. Note: La base débil posee un Hidrogeno menos que la sal respectiva. Recuerde que toda base débil, posee una Kb.

Importancia de los buffer en los sistemas vivos Todo organismo vivo, uni o pluricelular, posee dentro de sus células y fuera de ellas en caso de los pluricelulares, sistemas buffer que mantienen el p. H dentro de rangos muy constantes. Todo proceso metabólico, requiere de un p. H óptimo para realizarse y en cuál, los enzimas trabajan catalizando cada una de las reacciones. Si el p. H se altera, se alteran las funciones biológicas incluso se puede llegar a la muerte.

Sistemas buffer de importancia en los seres vivos Buffer de carbonato ( H 2 CO 3 / HCO 3 - ), es el más importante en la sangre y fluidos extracelulares. Buffer de Fosfatos ( H 2 PO 4 - / HPO 4 -2 ) Es el más importante buffer intracelular. Proteínas : tanto en la sangre como dentro de la célula participan en la regulación del p. H.

p. H fisiológico Es el rango de p. H, ideal ó adecuado, para un funcionamiento óptimo de los organismos. En el ser humano, el p. H fisiológico, es decir el p. H de la sangre, está dentro de: 7. 35 – 7. 45 Si el p. H baja y es menor de 7. 35, genera una condición conocida como Acidosis. Si el p. H aumenta y es mayor a 7. 45, genera una condición conocida como Alcalosis.

ACIDOSIS ( p. H sanguíneo menor de 7. 35 ) A- Respiratoria: Incremento de la [CO 2], debido a retención de CO 2, debido a inadecuada ventilación pulmonar o hipo ventilación. Ej: neumonía, enfisema, Asma, bloqueo de vías por cuerpo extraño. B-Metabólica: acumulación de ácidos ( Ej. Ácido láctico, cuerpos cetónicos), pérdida de bases, ej: diarrea, enfermedades renales, incapacidad de excretar orina ácida

ALCALOSIS ( p. H sanguíneo mayor de 7. 45) A-Respiratoria: disminución de la [CO 2], producida por hiperventilación ( ejercicio extenuante, tensión nerviosa). B-Metabólica: pérdida del contenido estomacal ( vómitos), sobredosis de bicarbonato, ó medicamentos para úlcera estomacal ( antiácidos e inhibidores de bomba de protones) enfermedad renal, abuso de diuréticos. Incremento en [ HCO 3 -].

Cómo actúa un Buffer ácido? A) Al añadir un ácido ( H+), la sal ( anión), se combina con el H+ forma el ácido débil, aumenta [ácido ] y disminuye [sal ]. Ej Buffer de H 2 CO 3 / HCO 3 – AÑADIMOS UN ÁCIDO H+ : HCO 3 - + H+ H 2 CO 3 (disminuye [HCO 3 -] ( la sal), aumenta [ H 2 CO 3] (el ácido) AÑADIMOS UNA BASE OH- : El ácido débil, dona un H +, que se combina con el OH- y forma agua. disminuye [ácido ]y aumenta [ sal ]. H 2 CO 3 + OH- HCO 3 - + H 2 O Disminuye [H 2 CO 3] ( el ácido) y aumenta [HCO 3 -]( la sal)
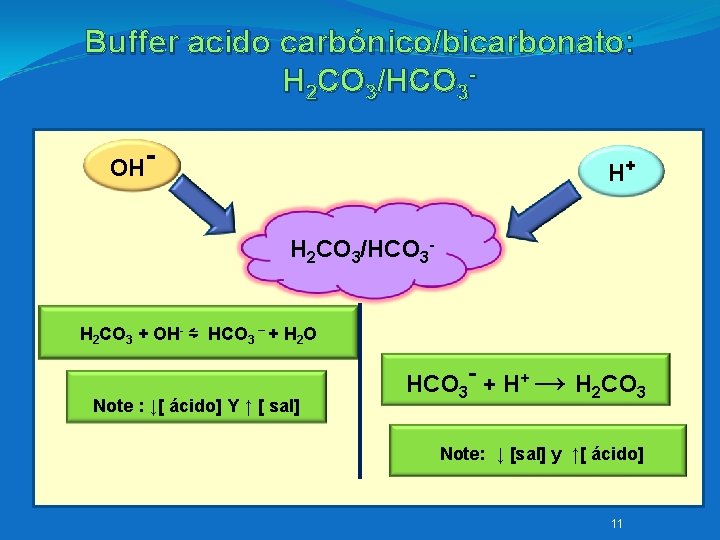
Buffer acido carbónico/bicarbonato: H 2 CO 3/HCO 3 OH- H+ H 2 CO 3/HCO 3 - H 2 CO 3 + OH- ⇋ HCO 3 – + H 2 O Note : ↓[ ácido] Y ↑ [ sal] HCO 3 - + H+ → H 2 CO 3 Note: ↓ [sal] y ↑[ ácido] 11
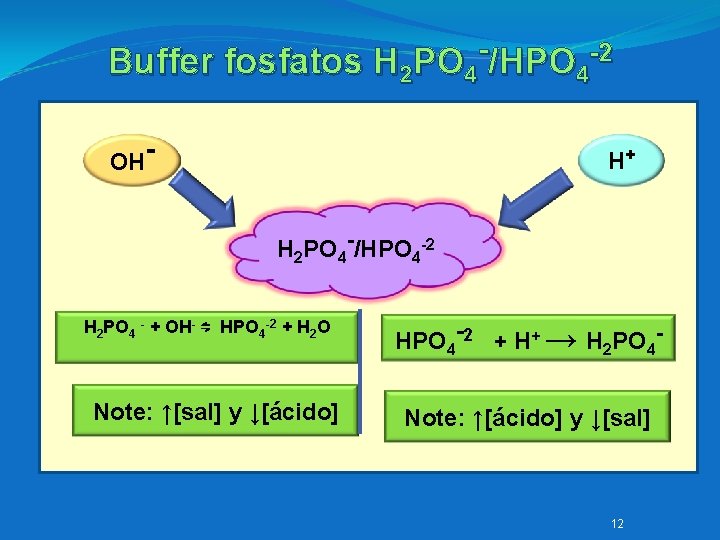
Buffer fosfatos H 2 PO 4 /HPO 4 -2 OH- H+ H 2 PO 4 -/HPO 4 -2 H 2 PO 4 - + OH- ⇋ HPO 4 -2 + H 2 O Note: ↑[sal] y ↓[ácido] HPO 4 -2 + H+ → H 2 PO 4 Note: ↑[ácido] y ↓[sal] 12
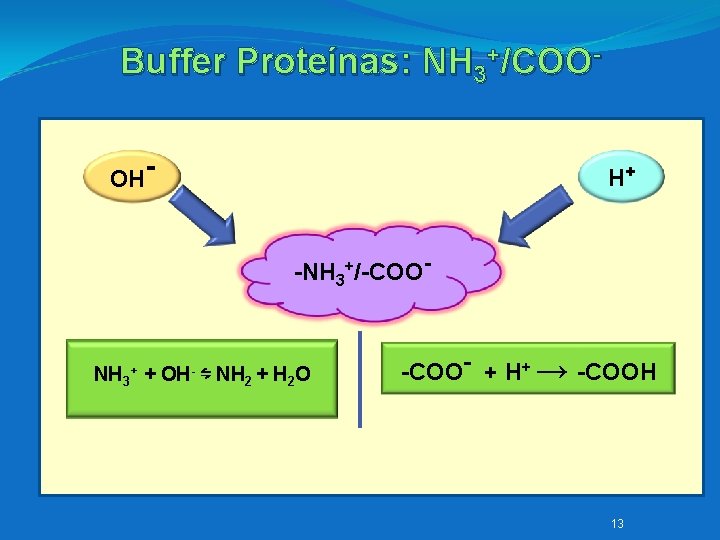
Buffer Proteínas: NH 3+/COOOH- H+ -NH 3+/-COO- NH 3+ + OH- ⇋ NH 2 + H 2 O -COO- + H+ → -COOH 13

Cómo actúa un buffer básico A) Al añadir un ácido, H+, la base lo acepta y forma la sal. Entonces aumenta [sal] y disminuye [base] Ejemplo NH 3 / NH 4+Cl -. NH 3 + H + NH 4+ Disminuye [NH 3]( la base) y aumenta [ NH 4 +](la sal) B) Al añadir una base OH-, la sal dona un H+, que se combina con el OH- y forma H 2 O. NH 4 + + OH- NH 3 + H 2 O Disminuye [NH 4+](la sal) y aumenta [NH 3](la base)

Fórmulas para calcular el p. H de los sistemas buffer: Se usaran las ecuaciones de Henderson-Hasselbach. A- Para Buffer ácidos: p. H = p. Ka + log [Sal]/ [Acido]. * Recordar que p. Ka, se calcula : p. Ka = -log Ka. * debe calcular la relación sal/ ácido y sacar el logaritmo. Como este puede ser positivo ó negativo, se sumará ó restará al p. Ka, según el caso.

Para buffer básicos 1) Calcular primero el p. OH, luego restarlo de 14. p. OH = p. Kb + log [Sal] [Base] Recordar que: p. Kb= - log Kb. Luego se calcula el p. H: ( recordar p. H + p. OH = 14 ) p. H = 14 - p. OH

Ejercicios. Calcule el p. H de un buffer de HCOOH 0. 2 M y HCOO-Na+ , 0. 27 M. Si Kb = 2. 1 x 10 -4. Procedimiento: Use p. H = p. Ka + log [sal] [acido] Calcule p. Ka : -log Ka p. Ka = -log 2. 1 x 10 -4 = 3. 67 p. H = 3. 67 + log [0. 27] [0. 20] p. H = 3. 67 + log 1. 35 p. H = 3. 67 +0. 13 = 3. 80 Respuesta = 3. 80

Ejercicio buffer básico. Calcule el p. H de una solución buffer formada por NH 3 0. 8 M y NH 4 Cl 0. 65 M. Kb= 1. 8 x 10 -5. Resolución, como es buffer básico, debe calcular primero el p. OH. Calcule p. Kb= -log Kb p. Kb= -log 1. 8 x 10 -5 p. Kb= 4. 74 p. OH = p. Kb +log [sal] [Base] p. OH = 4. 74 + log 0. 65 0. 80 p. OH = 4. 74 + log o. 81 p. OH = 4. 74 +( -0. 09) p. OH = 4. 65 Ahora calcule p. H así : p. H + p. OH = 14 p. H = 14 -p. OH p. H = 14 -4. 65 = 9. 35 p. H = 9. 35.

Ejemplo de buffer ácido añadiendo ácidos y bases. Calcule el p. H de una solución buffer de CH 3 COOH 0. 4 M y CH 3 COO-Na+ 0. 5 M. Ka = 1. 8 x 10 -5. Cuando: A) Se añade HCl 0. 08 M. Al añadir HCl, se está añadiendo H+, por lo tanto se incrementa [Acido] y disminuye [sal]. Ahora nuevas concentraciones: [CH 3 COOH]: 0. 4 + 0. 08 = 0. 48 [ Sal] : 0. 5 -0. 08 = 0. 42 Ahora calcule p. H: p. H = p. Ka + log [sal] / [acido] p. H= 4. 74 + log 0. 42 /0. 48 p. H = 4. 74+log 0. 875 p. H = 4. 74 + (-0. 058) p. H = 4. 68

Continuación de ejercicio: B- Se añade Na. OH 0. 06 M. Al añadir Na. OH, se está añadiendo OH-. Entonces disminuye [ácido] y aumenta [sal]. Las nuevas concentraciones son : [CH 3 COOH] = 0. 4 -0. 06 = 0. 34 [CH 3 COO-Na+] = 0. 5 +0. 06 = 0. 56. Ahora se calcula p. H: p. H = Pka + log [sal] [acido] p. H = 4. 74 + log 0. 56/0. 34 p. H = 4. 74 +log 1. 64 p. H = 4. 74 + 0. 21 = 4. 95

Comparación de el p. H, después de + añadir H y OH Si calculamos el p. H del buffer sino se le hubiera añadido H+ y OH-, tenemos: p. H = p. Ka + log [sal] [ácido] p. H = 4. 74 + log [CH 3 COONa] [CH 3 COOH] p. H = 4. 74 + log 0. 5/0. 4 p. H= 4. 74 + log 1. 25 p. H = 4. 74 + 0. 097 = 4. 84 Ahora vea al añadir el HCl ( ácido) bajo a 4. 68 Y al añadir Na. OH ( base). subió a 4. 95. usted puede ver que las variaciones fueron mínimas.

Ej: cálculo de p. H de buffer básico Calcule el p. H de un buffer formado por trimetilamina 0. 3 M ( Kb= 6. 0 x 10 -5 ) y cloruro de trimetilamonio 0. 4 M. Resolución en éste caso la trimetilamina es la base y el cloruro de trimetil amonio es la sal. Como es base, se calcula primero el p. OH usando la fórmula ya dada: p. OH = p. Kb +log [sal] / [Base] p. Kb= -log 6. 0 x 10 -5 = 4. 22 p. OH = 4. 22 + log 0. 4/0. 3 p. OH = 4. 22 +log 1. 33 po. H = 4. 22 + 0. 125 p. OH = 4. 34 Ahora calcule p. H: Recuerde que p. H + p. OH = 14 p. H = 14 – p. OH p. H = 14 - 4. 34 p. H = 9. 66

Cont. Ejercicios de Buffer básicos. Calcule el p. H de una solución buffer que contiene NH 3 0. 4 M y NH 4 Cl 0. 3 M. Kb = 1. 74 x 10 -5 Resolución : recuerde que es base, se calcula el p. OH primero y luego el p. H. p. OH = p. Kb + log Sal/ Base p. OH = 4. 76 + log 0. 3 / 0. 4 p. OH = 4. 76 + (-0. 125) p. OH = 4. 63 ahora calcule p. H = 14 –p. OH p. H = 14 – 4. 63 p. H = 9. 37. Que sucede si añadimos HCl 0. 07 M La base disminuye: 0. 4 – 0. 07 = 0. 33 y la sal aumenta 0. 3 + o. o 7 = 0. 37 p. OH=p. Kb + log sal/base p. OH = 4. 63+log 0. 37 / 0. 33 p. OH = 4. 68.

Lea y comenta “Química y salud”pág. 306 “Tampones en la sangre”.
- Slides: 24