SEMANA 13 AMORTIGUADORES O BUFFER QUMICA 2020 1

SEMANA 13 AMORTIGUADORES O BUFFER QUÍMICA 2020 1

SEMANA 12 BUFFER O AMORTIGUADORES Buffer (sistemas amortiguadores, soluciones reguladoras o tampón) Buffer: definición, componentes y función. Buffer sanguíneos. Buffer intracelular. Fórmula de Henderson Hasselbach. Cálculo de p. H de buffer ácidos y básicos después de haber agregado un ácido o una base. Acidosis y alcalosis: Definición y Clasificación -Respiratoria y Metabólica Importancia médica de la acidosis y alcalosis Aplicación de los conceptos en la salud. Lecturas en libro de texto - La Química en la Salud: “Disoluciones amortiguadoras en la sangre” Laboratorio: Soluciones Buffer

Definición • Los Buffer son soluciones que pueden mantener su p. H casi sin variar aún cuando se les agregan pequeñas cantidades de ácidos ó bases, evitando cambios bruscos de p. H. • Las soluciones Buffer tienen esta capacidad ya que pueden actuar reaccionando como ácidos o como bases, neutralizando las pequeñas cantidades tanto de ácidos como bases que se les agreguen. 3
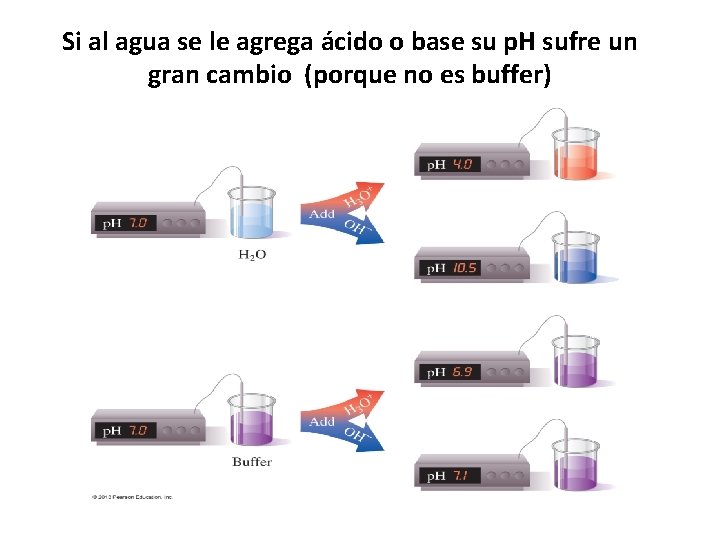
Si al agua se le agrega ácido o base su p. H sufre un gran cambio (porque no es buffer)

Los buffer pueden ser de dos tipos: • Buffer ácido: consiste en la mezcla de un ácido débil y su base conjugada. (puede neutralizar tanto ácidos y bases que se le agreguen). Se preparan disolviendo en agua un ácido débil y su sal (que formará la base conjugada). • Buffer básico: consiste en la mezcla de una base débil y su ácido conjugado. (puede neutralizar tanto ácidos y bases que se le agreguen). Se prepara disolviendo en agua una base débil y su sal (que formará el ácido conjugado).
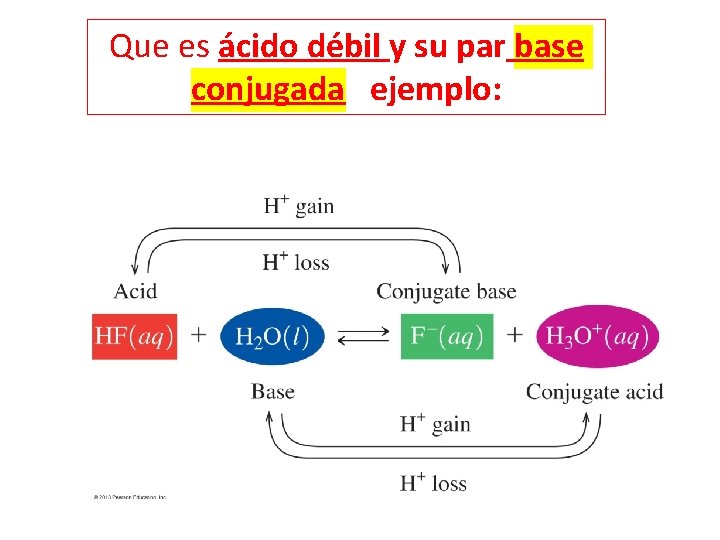
Que es ácido débil y su par base conjugada ejemplo:
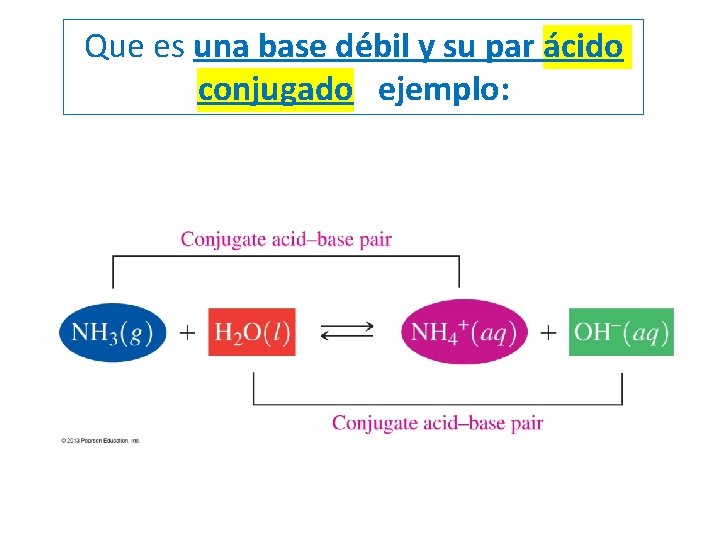
Que es una base débil y su par ácido conjugado ejemplo:
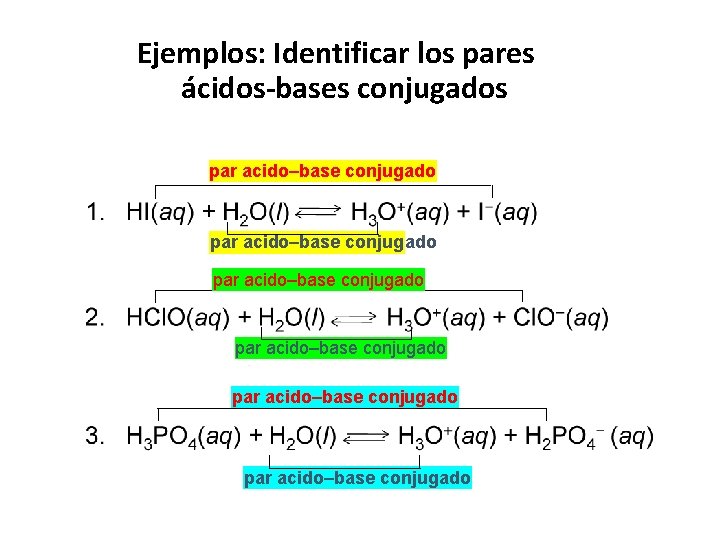
Ejemplos: Identificar los pares ácidos-bases conjugados par acido–base conjugado par acido–base conjugado

Otros ejemplos de pares conjugados 1. La base conjugada de HCO 3− es, CO 32−. 2. El ácido conjugado de HCO 3− es H 2 CO 3. 3. La base conjugada de H 2 O es OH−. 4. El ácido conjugado de H 2 O es H 3 O+.

Ejemplos de como se pueden representar los Buffer ácidos = ácido débil/sal ó base conjugada Ej: Buffer de Acetatos: CH 3 COOH / CH 3 COOBuffer de Carbonatos: H 2 CO 3 / HCO 3 Buffer de Fosfatos: H 2 PO 4 - / HPO 4 -2 (el que actúa como ácido es el que presenta más H) Buffer Básicos = base débil/sal ó ácido conjugado Buffer de Amoníaco: NH 3 /NH 4+ (el que actúa como base es el que presenta menos H) Todos los buffer por ser débiles tienen su Ka o Kb 10
![Como calcular el p. H de un Buffer: se despeja [OH-] o [H+] de Como calcular el p. H de un Buffer: se despeja [OH-] o [H+] de](http://slidetodoc.com/presentation_image_h/9bc281c716e45b0bfc7a61c037e1290b/image-11.jpg)
Como calcular el p. H de un Buffer: se despeja [OH-] o [H+] de la Ka o Kb y queda: BUFFER ÁCIDO BUFFER BÁSICO [H+] = Ka [ácido] [base conjug. o sal] [OH- ] = Kb [base] [ácido conjug. o sal] p. H= -log [H+] p. OH= -log [OH-] p. H= 14 - p. OH 11

Ejercicios de cálculo de p. H de Buffer 1. ¿Cuál es el p. H de un buffer preparado con ácido acético (CH 3 COOH) 0. 4 M y su sal acetato de sodio (CH 3 COONa ó CH 3 COO-) 0. 35 M? Ka= 1. 8 x 10 -5 [H+] = Ka [ácido] [H+] =1. 8 x 10 -5 [0. 4] = 2. 06 x 10 -5 M [0. 35] p. H= -log 2. 06 x 10 -5 [base conj. o sal] = 4. 69 p. H 2. ¿Cuál es el p. H de un buffer de amoníaco (NH 3) 0. 6 M y cloruro de amonio (NH 4 Cl ó NH 4+) 0. 55 M? Kb= 1. 8 x 10 -4 [OH- ] = Kb [base] [OH- ] =1. 8 x 10 -4 [ 0. 6 ] = 1. 96 x 10 -4 M [ácido conj. o sal] [0. 55] p. OH= -log 1. 96 x 10 -4 = 3. 71 p. OH p. H=14 – 4= 10. 29 p. H 12

Como reaccionan o neutralizan los componentes de un buffer al agregarles ácidos y bases para amortiguar o neutralizarlos y evitar cambios bruscos de p. H Ejemplos: Buffer de acetatos: CH 3 COOH(ácido débil)/CH 3 COO-(base conjugada) Al agregarle base (OH-): el CH 3 COOH + OH- ⇄ CH 3 COO- +H 2 O (Aumenta la concentración de CH 3 COO- y disminuye CH 3 COOH) Al agregarle ácido (H+): CH 3 COOH ⇄ CH 3 COO - + H+ (Aumenta la concentración de CH 3 COOH y disminuye CH 3 COO-) Buffer de amonio: NH 3(base débil) /NH 4+(ácido conjugado) Al agregarle ácido: NH 3 + H+ ⇄ NH 4+ (Aumenta la concentración de NH 4+ y disminuye NH 3) 13 Al agregarle base: NH 3 + H 2 O ⇄ NH 4+ + OH(Aumenta la concentración de NH 3 y disminuye NH 4+ )
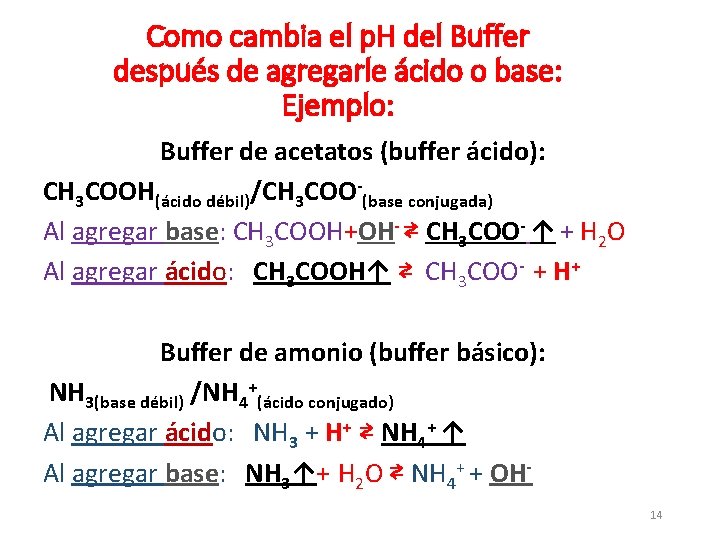
Como cambia el p. H del Buffer después de agregarle ácido o base: Ejemplo: Buffer de acetatos (buffer ácido): CH 3 COOH(ácido débil)/CH 3 COO-(base conjugada) Al agregar base: CH 3 COOH+OH- ⇄ CH 3 COO- ↑ + H 2 O Al agregar ácido: CH 3 COOH↑ ⇄ CH 3 COO- + H+ Buffer de amonio (buffer básico): NH 3(base débil) /NH 4+(ácido conjugado) Al agregar ácido: NH 3 + H+ ⇄ NH 4+ ↑ Al agregar base: NH 3↑+ H 2 O ⇄ NH 4+ + OH 14
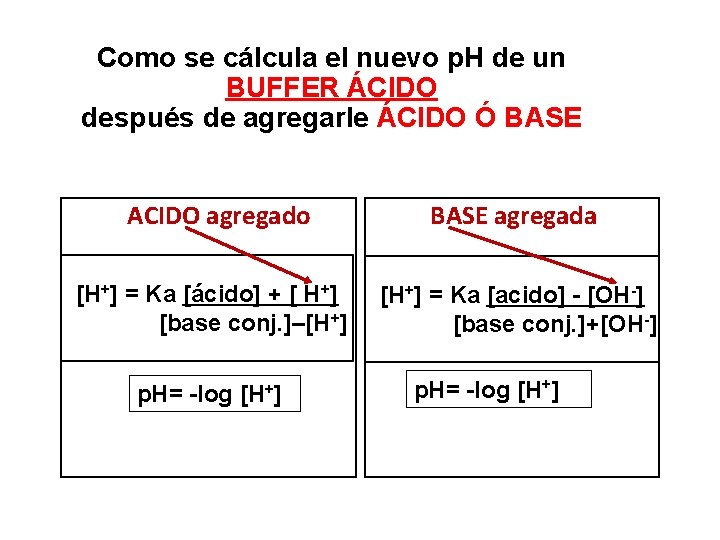
Como se cálcula el nuevo p. H de un BUFFER ÁCIDO después de agregarle ÁCIDO Ó BASE ACIDO agregado BASE agregada [H+] = Ka [ácido] + [ H+] [base conj. ]–[H+] = Ka [acido] - [OH-] [base conj. ]+[OH-] p. H= -log [H+] 15
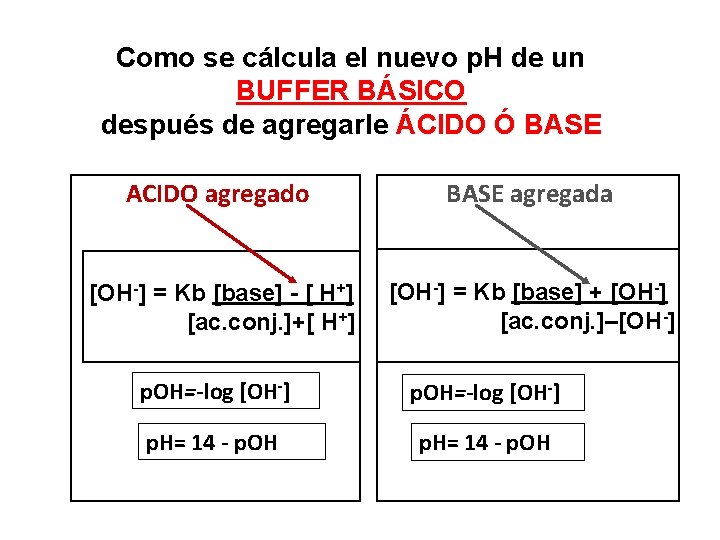
Como se cálcula el nuevo p. H de un BUFFER BÁSICO después de agregarle ÁCIDO Ó BASE ACIDO agregado BASE agregada [OH-] = Kb [base] - [ H+] [ac. conj. ]+[ H+] [OH-] = Kb [base] + [OH-] [ac. conj. ]–[OH-] p. OH=-log [OH-] p. H= 14 - p. OH 16
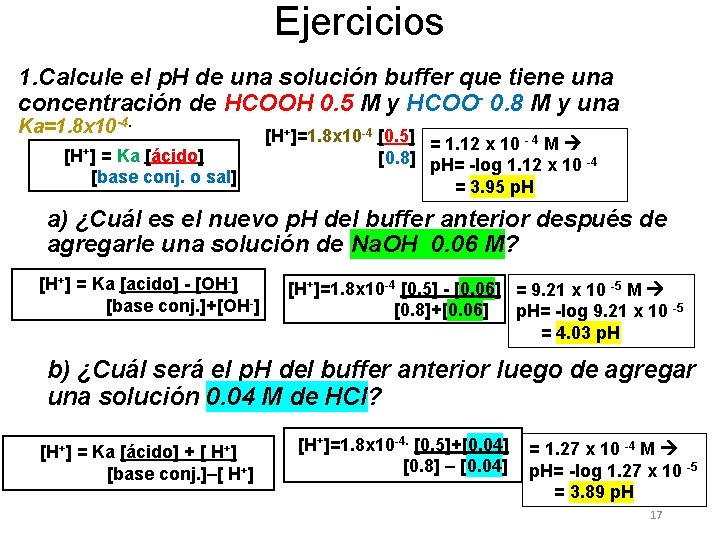
Ejercicios 1. Calcule el p. H de una solución buffer que tiene una concentración de HCOOH 0. 5 M y HCOO- 0. 8 M y una Ka=1. 8 x 10 -4. [H+] = Ka [ácido] [base conj. o sal] [H+]=1. 8 x 10 -4 [0. 5] = 1. 12 x 10 - 4 M [0. 8] p. H= -log 1. 12 x 10 -4 = 3. 95 p. H a) ¿Cuál es el nuevo p. H del buffer anterior después de agregarle una solución de Na. OH 0. 06 M? [H+] = Ka [acido] - [OH-] [base conj. ]+[OH-] [H+]=1. 8 x 10 -4 [0. 5] - [0. 06] = 9. 21 x 10 -5 M [0. 8]+[0. 06] p. H= -log 9. 21 x 10 -5 = 4. 03 p. H b) ¿Cuál será el p. H del buffer anterior luego de agregar una solución 0. 04 M de HCl? [H+] = Ka [ácido] + [ H+] [base conj. ]–[ H+] [H+]=1. 8 x 10 -4. [0. 5]+[0. 04] [0. 8] – [0. 04] = 1. 27 x 10 -4 M p. H= -log 1. 27 x 10 -5 = 3. 89 p. H 17

2. ¿Cuál es el p. H de un buffer de amoniaco (NH 3) 0. 2 M y cloruro de amonio (NH 4 Cl) 0. 18 M y Kb=1. 8 x 10 -5 [OH- ] =1. 8 x 10 -5 [0. 2] =2 x 10 -5 M [OH- ] = Kb [base] [0. 18] p. OH = -log 2 x 10 -5=4. 7 [ácido conj. o sal] p. H= 14 - 4. 7 = 9. 3 p. H a)¿Cuál es el nuevo p. H del buffer anterior después de agregar HCl 0. 01 M? [OH-]=1. 8 x 10 -5 [0. 2 -[ 0. 01] =1. 8 x 10 -5 M [OH-] = Kb [base] - [ H+] [0. 18]+[0. 01] p. OH= -log 1. 8 x 10 -5= 4. 74 [ac. conj. ]+[ H+] p. H= 14 - 4. 74 = 9. 25 p. H b)¿Cuál es el nuevo p. H si se agrega Na. OH 0. 02 M? [OH-] = Kb [base] + [OH-]=1. 8 x 10 -5 [0. 2]+[0. 02] =2. 48 x 10 -5 M [ac. conj. ]–[OH-] [0. 18]–[0. 02] p. OH =-log 2. 48 x 10 -5= 4. 6 p. H= 14 - 4. 6 = 9. 39 p. H 18

Importancia del p. H en los seres vivos p. H fisiológico normal: 7. 35 – 7. 45 • El p. H de la sangre debe mantenerse entre los valores normales 7. 35 – 7. 45 para que las enzimas catalicen las reacciones en los procesos metabólicos. Si el p. H sube ó baja de estos rangos, puede causar la muerte. • Si baja a menos de 7. 35 se produce ACIDOSIS • Si sube a más de 7. 45 se produce ALCALOSIS Para que se mantengan normales estos valores, el cuerpo cuenta con varios sistemas buffer que son: 19

Sistemas buffer sanguíneos 1. Buffer de Carbonatos: es el más importante en la sangre y en los fluídos extracelulares: H 2 CO 3 / HCO 3 - (también se puede escribir HCO 3 - /H 2 CO 3) (H 2 CO 3 actúa como ácido y HCO 3 - como base) 2. Buffer de Fosfatos: es el más importante intracelular: H 2 PO 4 - / HPO 4 -2 (también se puede escribir HPO 4 -2 /H 2 PO 4 -) (H 2 PO 4 - actúa como ácido y HPO 4 -2 como base) 3. Proteínas. (Recorar: el componente del buffer que tiene más H actúa como ácido, el de menos H actúa como base) 20

La alteración del p. H fisiológico puede causar: Acidosis: exceso de ácido (H+) en los líquidos del cuerpo, puede ser respiratoria ó metabólica. Acidosis Respiratoria: Aumento de concentración de ión hidrógeno (H+) debido a la retención de CO 2 por una hipo ventilación (CO 2 p. H ) Acidosis Metabólica: Acumulación de H+ del metabolismo e incapacidad para su eliminación, ó pérdida de bases (H+ p. H ) 21

Alcalosis: exceso de base (álcali) OH- en los líquidos del cuerpo, puede ser respiratoria ó metabólica. Alcalosis Respiratoria: Ocasionado por niveles bajos de CO 2 debido a hiperventilación (CO 2 p. H ) Alcalosis Metabólica: Exceso de bicarbonato HCO 3 - en la sangre y disminución del ión hidrógeno (H+ p. H ) 22

RESUMEN RESPIRATORIA CO 2 ↑ p. H ↓ METABOLICA H+ p. H ↓ ACIDOSIS RESPIRATORIA ↑ CO 2 ↓ p. H ↑ H+ ↑ ALCALOSIS METABOLICA ↓ p. H 23
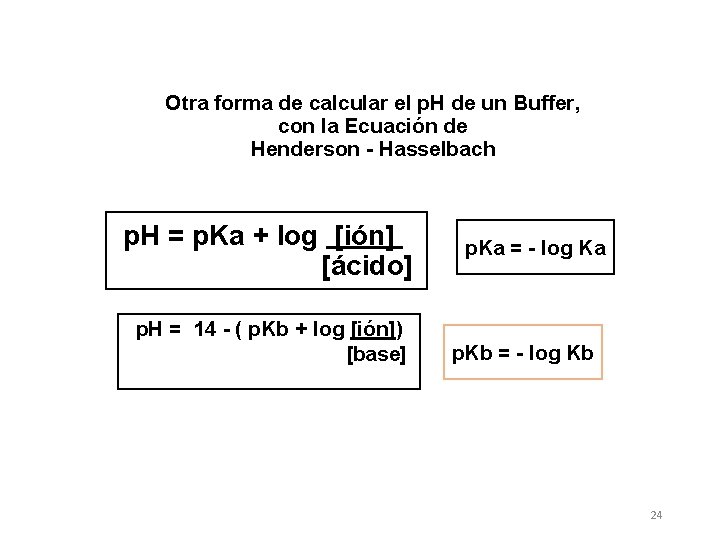
Otra forma de calcular el p. H de un Buffer, con la Ecuación de Henderson - Hasselbach p. H = p. Ka + log [ión] [ácido] p. H = 14 - ( p. Kb + log [ión]) [base] p. Ka = - log Ka p. Kb = - log Kb 24
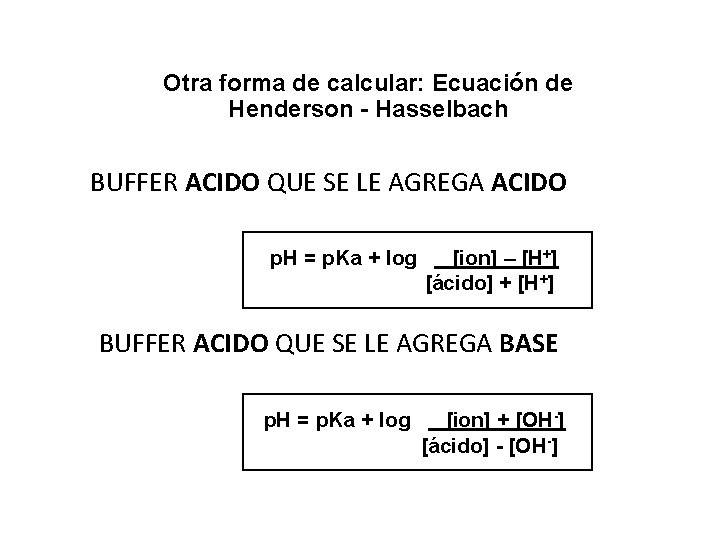
Otra forma de calcular: Ecuación de Henderson - Hasselbach BUFFER ACIDO QUE SE LE AGREGA ACIDO p. H = p. Ka + log [ion] – [H+] [ácido] + [H+] BUFFER ACIDO QUE SE LE AGREGA BASE p. H = p. Ka + log [ion] + [OH-] [ácido] - [OH-] 25
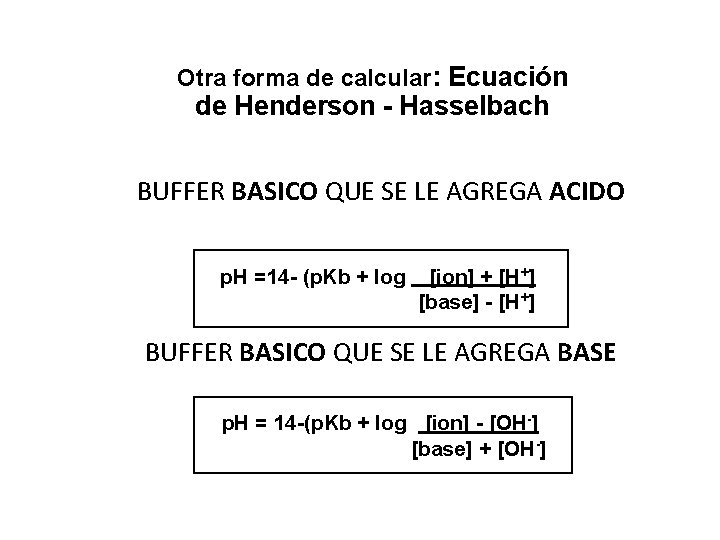
Otra forma de calcular: Ecuación de Henderson - Hasselbach BUFFER BASICO QUE SE LE AGREGA ACIDO p. H =14 - (p. Kb + log [ion] + [H+] [base] - [H +] BUFFER BASICO QUE SE LE AGREGA BASE p. H = 14 -(p. Kb + log [ion] - [OH-] [base] + [OH -] 26
- Slides: 26