SEMANA 12 CIDOS BASES Y ELECTROLITOS QUMICA 2019

SEMANA 12 ÁCIDOS, BASES Y ELECTROLITOS QUÍMICA 2019 1

Semana 12 ÁCIDOS, BASES Y ELECTROLITOS Definición de ácidos y bases según: Arrhenius, Bronsted-Lowry y Lewis. Definición de electrolitos: Fuertes y débiles. No electrolitos Ionización de: Agua (Kw) Ácidos y bases fuertes Ácidos y bases débiles (Ka, Kb y % de ionización) Escala de acidez. Definición de y cálculos de p. H, p. OH, [H+], [OH-] Neutralización Titulación ácido-base Aplicación de los conceptos en la salud y el ambiente. Lecturas en el libro de texto -La Química en el Ambiente “Lluvia àcida” -La Química en la Salud: “Àcido estomacal, HCl”. “Antiàcidos” - Otras que se informe. Laboratorio: MEDICIÓN DE PH, ELECTROLITOS Y TITULACIÓN 2

ACIDOS Y BASES ACIDO BASE, HIDROXIDO o ALCALI Del latín Acidus= agrio Ej: vinagre, jugo de limón, HCl, H 2 SO 4. Tienen un sabor agrio o ácido y pueden producir sensación de picazón en la piel. Ej: antiácidos, líquidos limpia vidrios y destapa-desagües, Na. OH, Al(OH)3 Que tiene un sabor amargo y sensación resbalosa en la piel. HAY VARIAS DEFINICIONES DE ACIDO Y BASE 3
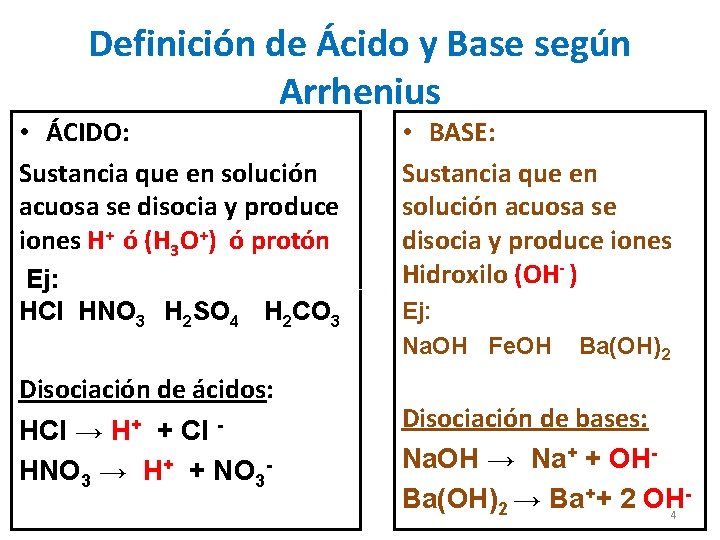
Definición de Ácido y Base según Arrhenius • ÁCIDO: Sustancia que en solución acuosa se disocia y produce iones H+ ó (H 3 O+) ó protón Ej: HCl HNO 3 H 2 SO 4 H 2 CO 3 Disociación de ácidos: HCl → H+ + Cl HNO 3 → H+ + NO 3 - • BASE: Sustancia que en solución acuosa se disocia y produce iones Hidroxilo (OH- ) Ej: Na. OH Fe. OH Ba(OH)2 Disociación de bases: Na. OH → Na+ + OHBa(OH)2 → Ba++ 2 OH 4
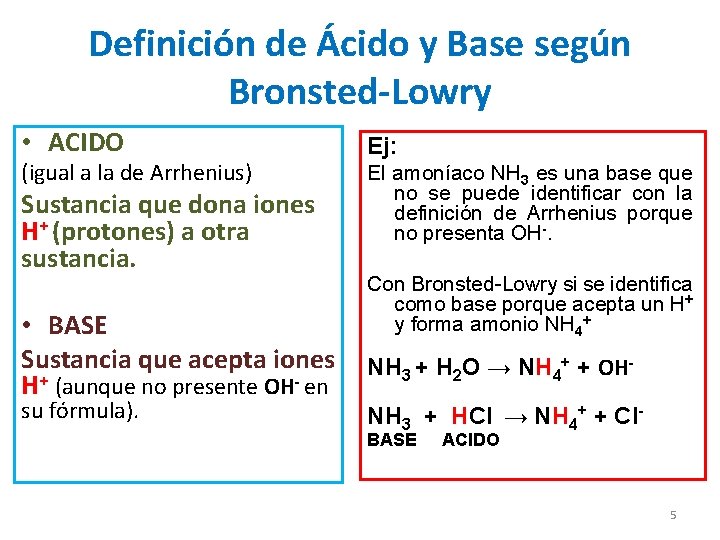
Definición de Ácido y Base según Bronsted-Lowry • ACIDO (igual a la de Arrhenius) Sustancia que dona iones H+ (protones) a otra sustancia. Ej: El amoníaco NH 3 es una base que no se puede identificar con la definición de Arrhenius porque no presenta OH-. Con Bronsted-Lowry si se identifica como base porque acepta un H+ y forma amonio NH 4+ • BASE Sustancia que acepta iones NH 3 + H 2 O → NH 4+ + OHH+ (aunque no presente OH- en su fórmula). NH 3 + HCl → NH 4+ + Cl. BASE ACIDO 5

Definición de Ácido y Base según LEWIS • ACIDO: Sustancia que puede aceptar un par de electrones de otra sustancia (aunque no tenga H) Ej: BF 3 • BASE: Sustancia que puede ceder un par de electrones a otra sustancia. Ej: NH 3 ACIDO BASE Enlace covalente dativo 6
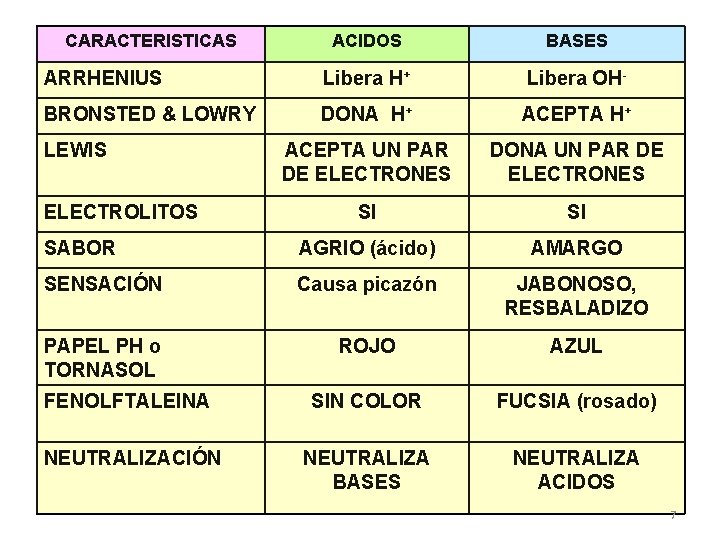
CARACTERISTICAS ACIDOS BASES ARRHENIUS Libera H+ Libera OH- BRONSTED & LOWRY DONA H+ ACEPTA UN PAR DE ELECTRONES DONA UN PAR DE ELECTRONES SI SI SABOR AGRIO (ácido) AMARGO SENSACIÓN Causa picazón JABONOSO, RESBALADIZO PAPEL PH o TORNASOL ROJO AZUL FENOLFTALEINA SIN COLOR FUCSIA (rosado) NEUTRALIZACIÓN NEUTRALIZA BASES NEUTRALIZA ACIDOS LEWIS ELECTROLITOS 7

ELECTROLITOS Sustancias (ácidos, bases o sales) que en solución acuosa se separan o disocian en iones y CONDUCEN LA ELECTRICIDAD. Según el grado o % en que se ionizan se clasifican en: electrolitos fuertes, débiles y no electrolito. ELECTROL. FUERTE ELECTROLITO DÉBIL § Se disocian al 100% § Se disocian en un pequeño % § Buen conductor de la § Conduce poco la electricidad § Su reacción de ionización es Su reacción de ionización reversible ⇄. Ej: es irreversible →. Ej: KOH → K+ + OH- H 2 CO 3 ⇄ 2 H+ + CO 3 - H 2 SO 4 → 2 H++ SO 4 -2 NH 3 + H 2 O ⇄ NH 4+ + OH- 8
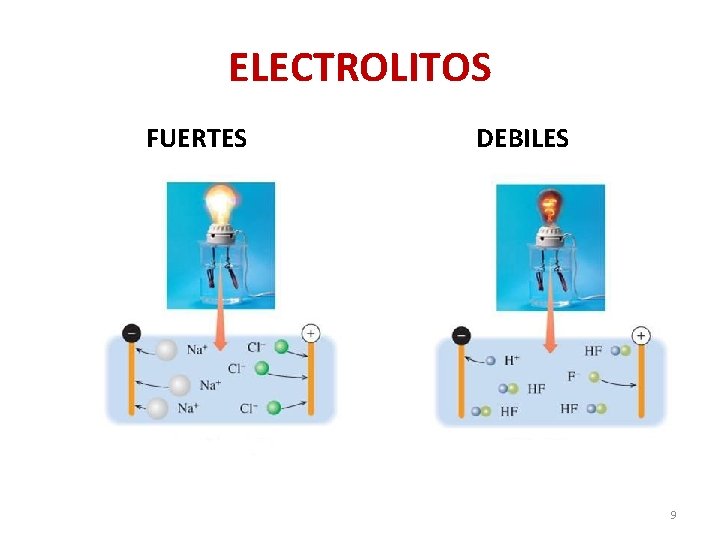
ELECTROLITOS FUERTES DEBILES 9

NO ELECTROLITO Sustancias que en estado líquido o solución, NO conduce la corriente eléctrica. Generalmente son compuestos orgánicos (con carbono). Ej: • Alcohol (CH 3 CH 2 OH) • Gasolina (C 7 H 16) • Azúcar (C 12 H 22 O 11) azúcar 10

• ACIDOS Y ACIDOS y BASES FUERTES: Se ionizan casi en un 100% Ej: BASES FUERTES + Una solución de HCl 0. 15 M produce 0. 15 M de H Una solución de 0. 12 Na. OH produce 0. 12 M de OH • Tienen una ionización irreversible • No tienen constantes de ionización (Ka), (Kb) Ej: HCl Ácido Clorhídrico HBr Ácido Bromhídrico HI Ácido Yodhídrico H 2 SO 4 Ácido sulfúrico HNO 3 Ácido Nítrico 11

ÁCIDOS DÉBILES • Se ionizan muy poco, menos de un 5% • Tienen una ionización reversible • Tienen constantes de ionización (Ka) Ej: Ácido Fórmico HCOOH Ka = 2. 1 x 10 - 4 Ácido fluorhídrico HF Ka = 7. 2 x 10 - 4 Acido cianhídrico HCN Ka = 4. 9 x 10 -10 Ácido láctico CH 3 CHOHCOOH Ka = 1. 4 x 10 - 4 12

BASES DÉBILES • Se ionizan muy poco, menos de un 5% • Tienen una ionización reversible • Tienen constantes de ionización (Kb) Ejemplos: Anilina C 6 H 5 NH 2 Kb: 4. 0 x 10 -10 Amoniaco NH 3 Kb = 1. 8 x 10 -5 13

Aplicación del % de Ionización en electrolitos fuertes y débiles 1. ¿Cuál es la [H+] y el % de ionización de una solución de HCl 0. 15 M ? 2. ¿Cuál es la [OH-] y el % de ionización de una solución de Na. OH 0. 22 M? 3. ¿Cuál es el % de ionización de una solución de CH 3 COOH 0. 13 M que tiene una [H+]de 0. 011 M? 4. ¿Cuál es la [OH-] de una solución de NH 3 (NH 4 OH) 0. 3 M que se ioniza en un 12% ? 14

Cálculo de la CONSTANTE DE IONIZACIÓN (Ka) para ÁCIDOS DÉBILES Como se ionizan muy poco y es reversible tienen su Expresión de la Constante de Equilibrio que se llamará Constante de ionización del Acido (Ka). Ejemplo: x x ácido acético CH 3 COOH ⇄ H+ + CH 3 COO De esta expresión se despeja y averigua la concentración de H+ que utilizaremos para calcular el p. H. 15

Cálculo de la CONSTANTE DE IONIZACIÓN (Ka) para BASES DÉBILES Como se ionizan muy poco y es reversible tienen su Expresión de la Constante de Equilibrio que se llamará Constante de ionización de la Base (Kb). Ejemplo: x x amoníaco NH 3 + H 2 O ⇄ NH 4+ + OH De esta expresión se despeja y averigua la concentración de OH- que utilizaremos para calcular el p. OH. 16 (NO se toma en cuenta el H 2 O en las expresiones de Kb y Ka)

IONIZACION DEL AGUA (Debido a que los ácidos y las bases se encuentran disueltos en soluciones acuosas y es allí donde liberan sus H+ y OH- , debemos conocer como se afectarán las concentraciones de H+ y OH- en el agua al agregarle ácidos o bases). El agua se ioniza muy poco. H 2 O + H 2 O ⇄ H 3 O+ + OHo así (H 2 O + H 2 O ⇄ H+ + OH-) A 25 o C el agua pura contiene concentraciones molares iguales de H+ y OH- (muy pequeñas) [H+] = 0. 0000001 = 1 x 10 – 7 M [OH-] = 0. 0000001 = 1 x 10 – 7 M 17

Cálculo de la CONSTANTE DEL PRODUCTO IÓNICO DEL AGUA (Kw) Como la ionización del agua pura en iones H+ y OH- es muy baja tienen su Expresión de la Constante de Equilibrio que se llamará Constante del producto iónico del agua (Kw). Kw = [H+] [OH-] =1. 0 x 10 -14 Kw: [1. 0 x 10 -7] [1 x 10 - 7] = 1. 0 x 10 -14 (De esta expresión se puede despejar y averiguar la concentración de [H+] [OH-] al agregar ácidos o bases al agua) 18
![En soluciones Acidas donde se agrego algún ácido (H+): [H+] es mayor que 1. En soluciones Acidas donde se agrego algún ácido (H+): [H+] es mayor que 1.](http://slidetodoc.com/presentation_image_h/e126a3ce2925638ad4125c7d9e71d138/image-19.jpg)
En soluciones Acidas donde se agrego algún ácido (H+): [H+] es mayor que 1. 0 x 10 -7 y [OH-] es menor que 1. 0 x 1 -7 En soluciones Alcalinas donde se agrego alguna base (OH-): [OH-] es mayor que 1. 0 x 10 -7 y [H+] es menor que 1. 0 x 10 -7 En soluciones Neutras: [H+] es igual a 1. 0 x 10 -7 y [OH-] es igual a 1. 0 x 10 -7 Ejemplo: Una muestra de bilis tiene una [OH-] de 1. 0 x 10 -5 ¿Cuál es la [H+] ? Se usa Kw: [H+] [OH-] =1. 0 x 10 -14 y se despeja [H+] R: [H +] = 1 x 10 -9 M (¿es ácida, básica o neutra? ) 19

¿Cómo cambian las concentraciones de iones hidrógeno (H+) e hidroxilo (OH-) del agua o de las soluciones acuosas, cuando se les agrega un ácido o una base? Recordar que Kw es un constante y no debe cambiar su valor 1. 0 x 10 -14 por lo tanto: Al agregar un ácido al agua se liberan H+ [ H+] Si ↑[ H+ ], [OH-] ↓ para que [ H+] x [OH-] = 1. 0 x 10 -14 influye la adición Al agregar una base al agua, se liberan OH- [OH-] Si ↑[OH-], [H+ ] ↓ para que [H+] x [OH-] = 1. 0 x 10 -14 La ecuación de la Kw nos permite calcular H+ y OH- Para facilitar el uso de concentraciones tan pequeñas, se 20 le aplicó logaritmo a estas expresiones y se obtiene el p. H:

p. H Potencial o logaritmo de la concentración de hidrógeno Es la medida de la concentración de iones [ H+] ó hidronio [H 3 O+ ] en una solución [H+]=10– p. H Y se calcula con: Ej: 1. ¿Cuál es el p. H de una solución ácida que tiene [H+] de 1 x 10 -6 ? p. H=6 2. ¿Cuál es el p. H de una solución que tiene 0. 00065 [H+]? p. H = -log 6. 5 x 10– 4 = 3. 18 21

LA ESCALA DE p. H es de 1 a 14 El agua pura tiene [H+] y [OH] = 1 x 10 -7 y un p. H 7 § Toda solución neutra tiene un p. H 7 § Toda solución ácida tiene un p. H menor 7 § Toda solución básica tiene un p. H mayor 7 NEUTRO 1 2 3 4 5 6 MAS ACIDO 7 8 9 10 11 12 13 14 MAS BASICO 22

p. H DE ALGUNAS SUSTANCIAS 23
![p. OH Es la medida de la concentración de iones hidroxilo [OH-] en una p. OH Es la medida de la concentración de iones hidroxilo [OH-] en una](http://slidetodoc.com/presentation_image_h/e126a3ce2925638ad4125c7d9e71d138/image-24.jpg)
p. OH Es la medida de la concentración de iones hidroxilo [OH-] en una solución [OH -] = 10 - p. OH y se calcula con la fórmula: En toda solución acuosa : Ejemplo: 1. ¿Cuál es el valor de p. OH de una solución si el p. H es 3. 2 ? 24
![2. Si [OH-] en una solución es 0. 05, calcular el valor del p. 2. Si [OH-] en una solución es 0. 05, calcular el valor del p.](http://slidetodoc.com/presentation_image_h/e126a3ce2925638ad4125c7d9e71d138/image-25.jpg)
2. Si [OH-] en una solución es 0. 05, calcular el valor del p. OH, el p. H, la concentració de [ H +], es ácida ò alclina? (Para calcular [H+ ] usar Kw : [ H+] [OH-] = 1 x 10 -14 ) 3. ¿Cual es el p. H de una solución de HCl 0. 066 M ? La [H+] es igual a la [HCl] por ser electrolito fuerte. p. H = - log [H + ] 4. Calcule el p. H de una solución de Na. OH 0. 024 M: La [OH-] es igual a la [Na. OH] por ser electrolito fuerte.
![Cálculo del valor de [H +] y [OH-] a partir de valores de p. Cálculo del valor de [H +] y [OH-] a partir de valores de p.](http://slidetodoc.com/presentation_image_h/e126a3ce2925638ad4125c7d9e71d138/image-26.jpg)
Cálculo del valor de [H +] y [OH-] a partir de valores de p. H • Se utilizan las siguientes fórmulas: Ej: 1. Calcule [H+] de una solución cuyo p. H es 3. 7 2. Calcule [OH-] si el p. OH de una solución es 2. 8
![Calcular el p. H de las siguientes soluciones: 1) [H+] = 2. 5 x Calcular el p. H de las siguientes soluciones: 1) [H+] = 2. 5 x](http://slidetodoc.com/presentation_image_h/e126a3ce2925638ad4125c7d9e71d138/image-27.jpg)
Calcular el p. H de las siguientes soluciones: 1) [H+] = 2. 5 x 10 -5 4) p. OH = 4. 2 2) Na. OH 0. 020 M 5) HCl 0. 50 M 3) [OH-] = 2. 0 x 10 -8 6) Na. OH 0. 28 M Calcule la [H+] y [OH-] en soluciones con : 7) p. H= 5. 5 8) p. OH = 4 9) p. H = 1. 8 27

EJERCICIOS con ácidos y bases débiles (electrolitos débiles) utilizando % de ionización y Ka, Kb. 1. ¿Cuál es el % de ionización del ácido acético (HC 2 H 3 O 2) 0. 10 M si la constante de ionización (Ka) del ácido es 1. 8 x 10 -5 ? HC 2 H 3 O 2 ⇄ H+ + C 2 H 3 O 22. Calcule el p. H y % de ionización de una solución de anilina (C 6 H 5 NH 2 ) 0. 05 M. Kb = 4. 5 x 10 -10. C 6 H 5 NH 2 ⇄ C 6 H 5 NH 3+ + OH 3. ¿Cuál es la Ka y el p. H de una solución de Acido fluorhídrico (HF) 0. 3 M ionizada un 3. 2%? HF ⇄ H+ + F 28

4. Calcule el p. H de una solución de 0. 3 M de trimetilamina (C 3 H 9 NH+) si Kb = 6. 0 x 10 -5 C 3 H 9 N + H 2 O ⇋ C 3 H 9 NH+ + OH- 0. 3 M x Kb= [C 3 H 9 NH+] [OH-] C 3 H 9 N 6 x 10 -5 = (x)(x) /0. 3 X 2 = (6 x 10 -5 )( 0. 3) = √ 1. 8 x 10 -5 = 4. 2 x 10 -3 como X = [OH -] [ OH-] = 4. 2 x 10 -3 • p. OH = –log 4. 2 x 10 -3 = 2. 38 29
![5. Calcular la [H+], el p. H y el % de ionización en una 5. Calcular la [H+], el p. H y el % de ionización en una](http://slidetodoc.com/presentation_image_h/e126a3ce2925638ad4125c7d9e71d138/image-30.jpg)
5. Calcular la [H+], el p. H y el % de ionización en una solución 0. 3 M de ácido acético (CH 3 COOH) con Ka=1. 8 x 10 -5 CH 3 COOH CH 3 COO- + H+ 0. 3 M x Como no conocemos el % de ionización, le asignamos X a los iones. Ka = [CH 3 COO -] [H+] 1. 8 x 10 -5 = (x)(x) l. 8 x 10 -5 = X 2 [CH 3 COOH ] 0. 3 X 2 = 1. 8 x 10 -5 (0. 3) X =√ 5. 4 x 10 -6 x = 2. 32 x 10 -3 Como x = [H+] = 2. 32 x 10 -3 p. H = -log [H+] = -log 2. 32 x 10 -3 = 2. 63 p. H = 2. 63 Ahora calcular el % de ionización: % ionización = [H+] x 100 [CH 3 COOH] % ionización = 2. 32 x 10 -3 x 100 = 0. 77 % 0. 3

Calculo de Ka y p. H a partir de el % de ionización: 6. Calcule Ka y el p. H de una solución 0. 25 M de ácido fórmico HCOOH si se ioniza en un 6 %. HCOOH ⇋ HCOO - + H + • Las concentraciones son [ HCOOH] = 0. 25 [HCOO -]y[H +] = 6 % = 1. 5 x 10 -2 M Ambas son iguales, se ionizan en la misma proporción Ka = [ HCOO - ] [ H + ] Ka = (1. 5 x 10 -2) ( 1. 5 x 10 -2) [ HCOOH ] ( 0. 25 ) Ka =2. 25 x 10– 4 p. H =-log [H+] p. H = -log 1. 5 x 10 - 2 = 1. 82 p. H = 14 - p. OH p. H = 14 -2. 38 =11. 62

NEUTRALIZACIÓN Es la reacción química donde un ácido y una base reaccionan y forman una sal y agua y el p. H queda neutro. Acido + Base Sal + H 2 O Ejemplo: HCl(ac) + KOH(ac) KCl(ac) + H 2 O TITULACIÓN ÁCIDO-BASE La titulación de un acido y/o base es un procedimiento que tiene como fundamento, la reacción de neutralización: Se utiliza para averiguar la concentración ó el volumen de un ácido ó una base. En el punto de equivalencia de la titulación (neutralización) se observa que el indicador cambia de color (viraje). En ese momento se anota el volumen agregado de ácido o base con la bureta y se aplica la siguiente fórmula: N = normalidad V = volumen N V =N V ácido base 32

TITULACIÓN: procedimiento en el laboratorio Es la determinación del volumen necesario de una solución de concentración conocida llamada solución estándar (en la bureta), para que reaccione (neutralice) hasta llegar al punto de equivalencia (viraje de color), con un volumen conocido de una solución de concentración desconocida llamada muestra (en el erlenmeyer) N ACIDO x VACIDO = N BASE x V BASE Conc. conocida Punto de equivalencia (cambio de color) muestra 33

Ejercicios 1. ¿Qué volumen de una solución 0. 25 N de HNO 3 se necesita para neutralizar 35 ml de una solución de Ca(OH)2 0. 95 N? 2. ¿Cuál es la N de una solución de Na. OH si 25 ml de ésta se neutralizaron con 15 ml de una solución de H 2 SO 4 0. 45 N? 3. Una solución de Na. OH se tituló con H 2 SO 4 0. 15 N. Si se neutralizaron 18. 4 ml de Na. OH con 26 ml H 2 SO 4 ¿Cuál es la normalidad de la base? 34
- Slides: 34