SEMANA 12 CIDOS BASES Y ELECTROLITOS QUMICA 2017

SEMANA 12 ÁCIDOS, BASES Y ELECTROLITOS QUÍMICA 2017 1

ÁCIDOS, BASES Y ELECTROLITOS • Definición de ácidos y bases según: Arrhenius, Bronsted-Lowry y Lewis • Definición de electrolitos: Fuertes y débiles No electrolitos • Ionización de: Agua (Kw) • Ácidos y bases fuertes • Ácidos y bases débiles (Ka, Kb y % de ionización) • Escala de acidez. • Definición y cálculos de p. H, p. OH, [H+], [OH-] • Aplicación de los conceptos en la salud y el ambiente. • Q. en el Ambiente: “Lluvia Ácida” • Laboratorio: Ácidos, bases y electrolitos. 2

ACIDOS Y BASES ACIDO BASE o HIDROXIDO Del latín Acidus= agrio Ej: vinagre, jugo de limón, HCl, H 2 SO 4. Tienen un sabor agrio o ácido y pueden producir sensación de picazón en la piel. Ej: antiácidos, líquidos limpia vidrios y destapa-desagües, Na. OH, Al(OH)3 Que tiene un sabor amargo y sensación resbalosa en la piel. HAY VARIAS DEFINICIONES DE ACIDO Y BASE 3

Definición de Ácido y Base según Arrhenius • ÁCIDO: Sustancia que al disociarse en solución acuosa produce iones H+ ó (H 3 O+) ó protón H + + H 2 O → H 3 O + Ej: HCl, HNO 3 , H 2 SO 4, H 2 CO 3 Disociación de ácidos: HCl → H+ + Cl HNO 3 → H+ + NO 3 - • BASE: Sustancia que al disociarse en solución acuosa produce iones Hidroxilo (OH- ) Ej: Na. OH, KOH, Ba(OH)2 Disociación de la base: Na. OH → Na+ + OHBa(OH)2 → Ba++ 2 OH- 4
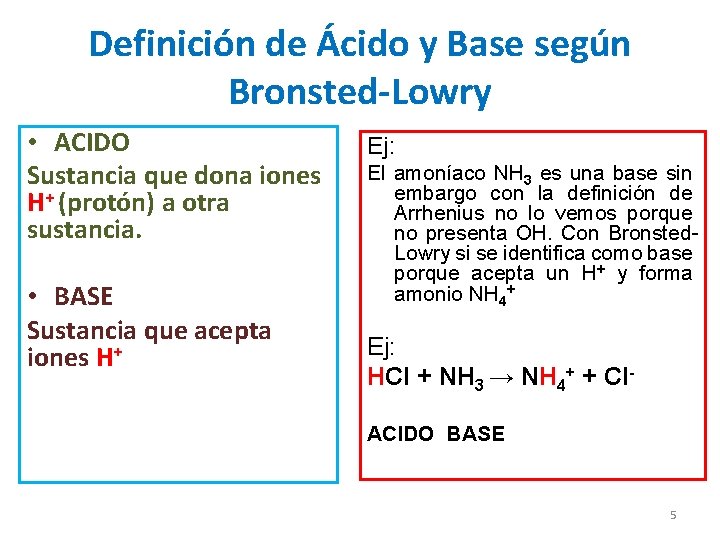
Definición de Ácido y Base según Bronsted-Lowry • ACIDO Sustancia que dona iones H+ (protón) a otra sustancia. • BASE Sustancia que acepta iones H+ Ej: El amoníaco NH 3 es una base sin embargo con la definición de Arrhenius no lo vemos porque no presenta OH. Con Bronsted. Lowry si se identifica como base porque acepta un H+ y forma amonio NH 4+ Ej: HCl + NH 3 → NH 4+ + Cl. ACIDO BASE 5
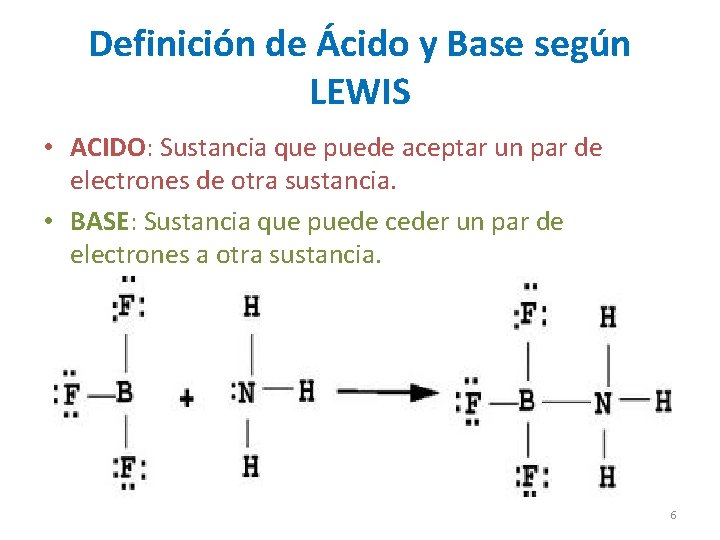
Definición de Ácido y Base según LEWIS • ACIDO: Sustancia que puede aceptar un par de electrones de otra sustancia. • BASE: Sustancia que puede ceder un par de electrones a otra sustancia. 6
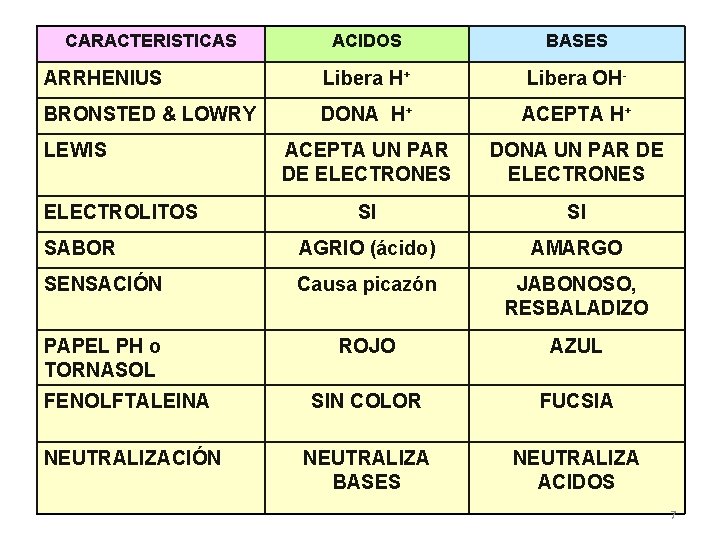
CARACTERISTICAS ACIDOS BASES ARRHENIUS Libera H+ Libera OH- BRONSTED & LOWRY DONA H+ ACEPTA UN PAR DE ELECTRONES DONA UN PAR DE ELECTRONES SI SI SABOR AGRIO (ácido) AMARGO SENSACIÓN Causa picazón JABONOSO, RESBALADIZO PAPEL PH o TORNASOL ROJO AZUL FENOLFTALEINA SIN COLOR FUCSIA NEUTRALIZACIÓN NEUTRALIZA BASES NEUTRALIZA ACIDOS LEWIS ELECTROLITOS 7

IONIZACIÓN Ó DISOCIACIÓN DE ACIDOS, BASES Y SALES Es la separación o disociación de un compuesto en sus iones (+) y iones (–) al estar en agua (solución acuosa). La disociación puede ser total, en un 100 % ( ) o parcial, en muy bajo + 5% (⇄ ). Ejemplo: HCl → H+ + Cl. KOH → K + + OHCH 3 COOH ⇄ CH 3 COO- + H+ NH 3 ⇄ NH 4+ + OHCa. Cl 2→ Ca +2 + 2 Cl- EN BASE A LA IONIZACIÓN SE CLASIFICAN ASI: 8

ELECTROLITOS Sustancias que en solución acuosa se disocian en iones y CONDUCEN LA ELECTRICIDAD. Según el grado de ionización se clasifican en: ELECTROL. FUERTE ELECTROLITO DÉBIL § Se disocian al 100% § Se disocian en un pequeño % § Buen conductor de la § Conduce poco la electricidad § Su reacción de ionización es Su reacción de ionización reversible. Ej: es irreversible. Ej: KOH → K+ + OH- H 2 CO 3 ⇄ 2 H+ + CO 3 - H 2 SO 4 → 2 H++ SO 4 -2 NH 3 + H 2 O ⇄ NH 4+ + OH 9

ELECTROLITOS FUERTES DEBILES 10

NO ELECTROLITO Sustancias que en estado líquido o solución, NO conduce la corriente eléctrica. Ej: • Alcohol • Gasolina • Azúcar azúcar 11

Aplicación del % de Ionización en electrolitos fuertes y débiles 1. ¿Cuál es la [H+] y el % de ionización de una solución de HCl 0. 15 M ? 2. ¿Cuál es la [OH-] y el % de ionización de una solución de Na. OH 0. 22 M? 3. ¿Cuál es el % de ionización de una solución de CH 3 COOH 0. 13 M que tiene una [H+]de 0. 011 M? 4. ¿Cuál es la [OH-] de una solución de NH 3 (NH 4 OH) 0. 3 M que se ioniza en un 12% ? 12

ACIDOS Y ACIDOS y BASES FUERTES: BASES FUERTES • Se ionizan casi en un 100% • Tienen una ionización irreversible • No tienen constantes de ionización (Ka), (Kb) Ej: HCl Ácido Clorhídrico HBr Ácido Bromhídrico HI Ácido Yodhídrico H 2 SO 4 Ácido sulfúrico HNO 3 Ácido Nítrico 13

ÁCIDOS DÉBILES § Se ionizan muy poco (es reversible) § Tienen una constante de ionización (Ka) que se encuentra en tablas y se puede calcular con la Expresión de la Constante de Equilibrio: Ejemplo: x x ácido acético HC 2 H 3 O 2 ⇄ H+ + C 2 H 3 O 2 Ka = [H+] [C 2 H 3 O 2 -] = (x) = ___x 2____ [HC 2 H 3 O 2] 14
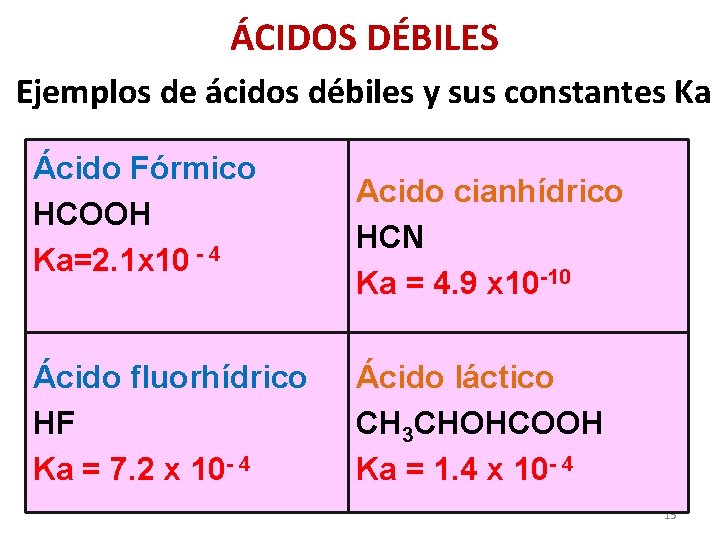
ÁCIDOS DÉBILES Ejemplos de ácidos débiles y sus constantes Ka Ácido Fórmico HCOOH Ka=2. 1 x 10 - 4 Ácido fluorhídrico HF Ka = 7. 2 x 10 - 4 Acido cianhídrico HCN Ka = 4. 9 x 10 -10 Ácido láctico CH 3 CHOHCOOH Ka = 1. 4 x 10 - 4 15

BASES DEBILES § Se ioniza muy poco y es reversible. § Tienen una constante de ionización (Kb) que se encuentra en tablas y se puede calcular con la Expresión de la constante de equilibrio Keq: x x § Ej: amoníaco NH 3 + H 2 O ⇄ NH 4+ + OH Kb = [ NH 4+] [ OH -] = x 2 [NH 3] (NO se toma en cuenta el H 2 O en las expresiones de Kb y Ka) 16
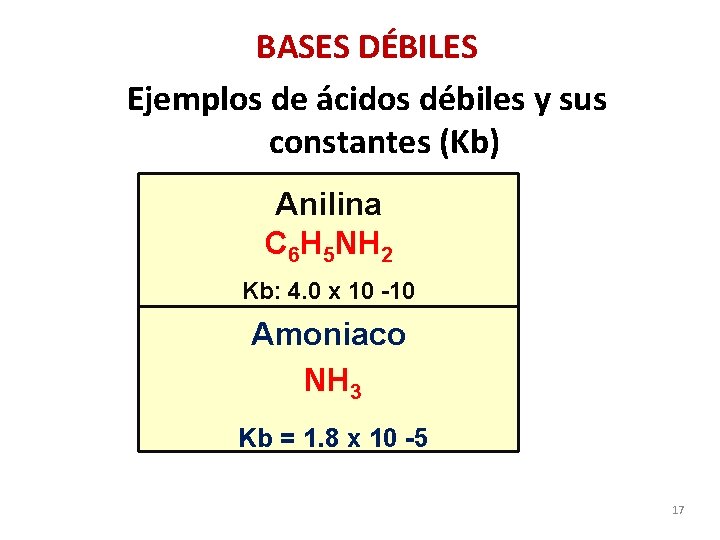
BASES DÉBILES Ejemplos de ácidos débiles y sus constantes (Kb) Anilina C 6 H 5 NH 2 Kb: 4. 0 x 10 -10 Amoniaco NH 3 Kb = 1. 8 x 10 -5 17

IONIZACION DEL AGUA (Debido a que los ácidos y las bases se encuentran disueltos en soluciones acuosas y es allí donde liberan sus H+ y OH- , debemos conocer como se afectarán las concentraciones de H+ y OH- que produce el agua). El agua se ioniza muy poco, por lo que es mala conductora de electricidad. H 2 O + H 2 O ⇄ H 3 O+ + OHA 25 o C el agua pura contiene concentraciones molares iguales de H+ y OH- (muy pequeñas) [H+] = 0. 00000010 = 1 x 10 -7 M [OH-] = 0. 00000010 = 1 x 10 – 7 M 18

Constante de Producto Iónico del agua (Kw ó Ka) (Como la ionización del agua en H+ y OH- es tan baja, se le puede calcular una constante de equilibrio que se llama Kw) Kw = [H+] [OH-] =1. 0 x 10 -14 Si el agua es pura, las concentraciones Molares de H+ y OH- en su Kw son: Kw =[1. 0 x 10 -7 ] [1 x 10 - 7] =1. 0 x 10 -14 Kw = 1. 0 x 10 -14 19
![+] es mayor que 1. 0 x 10 -7 En soluciones Acidas: [H Acidas +] es mayor que 1. 0 x 10 -7 En soluciones Acidas: [H Acidas](http://slidetodoc.com/presentation_image_h/b9c469d8c9f0f4d63058f1a4d55cd164/image-20.jpg)
+] es mayor que 1. 0 x 10 -7 En soluciones Acidas: [H Acidas En soluciones Alcalinas: [H Alcalinas +] es menor que 1. 0 x 10 -7 En soluciones Neutras: [H Neutras: +] es igual a 1. 0 x 10 -7 Aplicación: Una muestra de bilis tiene una [OH-] de 1. 0 x 10 -5 ¿Cuál es la [H+] ? Se usa Kw = [H+] [OH-] =1. 0 x 10 -14 y se despeja [H+] R: [H +] = 1 x 10 -9 M (¿es ácida, básica o neutra? ) 20

¿Cómo cambian las concentraciones de iones hidrógeno (H+) e hidroxilo (OH-) del agua o de las soluciones acuosas, cuando se les agrega un ácido o una base? Recordar que Kw es un constante y no debe cambiar su valor 1. 0 x 10 -14 por lo tanto: Al agregar un ácido al agua se liberan H+ [ H+] Si ↑[ H+ ], [OH-] ↓ para que [ H+] x [OH-] = 1. 0 x 10 -14 influye la adición Al agregar una base al agua, se liberan OH- [OH-] Si ↑[OH-], [H+ ] ↓ para que [H+] x [OH-] = 1. 0 x 10 -14 La ecuación de la Kw nos permite calcular H+ y OH- Para facilitar el uso de concentraciones tan pequeñas, se 21 le aplicó logaritmo a estas expresiones y se obtiene el p. H:

p. H (potencial de hidrógeno) Es la medida de la concentración de iones [ H+] ó hidronio [H 3 O+ ] en una solución [H+]=10– p. H Y se calcula con: p. H = - log [H+] Ej: 1. El p. H de una solución que tiene [H+] de 1 x 10 -6 p. H=6 2. El p. H de una solución que tiene 0. 00065 [H+] p. H = -log 6. 5 x 10– 4 = 3. 18 22

LA ESCALA DE p. H es de 1 a 14 El agua pura tiene [H+] y [OH] = 1 x 10 -7 y un p. H 7 § Toda solución neutra tiene un p. H 7 § Toda solución ácida tiene un p. H menor 7 § Toda solución básica tiene un p. H mayor 7 NEUTRO 1 2 3 4 5 6 MAS ACIDO 7 8 9 10 11 12 13 14 MAS BASICO 23

p. H DE ALGUNAS SUSTANCIAS 24
![p. OH Es la medida de la concentración de iones hidroxilo [OH-] en una p. OH Es la medida de la concentración de iones hidroxilo [OH-] en una](http://slidetodoc.com/presentation_image_h/b9c469d8c9f0f4d63058f1a4d55cd164/image-25.jpg)
p. OH Es la medida de la concentración de iones hidroxilo [OH-] en una solución [OH -] = 10 - p. OH y se calcula con la fórmula: p. OH = - log [OH-] En toda solución acuosa : p. H + p. OH = 14 Ejemplo: 1. ¿Cuál es el valor de p. OH de una solución si el p. H es 3. 2 ? 25
![2. Si [OH-] en una solución es 0. 05, calcular el valor del p. 2. Si [OH-] en una solución es 0. 05, calcular el valor del p.](http://slidetodoc.com/presentation_image_h/b9c469d8c9f0f4d63058f1a4d55cd164/image-26.jpg)
2. Si [OH-] en una solución es 0. 05, calcular el valor del p. OH, el p. H, la concentració de [ H +], es ácida ò alclina? (Para calcular [H+ ] usar Kw : [ H+] [OH-] = 1 x 10 -14 ) 3. ¿Cual es el p. H de una solución de HCl 0. 066 M ? La [H+] es igual a la [HCl] por ser electrolito fuerte. p. H = - log [H + ] 4. Calcule el p. H de una solución de Na. OH 0. 024 M La [OH-] es igual a la [Na. OH] por ser electrolito fuerte.
![Cálculo del valor de [H +] y [OH-] a partir de valores de p. Cálculo del valor de [H +] y [OH-] a partir de valores de p.](http://slidetodoc.com/presentation_image_h/b9c469d8c9f0f4d63058f1a4d55cd164/image-27.jpg)
Cálculo del valor de [H +] y [OH-] a partir de valores de p. H • Se utilizan las siguientes fórmulas: [H+]=10 – p. H [OH -]=10 - p. OH [H+]= _ 1___ antilog p. H Ej: 1. Calcule [H+] de una solución cuyo p. H es 3. 7 2. Calcule [OH-] si el p. OH de una solución es 2. 8
![Calcular el p. H de las siguientes soluciones: 1) [H+] = 2. 5 x Calcular el p. H de las siguientes soluciones: 1) [H+] = 2. 5 x](http://slidetodoc.com/presentation_image_h/b9c469d8c9f0f4d63058f1a4d55cd164/image-28.jpg)
Calcular el p. H de las siguientes soluciones: 1) [H+] = 2. 5 x 10 -5 4) p. OH = 4. 2 2) Na. OH 0. 020 M 5) HCl 0. 50 M 3) [OH-] = 2. 0 x 10 -8 6) Na. OH 0. 28 M Calcule la [H+] y [OH-] en soluciones con : 7) p. H= 5. 5 8) p. OH = 4 9) p. H = 1. 8 28
![Calcular la [H+], el p. H y el % de ionización en una solución Calcular la [H+], el p. H y el % de ionización en una solución](http://slidetodoc.com/presentation_image_h/b9c469d8c9f0f4d63058f1a4d55cd164/image-29.jpg)
Calcular la [H+], el p. H y el % de ionización en una solución 0. 3 M de ácido acético (CH 3 COOH) con Ka=1. 8 x 10 -5 - + H+ CH 3 COOH CH COO 3 x Como no conocemos el % de ionización, le asignamos el valor de X a cada una de las especies ionizadas: Ka = [CH -] [H+] 1. 8 x 10 -5 = (x)(x) l. 8 x 10 -5 = X 2 COO 3 [CH 3 COOH ] 0. 3 X 2 = 1. 8 x 10 -5 (0. 3) X =√ 5. 4 x 10 -6 x = 2. 32 x 10 -3 Como x = [H+] = 2. 32 x 10 -3 p. H = -log [H+] = -log 2. 32 x 10 -3 = 2. 63 p. H = 2. 63 Ahora calcular el % de ionización: % ionización = [H+] x 100 [CH 3 COOH] % ionización = 2. 32 x 10 -3 x 100 = 0. 77 % 0. 3

Calculo de Ka y p. H a partir de el % de ionización: Calcule Ka y el p. H de una solución 0. 25 M de ácido fórmico HCOOH si se ioniza en un 6 %. HCOOH ⇋ HCOO - + H + • Las concentraciones son [ HCOOH] = 0. 25 [HCOO -] = 6 % = 1. 5 x 10 -2 M Ambas son iguales, se ionizan en la misma proporción Ka = [ HCOO - ] [ H + ] Ka = (1. 5 x 10 -2) ( 1. 5 x 10 -2) [ HCOOH ] ( 0. 25 ) Ka = 2. 25 x 10 – 4 p. H = -log [H +] p. H = -log 1. 5 x 10 - 2= 1. 82 p. H = 14 -p. OH p. H = 14 -2. 38 =11. 62

EJERCICIOS con ácidos y bases débiles (electrolitos débiles) 1. Para una solución de ácido acético (HC 2 H 3 O 2) 0. 10 M calcular : El % de ionización del ácido acético si la constante de ionización (Ka) del ácido es 1. 8 x 10 -5. HC 2 H 3 O 2 ⇄ H+ + C 2 H 3 O 22. Calcule el p. H y % de ionización de una solución de anilina 0. 05 M, Kb = 4. 5 x 10 -10. C 6 H 5 NH 2 ⇄ C 6 H 5 NH 3+ + OH 3. ¿Cuál es la Ka y el p. H de una solución de Acido fluorhídrico (HF) 0. 3 M ionizada un 3. 2%? HF ⇄ H+ + F- 31

4. Calcule el p. H de una solución de 0. 3 M de trimetilamina C 3 H 9 N si Kb = 6. 0 x 10 -5 C 3 H 9 N + H 2 O ⇋ C 3 H 9 NH+ + OH- x Kb= [C 3 H 9 NH+] [OH-] C 3 H 9 N 6 x 10 -5 = (x)(x) /0. 3 X 2 = 6 x 10 -5 x 0. 3 = √ 1. 8 x 10 -5 =4. 2 x 10 -3 como X = [OH -] [ OH-] = 4. 2 x 10 -3 • p. OH = –log 4. 2 x 10 -3 = 2. 38 32
- Slides: 32