SEMANA 12 ACIDOS BASES Y ELECTROLITOS Acidus latn

SEMANA 12 ACIDOS, BASES Y ELECTROLITOS

Acidus latín (agrio)

La acidez y la basicidad constituyen el conjunto de propiedades características de dos importantes grupos de sustancias químicas: ácidos y bases.
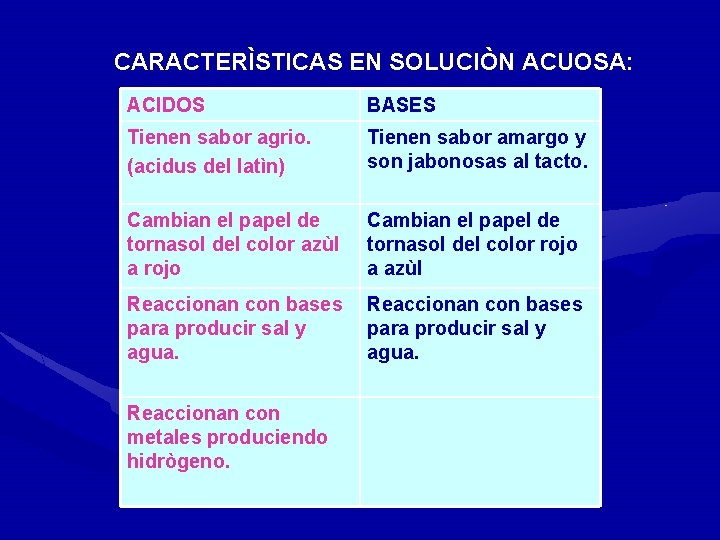
CARACTERÌSTICAS EN SOLUCIÒN ACUOSA: ACIDOS BASES Tienen sabor agrio. (acidus del latìn) Tienen sabor amargo y son jabonosas al tacto. Cambian el papel de tornasol del color azùl a rojo Cambian el papel de tornasol del color rojo a azùl Reaccionan con bases para producir sal y agua. Reaccionan con metales produciendo hidrògeno.
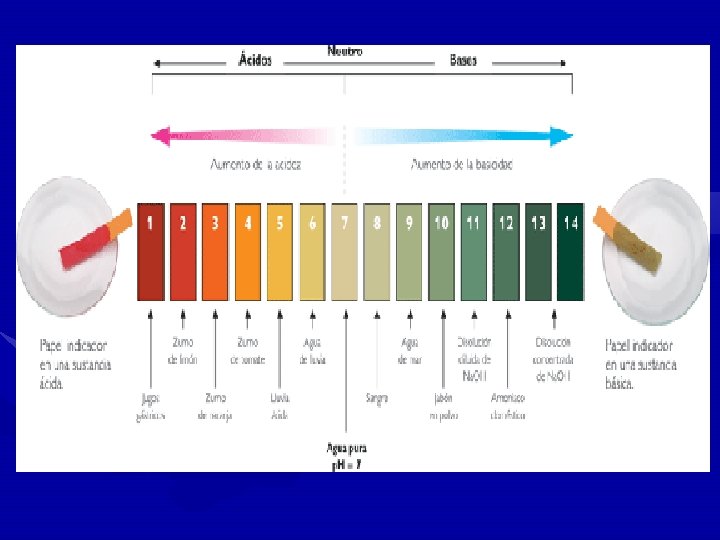

Teoría clásica o de Arrhenius Svante Arrhenius, Arrhenius (1859 -1927), llegó a la conclusión de que las propiedades características de las disoluciones acuosas de los ácidos se debían a los iones hidrógeno, H+, mientras que las propiedades típicas de las bases se debían a iones hidróxido, OH-

Ejemplos típicos de ácidos, según la definición de Arrhenius , son todos los ácidos clásicos, HCl , H 2 SO 4, HNO 3, etc, que al disolverse en agua se disocian o ionizan en la forma: HO HCl Cl- (ac) + H+ (ac) 2

Ejemplos de bases son todos los hidróxidos de metales (en particular los de los metales alcalinos y alcalinotérreos), que al disolverse en agua se disocian en la forma: H 2 O Na. OH Na+(ac) + OH- (ac)
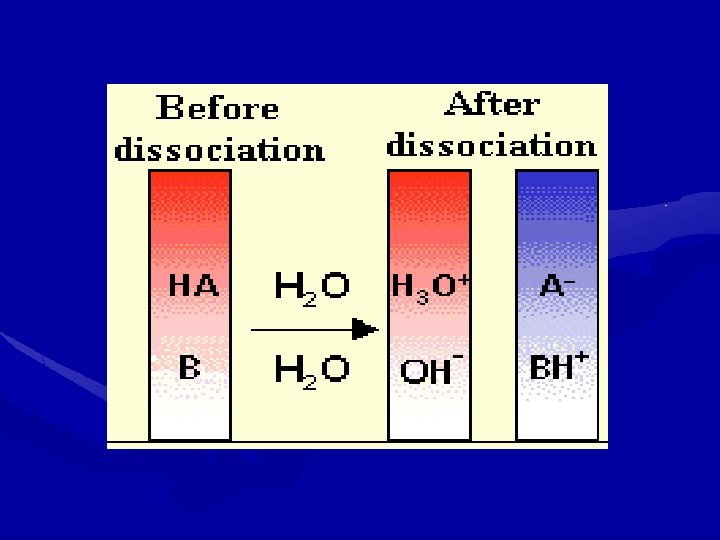

Con la teoría de Arrhenius se comprende fácilmente la capacidad de ácidos y bases de neutralizar sus propiedades características entre sí, a esto se le llama: REACCIÓN DE NEUTRALIZACIÓN

Lo anterior explica la desaparición de los iones desaparición característicos, H+ y OH-, que se combinan para formar moléculas de agua Cl- (ac) + H+ (ac) + Na+ (ac) + OH- (ac) H 2 O + Cl- (ac) + Na+ (ac)

Los iones Cl-(ac) y Na+(ac) prácticamente no han sufrido ninguna modificación, se llaman iones espectadores, por lo que la reacción de neutralización se reduce en esencia a: H+ (ac) + OH- (ac) H 2 O

Teoría de Brönsted y Lowry El ión hidrógeno: H+, no puede existir como tal en disolución acuosa, sino que se encuentra en forma de ión hidronio, H 3 O +.

Cuando un ácido se disuelve en agua, es lógico suponer que el ión hidronio se forma por la transferencia de un protón desde la molécula de ácido a una molécula de agua. HCl + H 20 H 3 O+ + Cl-

Teniendo esto en cuenta, se pueden explicar las propiedades de bases como el amoniaco, iones carbonato, etc. : H 2 O + NH 3 NH 4+ + OH-

Las consideraciones anteriores condujeron a los químicos J. N. Brönsted y T. M. Lowry a proponer (en 1923) una nueva definición conceptual de ácidos y bases, más general que la de Arrhenius y que puede aplicarse a disolventes no acuosos: ØBase es una sustancia capaz de aceptar un protón (de un ácido). ØÁcido es una sustancia capaz de ceder un protón (a una base). Las reacciones ácido-base según esta definición son reacciones de transferencia de protones.

Una reacción ácido-base se puede escribir en la forma general: AH + B ↔ BH+ + A- ácido 1 base 2 ácido 2 base 1 Las especies de cada pareja, AH/A- y BH+/B, que toman parte en toda reacción ácido-base, reciben el nombre de pares ácido-base conjugados.

Teoría de Lewis Para Lewis son bases las sustancias que tienen un par de electrones no compartidos que pueden ceder con mayor o menor facilidad. Por ejemplo: H 3 N: C 5 H 5 N:

La reacción de neutralización consiste en neutralización que el PAR de electrones de la partícula básica es aceptado por la partícula ácida, formándose un enlace covalente, y da lugar a compuestos de tipo salino.

Son tres teorías que explican las reacciones teorías ácido-base, pero no se contradicen mutuamente, sino que cada teoría expande el modelo anterior y adopta un perspectiva más amplia.

ACIDOS FUERTES Y DÈBILES ACIDOS FUERTES ACIDOS DÈBILES • Se ionizan totalmente en agua. • Su ionizaciòn es irreversible • Pueden ser mono, di ò poliproticos. • Ejemplos HCl, H 2 SO 4 HNO 3, HBr, HI • Se ionizan poco en agua. • Tienen una ionizaciòn reversible. • Poseen una constante de ionizaciòn (Ka). • Ejemplos: CH 3 COOH, H 3 BO 3 , H 2 CO 3

BASES FUERTES Y DÈBILES BASES FUERTES BASES DÈBILES • Se ionizan totalmente en agua. • Poseen una ionizaciòn irreversible. • Ejemplos Na. OH, KOH • Se ionizan parcialmente en agua. • Su ionizaciòn es reversible. • Tienen una constante de ionizaciòn (Kb) • Ejemplos: NH 3 , Mg (OH)2

IONIZACIÓN: Proceso mediante el cuál una sustancia al entrar en contacto con el agua, se disocia en sus iones respectivos.

Un electrolito es una sustancia que al disolverse en agua, da lugar a la formación de iones y por lo tanto conduce la corriente elèctrica. Los electrolitos pueden ser débiles o fuertes, según estén parcial o totalmente ionizados o disociados en medio acuoso.

Electrolito fuerte : Electrolito fuerte Es toda sustancia que al disolverse en agua, provoca exclusivamente la formación de iones con una reacción de disolución prácticamente irreversible y conduce la electricidad fuertemente. por ejemplo: KOH HCl
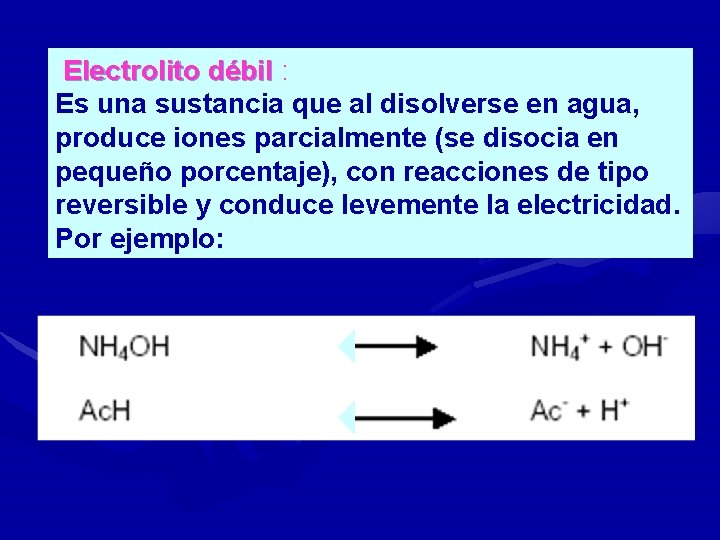
Electrolito débil : Electrolito débil Es una sustancia que al disolverse en agua, produce iones parcialmente (se disocia en pequeño porcentaje), con reacciones de tipo reversible y conduce levemente la electricidad. Por ejemplo:

El agua pura se dice que es una sustancia no agua pura conductora de la electricidad , pero , en realidad, tiene una conductividad muy pequeña que puede medirse con aparatos muy sensibles. Esta conductividad indica que en agua pura deben existir iones , aunque en concentraciones extremadamente pequeñas.

Puesto que el agua es un electrolito débil y puede actuar como ácido y como base(anfótera), cada solución acuosa está caracterizada por el proceso de auto-ionización.

Esto significa que , si bien en pequeñísima proporción , el agua debe estar disociada (este proceso se llama , a veces, autoionización (Arrhenius) o autoprotólisis del agua (Brönsted. Lowry) ) en la forma: H 2 O + H 2 O H 3 O+ + OH- ácido 1 base 2 ácido 2 base 1

Esta ecuación representa el concepto de Bronsted. Lowry de lo que ocurre; una molécula de agua que actúa como ácido , dona un protón a otra molécula de agua, que actúa como base. El agua está en equilibrio con iones hidronio e iones hidróxido, pero el equilibrio está desplazado a la izquierda.

La concentración de iones hidronio en el agua pura a 25ºC es 0. 00000010 ó 1. 0 x 10 -7 y la concentración de hidróxido en el agua a 25ºC también es 0. 00000010 ó 1. 0 x 10 -7
![La constante de equilibrio sería: Keq = [H 3 O+][OH-] [H 2 O] Teniendo La constante de equilibrio sería: Keq = [H 3 O+][OH-] [H 2 O] Teniendo](http://slidetodoc.com/presentation_image_h/7b504dc3e0bc79d576bf80e93c02f87f/image-32.jpg)
La constante de equilibrio sería: Keq = [H 3 O+][OH-] [H 2 O] Teniendo en cuenta que la concentración del agua es prácticamente constante , se puede incluir en la constante de equilibrio , que se expresa entonces en la forma : +][OH-] = 1, 0 x 10 – 14 Kw = =[H O Kw 3 (a 25 ºC) Esta constante , Kw, se llama: Kw PRODUCTO IÓNICO DEL AGUA Kw = [H 3 O+][OH-] = 1, 0 x 10 – 14
![A 25º C, en mol/litro Neutra [H+] = [OH-] = 10 -7 Ácida A 25º C, en mol/litro Neutra [H+] = [OH-] = 10 -7 Ácida](http://slidetodoc.com/presentation_image_h/7b504dc3e0bc79d576bf80e93c02f87f/image-33.jpg)
A 25º C, en mol/litro Neutra [H+] = [OH-] = 10 -7 Ácida [H+] > 10 -7 [OH-] < 10 -7 Básica [H+] < 10 -7 [OH-] > 10 -7

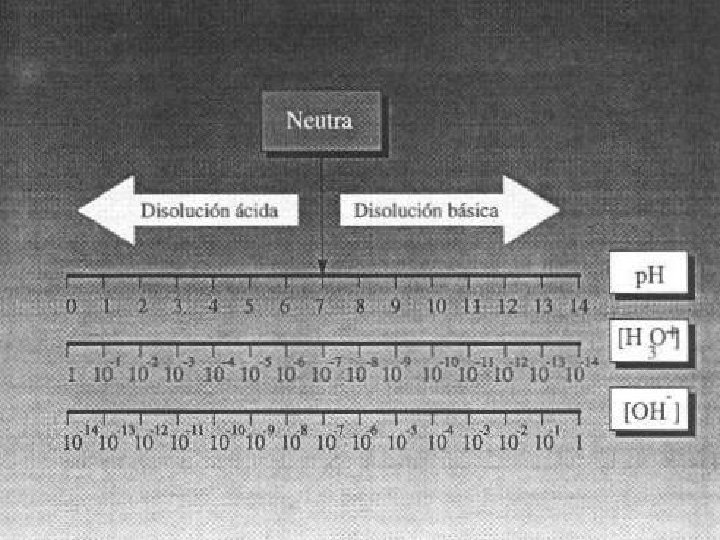
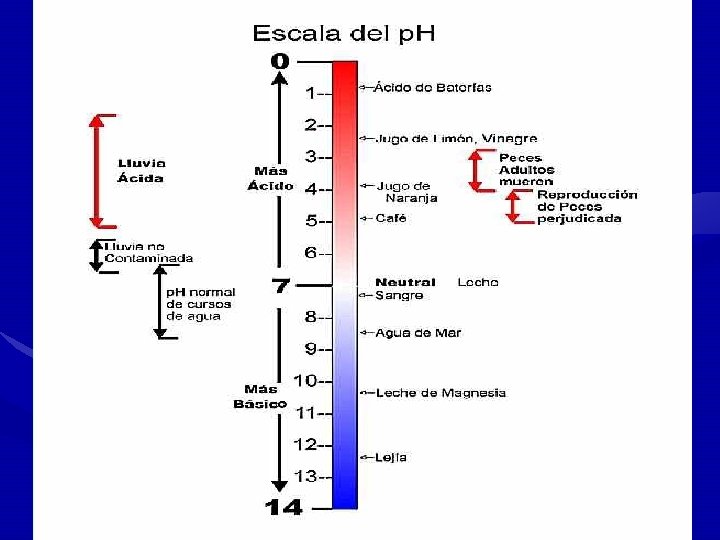
p. H= El negativo del logaritmo de la concentración de iones p. H= hidrógeno. p. H = - log [H+] Conviene tener muy en cuenta que , debido al cambio de signo en el logaritmo , la escala de p. H va en sentido contrario al de la concentración de iones H+ , es decir, que el p. H de una disolución aumenta a medida que disminuye [H+] , o sea la acidez.

Para poder expresar las concentraciones de soluciones ácidas o básicas mediante números sencillos , se utiliza el número del exponente para expresar la acidez. La escala de acidez de Sörensen se conoció más tarde como la escala de p. H, del francés pouvoir hydrogène”poder del hidrógeno”

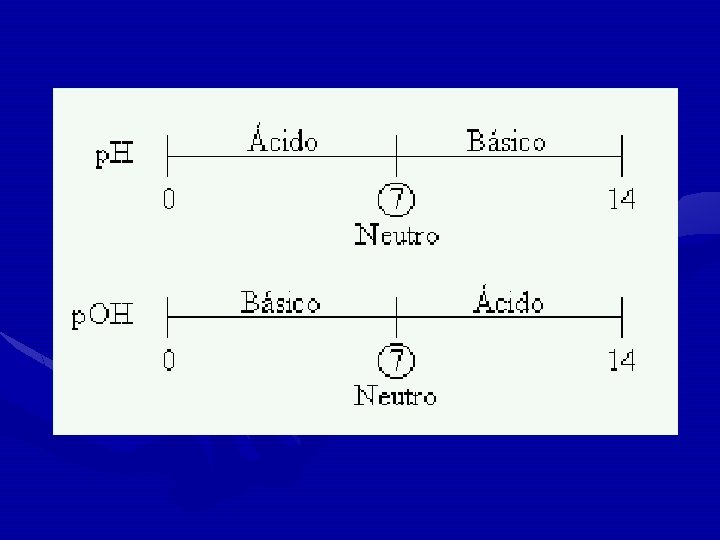
De la misma forma que el p. H, se define también el p. OH como el logaritmo decimal negativo, concentración de iones OH-. p. OH = -log [OH-] Teniendo en cuenta la expresión del producto iónico del H 2 O, se deduce que a 25ºC se cumple: p. H + p. OH = 14
![DISOLUCIÓN p. H [H 3 O+] [OH-] 14 13 12 11 10 9 8 DISOLUCIÓN p. H [H 3 O+] [OH-] 14 13 12 11 10 9 8](http://slidetodoc.com/presentation_image_h/7b504dc3e0bc79d576bf80e93c02f87f/image-40.jpg)
DISOLUCIÓN p. H [H 3 O+] [OH-] 14 13 12 11 10 9 8 10 -14 10 -13 10 -12 10 -11 10 -10 10 -9 10 -8 100 = 1 10 -2 10 -3 10 -4 10 -5 10 -6 Neutra 7 10 -7 Ácida 6 5 4 3 2 1 0 10 -6 10 -5 10 -4 10 -3 10 -2 10 -1 10 -0 10 -8 10 -9 10 -10 10 -11 10 -12 10 -13 Básica
![1. ¿Cuál es el p. H de una solución con una [H+] de 5. 1. ¿Cuál es el p. H de una solución con una [H+] de 5.](http://slidetodoc.com/presentation_image_h/7b504dc3e0bc79d576bf80e93c02f87f/image-41.jpg)
1. ¿Cuál es el p. H de una solución con una [H+] de 5. 2 x 10 -3 M ? R/ p. H 2. 28
![2. Cuál es la [H+] del jugo de limón, cuyo p. H es de 2. Cuál es la [H+] del jugo de limón, cuyo p. H es de](http://slidetodoc.com/presentation_image_h/7b504dc3e0bc79d576bf80e93c02f87f/image-42.jpg)
2. Cuál es la [H+] del jugo de limón, cuyo p. H es de 3. 15 -4 R/ 7. 079 x 10

3. ¿Cuál es el p. OH de una solución cuyo p. H es de 3. 33? R/ p. OH= 10. 67
![4. Una solución tiene una [H+] de 0. 027 M ¿Cuál es la [OH-]? 4. Una solución tiene una [H+] de 0. 027 M ¿Cuál es la [OH-]?](http://slidetodoc.com/presentation_image_h/7b504dc3e0bc79d576bf80e93c02f87f/image-44.jpg)
4. Una solución tiene una [H+] de 0. 027 M ¿Cuál es la [OH-]? R/ 3. 70 X 10 -13 M

ACIDOS Y BASES DÉBILES (Disociación y problemas) EJERCICIOS. CH 3 COOH H 3 BO 3 H 2 CO 3

- Slides: 46