SEMANA 11 VELOCIDAD DE REACCIN Y EQUILIBRIO QUIMICO

SEMANA 11 VELOCIDAD DE REACCIÓN Y EQUILIBRIO QUIMICO Cinética química. Teoría de colisiones. Velocidad de reacción Factores que la afectan: temperatura, concentración, catalíticos, área superficial. Reacciones reversibles. Equilibrio químico Factores que lo afectan: concentración, presión y temperatura Principio de Le Chatelier. Ley de Acción de Masas Constante de equilibrio(Keq), expresión y cálculos. Ejercicios

Cinética Química Es el estudio de las velocidades de las reacciones químicas y los factores que afectan a la velocidad de reacción. TEORIA DE COLISIONES Explica que una reacción se realiza solo cuando las moléculas ó átomos de los reactivos, chocan ó colisionan entre sí, con la orientación adecuada y suficiente energía. Pueden ocurrir muchas colisiones, pero muy pocas conducen a la formación de productos. 2

Condiciones indispensables para que ocurra una reacción • 1. Colisión : los reactivos deben chocar es decir colisionar entre ellos. • 2. Orientación: los reactivos deben alinearse correctamente para romper y formar enlaces. • 3. Energía : la colisión debe suministrar suficiente energía para alcanzar la energía de activación necesaria para esa reacción. 3
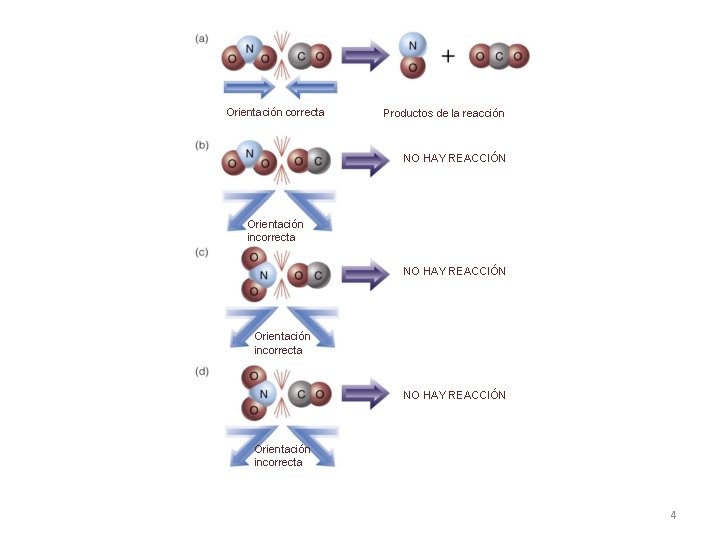
Orientación correcta Productos de la reacción NO HAY REACCIÓN Orientación incorrecta 4
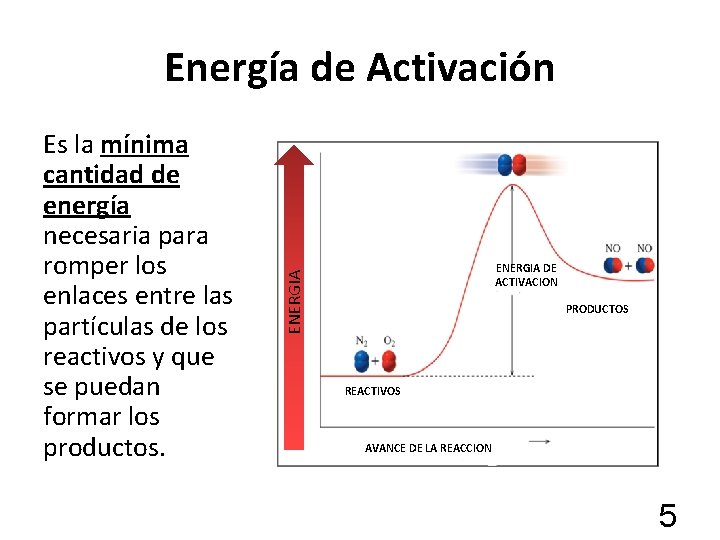
Energía de Activación ENERGIA DE ACTIVACION ENERGIA Es la mínima cantidad de energía necesaria para romper los enlaces entre las partículas de los reactivos y que se puedan formar los productos. PRODUCTOS REACTIVOS AVANCE DE LA REACCION 5

Velocidad de Reacción Se define como la cantidad de reactivo consumido o de producto obtenido en un periodo dado de tiempo. Factores que afectan la velocidad de reacción 1. Concentración de reactivos 2. Temperatura 3. Catalizadores ( catalíticos) 4. Area superficial 6

1. Concentración de reactivos Al aumentar la concentración de las partículas reaccionantes, aumenta el número de colisiones y la reacción avanza más rápido. [Reactivos] Velocidad de reacción 2. Temperatura A temperaturas más altas, aumenta la energía cinética de las partículas, se mueven más rápido, chocan más veces y con suficiente energía para formar productos, por lo tanto la velocidad de reacción aumenta. Temperatura velocidad de reacción 7
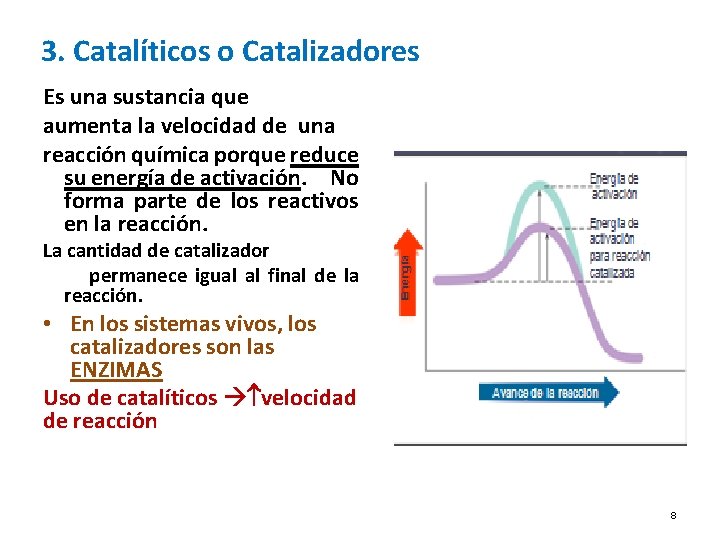
3. Catalíticos o Catalizadores Es una sustancia que aumenta la velocidad de una reacción química porque reduce su energía de activación. No forma parte de los reactivos en la reacción. La cantidad de catalizador permanece igual al final de la reacción. • En los sistemas vivos, los catalizadores son las ENZIMAS Uso de catalíticos velocidad de reacción 8

4. Área Superficial Si las partículas del reactivo son más pequeñas, su área superficial es mayor, lo que permite aumentar la frecuencia de colisión. Área superficial Velocidad de reacción 9

Reacciones Reversibles Son las reacciones que pueden llevarse a cabo en uno y otro sentido, hasta llegar al equilibrio. Reacción directa: A B (las estudiadas hasta hoy) Reacción inversa: A B Reacción reversible: A ⇄ B En estas reacciones, se forman los productos, luego éstos interactúan y chocan y pueden formar los reactivos nuevamente hasta alcanzar el EQUILIBRIO QUÍMICO 10

Equilibrio Químico • Punto en el cual la velocidad de la reacción directa A B es igual a la velocidad de la reacción Inversa A B. • Los reactivos forman productos a la misma velocidad que los productos forman reactivos. A ⇄ B • Al alcanzar el equilibrio, las concentraciones de reactivos y productos permanecen constantes (no iguales). 11

Equilibrio Homogéneo En el que todos los reactivos y productos se encuentran en el mismo estado físico. 2 SO 2(g) + O 2(g) 2 SO 3(g) Equilibrio Heterogéneo En el que uno o varios reactivos ó productos están en diferente estado físico. 4 HCl(l) + O 2(g) 2 H 2 O(l) + 2 Cl 2(g) 12

Ley de Acción de Masas ó Expresión de la Constante de Equilibrio Establece que cuando una reacción reversible alcanza el equilibrio, se le puede calcular su Constante de equilibrio ( Keq), a una temperatura dada Y se expresa de la manera siguiente: Keq = [C] c [D] d Los corchetes [ ] significan conc. Molar (m/L) [ A] a [ B ]b (los exponentes son los coeficientes) Para la reacción a. A + b. B ⇋ c. C + d. D N 2 (g) + 3 H 2 (g) ⇄ 2 NH 3 (g) 13

La Keq nos ayuda a predecir , hacia donde se desplaza una reacción Keq = 1 el equilibrio no se desplaza Keq > 1 el equilibrio se desplaza a la formación de producto Keq < 1 el equilibrio se desplaza a la formación de reactivos.
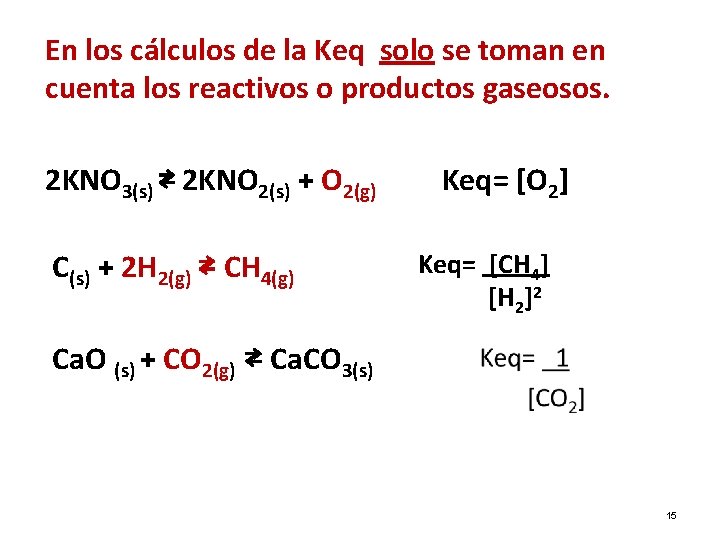
En los cálculos de la Keq solo se toman en cuenta los reactivos o productos gaseosos. 2 KNO 3(s) ⇄ 2 KNO 2(s) + O 2(g) C(s) + 2 H 2(g) ⇄ CH 4(g) Keq= [O 2] Keq= [CH 4] [H 2]2 Ca. O (s) + CO 2(g) ⇄ Ca. CO 3(s) 15

Cálculo de Keq: 1. Calcule la Keq para la reacción y analice hacia donde se desplaza el equilibrio : N 2 (g) + 3 H 2 (g) ⇄ 2 NH 3 (g) Sabiendo que en el equilibrio : [N 2]= 0. 2 [H 2] = 0. 4 [ NH 3]= 0. 3 Keq = [ NH 3] 2 Keq = (0. 3)2 _ [ N 2] [H 2] 3 (0. 2)(0. 4) 3 Keq= 7. 03 Si es mayor de 1, la reacción se desplaza al lado de los productos (hacia la derecha). 16

Cálculo de la concentración de uno de los reactivos ó productos conociendo Keq 2. Calcule la [H 2] para la siguiente reacción en equilibrio , conociendo la Keq = 0. 8 y las concentraciones : CO (g) + H 2 O (g) ⇄ CO 2 (g) + H 2 (g) [CO] = 0. 2 [H 2 O] = 0. 1 [CO 2] = 0. 4 Keq = [CO 2][ H 2] 0. 8 = (0. 4) ( x ) [ CO ][H 2 O] (0. 2) (0. 1) ( x) = 0. 8 (0. 2) (0. 1) / (0. 4) = 0. 04 [H 2 ] = 0. 04 17

Ejercicios: 1. Escriba las expresiones para las constantes de equilibrio de las siguientes reacciones e indique el tipo de equilibrio (homogéneos ó heterogéneos): a) PCl 5 (g) ⇄ PCl 3 (g) + Cl 2(g) b) NH 3(g) + 5 O 2(g) ⇄ 4 NO(g) + 6 H 2 O(g) c) 2 Na. HCO 3 (s) ⇄ Na 2 CO 3 (s) + CO 2(g) + H 2 O(g) 2. Dadas las [ ] en equilibrio calcule el valor de la Keq: 2 A+B⇄3 C+D [A] = 0. 35 M; [B] = 0. 9 M; [C] = 0. 10 M; [D] = 0. 50 M 18

3. ¿Cuál es el valor de la constante de equilibrio ( K eq ) para la siguiente reacción? CO 2(g) + H 2(g) ⇄CO(g) + H 2 O(g) 4. La Keq de la reacción siguiente es 0. 212. Cuando [NO 2] = 0. 40 M, ¿Cuál es la [N 2 O 4] en el equilibrio? N 2 O 4(g) ⇄ 2 NO 2(g) 19

Principio de Le Chatelier Si se aplica una alteración (como un cambio de concentración, presión o temperatura) en una reacción en equilibrio, el equilibrio se desplaza en la dirección que disminuya la alteración. • Es decir, el sistema responde cambiando la velocidad de reacción hacia la derecha o a la izquierda, para minimizar la perturbación y restablecer el equilibrio. • 20

Factores que afectan el equilibrio: Concentración, presión y temperatura 1. Concentración Si se aumenta la [reactivos ] el equilibrio se desplaza a mayor formación de productos (derecha →). Si se disminuye la [reactivos ] el equilibrio se desplaza a mayor formación de reactivos (izquierda ←). Si se aumenta la [productos ] el equilibrio se desplaza a mayor formación de reactivos ( izquierda ←). Si se disminuye la [ productos ]el equilibrio se desplaza a mayor formación de productos (→ derecha).

2. Temperatura: En las Reacciones endotérmicas: necesitan calor, se puede considerar al calor como reactivo para predecir el desplazamiento del equilibrio. 2 KCl. O 3 + calor ⇄ 2 KCl + 3 O 2 ↑ de T el equilibrio se desplaza a la → ↓ de T el equilibrio se desplaza a la ← En las Reacciones exotérmicas: liberan calor, se puede considerar al calor como uno de los productos. N 2 (g) + 3 H 2(g) ⇄ 2 NH 3 (g) + calor ↑ de T el equilibrio se desplaza a la ← ↓de T el equilibrio se desplaza a la → 22
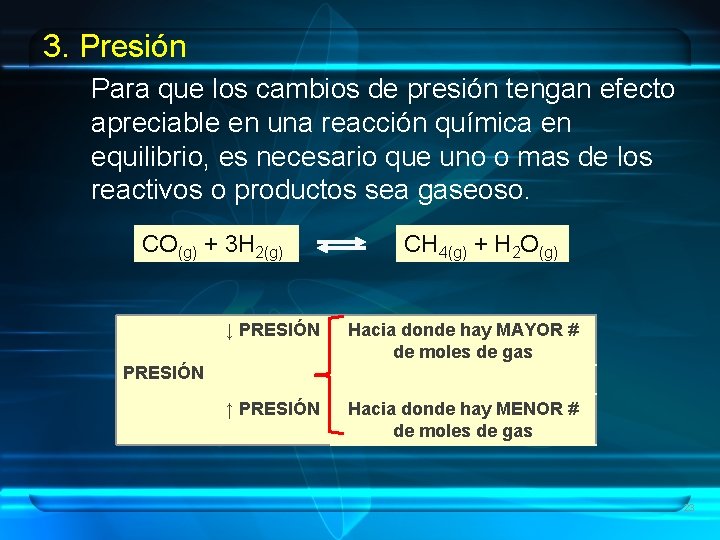
3. Presión Para que los cambios de presión tengan efecto apreciable en una reacción química en equilibrio, es necesario que uno o mas de los reactivos o productos sea gaseoso. CO(g) + 3 H 2(g) CH 4(g) + H 2 O(g) ↓ PRESIÓN Hacia donde hay MAYOR # de moles de gas ↑ PRESIÓN Hacia donde hay MENOR # de moles de gas PRESIÓN 23

Principio de Le Chatelier Si se aplica una alteración (como un cambio de concentración, presión o temperatura) en una reacción en equilibrio, el equilibrio se desplaza en la dirección que disminuya la alteración. • Es decir, el sistema responde cambiando la velocidad de reacción hacia la derecha o a la izquierda, para minimizar la perturbación y restablecer el equilibrio. • 24
![FACTOR CONCENTRACION Alteración Desplazamiento del Equilibrio ↓ [ ] productos ↑ [ ] reactivos FACTOR CONCENTRACION Alteración Desplazamiento del Equilibrio ↓ [ ] productos ↑ [ ] reactivos](http://slidetodoc.com/presentation_image_h/a4cf1e6c5d3bf73de9a9ae86c6ef053f/image-25.jpg)
FACTOR CONCENTRACION Alteración Desplazamiento del Equilibrio ↓ [ ] productos ↑ [ ] reactivos Derecha ↓ [ ] reactivos ↑ [ ] productos Izquierda Si ↑ T° Endotérmicas Si ↓ T° TEMPERATURA Si ↑ T° Exotérmicas Si ↓ T° → ← Derecha → Izquierda ← Derecha → Si ↓ Presión Hacia donde hay MAYOR # de moles de gas Si ↑ Presión Hacia donde hay MENOR # de moles de gas PRESION 25

Ejercicios: 1. Considere el siguiente sistema: C 2 H 6 (g) ⇄ C 2 H 4(g) + H 2 (g) + Calor Prediga hacia donde se desplaza el equilibrio si: a) Aumentamos la temperatura_______ b) Disminuimos [ C 2 H 4] ______ c) Aumentamos [ H 2 ]________ d) Disminuimos la presión _____ e) Disminuimos la temperatura ______

2. Para la reacción en equilibrio 2 NO 2(g) ⇄ 2 NO (g)+ O 2(g) + calor A) Es exotérmica ó endotérmica? B) Escriba la constante de equilibrio : C) Es equilibrio homogéneo ó heterogéneo? Hacia donde (IZQUIERDA Ó DERECHA) desplazará el equilibrio si se: D) Aumenta la temperatura: E) Disminuye [ NO] : F) Disminuye la temperatura: G) Aumenta [ NO 2]: H) Aumenta la presión: 27

3. En la reacción : PCl 5(g) + calor ⇄ PCl 3(g) + Cl 2(g) En qué sentido se desplaza el equilibrio al : a)Extraer Cl 2 b) Disminuir la temperatura c)Agregar PCl 3 d)Extraer PCl 5 e)Aumentar la presión 28
- Slides: 28