Semana 11 2021 VELOCIDAD DE REACCIN Y EQUILIBRIO

Semana 11 -2021 VELOCIDAD DE REACCIÓN Y EQUILIBRIO QUÍMICO LICDA : ISABEL FRATTI DE DEL CID IMÁGENES, ILUSTRACIONES, CUADROS PROPORCIONADOS POR LICDA. LILIAN GUZMÁN

Cinética Química 2 Es el estudio de las velocidades de reacción y los factores que afectan la velocidad de reacción. TEORIA DE COLISIONES Indica que una reacción tiene lugar solo cuando los Reactivos (moléculas , átomos, iones), chocan con la orientación adecuada y suficiente energía. Pueden ocurrir muchas colisiones, pero muy pocas son efectivas, es decir; conducen a la formación de productos.

3 Condiciones indispensables para que ocurra una reacción A- Colisión : las partículas ( moléculas, átomos e iones) de los reactivos deben chocar es decir colisionar entre ellos. B-Orientación: Los reactivos deben alinearse correctamente para que al chocar se puedan romper y formar enlaces. C- Energía : La colisión debe suministrar suficiente energía para alcanzar la energía de activación necesaria para esa reacción.
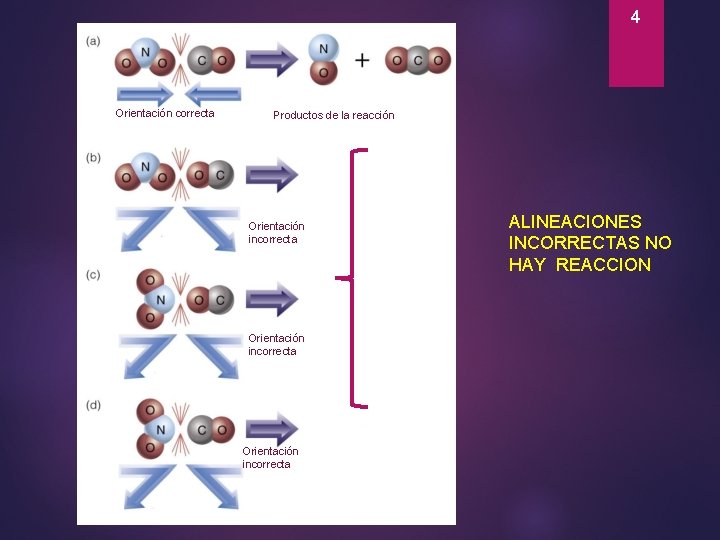
4 Orientación correcta Productos de la reacción Orientación incorrecta ALINEACIONES INCORRECTAS NO HAY REACCION

5 Energía de Activación Es la cantidad mínima de energía necesaria para romper los enlaces entre los átomos de los reactivos de tal manera que estos se conviertan en productos. Si la energía que resulta de la colisión es menor que la energía de activación, los reactivos, chocan y rebotan, pero no se transforman en productos, es decir no hay reacción.
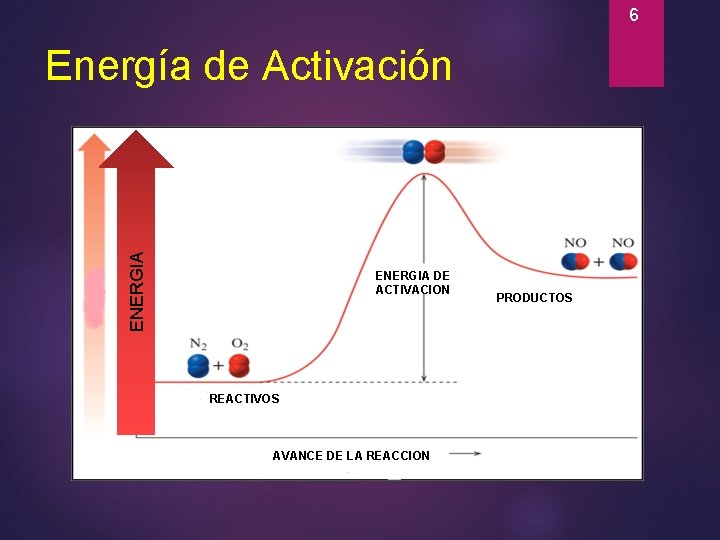
6 ENERGIA Energía de Activación ENERGIA DE ACTIVACION REACTIVOS AVANCE DE LA REACCION PRODUCTOS

7 Velocidad de Reacción Se define como la cantidad de reactivo consumido o de producto obtenido en un periodo dado de tiempo. Velocidad de reacción = Cambio en [Reactivo o Producto] Unidad de tiempo

8 Factores que afectan la velocidad de reacción 1. Temperatura 2. Concentración de reactivos 3. Catalizadores ( catalíticos)

9 1 -Temperatura Al aumentar la temperatura , aumenta la energía cinética de las partículas, (Recordar qué energía cinética es E k= ½ mv 2 ) por lo tanto se mueven más rápido, chocan más veces por unidad de tiempo. Además al moverse más rápido llevan más energía y es más probable que mayor numero de reactivos alcancen la energía de activación necesaria para de formación de productos. Todo esto aumenta la velocidad de reacción. Temperatura velocidad de reacción

10 2. Concentración de reactivos Al aumentar la concentración de las partículas reaccionantes, aumenta el número de colisiones y la reacción avanza más rápido : [Reactivos] Velocidad de reacción
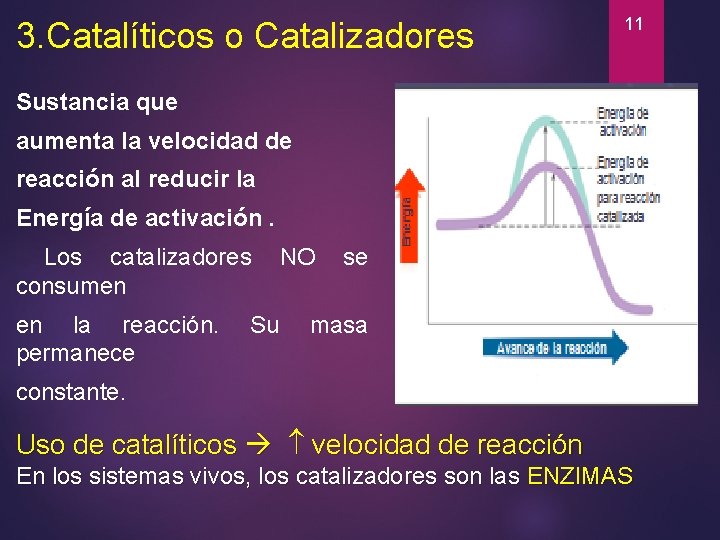
3. Catalíticos o Catalizadores 11 Sustancia que aumenta la velocidad de reacción al reducir la Energía de activación. Los catalizadores consumen en la reacción. permanece Su NO se masa constante. Uso de catalíticos velocidad de reacción En los sistemas vivos, los catalizadores son las ENZIMAS

12 Reacciones Reversibles En algunas reacciones, se forman los productos y éstos interactúan y chocan para formar los reactivos nuevamente. Es decir, éstas reacciones, pueden llevarse a cabo en uno u otro sentido, hasta llegar al equilibrio. Reacción directa : Reacción Inversa: Reacción reversible: A B A ⇄ B

Equilibrio Químico 13 Punto en el cual la velocidad de la reacción directa es igual a la velocidad de la reacción inversa. Los reactivos forman productos con la misma frecuencia que los productos forman reactivos. En el equilibrio : Las velocidades de las reacciones directa e inversa son iguales. Las concentraciones de reactivos y productos permanecen constantes ( no iguales ), es decir ya no hay cambios en las concentraciones de reactivos y productos.

14 https: //www. youtube. com/watch? v=J 0 j 61 P_ok 5 Y

Ley de Acción de Masas 15 Establece que cuando una reacción reversible alcanza el equilibrio, se le puede calcular a una temperatura dada su Constante de equilibrio ( Keq), la cual se expresa de la manera siguiente: Para la reacción a. A+b. B ⇋ c. C +d. D Keq = [C] c [D] d Concentraciones molares de los productos [A] a [B ] b Concentraciones molares de reactivos Los exponentes corresponden a los coeficientes en la ecuación balanceada

16 El valor numérico de la Keq se obtiene al dividir el producto de las concentraciones molares en el equilibrio de los productos dentro del producto de las concentraciones molares de los reactivos, cada una elevada a la potencia que corresponde a su coeficiente en la ecuación balanceada. a. A + b. B ⇄ c. C + d. D

17 Uso del valor de la Keq : Nos ayuda a predecir hacia donde se desplaza mayoritariamente la reacción. Keq = 1 : [Reactivos] [Productos] reacción moderada. Keq 1: [Reactivos] menor que [ Productos] el equilibrio está más desplazado a la formación de productos ( desplazado a la derecha) Keq 1: [ Reactivos] mayor que [ Productos ] el equilibrio se desplaza a la formación de reactivos desplazado a la izquierda ) (

Equilibrio Homogéneo 18 Es aquel en el cual todos los reactivos y productos se encuentran en el mismo estado físico ( Ejemplo todos son gases). Equilibrio Heterogéneo Es aquel en el que uno o mas de los reactivos ó productos no están en el mismo estado ( ejemplo unos son gases y otros sólidos)

En un equilibrio heterogéneo los reactivos o productos 19 SÓLIDOS sin disolver no se colocan en la constante de equilibrio. puesto que sus concentraciones no varían significativamente. Ejemplos : 2 KNO 3(s) ⇄ 2 KNO 2(s) + O 2(g) C(s) + 2 H 2(g) ⇄ CH 4(g) Ca. O (s) + CO 2 (g) ⇄ Ca. CO Keq= [O 2] Keq= [CH 4 ] [H 2]2 3 (s) Keq = 1_ [ CO 2] Nota: la concentración de los sólidos no se escriba en la expresión y cálculo de Keq.

En el equilibrio homogéneo 20 Se toman en cuenta todos los participantes en la reacción: Ejemplo: 2 SO 2 (g) + 2 H 2 O (g) ⇄ 2 H 2 S (g) + 3 O 2 (g) Keq = [H 2 S]2[O 2]3 [ SO 2]2 [H 2 O] 2

21 Ejemplo de cálculo de Keq: Calcule la Keq y diga hacia donde se halla desplazado el equilibrio para la reacción: N 2 (g) + 3 H 2 (g) ⇄ 2 NH 3 (g) Sabiendo que en el equilibrio : [N 2]= 0. 2 [H 2] = 0. 4 [ NH 3]= 0. 3 Keq. [ NH 3] 2 Keq = (0. 3)2 _ [ N 2] [H 2] 3 (0. 2)(0. 4) 3 Keq= 7. 03, como es mayor de 1. ( >1 ), la reacción se halla más desplazada al lado de los productos es decir hacia la derecha.

22 Ejemplo 1: de cálculo de la concentración de uno de los reactivos ó productos conociendo Keq Calcule la [H 2], para la siguiente reacción : CO (g) + H 2 O (g) ⇄ CO 2 (g) + H 2 (g) si Keq = 0. 8 y en el equilibrio las concentraciones son: [CO] = 0. 2 [H 2 O] = 0. 1 [CO 2] = 0. 4 Resolucion: Escriba ecuación de Keq y sustituya con valores Keq = [CO 2][ H 2] [ CO ][H 2 O] 0. 8 = (0. 4) ( x ) despejar x (0. 2)(0. 1) ( x) = 0. 8 (0. 2) (0. 1) / (0. 4) = 0. 04 [ H 2 ] = 0. 04 Resp. [H 2 ] = 0. 04

23 Ejemplo 2: Escriba las expresiones de las constantes de equilibrio de las siguientes reacciones: y diga si son equilibrios homogéneos ó heterogéneos. a) PCl 5 (g) ⇄ PCl 3 (g) + Cl 2(g) b) 4 NH 3(g) + 5 O 2(g) ⇄ 4 NO(g) + 6 H 2 O(g) c) 2 Na. HCO 3 (s) ⇄ Na 2 CO 3 (s) + CO 2(g) + H 2 O(g)

24 Ejemplo 3: Dadas las concentraciones en equilibrio calcule el valor de la constante de equilibrio y diga hacia donde se desplaza el equilibrio. 2 A+B⇄3 C+D [A] = 0. 35 M; [B] = 0. 9 M; [C] = 0. 10 M; [D] = 0. 50 M

25 Ejemplo 4: ¿Cuál es el valor de la constante de equilibrio ( K eq ) para la siguiente reacción? CO 2(g) + H 2(g) ⇄CO (g) + H 2 O(g) Si [CO] =0. 25 M, [H 2 O] =0. 4 M, [CO 2]=0. 50 M [H 2]=0. 1 M La Keq de la reacción siguiente es 0. 212. Cuando [NO 2] = 0. 40 M, ¿Cuál es la [N 2 O 4] en el equilibrio? N 2 O 4(g) ⇄ 2 NO 2(g)
![Calcular Keq para la siguiente reacción: C(S) + H 2 O(g) SÍ: [C] = Calcular Keq para la siguiente reacción: C(S) + H 2 O(g) SÍ: [C] =](http://slidetodoc.com/presentation_image_h2/47466204a2efe8e84cc60e9b2d5fe090/image-26.jpg)
Calcular Keq para la siguiente reacción: C(S) + H 2 O(g) SÍ: [C] = 0. 3 CO(g) + H 2(g) [CO] = 0. 4 [H 2 O] = 0. 2 [H 2(g)]= 0. 3 y diga hacia donde se desplaza l equilibrio 26

27 Factores que afectan el equilibrio 1 - Concentración de Reactivos y Productos. 2 - Temperatura 3 - Presión
![28 Factores que afectan el equilibrio Concentración Si se aumenta la [Reactivos ] el 28 Factores que afectan el equilibrio Concentración Si se aumenta la [Reactivos ] el](http://slidetodoc.com/presentation_image_h2/47466204a2efe8e84cc60e9b2d5fe090/image-28.jpg)
28 Factores que afectan el equilibrio Concentración Si se aumenta la [Reactivos ] el equilibrio se desplaza a mayor formación de productos. Es decir hacia la derecha. (derecha →) Si se disminuye la [Reactivos ] el equilibrio se desplaza a la izquierda a mayor formación de reactivos ( Izquierda ←) -Si se aumenta la [productos ] el equilibrio se desplaza a mayor formación de reactivos ( izquierda ←) -Si se disminuye la [ productos ] el equilibrio se desplaza a mayor formación de productos (→ derecha)

Cambios en la Temperatura en reacciones endotérmicas 29 Reacciones endotérmicas: necesitan calor se puede considerar al calor como reactivo (componente del lado izquierdo) para predecir el desplazamiento del equilibrio. Entonces: Si aumenta calor, aumenta la izquierda el equilibrio se desplaza a la derecha ( contra el aumento). Si disminuye Temperatura, disminuye izquierda, se desplaza hacia izquierda ( a favor de la disminución) 2 KCl. O 3 + calor ⇄ 2 KCl + 3 O 2 Endotérmica ↑ de Temperatura el equilibrio se desplaza hacia la derecha → ENDOTERMICA ↓ de Temperatura el equilibrio se desplaza hacia la izquierda ←

30 Cambios en la Temperatura, en reacciones exotérmicas Reacciones exotérmicas: Liberan calor ; se puede considerar al calor como uno de los productos (un componente del lado derecho). Entonces : Al aumentar temperatura (AUMENTA DERECHA), el equilibrio se desplaza hacia la izquierda( en contra del aumento) Al disminuir la temperatura ( DISMINUYE DERECHA) EL EQUILIBRIO se desplaza hacia la derecha ( a favor de la disminución) N 2 (g) + 3 H 2(g) ⇄ 2 NH 3 (g) + calor Exotérmica ↑ de T el equilibrio ← EXOTERMICA ↓de T el equilibrio →
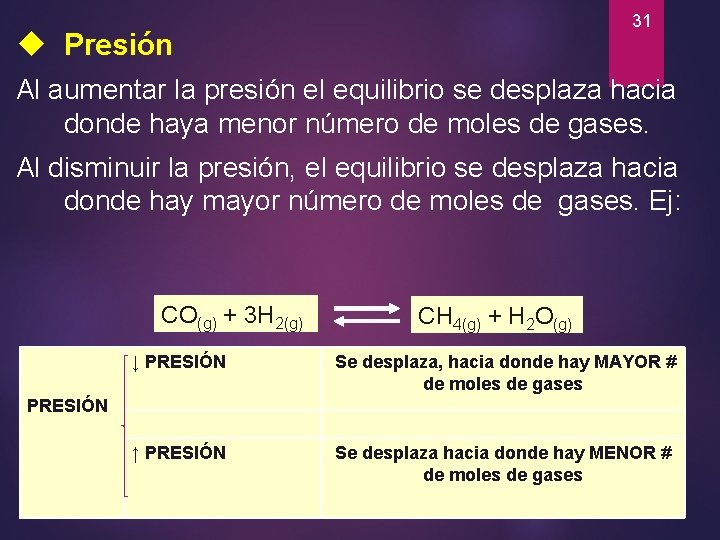
31 Presión Al aumentar la presión el equilibrio se desplaza hacia donde haya menor número de moles de gases. Al disminuir la presión, el equilibrio se desplaza hacia donde hay mayor número de moles de gases. Ej: CO(g) + 3 H 2(g) CH 4(g) + H 2 O(g) ↓ PRESIÓN Se desplaza, hacia donde hay MAYOR # de moles de gases ↑ PRESIÓN Se desplaza hacia donde hay MENOR # de moles de gases PRESIÓN

32 Principio de Le Chatelier Si se aplica una alteración (como un cambio de concentración, presión o temperatura) en una reacción en equilibrio, el equilibrio se desplaza en la dirección que disminuya la perturbación. Es decir, el sistema responde cambiando la velocidad de reacción hacia la derecha o a la izquierda, para minimizar la alteración y restablecer el equilibrio.

33 Generalmente: «El equilibrio se desplaza en contra del aumento y a favor de la disminución» . Es decir: Si aumentamos algo que esta en la derecha, el equilibrio se desplaza a la izquierda. ( contra el aumento) Si disminuimos algo que está en la derecha, el equilibrio se desplaza a la derecha ( a favor de la disminución). Si aumentamos algo que está en la izquierda, el equilibrio Se desplaza hacia la derecha (contra el aumento). Si disminuimos algo que esta en la izquierda el equilibrio se desplaza hacia la izquierda ( a favor de la disminución) Las prediciones de Le Chatelier acerca de las alteraciones o perturbaciones del equilibrio se resumen en el siguiente cuadro.
![34 FACTOR CONCENTRACION Perturbación ↓ [ productos ] ↑ [ reactivos ] Derecha ↓ 34 FACTOR CONCENTRACION Perturbación ↓ [ productos ] ↑ [ reactivos ] Derecha ↓](http://slidetodoc.com/presentation_image_h2/47466204a2efe8e84cc60e9b2d5fe090/image-34.jpg)
34 FACTOR CONCENTRACION Perturbación ↓ [ productos ] ↑ [ reactivos ] Derecha ↓ [ reactivos ] ↑ [ productos ] Izquierda Si ↑ T Endotérmicas A + calor B Si ↓ T TEMPERA TURA Si ↑ T Exotérmicas A B + calor Desplazamiento del Equilibrio Si ↓ T → ← Derecha → Izquierda ← Derecha → Si ↓ Presión Hacia donde hay MAYOR # de moles de gas Si ↑ Presión Hacia donde hay MENOR # de moles de gas PRESION

35 Para la reacción en equilibrio 2 NO 2(g) ⇄ 2 NO (g)+ O 2(g) + calor A-Es exotérmica ó endotérmica. ? R: Exotérmica B-Escriba la constante de equilibrio : Keq = [ O 2 ] [ NO] 2 [ NO 2 ] 2 C-Es equilibrio homogéneo/ heterogéneo? R: Homogéneo DHacia que dirección ( IZQUIERDA Ó DERECHA ) de desplazará el equilibrio si se: D. 1 - Aumenta la temperatura: R: Izquierda ( ) D. 2 - Disminuye [ NO] : R: Derecha ( ) D- 3 - Disminuye la temperatura. R: Derecha ( ) D-4 - Aumenta [ NO 2]. R: Derecha ( ) D-5 - Aumenta la presión. R: Izquierda ( ) ( hay menor número de moles de gases.

36 Ejemplo: Si se aumenta la presión en la siguiente reacción: CO(g) + 3 H 2(g) ⇄ CH 4 (g) + H 2 O (g) El equilibrio se desplaza hacia la derecha pues allí hay menos número de moles de gases. Entonces : [CH 4] y [CO] [H 2 O] y [ H 2]

Resuelva lo siguiente: 1. Considere el siguiente sistema: C 2 H 6 (g) ⇄ C 2 H 4(g) + H 2 (g) + Calor Prediga hacia donde se desplaza el equilibrio si: a) Aumentamos la temperatura_____ b) Disminuimos [ C 2 H 4]_______ c) Aumentamos [ H 2 ]. ______ d) Disminuimos la presión: _______ e) Disminuimos la temperatura____ 37

38 Ejercicio 2. Para la reacción en equilibrio 2 NO 2(g) ⇄ 2 NO (g)+ O 2(g) + calor a) Escriba la constante de equilibrio b) Hacia que dirección de desplazará el equilibrio (izquierda derecha) si se: - Disminuye la temperatura__________ - Disminuye el NO de sistema_________ - Aumenta la temperatura___________ - Aumenta la concentración de NO 2: ________ - Cambio de volumen de sistema de 1 a 1. 5 Litros - Aumenta la presión: _______

39 Efecto en las concentraciones de reactivos y productos al provocar cambios en un sistema en equilibrio Si equilibrio se desplaza hacia la derecha A) Aumenta [ productos ] B) Disminuye [ reactivos ] Si equilibrio se desplaza hacia izquierda A: Aumenta [ Reactivos ] B: Disminuye [Productos]
![Resuelva el siguiente ejercicio. DESPLAZAMIENTO DEL EQUILIBRIO 40 ENTONCES a) Aumenta la T° [CO]____ Resuelva el siguiente ejercicio. DESPLAZAMIENTO DEL EQUILIBRIO 40 ENTONCES a) Aumenta la T° [CO]____](http://slidetodoc.com/presentation_image_h2/47466204a2efe8e84cc60e9b2d5fe090/image-40.jpg)
Resuelva el siguiente ejercicio. DESPLAZAMIENTO DEL EQUILIBRIO 40 ENTONCES a) Aumenta la T° [CO]____ [H 2] ____ [CH 4]____ [H 2 O] ____ b) Disminuye [H 2] CO]____ [H 2] ____ [CH 4]____ [H 2 O] _______ c) Disminuye [CH 4 ] CO]____ [H 2] ____ [CH 4]____ [H 2 O] _______ d) Disminuye la presión CO]____ [H 2] ____ [CH 4]____ [H 2 O] _______ e) Aumenta [CO] CO]____ [H 2] ____ [CH 4]____ [H 2 O] _______

41 ESPACIO PARA RESOLVER DUDAS DE PRÁCTICA DE LABORATORIO Fin
- Slides: 41