SEMANA 10 COLOIDES Y SUSPENSIONES Captulo 7 SOLUCIONES
























- Slides: 30

SEMANA 10 COLOIDES Y SUSPENSIONES Capítulo 7

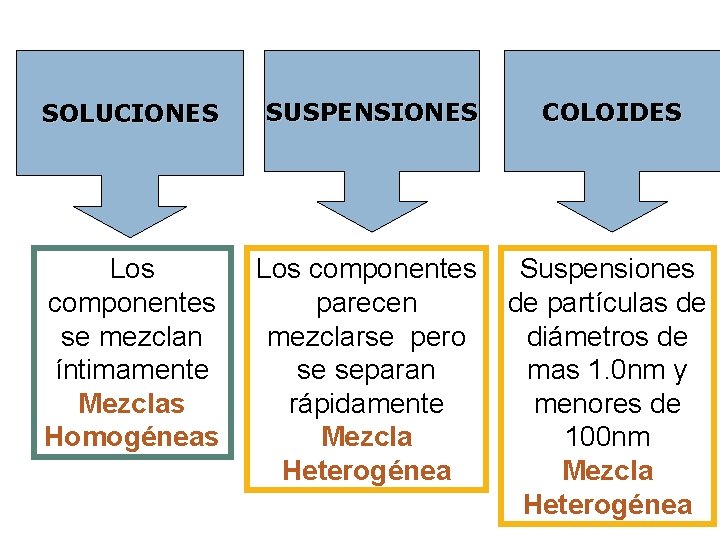
SOLUCIONES SUSPENSIONES COLOIDES Los componentes se mezclan íntimamente Mezclas Homogéneas Los componentes parecen mezclarse pero se separan rápidamente Mezcla Heterogénea Suspensiones de partículas de diámetros de mas 1. 0 nm y menores de 100 nm Mezcla Heterogénea

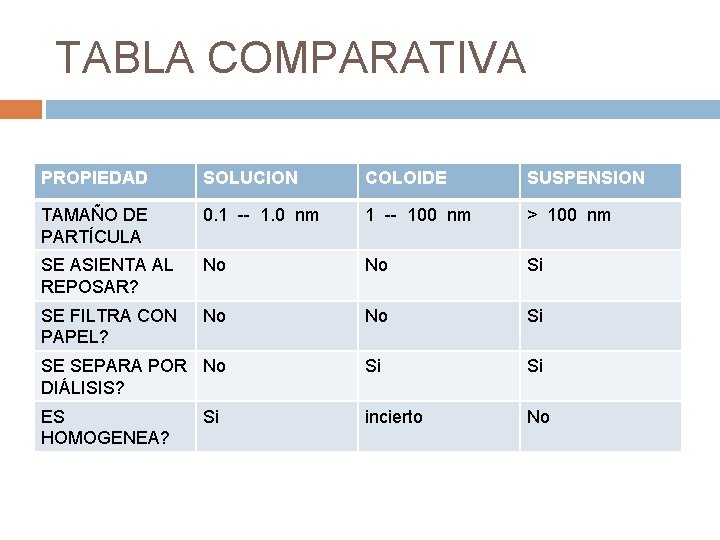
TABLA COMPARATIVA PROPIEDAD SOLUCION COLOIDE SUSPENSION TAMAÑO DE PARTÍCULA 0. 1 -- 1. 0 nm 1 -- 100 nm > 100 nm SE ASIENTA AL REPOSAR? No No Si SE FILTRA CON PAPEL? No No Si SE SEPARA POR No DIÁLISIS? Si Si ES HOMOGENEA? incierto No Si

COLOIDES Coloide proviene de la raíz griega kolas = que puede pegarse Esto refiere a una de sus principales propiedades, que es la tendencia espontánea a agregar o formar coágulos Se pueden definir como aquellos sistemas en los que un componente se encuentra disperso en otro, pero las entidades dispersas son mucho mayores que las moléculas del disolvente.

PROPIEDADES Sistemas heterogéneos formados por una fase dispersante y una o más fases dispersas Sus partículas no pueden ser observadas a simple vista y se les denomina micelas. Son opalescentes, tienen aspecto lechoso o nebuloso. No pueden semipermeables atravesar las membranas

PROPIEDADES Sus partículas presentan browniano y efecto de Tyndall movimiento Las partículas dispersas tienen un tamaño mayor de 0. 1 nm pero menor de 100 nm. El tamaño de partícula no es constante sino que varía dentro de un amplio rango.

Movimiento Browniano Las partículas de una dispersión coloidal real son tan pequeñas que el choque incesante con las moléculas del medio es suficiente para mantener las partículas en suspensión; el movimiento al azar de las partículas bajo la influencia de este bombardeo molecular se llama movimiento browniano. Este movimiento de las partículas es el que impide que éstas se sedimenten cuando el coloide se deja en reposo.

Efecto de Tyndall Las micelas de los coloides pueden hacer reflejar y refractar la luz (la luz dispersada está polarizada), debido a que cada partícula se convierte en un centro emisor de luz y de esa forma se logra observar la trayectoria de un rayo luminoso.

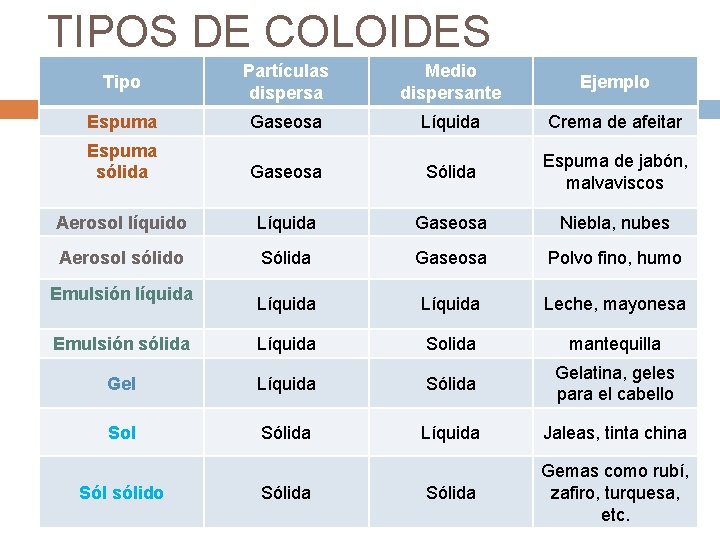
TIPOS DE COLOIDES Tipo Partículas dispersa Medio dispersante Ejemplo Espuma Gaseosa Líquida Crema de afeitar Espuma sólida Gaseosa Sólida Espuma de jabón, malvaviscos Aerosol líquido Líquida Gaseosa Niebla, nubes Aerosol sólido Sólida Gaseosa Polvo fino, humo Líquida Leche, mayonesa Emulsión sólida Líquida Solida mantequilla Gel Líquida Sólida Gelatina, geles para el cabello Sol Sólida Líquida Jaleas, tinta china Sólida Gemas como rubí, zafiro, turquesa, etc. Emulsión líquida Sól sólido Sólida

Nubes (aerosol líquido) Humo (aerosol sólido) Gelatina (gel) Espuma de jabón (espuma) Leche (emulsión) Zafiro (sol sólido)

Los AGENTES EMULSIFICANTES mantienen dispersas las partículas, o sea estabilizan las emulsiones. Ej. : caseína en la leche, las sales biliares en la digestión de las grasas.

Ejemplos de Coloides y Soluciones Sangre Orina Bilis Jugo gástrico Jugo pancreático


DIFUSION Es el movimiento de moléculas de una región de alta concentración a otra de menor concentración, producido por la energía cinética de las moléculas. La VELOCIDAD de difusión es una FUNCION del TAMAÑO de la molécula y la TEMPERATURA. Son dos casos particulares de difusión:


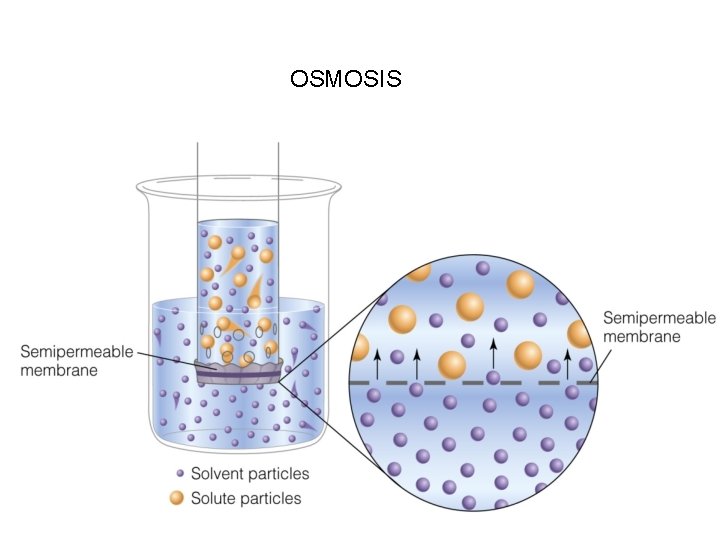
OSMOSIS Es la difusión de AGUA o moléculas de SOLVENTE a través de una membrana semipermeable (en sistemas vivos el solvente es casi siempre AGUA).

OSMOSIS

DIALISIS Difusión selectiva de una sustancia DISUELTA (iones y moléculas pequeñas junto con el disolvente), y retención de las moléculas grandes y partículas coloidales por una membrana dotada de permeabilidad diferencial.

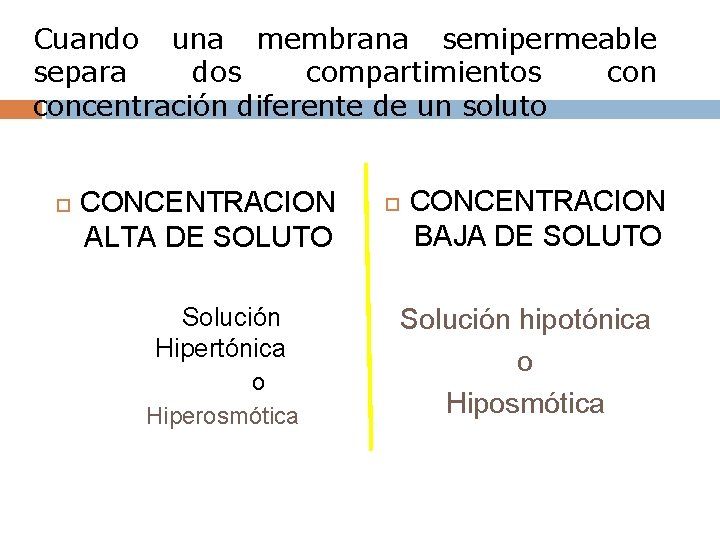
Cuando una membrana semipermeable separa dos compartimientos concentración diferente de un soluto CONCENTRACION ALTA DE SOLUTO Solución Hipertónica o Hiperosmótica CONCENTRACION BAJA DE SOLUTO Solución hipotónica o Hiposmótica

La mayoría de las células mantienen un volumen apropiado al desplazar iones hacia adentro y afuera de la célula hasta que la concentración interna del soluto sea igual a la concentración externa del soluto, entonces, los líquidos interno y externo son ISOTÓNICOS O ISOSMÓTICOS.

Propiedades coligativas Son aquellas que dependen de manera directa del número de partículas de soluto presentes en la solución. Tal es el caso de la elevación del punto de ebullición y la depresión del punto de congelación.

Ejemplos • Una solución 1. 0 molar de azúcar hierve a 100. 52°C, mientras que el agua pura hierve a 100. 0°C a 1 atm. • Una solución 1. 0 molar de azúcar se congela a -1. 86°C mientras que el agua pura se congela a 0°C a 1 atm.

Las propiedades coligativas están relacionadas con la concentración de las partículas de soluto disueltas, sin que importe su identidad, para los sistemas vivos la propiedad coligativa más importante es la presión osmótica

Presión osmótica ∏ Cantidad exacta de presión que se requiere para detener el flujo neto de disolvente, de la solución diluida hacia la solución más concentrada. La magnitud de la presión osmótica depende de la concentración de todas las partículas disueltas en la solución.

La presión osmótica está dada en osmoles Osmolaridad = Molaridad x Número de partículas de soluto que se obtienen en solución por mol de soluto EJEMPLO: Na. Cl Na+ + Cl- (2 particulas/mol) Ejercici os

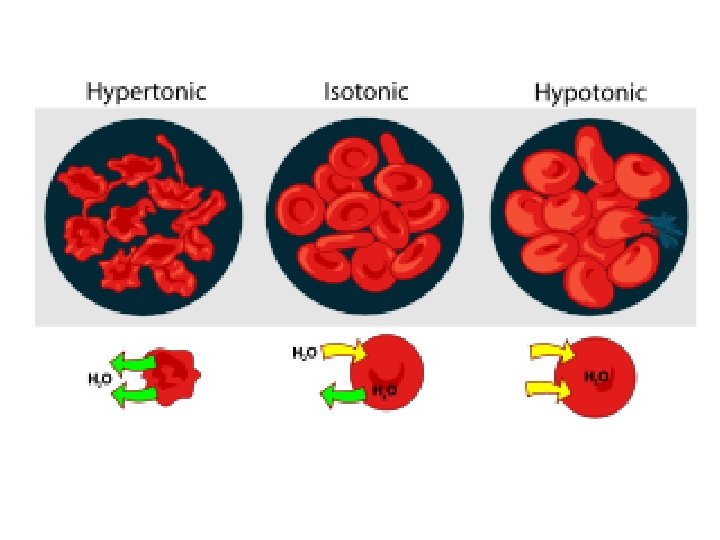
Tonicidad de una solución: Relación entre osmolaridad de una solución y osmolaridad del citoplasma de una célula Solución Isotónica (normal) [ ] de Solutos = [ ] de Solutos de la Célula Osmolaridad = 0. 28 -0. 32 Solución Hipotónica (Hincha) [ ] de Solutos < [ ] de Solutos de la Célula Osmolaridad<0. 28 Solución Hipertónica (Encoge) [ ] de Solutos > [ ] de Solutos de la Célula Osmolaridad>0. 32




Ejercicios de osmolaridad A) Cuál es la osmoralidad de una solución de Na. Cl 0. 9% p/v B) Una solución contiene 5 g de Ca. Cl 2 disueltos en 300 ml de solución, calcule: osmolaridad, tonicidad y prediga, ¿Qué le sucederá a un eritrocito al colocarlo dentro de la solución? C) Una solución de urea contiene 2 g de urea CO(NH 2)2 en 250 ml de solución, ¿Cuál es su osmolaridad? D) Cuántos gramos de KCl se deben disolver en de 1 litro de solución para que ésta sea Isotónica?