Semana 1 Generalidades Antibiticos activos sobre Cocos Gram

� Semana 1: Generalidades � Antibióticos activos sobre Cocos Gram Positivos � Parte 1: Trimetoprim-Sulfametoxazole � � Semana 2: Parte 2: ß-Lactámicos y Glicopéptidos � � Semana 3: Parte 3: , Macrólidos, Estreptograminas, � Oxazolidinonas � � Semana 4: Antibióticos activos sobre Bacilos Gram Negativos: � Antibióticos de uso urinario: Nitrofuranos Quinolonas � � Semana 5: Antivirales � Semana 6: Antibióticos activos sobre Bacilos Gram Negativos de � uso Hospitalario: Oxiiminocefalosporinas, � Carbapenems y Aminoglucósidos

ANTIBIOTICOS: 1. Generalidades y Métodos de Estudio 2. Antibióticos activos sobre cocos Gram positivos 1 era Parte Trimetoprim/Sulfametoxazol

Antibiótico Molécula natural, sintética o semisintética capaz de inducir la muerte o detener el crecimiento de una población bacteriana. Clasificaciones: Según efecto Bactericida vs Bacteriostático
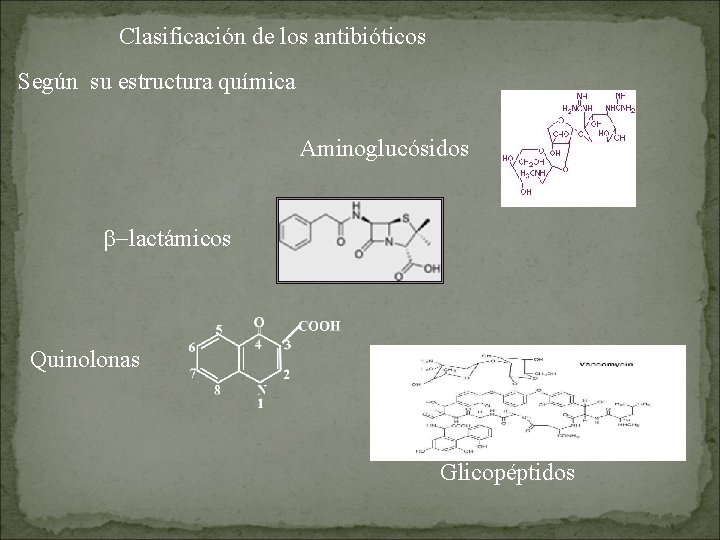
Clasificación de los antibióticos Según su estructura química Aminoglucósidos b-lactámicos Quinolonas Glicopéptidos
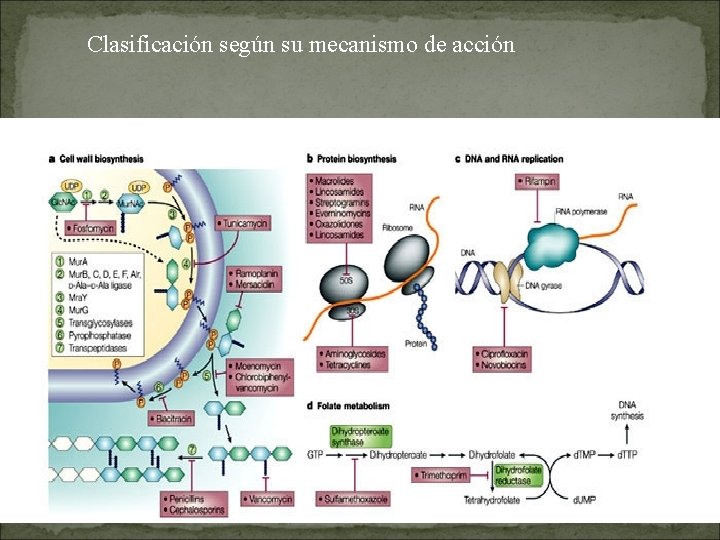
Clasificación según su mecanismo de acción
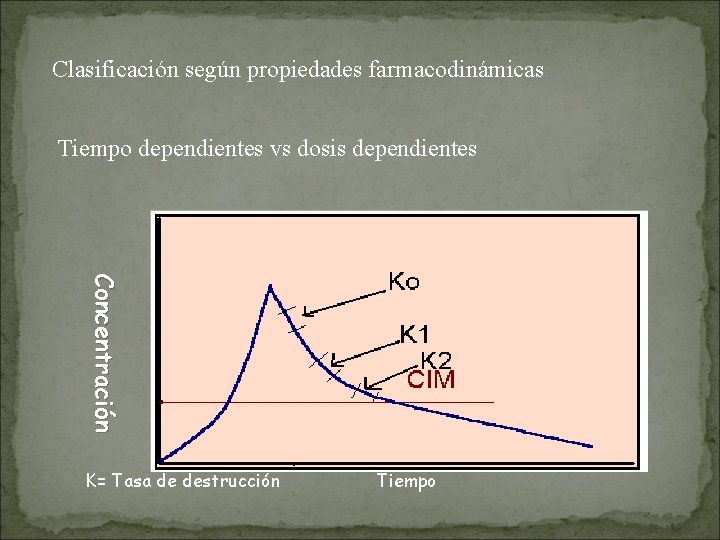
Clasificación según propiedades farmacodinámicas Tiempo dependientes vs dosis dependientes C o n c en t r a c i ó n K= Tasa de destrucción Tiempo
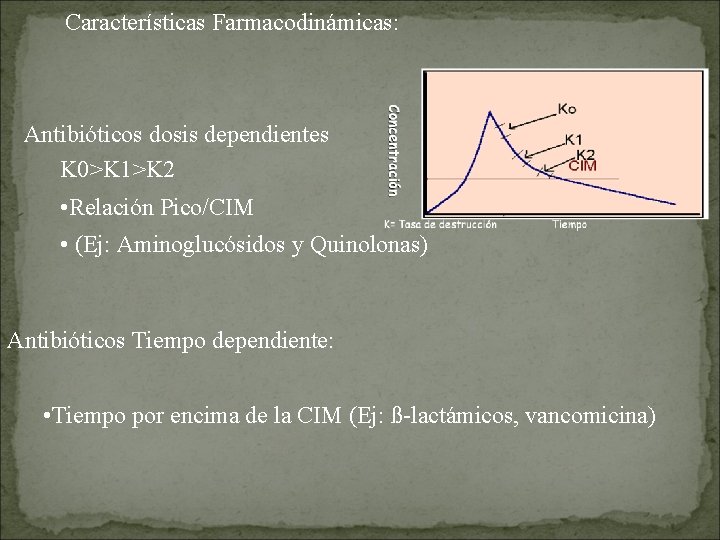
Características Farmacodinámicas: Antibióticos dosis dependientes K 0>K 1>K 2 • Relación Pico/CIM • (Ej: Aminoglucósidos y Quinolonas) Antibióticos Tiempo dependiente: • Tiempo por encima de la CIM (Ej: ß-lactámicos, vancomicina)


Historia de los antibióticos Linea temporal de eventos 1932, Descubrimiento de las Sulfonamides 1952, 1956, Descubrimiento Se introduce la de la Vancomicina Erythromycin Disponible el Linezolid 2000 1928, Descubrimiento de la Penicillina 1962, 1980’s, 1940’s: Penicilina Surgimiento de Disponibles las comienza a las Quinolones Fluoroquinolonas comercializarse, sintesis de cefalosporinas

Luego de la introducción de un nuevo antibiotico tarde o temprano se desarrolla resistencia al mismo

Capacidad de una cepa bacteriana dada de resistir la acción de cierto antibiótico.

TIPOS DE RESISTENCIA NATURAL: propia del microorganismo. Por ejemplo: resistencia a la vancomicina en bacilos gram negativos ADQUIRIDA: es aquel tipo de resistencia que determinada especie ha adquirido a lo largo del tiempo. Por ejemplo: resistencia a penicilina en S. pneumoniae

Se habla de resistencia en tres niveles: 1 -Mecanismo de resistencia: codificado por la célula bacteriana 2 -Resistencia poblacional 3 -Resistencia de una población que esta produciendo una infección-

1. MECANISMOS DE RESISTENCIA Mecanismo molecular utilizado por la célula bacteriana para resistir la acción de los antimicrobianos. HIDRÓLISIS O INACTIVACION ENZIMÁTICA TRASTORNOS DE PERMEABILIDAD ØAlteración de influjo ØEflujo ALTERACIONES DEL SITIO DE ACCION
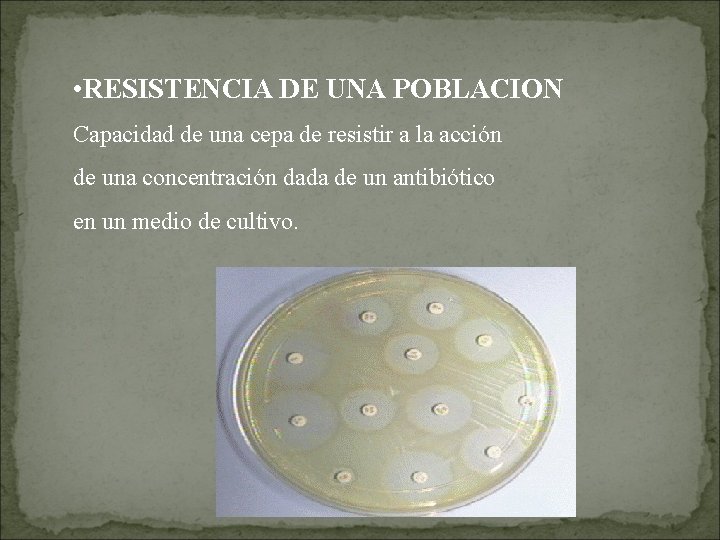
• RESISTENCIA DE UNA POBLACION Capacidad de una cepa de resistir a la acción de una concentración dada de un antibiótico en un medio de cultivo.

¿Cómo predecir desde el laboratorio el éxito terapéutico? • PRUEBAS CUANTITATIVAS • PRUEBAS CUALITATIVAS

• PRUEBAS CUANTITATIVAS ESTANDARIZADOS: CLSI CIM-mínima concentración de antibiótico capaz de inhibir el crecimiento de una población bacteriana (inoculo estandarizado 5 10 5 UFC/ml). CBM- mínima concentración de antibiótico capaz de matar el 99, 9% de una población bacteriana (inoculo estandarizado inicial). MACRO Y MICRODILUCION EN CALDO, DILUCION EN AGAR, GRADIENTE ANTIBIOTICO
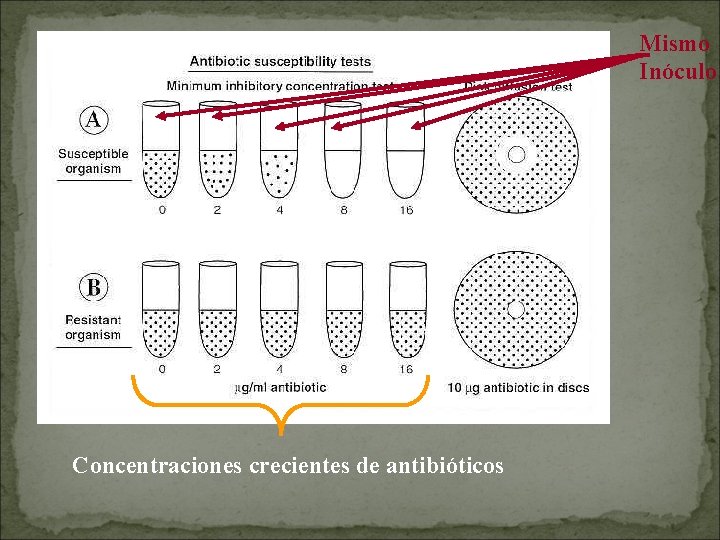
Mismo Inóculo Concentraciones crecientes de antibióticos

E-TEST
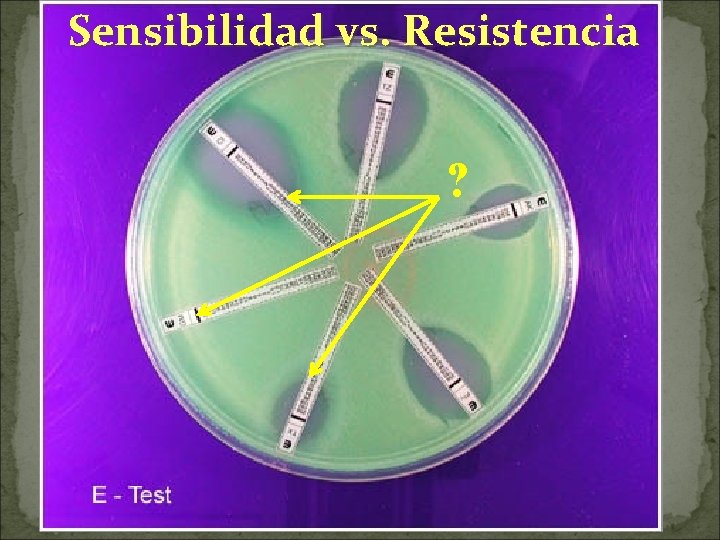
Sensibilidad vs. Resistencia ?

Sensibilidad vs. Resistencia Puntos de quiebre o puntos de corte microbiológicos: Valores de CIM o de diámetro de halo que delimitan la sensibilidad y la resistencia

Se establecen de acuerdo a: COMPORTAMIENTO BACTERIANO � Distribución poblacional � Presencia de mecanismos de resistencia FARMACOCINÉTICA. Y FARMACODINAMIA DE LAS DROGAS � Biodisponibilidad � Efecto post antibiótico RESPUESTA CLÍNICA Y MICROBIOLÓGICA.

PRUEBAS CUALITATIVAS DISCO DIFUSION Método estandarizado de acuerdo a CLSI Preparación y estandarización del inoculo Inoculación de las placas Aplicación de discos Incubación Medida de zonas de inhibición Control de calidad
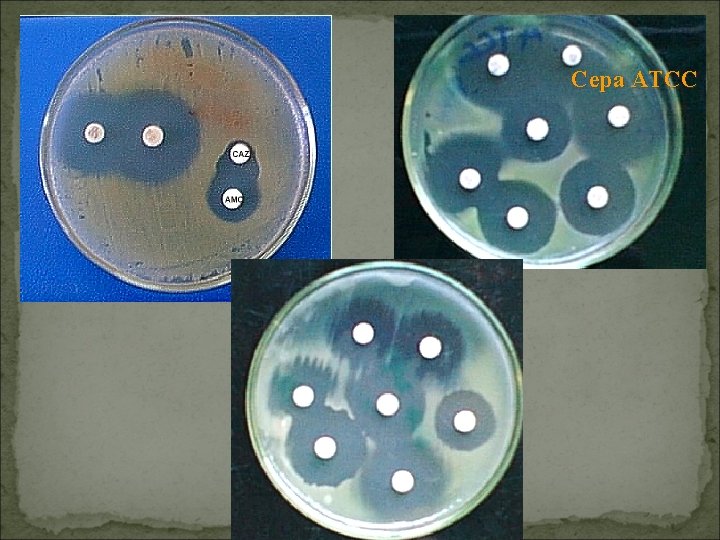
Cepa ATCC
• RESISTENCIA DE UNA POBLACION PRODUCIENDO UNA INFECCION Eficacia Terapéutica

Trimetoprim-Sulfametoxazol

Estructura química �Las sulfonamidas representan el genérico de la sulfanilamida. Estos fármacos contienen un grupo sulfuro unido a un anillo de benceno y grupos NH 2 que le confieren a la molécula la actividad antibacteriana. �Trimetoprim es una 2, 4 -diamino-5 -(3′, 4′, 5′- trimetoxibenzil) pirimidina. A pesar de tener actividad antimicrobiana propia esta droga fue sintetizada como un inhibidor de la enzima dihidrofolato reductasa (DHFR) con la finalidad de potenciar la actividad de las sulfonamidas.

Actividad antimicrobiana � Las sulfonamidas interfieren con la formación de ácido fólico en las bacterias mediante la inhibición competitiva de la enzima bacteriana dihidropteroato sintasa. Desde un punto de vista microbiológico las sulfonamidas sintéticas son un único agente que opera por homología estructural con el ácido paraaminobenzoico (PABA) en la vía metabólica que lleva al ácido fólico. � El Trimetoprim es también un agente antibacteriano sintético que pertenece al grupo de compuestos diaminopiridinas. Puede verse como un antifolato, un análogo del ácido fólico, que inhibe competitivamente la reducción del dihidrofolato al tetrahidrofolato mediante la enzima dihidrofolato reductasa (DHFR). � Esta reacción enzimática es crucial en todas las células, ya que es necesaria para la síntesis del nucleótido Timina (ADN). � Ambos ejercen un efecto bacteriostático.
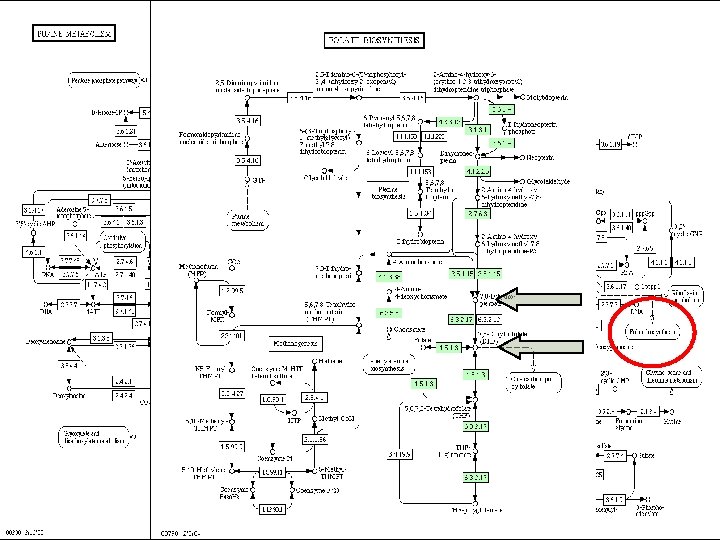
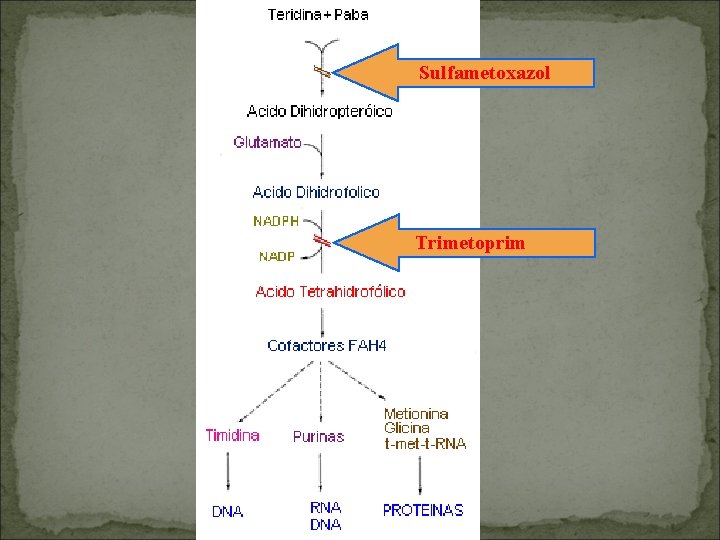
Sulfametoxazol Trimetoprim

Espectro de actividad antimicrobiana �El TMP-SMX es activo contra algunas cepas de Cocos gram (+), Bacilos gram (-), Cocobacilos gram (-) y algunos otros como Chlamydia trachomatis, Nocardia y Pneumocystis carinii. �No cubre a los anaerobios, las micobacterias ni Treponema pallidum

Farmacología �Vías de Administración: �Oral: Alcanza picos en suero de 1 μg/ml luego de 1 -4 horas después de la ingestión �Intravenosa: Se logran concentraciones en suero de 3. 4 μg/m. L luego de 1 hora de administrado. Con dosis repetidas el pico de trimetoprim puede aproximarse a los 9 μg/m. L. Es posible alcanzar niveles similares con la terapia oral pero solamente después de 2 -4 horas de ingerido el antibiótico.

Farmacocinética � El TMP-SMX se absorbe de forma rápida y completa (95%) a nivel del TGI (El TMP en 2 horas y el SMX en 4 horas). � Para obtener el máximo efecto sinérgico la relación en las concentraciones séricas pico debe ser de 20: 1 de SMX a TMP, lo cual se logra al utilizar dosis en una relación de 5: 1 (Ej. : Bactrim). � El 45% del TMP y el 70% del SMX se unen a proteínas. La vida media plasmática para el TMP es de 6 a 17 horas vs. 9 horas para el SMX. El TMP al ser más lipofílico que el SMX, alcanza concentraciones más altas en varios tejidos y fluídos corporales. � Ambos compuestos se distribuyen ampliamente en diferentes tejidos y secreciones. También atraviesan la placenta y se excretan por la leche materna. � Estos compuestos se eliminan como metabolitos inactivos o sin modificación en un 80% por vía renal y 20% por vía hepática. Se necesita ajustar la dósis si está comprometida la función renal.

Toxicidad e interacciones � Efectos adversos gastrointestinales: Puede producir anorexia, náuseas, vómitos y diarrea en un 10% de los pacientes. � Reacciones de Hipersensibilidad: Principalmente en la forma de rash o fiebre; ocurre en el 3 al 5% de los pacientes. Las reacciones de hipersensibilidad son más frecuentes en los pacientes con VIH. � Otros: Hipercalemia, meninigitis aséptica y meninigoencefalitis, eritema multiforme, síndrome de Steven Johnson, anemia aplásica, agranulocitosis, trombocitopenia, hemólisis, necrosis hepática fulminante, hepatitis y nefritis Intersticial � Interacciones: Potencia efecto de Warfarina, hipoglicemiantes orales, Fenitoína y Metrotexate, por desplazarlos de las proteínas.

Uso Clínico � 1. Infecciones urinarias no complicadas (por patógenos no resistentes). 2. ITU crónica o recurrente (por patógeno sensible) Ap. genitourinario 3. Prostatitis, orquitis y epididimitis. � 1. Exacerbaciones agudas de la bronquitis crónica. 2. Neumonía por Legionella y Pneumocystis carinii. Ap. respiratorio 3. Nocardiosis, ya sea pulmonar o en otros órganos. 4. Granulomatosis de Wegener, (limitada a pulmón o sin vasculitis diseminada) 5. Neumonía Adquirida en la Comunidad (Aunque hay muchos neumococos resistentes) � 1. Sinusitis aguda. Oido-Nariz-Laringe 2. Otitis media aguda. � 1. Diarrea del viajero causada por E. Coli productora de enterotoxinas. 2. Shigellosis, isosporiasis , ciclosporiasis, fiebre tifoidea (Salmonella) y diarrea por Vibrio cholera. 3. Profilaxis de los pacientes con alto riesgo de desarrollar peritonitis bacteriana primaria. T. G. I.

Mecanismos de Resistencia � Cromosómica: La resistencia a Trimetoprim está dada por mutaciones en el gen dfr que determinan una mayor expresión de la enzima dihidrofolato reductasa o enzimas con menor afinidad por el antibiótico. La resistencia a sulfonamidas consistiría en mutaciones en el gen fol. P (dihidropteroato sintasa), resultando en una menor afinidad del antibiótico por la enzima mutada. � Otros mecanismos incluyen la sobreproducción de PABA y alteraciones en la permeabilidad de la membrana celular. � Plasmídica: La resistencia a ambos antibióticos se da por la presencia de variantes no alélicas de las enzimas blanco cromosómicas (dihidrofolato reductasa y dihidropteroato sintasa) resistentes a ambas drogas

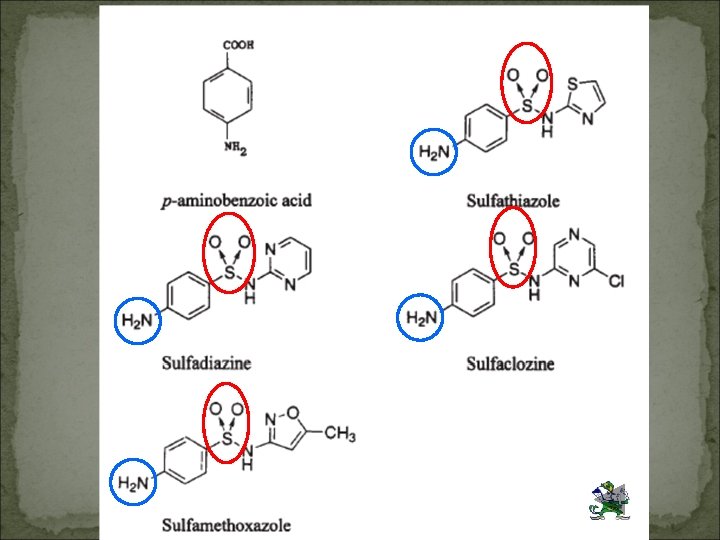
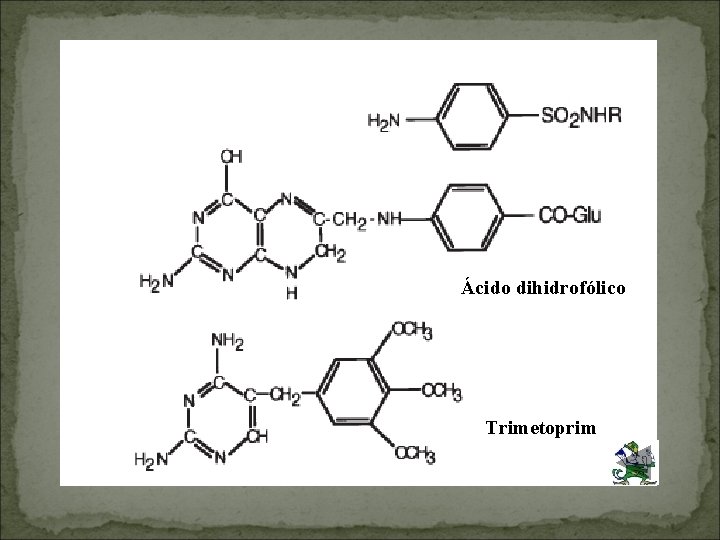
Ácido dihidrofólico Trimetoprim
- Slides: 39