SEMANA 1 ESTRUCTURA ATMICA Y TABLA PERIDICA QUMICA

SEMANA 1 ESTRUCTURA ATÓMICA Y TABLA PERIÓDICA QUÍMICA 2016 1

CURSO DE QUIMICA, PRIMER AÑO, CICLO 2016 LIBRO DE TEXTO: Timberlake, Karen. Química general, orgánica y biológica. Estructuras de la vida. 4 a. ed. Mexico: Pearson Educación; 2013. 936 p. PROGRAMA CORTO: TEMAS Y SUBTEMAS 2

• Semana 1: ESTRUCTURA ATÓMICA Y TABLAPERIÓDICA • Estructura atómica. • Partículas subatómicas fundamentales (protón, neutrón, electrón). • Tabla periódica • Número atómico. • Número másico. • Isótopo. Definición, representaciones y aplicaciones médicas de isótopos radioactivos. • Peso atómico. 3

• Diagramas de Bohr (para átomos e iones). • Configuración electrónica de átomos e iones, semidesarrollada y abreviada. • Electrones de valencia. • Grupos y períodos en la tabla periódica. • Clasificación de los elementos (incluir diatómicos). Nomenclatura básica de compuestos inorgánicos según reglas UIQPA (estudio en casa, ver guía de estudio) 4

ÁTOMO • Es la partícula más pequeña (con características determinadas) que forma la materia (los elementos). • Está formado por partículas subatómicas fundamentales siendo las principales: protón (carga +1, peso 1 uma), neutrón (carga 0, peso 1 uma), electrón (carga – 1, peso 0). • Es eléctricamente neutro (cargas + = - ) 5
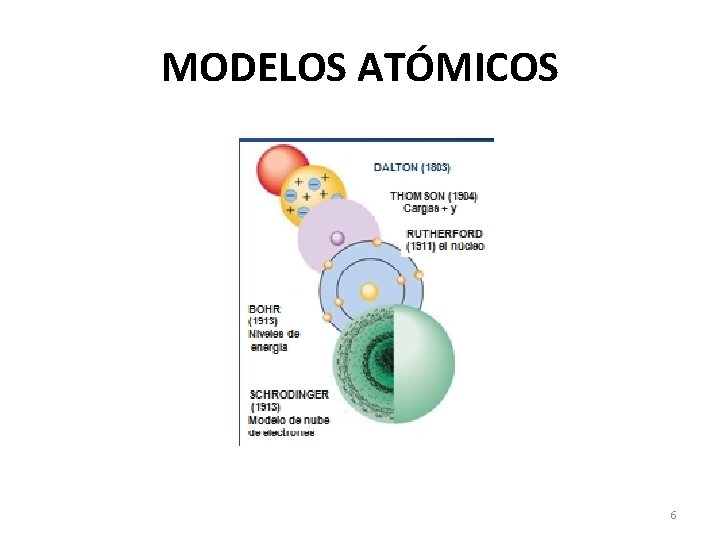
MODELOS ATÓMICOS 6

PARTES DEL ÁTOMO 7

PARTES DEL ÁTOMO NÚCLEO: • Parte central, del átomo donde está contenida la mayor parte de su masa, contiene los protones y neutrones. Tiene carga positiva. NUBE ELECTRÓNICA: • Espacio alrededor del núcleo donde hay una máxima probabilidad de encontrar sus electrones en constante movimiento. Tiene carga negativa. • En los átomos neutros (como están en la Tabla Periódica), el # de electrones = # de protones. 8

NÚMERO ATÓMICO • Se refiere al número de protones que tienen los átomos de cada elemento. • No hay átomos de diferentes elementos con el mismo número atómico. • No hay átomos de un mismo elemento con diferente número atómico. • Es el dato que identifica un elemento. 9
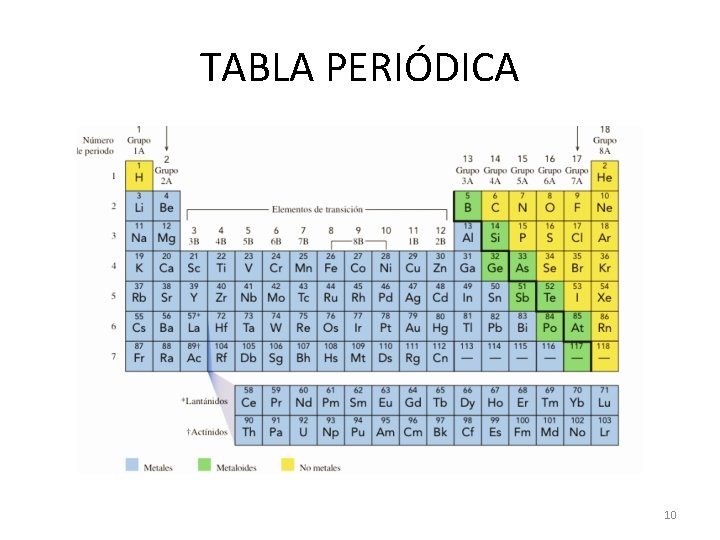
TABLA PERIÓDICA 10

NÚMERO MÁSICO ó DE MASA • Se refiere a la suma de neutrones y protones presentes en el núcleo de un átomo y representan el peso del átomo en umas. (No debe confundirlo con el peso atómico de los elementos en la Tabla Periódica). • El número másico no se encuentra en la Tabla Periódica, se da en otras tablas. 11
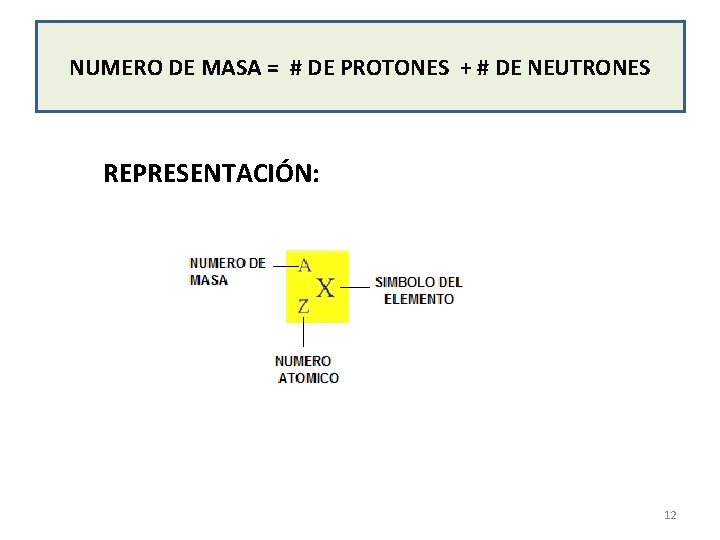
NUMERO DE MASA = # DE PROTONES + # DE NEUTRONES REPRESENTACIÓN: 12
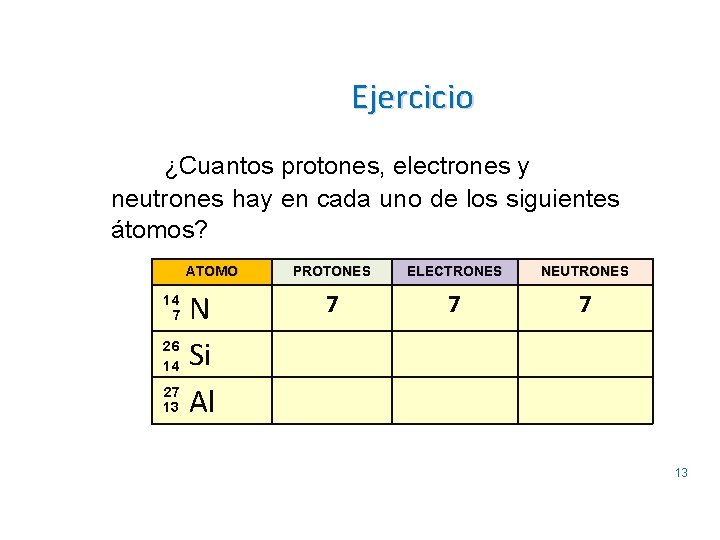
Ejercicio ¿Cuantos protones, electrones y neutrones hay en cada uno de los siguientes átomos? ATOMO N 26 14 Si 27 13 Al 14 7 PROTONES ELECTRONES NEUTRONES 7 7 7 13
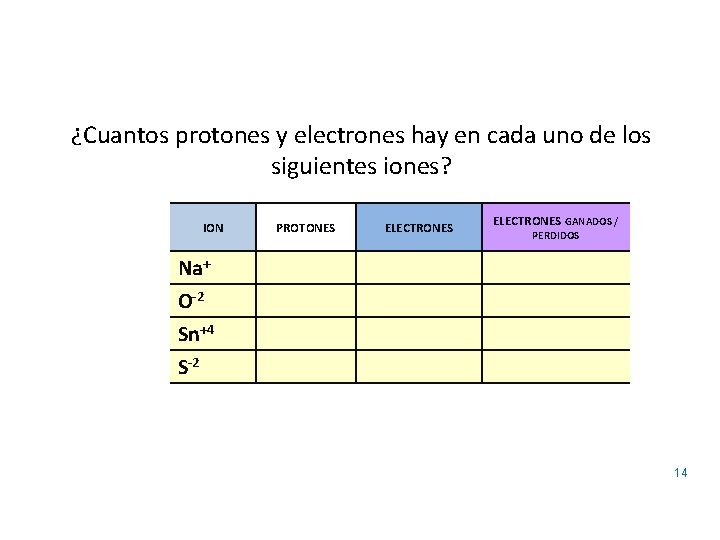
¿Cuantos protones y electrones hay en cada uno de los siguientes iones? ION PROTONES ELECTRONES GANADOS / PERDIDOS Na+ O-2 Sn+4 S-2 14
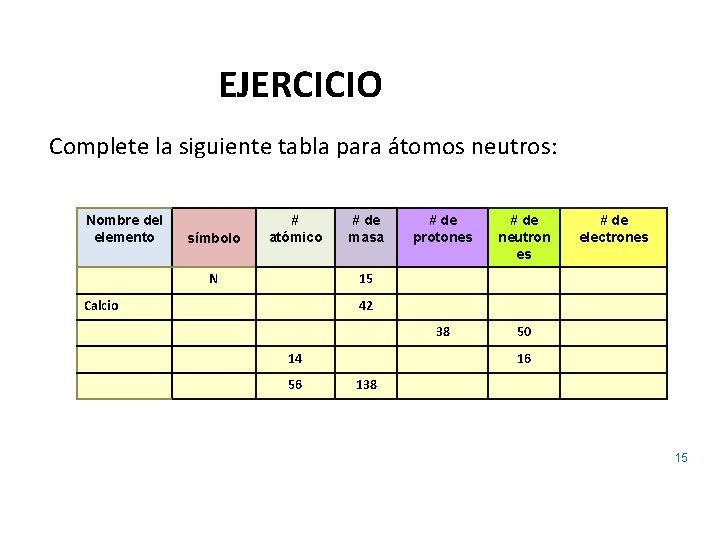
EJERCICIO Complete la siguiente tabla para átomos neutros: Nombre del elemento símbolo # atómico N # de masa # de protones # de neutron es 38 50 # de electrones 15 Calcio 42 14 56 16 138 15

ISOTOPOS • Átomos del mismo elemento con el mismo número atómico (# de protones), pero con distinto número másico (# de neutrones). Reaccionan igual. Algunos son radiactivos. 16

FORMAS DE REPRESENTAR LOS ISOTOPOS Ejemplo: magnesio-24 24 12 Mg Mg-24 17

EJERCICIOS 1. Los dos isotopos mas abundantes del estaño tienen números de masa 120 y 118. ¿Cuántos protones y neutrones tiene cada isotopo? 2. Escriba el símbolo atómico para isotopos con la siguiente información: a) 4 protones y 5 neutrones b) 26 electrones y 30 neutrones c) Un número de masa 24 y 13 neutrones 18

Isotopos estables/Isotopos inestables • Los isotopos de elementos con # atómicos hasta 19 tienen núcleos estables, son isotopos estables, no emiten radiación. • Los isotopos con # atómico de 20 o más tienen núcleos menos estables y presentan uno a más isotopos inestables que emiten radiación y se conocen como Isótopos Radiactivos o Radioisotopos. Algunos tienen aplicaciones medicas. 19
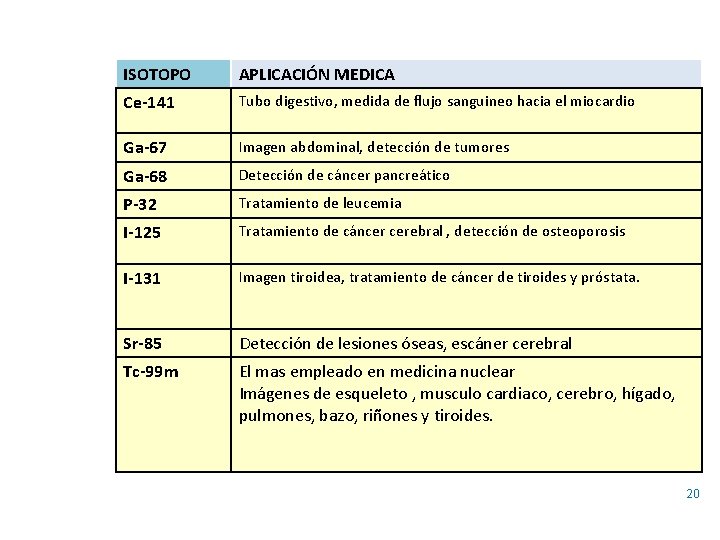
ISOTOPO APLICACIÓN MEDICA Ce-141 Tubo digestivo, medida de flujo sanguineo hacia el miocardio Ga-67 Imagen abdominal, detección de tumores Ga-68 Detección de cáncer pancreático P-32 Tratamiento de leucemia I-125 Tratamiento de cáncer cerebral , detección de osteoporosis I-131 Imagen tiroidea, tratamiento de cáncer de tiroides y próstata. Sr-85 Detección de lesiones óseas, escáner cerebral Tc-99 m El mas empleado en medicina nuclear Imágenes de esqueleto , musculo cardiaco, cerebro, hígado, pulmones, bazo, riñones y tiroides. 20

PESO ATÓMICO o MASA ATÓMICA de los ELEMENTOS • Es un valor que se encuentra en la Tabla Periódica, para cada elemento. • Se calculó utilizando el peso promedio de los diferentes isótopos de un mismo elemento, tomando en cuenta su peso y su abundancia en la naturaleza. 21
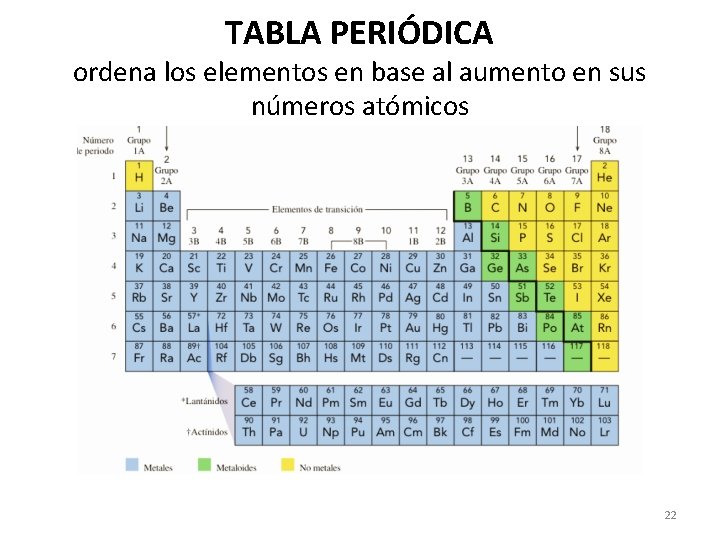
TABLA PERIÓDICA ordena los elementos en base al aumento en sus números atómicos 22

PERIODOS Son las 7 filas horizontales de elementos. El # de período indica cuantos niveles de energía tienen los átomos. I A METALES ALCALINOS II A METALES ALCALINOTERREOS III A FAMILIA DEL BORO IV A FAMILIA DEL CARBONO V A FAMILIA DEL NITROGENO VI A FAMILIA DEL OXIGENO VII A FAMILIA DE LOS HALOGENOS VIII A FAMILIA DE LOS GASES NOBLES GRUPOS o FAMILIAS Son las columnas verticales de elementos ( tienen propiedades similares). Tienen nombres específicos. El # de columna indica cuantos electrones de valencia tienen los átomos. 23
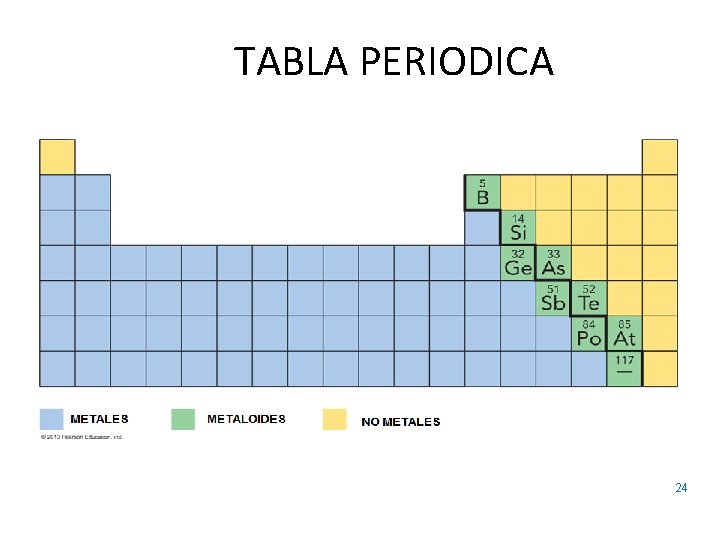
TABLA PERIODICA 24
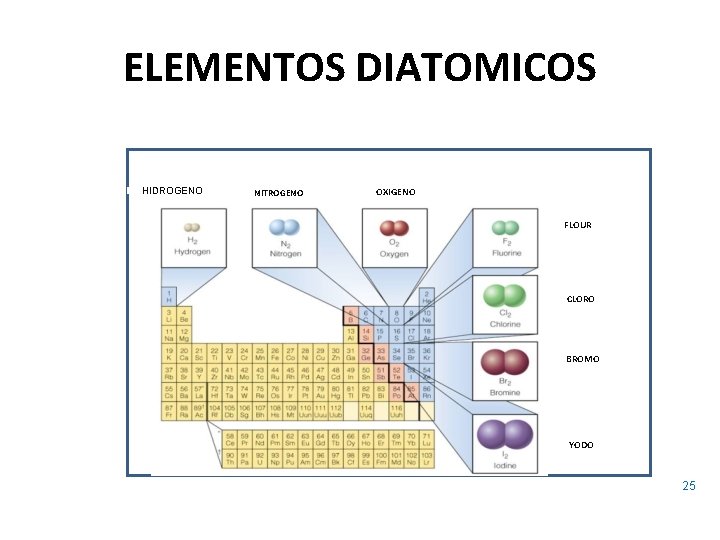
ELEMENTOS DIATOMICOS HIDROGENO NITROGENO OXIGENO FLOUR CLORO BROMO YODO 25
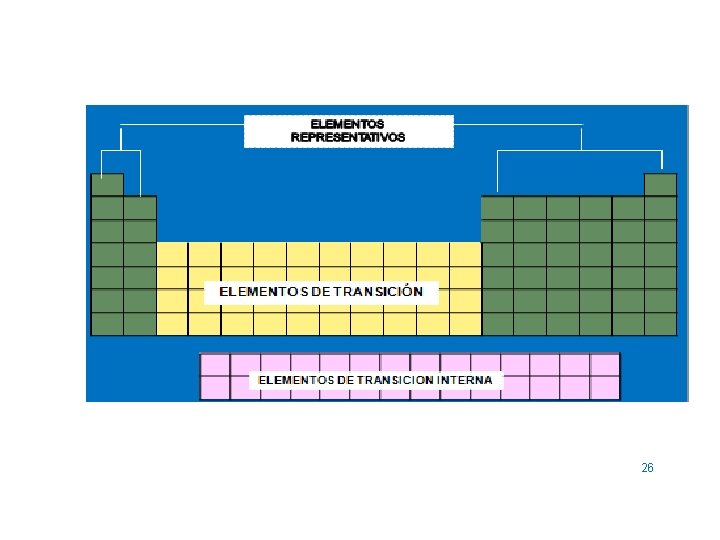
26

CONFIGURACIÓN ELECTRÓNICA DE ÁTOMOS Y DE IONES • Se refiere al arreglo u ordenamientos que tienen los electrones (según el # atómico)alrededor del núcleo en la nube electrónica de los átomos. • (Los electrones determinan las propiedades químicas y físicas de los elementos) • Alrededor del núcleo existen 7 niveles de energía (según el período donde está el elemento) n=1, n=2, n=3, n=4, n=5, n=6, n=7 • El n=1 es el de menor energía (cercano al núcleo) • El n=7 es el de mayor energía (alejado del núcleo) 27

DIAGRAMAS DE BOHR • Niels Bohr propuso un modelo atómicos donde se distribuyen los electrones alrededor del núcleo del átomo en espacios definidos de energía (niveles). • Según este diagrama, los electrones giran alrededor del núcleo en niveles de energía que pueden ir del n=1 al n=7. • En modelos posteriores ya se utilizan niveles, subniveles, orbitales para las configuraciones electrónicas. • El # máximo de electrones por cada nivel = 2 n 2 28
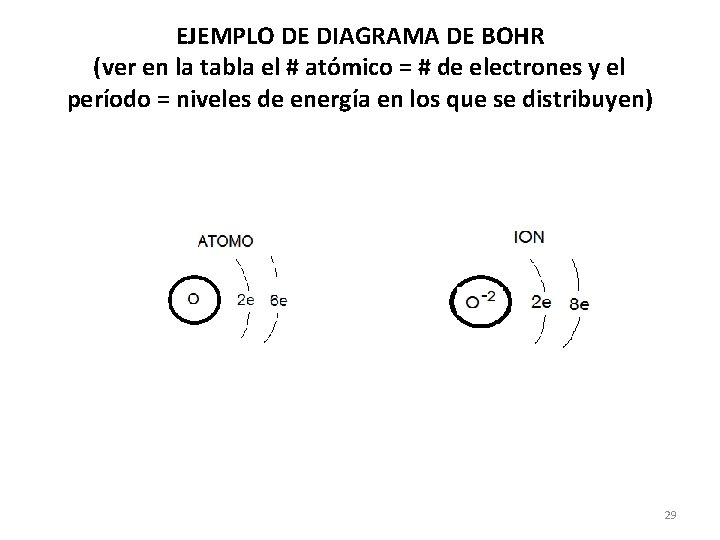
EJEMPLO DE DIAGRAMA DE BOHR (ver en la tabla el # atómico = # de electrones y el período = niveles de energía en los que se distribuyen) 29

En el modelo actual cada nivel de energía tiene un número de subniveles igual al # del nivel, que se identifican como s, p, d, f. Además cada subnivel tiene un número de orbitales (debe aprenderlos, ver el cuadro). Cada orbital acepta un máximo de 2 electrones girando en dirección opuesta (spin opuesto). Pueden estar apareados o no apareados (solo 1 electrón en el orbital). Sub-nivel No. de orbitales No. máximo de electrones s 1 2 p 3 6 d 5 10 f 7 14 g 9 18 30
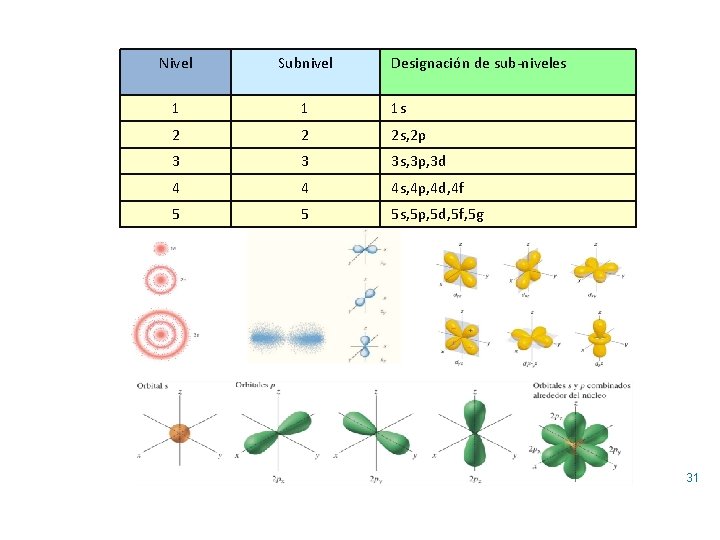
Nivel Subnivel Designación de sub-niveles 1 1 1 s 2 2 2 s, 2 p 3 3 3 s, 3 p, 3 d 4 4 4 s, 4 p, 4 d, 4 f 5 5 5 s, 5 p, 5 d, 5 f, 5 g 31
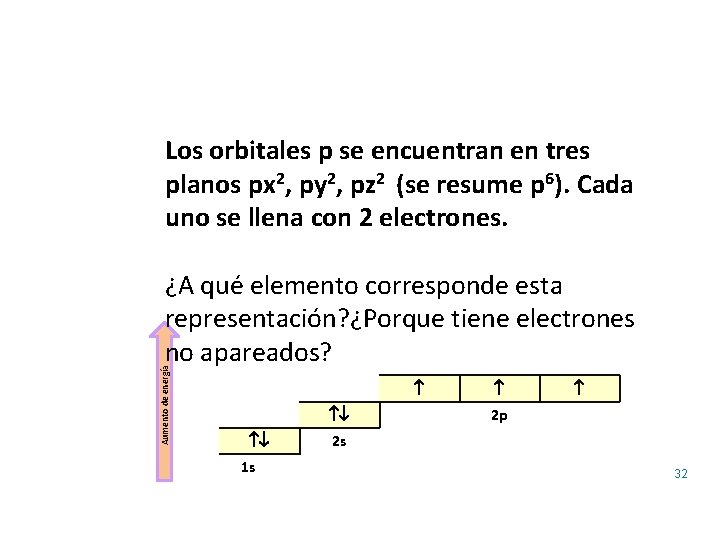
32 Los orbitales p se encuentran en tres planos px 2, py 2, pz 2 (se resume p 6). Cada uno se llena con 2 electrones. Aumento de energía ¿A qué elemento corresponde esta representación? ¿Porque tiene electrones no apareados? 1 s 2 p 2 s 32

Como escribir la configuración electrónica: Ej: 1 s 2 (1=nivel, s=subnivel, 2=electrones) • Ej: El Sodio (Na, #atómico 11) se encuentra en el 3 er período de la tabla, tiene 3 niveles de energía, n 1, n 2 y n 3 y 11 electrones. • 1 s 2, 2 p 6, 3 s 1 33
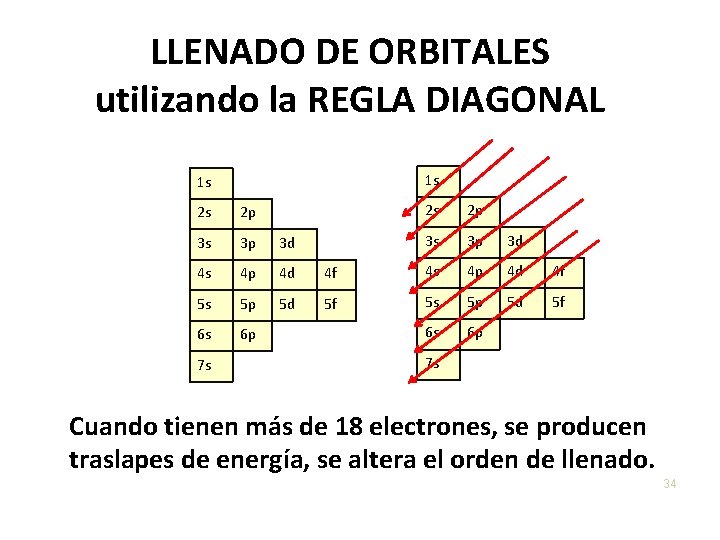
LLENADO DE ORBITALES utilizando la REGLA DIAGONAL 1 s 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 5 s 5 p 5 d 6 s 6 p 7 s 2 s 2 p 3 s 3 p 3 d 4 f 4 s 4 p 4 d 4 f 5 f 5 s 5 p 5 d 5 f 6 s 6 p 7 s Cuando tienen más de 18 electrones, se producen traslapes de energía, se altera el orden de llenado. 34

CONFIGURACIÓN ELECTRÓNICA SEMIDESARROLLADA • Hierro, Fe, # atómico 26=26 electrones, 4º período=4 nivele de energía. • Fe: 1 s 2, 2 p 6, 3 s 2, 3 p 6, 4 s 2, 3 d 6 • Presenta traslape de energía entre el nivel 4 s y el subnivel 3 d. 35

CONFIGURACIÓN ELECTRÓNICA ABREVIADA • Se busca el gas noble anterior al elemento , se encierra en corchetes su símbolo, se escriben solo los electrones que hacen falta. • Ej: Fe: 1 s 2, 2 p 6, 3 s 2, 3 p 6, 4 s 2, 3 d 6 • [Ar] 4 s 2, 3 d 6 36

Ejercicios 1. Escriba la configuración electrónica semidesarrollada y abreviada para los siguientes átomos a) azufre (S) b) potasio (K) c) Magnesio (Mg) 2. Escriba la configuración electrónica para los siguientes iones d) ion calcio (Ca+2) e) S-2 37

ELECTRONES DE VALENCIA • Son los electrones que se encuentran en el último nivel de energía, son los más externos en el átomo. • Son los que intervienen en las reacciones química y forman compuestos. • En los elementos representativos el # de columna corresponde a los electrones de valencia. 38

Ejemplos : 39 Cuantos electrones de valencia presentan los siguientes átomos a) Na b)Ge c) Mg d) S e) F FIN
- Slides: 39