SEMANA 1 ESTRUCTURA ATMICA Y TABLA PERIDICA QUMICA

SEMANA 1 ESTRUCTURA ATÓMICA Y TABLA PERIÓDICA QUÍMICA 2019 1

Semana 1 ESTRUCTURA ATÓMICA Y TABLAPERIÓDICA Estructura atómica. Partículas subatómicas fundamentales (protón, neutrón, electrón). Tabla periódica Número atómico. Número másico. Isótopos. Definición, representaciones. Aplicaciones médicas de la radiactividad (libro de texto, página 146). Peso atómico. Diagramas de Bohr (para átomos e iones). Diagrama de orbitales Configuración electrónica de átomos e iones, semidesarrollada y abreviada. Electrones de valencia. Grupos y períodos en la tabla periódica. Clasificación de los elementos (incluir diatómicos). Aplicación de los conceptos en la salud y el ambiente: Lecturas En libro de texto: La Química en el Ambiente “Toxicidad del Mercurio” “Radon en los hogares” “Bombillas fluorescentes ahorradoras de energía” -La Química en la Salud: “Nombres en latín de elementos de uso clínico” “Elementos esenciales para la salud” “Otros métodos de diagnóstico por imágenes” “Braquiterapia” Otras que se indiquen. Nomenclatura básica de compuestos inorgánicos Según reglas UIQPA. (estudio en casa) 2 Laboratorio: Normas de seguridad en el laboratorio de Química.

ÁTOMO • Es la partícula más pequeña con características determinadas que forma la materia o sustancia (o sea, todos los elementos de la tabla periódica). • Está formado por partículas subatómicas fundamentales siendo las principales: protón (carga +1, peso 1 uma), neutrón (carga 0, peso 1 uma), electrón (carga – 1, peso 0). • Es eléctricamente neutro (#cargas + = # cargas -) 3
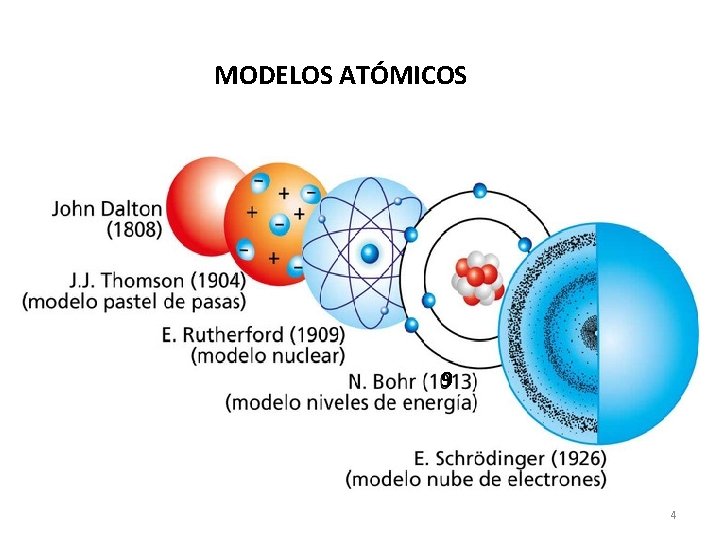
MODELOS ATÓMICOS 9 4

PARTES DEL ÁTOMO NÚCLEO: • Parte central, del átomo donde está contenida la mayor parte de su masa, contiene los protones y neutrones. Tiene carga positiva. NUBE ELECTRÓNICA: • Espacio alrededor del núcleo que contiene los electrones en constante movimiento. Es donde hay una máxima probabilidad de encontrar los electrones. Tiene carga negativa. • En los átomos neutros (como están en la Tabla Periódica), el # de electrones = # de protones. • Los electrones de los átomos son los que producen las reacciones químicas. 5

NÚMERO ATÓMICO • Se busca en la tabla periódica. Se refiere al número de protones que tienen un átomo de un elemento. • Cada átomo de los diferentes elementos tiene su propio # atómico. • Es el dato que identifica a los átomos de un elemento. Ej: si un átomo tiene 56 protones, es un átomo que se encuentra solo en el elemento Bario. • Si el átomo es neutro (no tiene carga), el # de protones es igual al # de electrones. 6
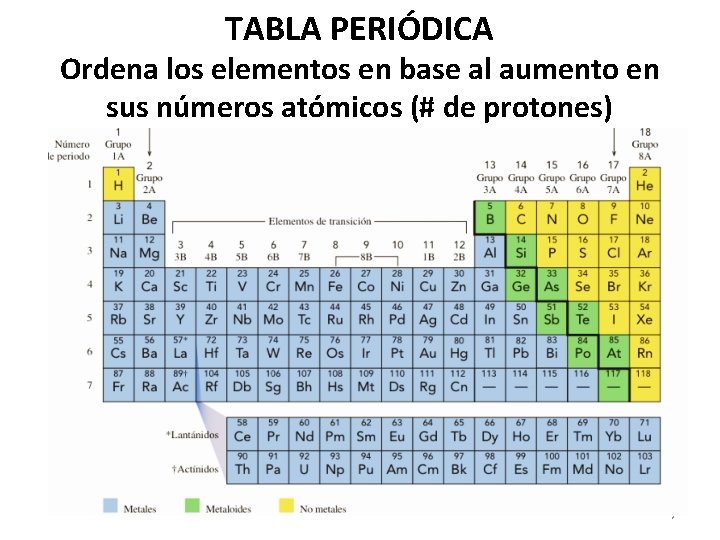
TABLA PERIÓDICA Ordena los elementos en base al aumento en sus números atómicos (# de protones) 7

NÚMERO MÁSICO ó # DE MASA (no es el peso atómico) • Se refiere a la suma de neutrones y protones presentes en el núcleo de un átomo y representan el peso del átomo en umas. (No debe confundirlo con el peso atómico de los elementos en la Tabla Periódica). • El número másico no se encuentra en la Tabla Periódica, se busca en otras tablas. • El # másico se aplica en los ISOTOPOS. 8
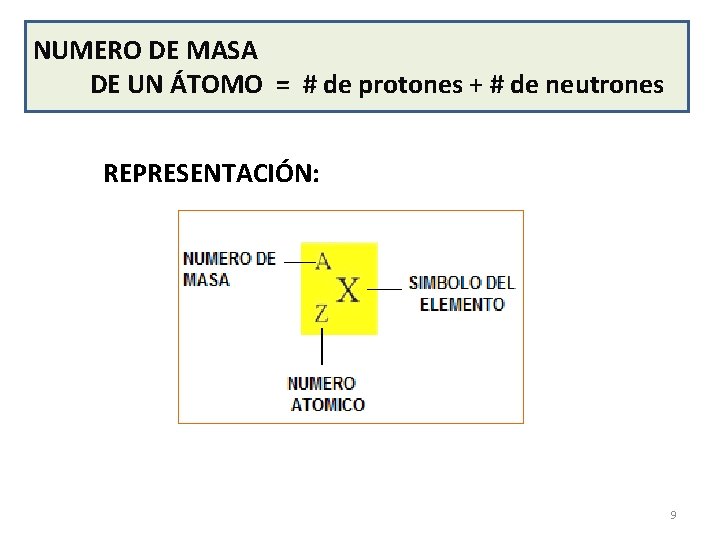
NUMERO DE MASA DE UN ÁTOMO = # de protones + # de neutrones REPRESENTACIÓN: 9
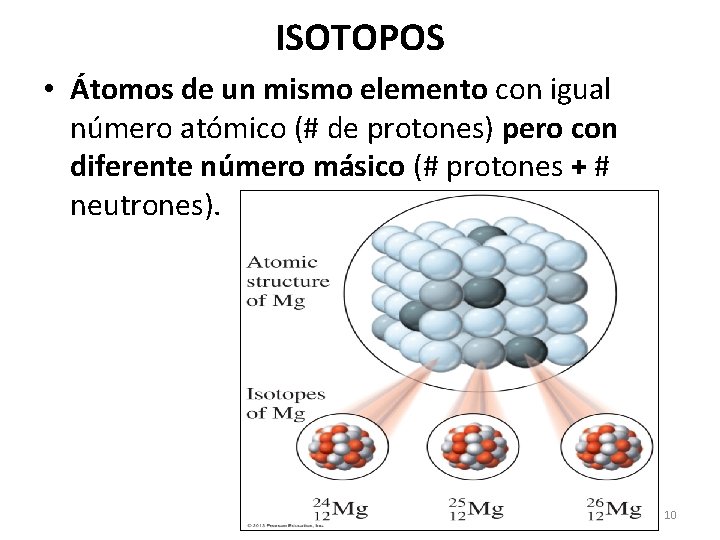
ISOTOPOS • Átomos de un mismo elemento con igual número atómico (# de protones) pero con diferente número másico (# protones + # neutrones). 10
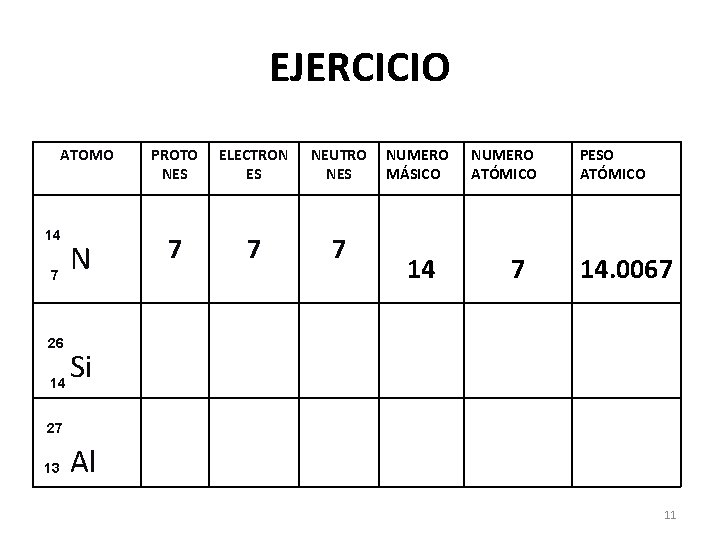
EJERCICIO ATOMO 14 7 26 14 N PROTO NES ELECTRON ES NEUTRO NES 7 7 7 NUMERO MÁSICO 14 NUMERO ATÓMICO 7 PESO ATÓMICO 14. 0067 Si 27 13 Al 11
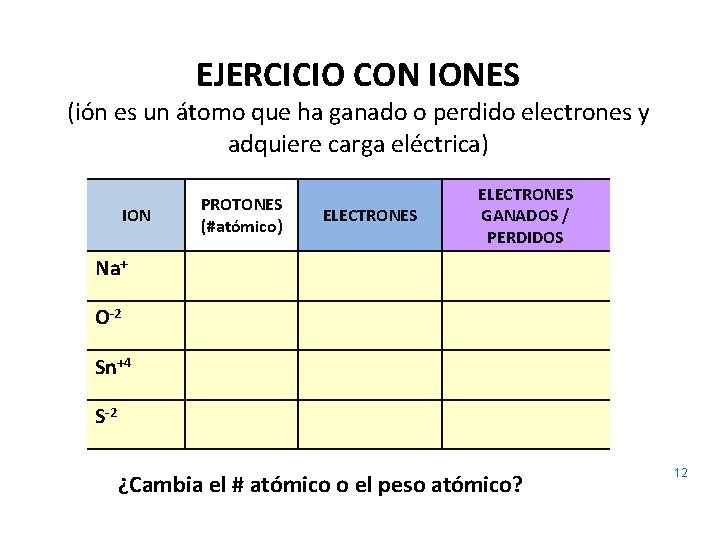
EJERCICIO CON IONES (ión es un átomo que ha ganado o perdido electrones y adquiere carga eléctrica) ION PROTONES (#atómico) ELECTRONES GANADOS / PERDIDOS Na+ O-2 Sn+4 S-2 ¿Cambia el # atómico o el peso atómico? 12
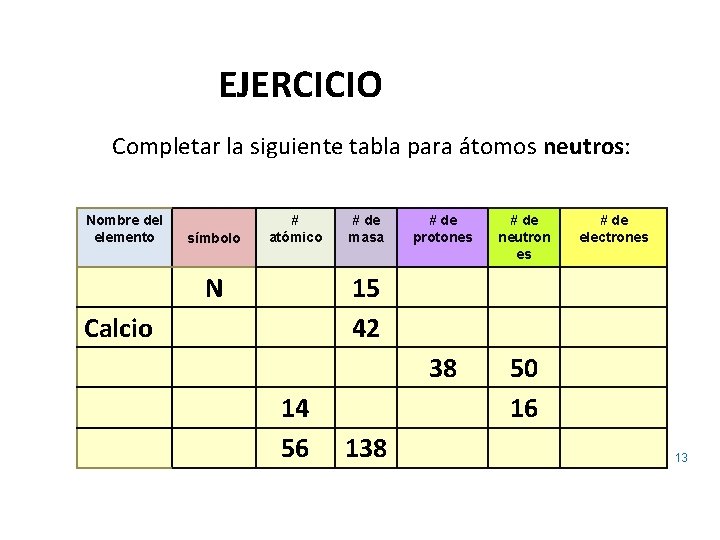
EJERCICIO Completar la siguiente tabla para átomos neutros: Nombre del elemento símbolo # atómico N # de masa # de protones # de neutron es 38 50 16 # de electrones 15 42 Calcio 14 56 138 13

Formas de representar isotopos Mg-24 magnesio-24 Ejercicio: El Carbono tiene tres isotopos: C-12, C-13, y C-14 Complete lo siguiente: C-12 C-13 C-14 Protones ______ Neutrones ______ Electrones ______ 14

EJERCICIO 1. 1. ¿Cuál de los siguientes pares de isotopos corresponden al mismo elemento y cuál es el símbolo del elemento? 2. 2. ¿En cuál par de isótopos los dos átomos tienen 8 neutrones? A. 12 6 B. 12 6 C. 15 7 X 15 7 Z 14 6 Z 16 8 X Z Z

EJERCICIOS 1. Los dos isotopos mas abundantes del estaño tienen números de masa 120 y 118. ¿Cuántos protones y neutrones tiene cada isotopo? 2. Escriba el símbolo atómico para isotopos con la siguiente información: a) 4 protones y 5 neutrones b) 26 electrones y 30 neutrones c) Un número de masa 24 y 13 neutrones 16

Isotopos estables/Isotopos inestables • Los isotopos de elementos con # atómicos hasta 19 generalmente tienen núcleos estables, son isotopos estables, no emiten radiación. • Los isotopos con # atómico de 20 o más generalmente tienen núcleos menos estables y presentan uno a más isotopos inestables que emiten radiación y se conocen como Isótopos Radiactivos o Radioisotopos. Algunos tienen aplicaciones medicas. 17
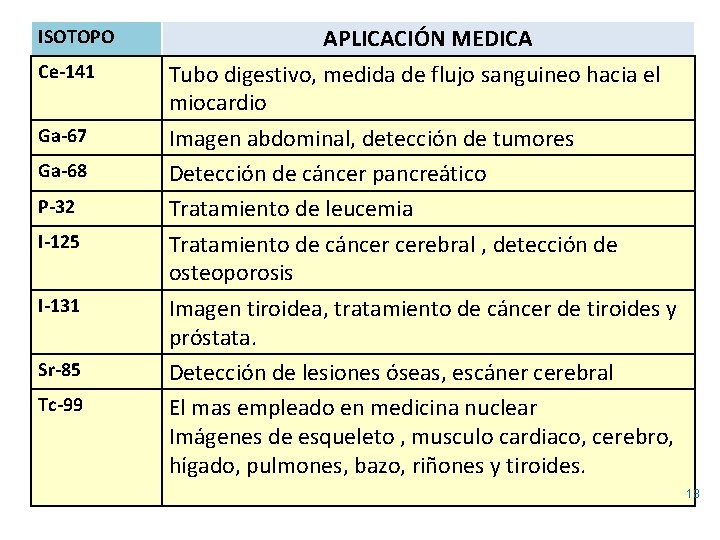
ISOTOPO Ce-141 Ga-67 Ga-68 P-32 I-125 I-131 Sr-85 Tc-99 APLICACIÓN MEDICA Tubo digestivo, medida de flujo sanguineo hacia el miocardio Imagen abdominal, detección de tumores Detección de cáncer pancreático Tratamiento de leucemia Tratamiento de cáncer cerebral , detección de osteoporosis Imagen tiroidea, tratamiento de cáncer de tiroides y próstata. Detección de lesiones óseas, escáner cerebral El mas empleado en medicina nuclear Imágenes de esqueleto , musculo cardiaco, cerebro, hígado, pulmones, bazo, riñones y tiroides. 18

PESO ATÓMICO o MASA ATÓMICA de los ELEMENTOS • Es un valor que se encuentra en la Tabla Periódica, para cada elemento. • Se calculó utilizando el peso promedio de los diferentes isótopos de un mismo elemento, tomando en cuenta su peso y su abundancia en la naturaleza. 19

DIAGRAMAS DE BOHR (Niels Bohr) una forma simple de representar los electrones en el átomo • Es un modelo atómicos que representa los electrones girando alrededor del núcleo del átomo en espacios definidos de energía llamados niveles de energía. • Como averiguar cuantos niveles de energía tiene un átomo? Se ve en que período o fila horizontal de la tabla periódica se encuentra. Si esta en el primer período tiene un nivel n=1 (con mínima energía), si esta en el segundo tiene dos n=2, n=3, n=4, n=5, n=6 hasta un máximo de n=7 (con mayor energía). • En modelos posteriores ya se utilizan niveles, subniveles, orbitales para ubicar los electrones en las configuraciones electrónicas. • El número máximo de electrones por nivel se calcula con # max. electrones por nivel=2 xn 2 (n=# de nivel). 20
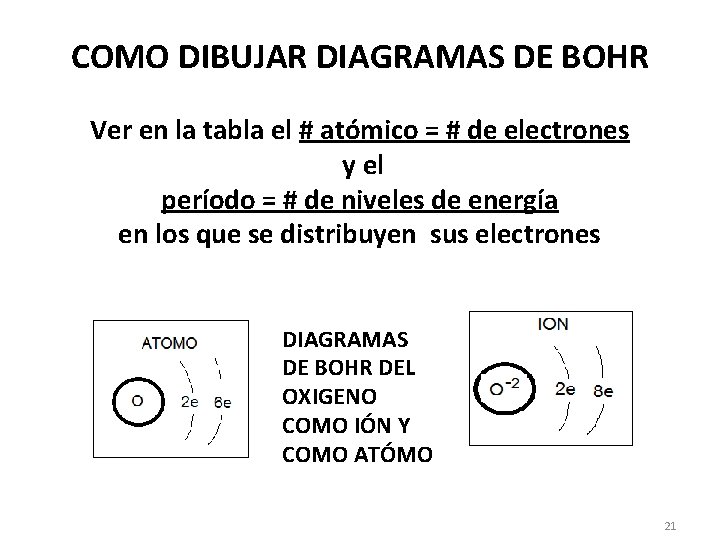
COMO DIBUJAR DIAGRAMAS DE BOHR Ver en la tabla el # atómico = # de electrones y el período = # de niveles de energía en los que se distribuyen sus electrones DIAGRAMAS DE BOHR DEL OXIGENO COMO IÓN Y COMO ATÓMO 21
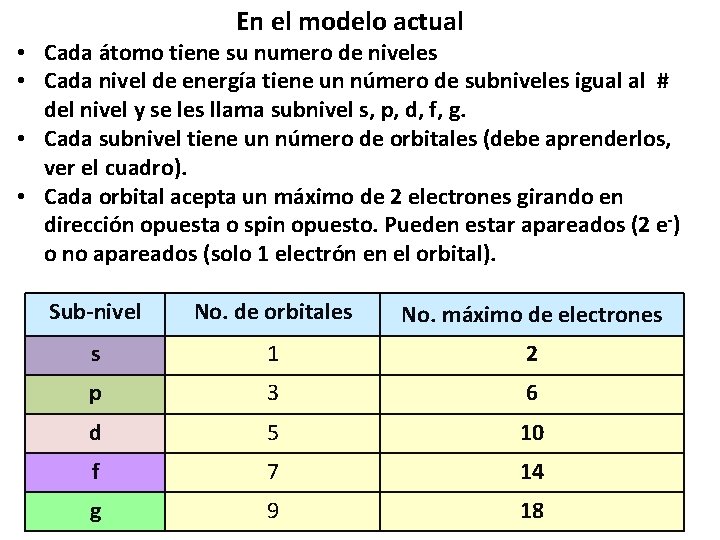
En el modelo actual • Cada átomo tiene su numero de niveles • Cada nivel de energía tiene un número de subniveles igual al # del nivel y se les llama subnivel s, p, d, f, g. • Cada subnivel tiene un número de orbitales (debe aprenderlos, ver el cuadro). • Cada orbital acepta un máximo de 2 electrones girando en dirección opuesta o spin opuesto. Pueden estar apareados (2 e -) o no apareados (solo 1 electrón en el orbital). Sub-nivel No. de orbitales No. máximo de electrones s 1 2 p 3 6 d 5 10 f 7 14 g 9 18 22
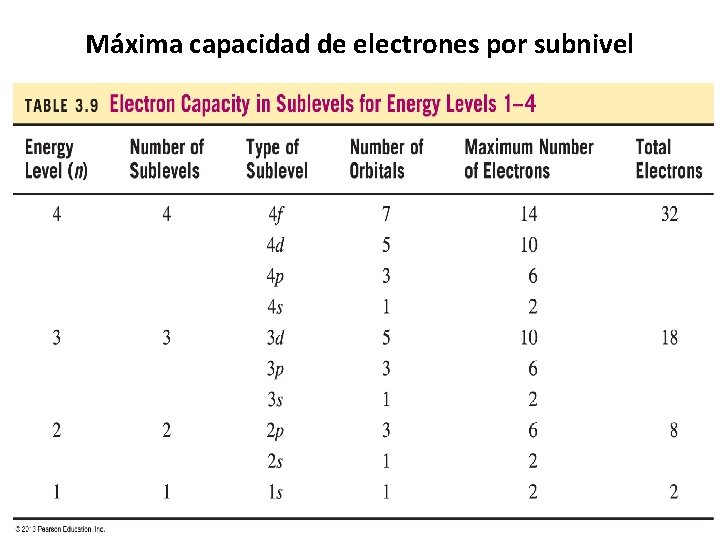
Máxima capacidad de electrones por subnivel 23

CONFIGURACIÓN ELECTRÓNICA DE ÁTOMOS Y DE IONES • Es la representación del arreglo u ordenamiento que tienen los electrones alrededor del núcleo en la nube electrónica de los átomos. • (Los electrones determinan las propiedades químicas y físicas de los elementos) • Alrededor del núcleo existen 7 niveles de energía (según el período donde está el elemento) n=1, n=2, n=3, n=4, n=5, n=6, n=7 • El n=1 es el de menor energía (cercano al núcleo) • El n=7 es el de mayor energía (alejado del núcleo) 24

Como escribir configuraciones electrónicas Ej: 1 s 2 significa: 1=nivel, s=subnivel, 2=electrones • Ej: El Sodio (Na, #atómico 11) se encuentra en el 3 er período de la tabla, tiene 3 niveles de energía, n 1, n 2 y n 3 y 11 electrones. 1 s 2, 2 p 6, 3 s 1 25
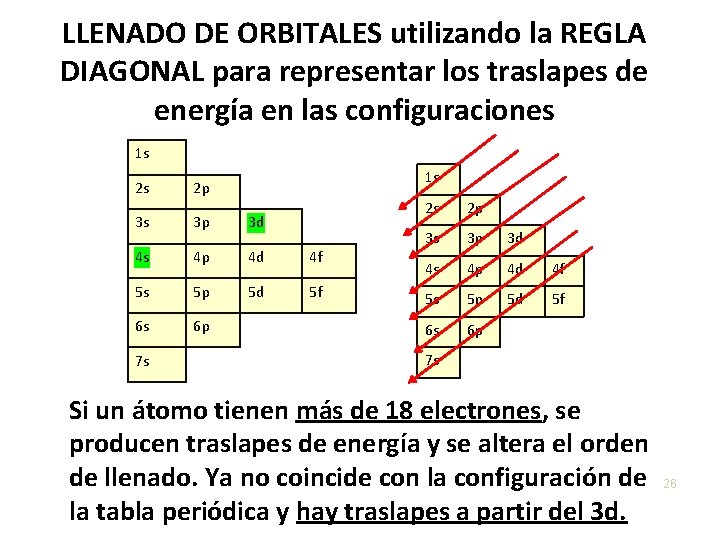
LLENADO DE ORBITALES utilizando la REGLA DIAGONAL para representar los traslapes de energía en las configuraciones 1 s 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s 5 p 5 d 5 f 6 s 6 p 7 s Si un átomo tienen más de 18 electrones, se producen traslapes de energía y se altera el orden de llenado. Ya no coincide con la configuración de la tabla periódica y hay traslapes a partir del 3 d. 26

CONFIGURACIÓN ELECTRÓNICA SEMIDESARROLLADA Hierro, Fe: # atómico 26 (26 electrones) 4º período (4 nivele de energía). Configuración semidesarrollada: • Fe: 1 s 2, 2 p 6, 3 s 2, 3 p 6, 4 s 2, 3 d 6 • Presenta traslape de energía entre el nivel 4 s y el subnivel 3 d. 27

CONFIGURACIÓN ELECTRÓNICA ABREVIADA • Se busca el gas noble anterior al elemento , se encierra en corchetes su símbolo, se escriben solo los electrones que hacen falta. • Ej: Fe: 1 s 2, 2 p 6, 3 s 2, 3 p 6, 4 s 2, 3 d 6 Fe: [Ar] 4 s 2, 3 d 6 28
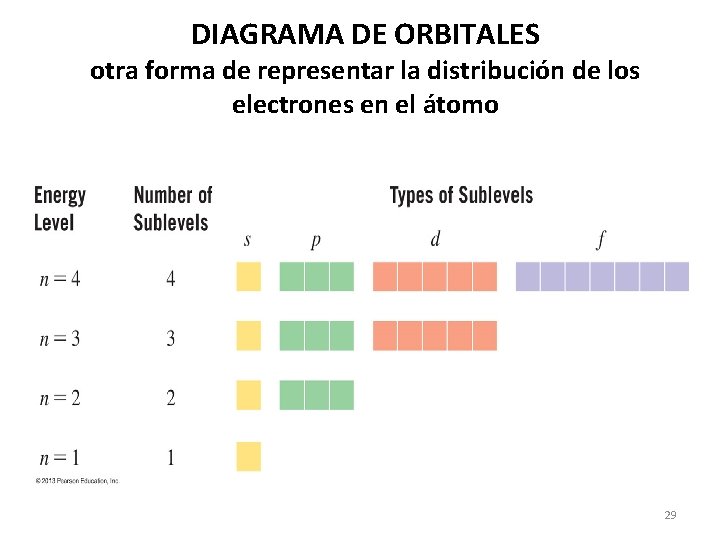
DIAGRAMA DE ORBITALES otra forma de representar la distribución de los electrones en el átomo 29
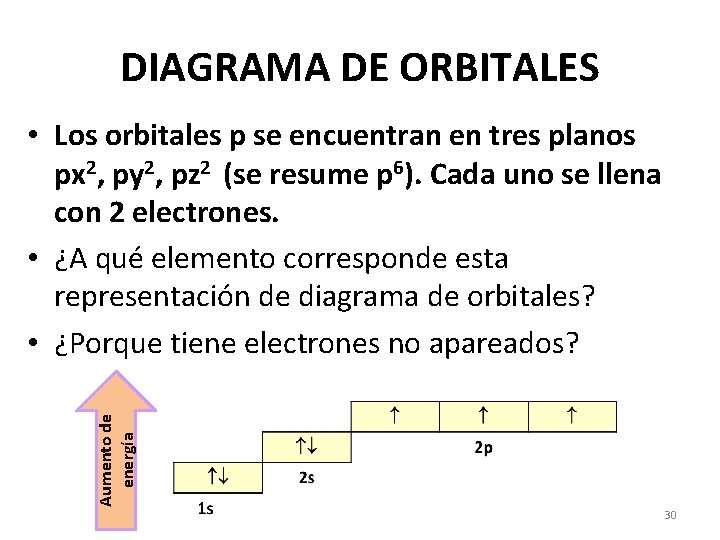
DIAGRAMA DE ORBITALES Aumento de energía • Los orbitales p se encuentran en tres planos px 2, py 2, pz 2 (se resume p 6). Cada uno se llena con 2 electrones. • ¿A qué elemento corresponde esta representación de diagrama de orbitales? • ¿Porque tiene electrones no apareados? 30
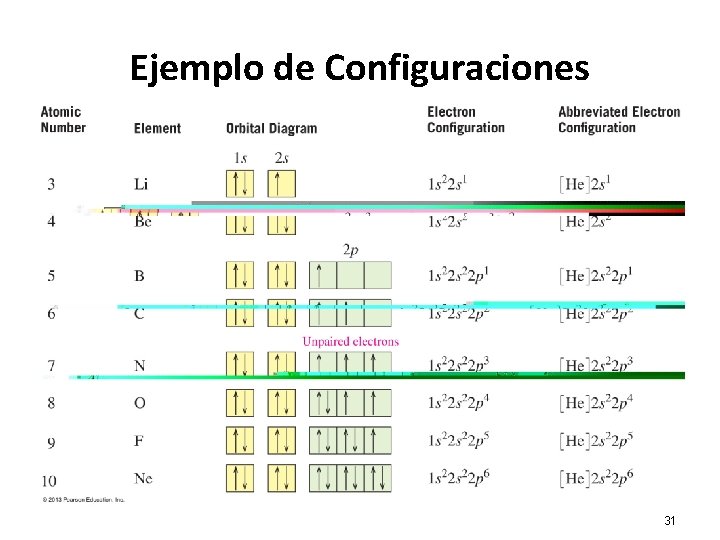
Ejemplo de Configuraciones 31
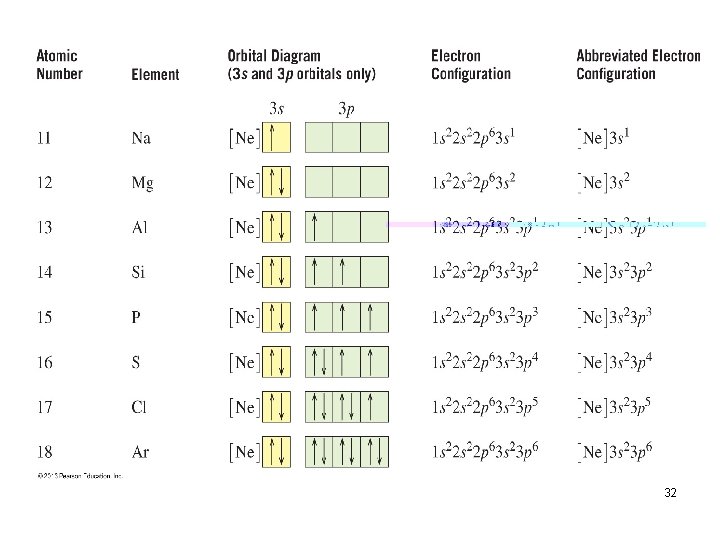
32

Ejercicios 1. Escriba la configuración electrónica semidesarrollada y abreviada para los átomos: a) Potasio (K) b) Aluminio (Al) c) Selenio (Se) 2. Escriba la configuración electrónica para los iones: d) ion calcio (Al+3) e) ion selenio (Se-2) 33

LA TABLA PERIÓDICA 34

PERIODOS Son las 7 filas horizontales de elementos. El # deperíodo indica cuantos niveles de energía tienen los átomos. GRUPOS O FAMILIAS I A METALES ALCALINOS II A METALES ALCALINOTERREOS III A FAMILIA DEL BORO IV A FAMILIA DEL CARBONO Son las columnas verticales de elementos ( tienen propiedades similares). Tienen nombres específicos. V A FAMILIA DEL NITROGENO VI A FAMILIA DEL OXIGENO VII A FAMILIA DE LOS HALOGENOS VIII A FAMILIA DE LOS GASES NOBLES El # de columna indica cuantos electrones de valencia tienen los átomos. 35

ELECTRONES DE VALENCIA • Son los electrones que se encuentran en el último nivel de energía, son los más externos en el átomo. • Son los que intervienen en las reacciones química y forman compuestos. • En los elementos representativos el # de columna corresponde a los electrones de valencia. 36

Ejemplos : 37 Cuantos electrones de valencia presentan los siguientes átomos: a) Li b) Ba c) Al d) N e) Br
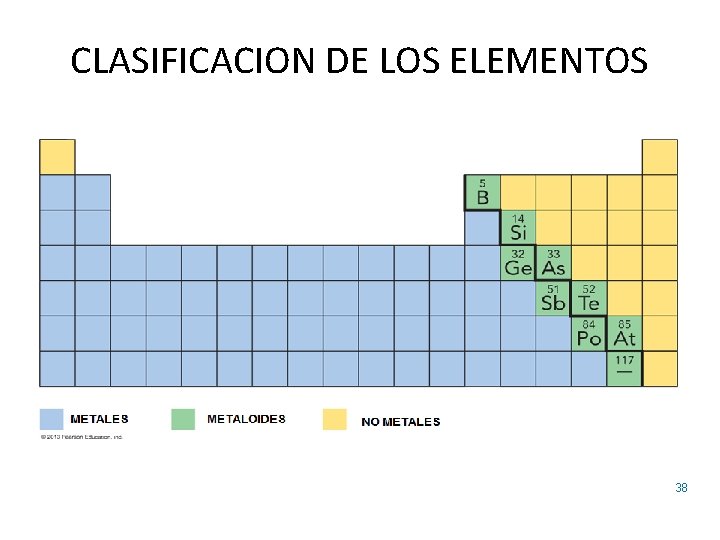
CLASIFICACION DE LOS ELEMENTOS 38
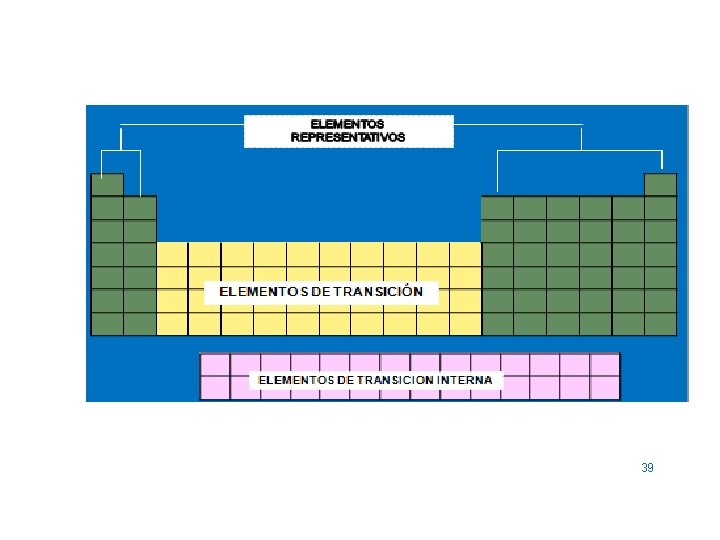
39
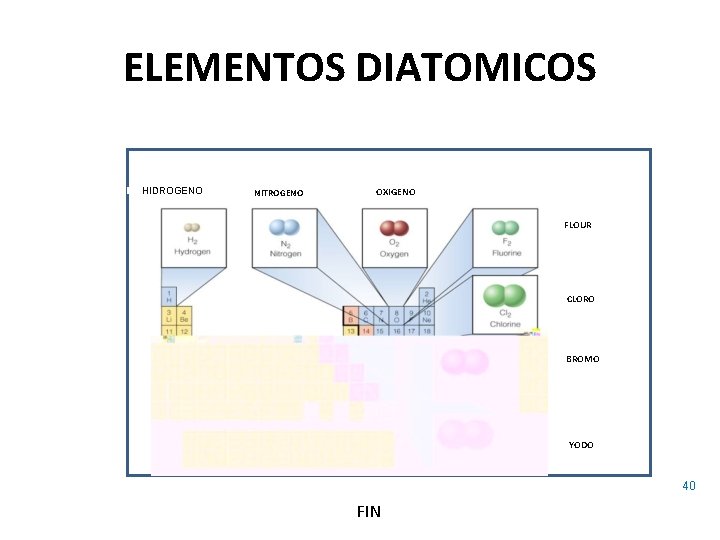
ELEMENTOS DIATOMICOS HIDROGENO NITROGENO OXIGENO FLOUR CLORO BROMO YODO 40 FIN
- Slides: 40